日益严重的水污染使污水处理问题在全球范围内广受关注,而工业污水含有各种难降解有机污染物,具有高盐、高毒等特性,不能采用生物法有效处理,传统的吸附等物理方法又容易引起二次污染,因此,高级光催化氧化技术成为目前处理工业废水的研究热点(Fang et al., 2009).
金属卟啉作为高级光催化氧化剂,具有在温和条件下活化分子氧催化降解有机污染物的特性,但制备困难,产率仅在30%左右(Littler et al., 2009; 高德等,1994). 本文以经济易得的氯化血红素为原料,通过改变中心金属离子种类、在卟啉环meso-位引入吸电子的硝基取代基(王兰芝等,2005)的方法制得硝基取代的锌卟啉化合物.
由于金属卟啉分子在水溶液中易发生团聚(王攀等,2011),催化活性点位不能充分发挥作用,而且回收困难.因此,本文将其共价键合到具有磁性的载体上,以制得稳定性强、催化活性高、易于分离回收的负载型可见光催化剂.同时利用热重分析仪(TG)、透射电子显微镜(TEM)、扫描电子显微镜(SEM)和振动磁强计(VSM)对催化剂进行表征,并研究催化剂的催化降解性能.
2 材料与方法(Materials and methods) 2.1 实验材料及试剂三聚氯氰购于天津越过化工有限公司,分析纯;氯化血红素购于天津市生命科学应用研究所,食品级;其他试剂包括微晶纤维素、氢氧化钠、尿素、无水乙醇、浓硫酸、浓盐酸、浓硝酸、石油醚、磷酸三丁酯、乙酸锌、四氢呋喃、无水碳酸钠、浓盐酸、吡啶、乙酸锌、BPA、对苯二酚(HQ)、PNP、甲基橙(HIn)、N,N-二甲基甲酰胺(DMF)、硝酸银、叔丁醇(TBA)、对苯醌(BQ)等均为分析纯,购于天津市江天统一科技有限公司;活性红染料废水取自工厂生产废水;所有实验用水均为蒸馏水.
2.2 催化剂的制备催化剂载体的制备:按文献(闫绍轩等,2012; 吴景悦等,2014)方法,将实验室自制的纳米Fe3O4微球分散到乙醇中,边搅拌边滴加纤维素溶液(Mao et al., 2006)制备纤维素包覆纳米Fe3O4微球的磁性载体.
氯化血红素改性:按照文献(徐锐等,2009)方法由氯化血红素(PFe-Cl)得到原卟啉二甲酸(PDMA),再将原卟啉二甲酸溶于浓硫酸中,在0 ℃下,边搅拌边滴加浓硝酸,滴加完后停止冰浴,使反应体系逐渐升温至室温,2 h后停止反应;将反应液倒入冰水中析出沉淀,洗涤后烘干,用1 ∶ 3的氯仿/甲醇混合溶液重结晶,得二硝基原卟啉二甲酸(Dinitro-PDMA)(Bonnett et al., 1965).
硝基取代锌卟啉(Dinitro-PZn)合成(Guo et al., 2003):将Dinitro-PDMA溶于适量DMF中,加热回流,分批加入与卟啉等物质的量的醋酸锌,回流反应4 h后停止,将反应液冷却至室温后,于低温下静置过夜;过滤沉淀,滤饼分别用稀醋酸、水和乙醇洗涤,收集固体干燥即得产物.
磁微球负载硝基锌卟啉光催化剂的制备:按照文献(吴景悦等,2014;Yang et al., 2014)方法将改性后的血红素负载到载体上制备得到磁微球负载硝基锌卟啉光催化剂.
2.3 催化剂的表征采用U-3900H型紫外-可见分光光度计测试分析改性前后血红素的光吸收特性;Philips Tacni G2F20型透射电子显微镜观测催化剂的形貌;ZEISS MERLIN Compact 扫描电子显微镜表征催化剂的表面特征;Netzsch TG209F3热重分析仪对催化剂进行热重分析;LDJ9600型振动磁强计测试催化剂的磁滞回线.
2.4 催化剂催化性能评价 2.4.1 单一有机污染物降解配制20 mg · L-1的溶液,模拟有机污染物废水.室温下,4种溶液分别取50 mL加入10 mg催化剂,在光化学反应仪(300W汞灯光源)中进行光催化降解反应.上述4种溶液,每隔1 h分别取5 mL,通过紫外-可见分光光度扫描仪(UV-Vis)检测有机物降解效果,采用标准曲线定量法得到不同时刻有机物的浓度,并按照以下公式计算降解率η:
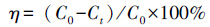
式中,C0和Ct分别代表降解前和降解t小时后各待降解物的浓度.
2.4.2 活性红染料废水降解以直接取自工厂的高含盐、高浓度活性红染料废水为试样,用水稀释1000倍后,取50 mL加入10 mg催化剂,按照单一有机污染物降解方法,考察催化剂的催化活性.
3 结果与讨论(Results and discussion) 3.1 催化剂的表征图 1为铁卟啉、脱铁卟啉及经过硝化和络合锌 离子后的硝基锌卟啉的UV-Vis光谱图.其中,铁卟啉(曲线a)的最大吸收峰在382 nm处,在500~600 nm的区域有两个弱的吸收峰.而脱铁后的卟啉,即图中的曲线b和c,最大吸收峰红移至可见光区(>400 nm),并且在500~650 nm的区域出现4个弱吸收峰.改性得到的硝基取代锌卟啉(曲线d),最大吸收峰红移至422 nm且吸光强度增大,在550 nm和571 nm有两个弱的吸收峰,呈现出金属卟啉的特征,说明已成功络合了锌离子(王兰芝等,2008).
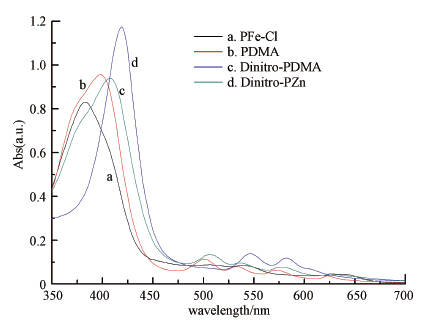 |
| 图 1 氯化血红素及各改性产物的UV-Vis谱图 Fig. 1 UV-Vis spectra of hemin and its modified products |
硝基锌卟啉光催化剂的形貌特征通过TEM和SEM测试,结果见图 2.由图 2可知,催化剂呈球状且粒度均匀,颗粒颜色明显呈现出中心深边缘浅的特点.10 nm分辨率的图片(图 2a)显示,中心颜色深的区域有清晰的条纹结构,归属于纤维素-Fe3O4复合微球,边缘则是键合到载体上的硝基锌卟啉.
 |
| 图 2 催化剂的形貌表征(a,b为TEM,c为SEM) Fig. 2 Morphology characterization of the catalyst |
图 3是催化剂的热失重曲线,在40~800 ℃的范围内,该曲线呈现出3个明显的失重区,其中,100 ℃以内减少的4.68%是催化剂吸附的水分子质量,第2个失重区损失的是卟啉的质量,失重温度在300 ℃左右,失重率为32.06%,即催化剂负载率为32.06%.在340~700 ℃范围内缓慢减少的质量为复合载体中的纤维素(Nada et al., 2002),失重率为17.43%.剩余的质量为载体中的四氧化三铁,质量含量为45.83%.另外,从热失重曲线也可以看出,在300 ℃以下,催化剂可以稳定存在,具有较好的热稳定性.
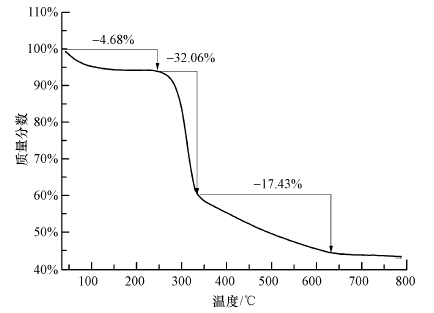 |
| 图 3 催化剂的热失重曲线 Fig. 3 TGA curves of the catalyst |
磁微球负载的硝基锌卟啉催化剂的磁性性能由图 4中的磁滞回线来表征.由图 4可知,催化剂无明显磁滞现象,根据磁化率定义:χ=M/H,可知χ>0,改性血红素光催化剂具有顺磁性.矫顽力和剩磁的检测值接近于0,饱和磁场强度为35.12 emu · g-1,因此,在外加磁场存在的情况下,催化剂可以通过磁性收集,从降解液中分离出来,当取消外加磁场后,催化剂可再次分散于降解溶液中,从而实现方便的回收和重复使用.
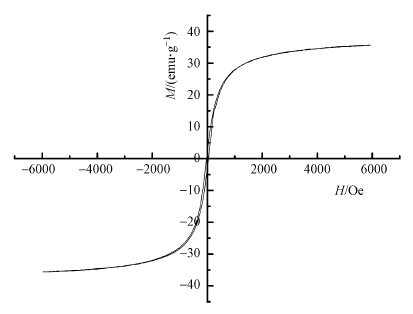 |
| 图 4 催化剂的磁滞回线图 Fig. 4 Hysteresis loop of the catalyst |
分别以BPA、HIn、HQ及PNP为待降解物,考察催化剂的催化活性.结果表明,降解反应主要集中在前2 h内,虽然催化剂对以上4种物质的降解速率不同,但降解3 h后降解率皆能达到80%以上,5 h后最高能达到98%左右(图 5).
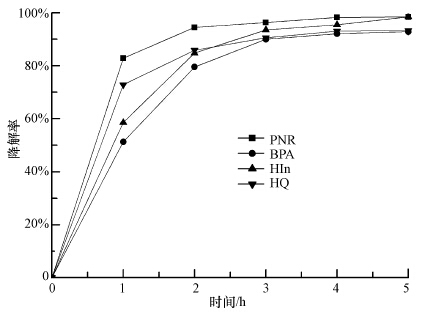 |
| 图 5 BPA、HIn、HQ及PNP(浓度均为20 mg · L-1)的降解曲线 Fig. 5 Degradation ratio of BPA,HIn,HQ and PNP(20 mg · L-1) |
参照污水排放标准,设定pH变化范围为6~9,使用赛多利斯PB-10酸度计通过滴加稀盐酸或稀氢氧化钠溶液来调节待降解溶液的pH值,考察了pH值在6~9范围内催化剂的光降解效率.图 6为光降解3 h后不同pH值下各有机物的降解率.结果表明,4种物质均在pH=7时降解率最高,且在pH值6~9范围内,降解率均超过80%,说明催化剂在整个排水许可pH范围内都有较好的催化效果.在弱酸性条件下,H+存在抑制了· OH的产生;弱碱性条件下,OH-的存在使催化剂中心Zn2+活化分子氧产生· OH的过程被抑制(Gokakakar et al., 2009).
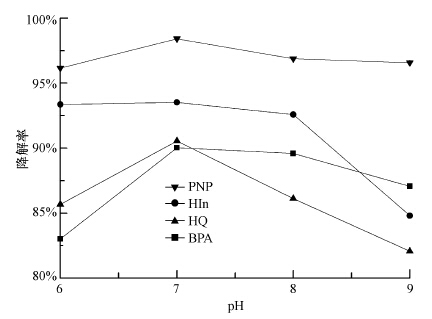 |
| 图 6 溶液pH对降解率的影响 Fig. 6 Effect of pH on the degradation ratio |
用水稀释1000倍后的活性红工业废水,经6 h处理后溶液的颜色基本消失,降解率达83.67%.相比于降解单一有机污染物的PNP等,废水的降解速率较慢且降解率低.这是由于工业废水成分复杂,活性红分子量大且结构稳定所致.
溶液pH对活性红工业废水降解率的影响与单一有机物的结果基本一致,在中性环境下降解效果最好,结果见图 7.但研究发现,当溶液pH偏离7~8时,活性红的降解率下降比较明显,除H+和OH-的抑制作用外,酸性条件下,催化剂表面的羟基会结合溶液中的H+形成氢键而带正电,而活性红染料因结构中的磺酸基含有高负电性的氧而容易在催化剂表面大量吸附(董永春等,2007),阻碍了自由基的传递及活性物种的生成;当溶液呈碱性时,大量的OH-与负电性的染料分子竞争催化剂表面的活性位点,使染料分子与催化剂分子不能充分接触,降解率下降.
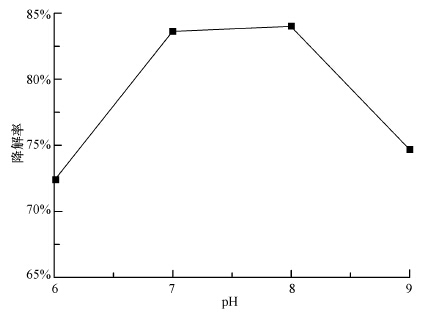 |
| 图 7 溶液pH对活性红废水降解率的影响 Fig. 7 Effect of pH on the degradation ratio of reactive red waste-water |
金属卟啉在光催化降解过程中,激发态卟啉能活化分子氧产生一系列强氧化性物种,从而实现对难降解有机污染物的处理.本文采用不同捕获剂研究了改性血红素的光催化反应机理,结果见图 8.结果表明,当加入电子捕获剂(AgNO3)、空穴捕获剂(DMF)、· OH捕获剂(TBA)和O- · 2捕获剂(BQ)以后,与未加捕获剂的降解体系相比4种物质的降解率都有所下降,其中,DMF和TBA的影响大于AgNO3和BQ的影响.这是由于DMF容易吸附在纤维素载体的表面,猝灭催化剂产生的空穴,进而影响自由基的生成,而AgNO3以离子形态存在于溶液中,主要猝灭溶液中的电子,故而DMF影响较大.而作为自由基的捕获剂,TBA与BQ只对自由基产生猝灭,由其结果的差异可以推出,在催化反应过程中,羟基和溶液中的水分子被激发产生的· OH对于降解反应的作用大于氧分子被激发产生的O- · 2的作用.总体来说,空穴、电子、· OH和O- · 2都是影响光催化效率的活性物种.
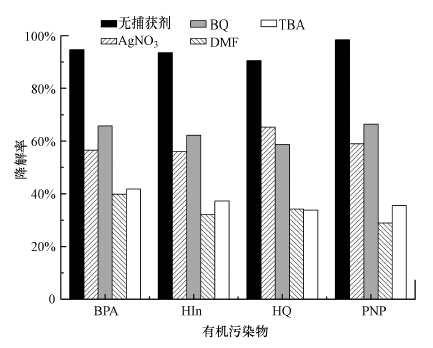 |
| 图 8 捕获剂(1 mmol · L-1)对有机污染物降解率的影响 Fig. 8 Effect of capture agents on the degradation ratio |
图 9为降解产物的实验跟踪结果,以BPA和PNP为例,记录降解过程中溶液的紫外吸收光谱.其中,曲线a、b、c分别代表降解前、降解1 h及降解5 h后的溶液.
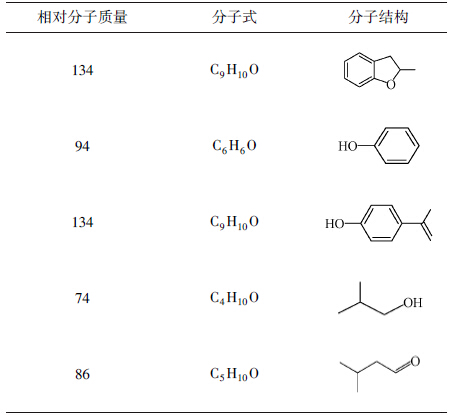
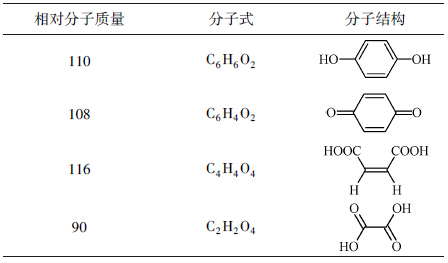
紫外吸收光谱的结果表明,在降解过程中,有机污染物的特征吸收峰逐渐消失,且没有产生新的吸收峰,近紫外区的吸光度逐渐趋于零.说明溶液中的有机污染物逐渐被降解为小分子饱和烷烃、CO2和H2O.为了进一步研究有机物的降解历程,利用GC-MS对BPA和PNP进行中间产物的分析,结果见表 1和表 2.
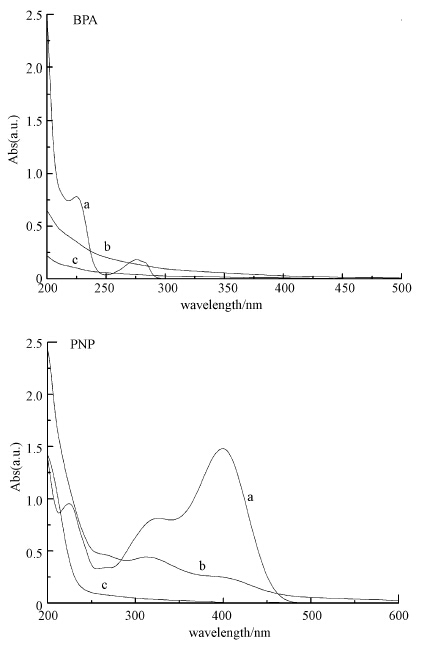 |
| 图 9 BPA和PNP降解过程的紫外吸收光谱 Fig. 9 UV-Vis spectra of BPA and PNP during degradation |
| 表 1 BPA光催化降解中间产物 Table 1 Intermediate products of BPA photocatalytic degradation |
| 表 2 BPA光催化降解中间产物 Table 2 Intermediate products of BPA photocatalytic degradation |
由此推断,BPA和PNP的降解历程分别为:
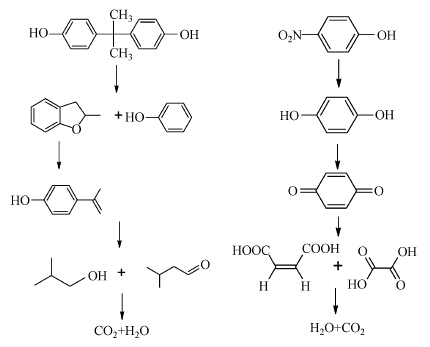
通过外加磁场将使用过的催化剂与溶液分离,经醇洗、水洗后干燥.在相同条件下重复光催化降解反应,结果证明,经过5次使用后,降解率下降约为7%(图 10).说明固载后能有效减少因卟啉团聚带来的催化性能下降,同时,磁性载体的负载使催化剂容易回收重复使用,大大降低了工业废水的处理成本.
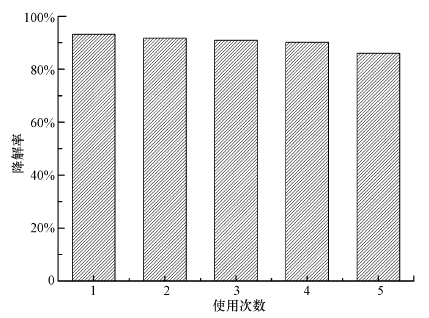 |
| 图 10 催化剂重复使用次数对降解率的影响 Fig. 10 Effect of cycling runs on degradation |
以经济、易得的天然血红素为原料,经改性制备的磁负载硝基锌卟啉催化剂在氙灯模拟太阳光下对双酚A、甲基橙、对苯二酚及对硝基苯酚均有高于90%的降解效果,对于活性红工业废水的降解也取得了较好的效果;通过对其降解机理的研究,证实在催化反应过程中的活性物种是空穴、电子、· OH和O- · 2,其中,空穴和· OH起主要作用;UV-Vis光谱跟踪显示光催化降解产物为小分子饱和烷烃、CO2和H2O,使有机污染物部分矿化.
| [1] | Bonnett R,Stephenson G F.1965.The meso reactivity of porphyrins and related compounds.I.Nitration[J].The Journal of Organic Chemistry,30(8):2791-2798 |
| [2] | 董永春,王秋芳,顿咪娜,等.2007.不同结构偶氮染料在TiO2纳米颗粒表面的吸附和光催化降解[J].过程工程学报,7(4):668-673 |
| [3] | Fang H,Kambala VS R,Srinivasan M,et al.2009.Tailored titanium dioxide photocatalysts for the degradation of organic dyes in wastewater treatment:A review[J].Applied Catalysis A:General,359(1/2):25-40 |
| [4] | 高德,郑国栋,杨国星,等.1994.几种卟啉及其配合物合成方法的改进[J].有机化学,14(3):310-313 |
| [5] | Gokakakar S D,Saler A V.2009.Solar assisted photocatalytic degradation of methyl orange over synthesized copper,silver and tin metalloporphyrins[J].Indian Journal of Chemical Technology,16(6):492-498 |
| [6] | Guo C C,Chu M F,Liu Q,et al.2003.Effective catalysis of simple metalloporphyrins for cyclohexane oxidation with air in the absence of additives and solvents[J].Applied Catalysis A:General,246(2):303-309 |
| [7] | Littler B J,Ciringh Y,Lindsey J S.2009.Investigation of conditions giving minimal scrambling in the synthesis of trans-porphyrins from dipyrromethanes and aldehydes[J].The Journal of Organic Chemistry,64(8):2864-2872 |
| [8] | Mao Y,Zhou J P,Cai J,et al.2006.Effects of coagulants on porous structure of membranes prepared from cellulose in NaOH/urea aqueous solution[J].Journal of Membrane Science,279(1/2):246-255 |
| [9] | Nada A M A,Yousef H A,El-Gohary S.2002.Thermal degradation of hydrolyzed and oxidized lignins[J].Journal of Thermal Analysis and Calorimetry,68(1):265-273 |
| [10] | 王兰芝,佘远斌,徐未未,等.2005.金属卟啉类模拟酶催化剂研究[J].化学进展,17(4):678-685 |
| [11] | 王兰芝,佘远斌.2008.取代金属(铁、锰、钴、铜、锌)卟啉的光谱分析[J].光谱学与光谱分析,28(10):2312-2317 |
| [12] | 王攀,罗光富,曹婷婷,等.2011.金属卟啉类化合物特性及光催化机理与应用研究[J].三峡大学学报(自然科学版),33(5):84-92 |
| [13] | 吴景悦,刘欣阳,李乃瑄.2014.双配体仿酶催化剂的制备及其光催化降解水中对苯二酚[J].应用化学,31(4):417-423 |
| [14] | 徐锐,王君,杨琦,等.2009.氯化血红素脱铁新工艺的研究[J].当代化工,31(3):128-131 |
| [15] | 闫绍轩,王何园,靳松,等.2012.磁微球负载氯化血红素仿酶催化剂制备及催化降解DMP[J].分子催化,26(6):560-565 |
| [16] | Yang Z H,Yan S X,Zhang Z Y,et al.2014.Photocatalytic degradation of bisphenol A in water using A visible light-activated biomimetic catalyst[J].Fresenius Environmental Bulletin,23(2):523-530 |
 2015, Vol. 35
2015, Vol. 35