多环芳烃(Polycyclic Aromatic Hydrocarbons,PAHs)是一类广泛存在于环境中的有机污染物(Bostrm et al.,2002).近年来,随着经济的增长、城镇化的推进和能源需求量的增大,大量的PAHs释放到自然环境中.我国水环境中PAHs污染状况较为严重,水体和沉积物中均有不同含量的PAHs检出.据报道,在我国的天津和大亚湾地区,地表水中PAHs的含量分别为1765~35210 ng · L-1和4228~29325 ng · L-1(Zhou et al.,2003; Cao et al.,2005).研究表明,在长江武汉段的水中总PAHs的最大浓度为6.235 μg · L-1(Feng et al.,2007),而在三峡地区重庆段河流中检测到的总PAHs最大浓度为1.477 μg · L-1(郭志顺,2006).由于PAHs在环境中的广泛存在及对人体健康存在的潜在危险,该类化合物已受到广泛关注.
越来越多的证据表明,PAHs具有抗雌激素活性,可严重影响哺乳动物的繁殖(Borman et al.,2000; Zenzes,2000; Archibong et al.,2012).有研究表明,PAHs暴露可显著降低雄性大鼠睾酮的水平和精子活力(Inyang et al.,2003).此外,PAHs对水生生物也产生一定的毒理学效应.如暴露后,会引起鱼类产卵量降低,卵巢发育受损和性激素水平下降,从而表现出一定的生殖毒性(Hoffmann et al.,2006; Zheng et al.,2006).
尽管先前的研究已报道我国水体,包括长江中PAHs的含量(Feng et al.,2007; Cui et al.,2009),但有关其环境风险的研究仍然较少,尤其是对长江上游濒临灭绝的、珍稀特有鱼类的风险评估更是非常有限.三峡大坝位于长江中游,自2009年蓄水以来,长江上游库区水体中污染物的含量很可能会增加(Wu et al.,2004).先前的研究表明,PAHs是三峡库区中除邻苯二甲酸酯之外的主要污染物,总含量在0.23~0.99 μg · L-1的范围内(Cui et al.,2009).然而目前还缺乏对三峡库区PAHs对长江上游库区鱼类的潜在环境风险研究.
稀有鮈鲫(Gobiocypris rarus)是我国的特有模式鱼类,被广泛用来评价各种化学品潜在的内分泌干扰效应(Zha et al.,2008; 曹文宣等,2003).该鱼分布于长江上游的水域中,具有个体小、易饲养、繁殖周期短、实验条件下可周年产卵、胚胎透明等特点.在鱼类中,下丘脑-垂体-性腺轴(hypothalamic-pituitary-gonadal axis,HPG)对内分泌干扰物的影响非常敏感,同时,也可用来揭示污染物作用的潜在分子机制(Ankley et al.,2007).
因此,本研究选择苯并芘(BaP)为PAHs中的代表性污染物,检测不同浓度的BaP暴露后,稀有鮈鲫血清中性激素水平,以及HPG轴相关基因和肝脏中卵黄蛋白原(Vitellogenin,VTG)、雌激素受体(Estrogen receptors,ERs)基因的转录水平.以评价PAHs对稀有鮈鲫潜在的内分泌干扰效应,为预测PAHs对长江上游鱼类的潜在影响提供科学依据.
2 材料与方法(Materials and methods) 2.1 材料与试剂苯并芘(BaP,CAS:50-32-8)购自美国AccuSt and ard公司,助溶剂为二甲基亚砜(DMSO),购自美国Amresco公司.RNA提取试剂(RNAiso Plus reagent)和逆转录试剂盒(PrimerScript RTreagent Kit)为Takara(中国)生产.荧光定量试剂盒(SYBR Green PCR Kit)购自日本Toyobo公司.睾酮和雌二醇酶联免疫试剂盒(Testosterone EIA Kit和Estradiol EIA Kit)购自美国Cayman公司.其他所有试剂均为分析纯.
2.2 稀有鮈鲫的饲养和暴露实验将稀有鮈鲫以16 h/8 h的光暗周期饲养在经活性炭过滤且充分曝气的自来水中,水温保持在(25±1)℃,饲养期间每天投喂饲料2次,小颗粒商品饵料和刚孵化的丰年虫幼虫.暴露实验开始前,性成熟的稀有鮈鲫(7月龄)以半静态条件在盛20 L水的缸中驯养两周.每个缸中放置8条雌鱼和8条雄鱼,每天清除多余饵料和排泄物.适应期后,稀有鮈鲫暴露于0、0.1、0.3、1.0、3.0 μg · L-1 的BaP暴露液中28 d.暴露结束前一天下午停止喂食,使实验鱼空腹.暴露组和溶剂对照组中DMSO的终浓度为0.001%(体积比).每个浓度包括3个平行缸,暴露期间每天更换1/2的暴露液.28 d后,用0.03%的MS-222将鱼麻醉,并用滤纸吸干,称量并记录体长和体重,断尾取血用于激素测定.准确分离脑、肝脏和性腺并称重,于液氮中瞬间冷冻,保存于-80 ℃中待测.各形态学指标的计算方法如下:
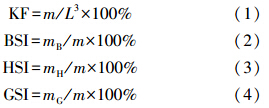
式中,KF为条件因子,m为体重(g),L为体长(cm),BSI为脑指数,mB为脑质量(g),HSI为肝脏指数,mH为肝脏质量(g),GSI为性腺指数,mG为性腺质量(g).
2.3 性激素的抽提与测定暴露结束后,MS-222(0.03%)麻醉实验鱼,断尾取血.每两尾鱼的血混合在一起作为一个平行样,每个浓度雌雄鱼各4个平行样.于4 ℃、7000 r · min-1下离心5 min后,取上清(10 μL)用于性激素的检测.激素抽提方法参照文献(Wang et al.,2013).每个样品(10 μL血清)中加入390 μL Milli-Q水,涡旋混匀,加入2 mL乙醚,混匀器混匀后于4 ℃、5000 r · min-1下离心10 min,取上清,再用2 mL乙醚按照上述方法抽提一次,将两次抽提上清收集于一个洁净离心管,氮气吹干后保存于-80 ℃.所得样品用试剂盒中120 μL EIA buffer溶解,按照Cayman Chemical Company 公司的睾酮和雌二醇试剂盒说明书测量激素含量,睾酮的检测限为6 pg · mL-1,雌二醇的检测限为19 pg · mL-1.
2.4 荧光定量PCR雌雄鱼各不同组织总RNA提取、纯化、定量及cDNA合成法参照Wang等(2013)的方法.为避免基因组DNA的可能污染,初提取物的总RNA用无RNase的DNase I进行消化并纯化.用分光光度计测定样品在260 nm和280 nm下的吸光值,同时用1%的琼脂糖凝胶电泳进一步检测RNA的纯度.取1 μg总RNA进行反转录得到cDNA,用SYBR Green I染料法对目标基因进行定量检测(ABI 7300,Applied Biosystem,USA).反应体系均为20 μL,其中包括SYBR Green PCR master mix(Toyobo,Japan)10 μL、ROX 0.4 μL、5 μmol · L-1正义和反义引物各0.5 μL及cDNA 1 μL和ddH2O.实时定量PCR程序为:95 ℃预变性10 min;95 ℃变性30 s,58 ℃复性20 s,72 ℃延伸1 min,40个循环.内参基因选择β-actin,内参及目标基因引物见表 1.所有样品的定量检测至少重复3次,每次3个平行.以delta-delta Ct法计算目标基因mRNA的相对表达量.
| 表 1 实时荧光定量PCR基因引物 Table 1 Primer sequences for the quantitative real-time polymerase chain reaction assays used in this study |
所有数据都用平均值±标准误(SEM)表示.通过Kolmogorov-Smirnov方法检测数据的正态性,通过Levene′s检验方法分析数据的方差同质性.数据满足方差同质性,使用SPSS 13.0软件(SPSS,Chicago,IL,USA)通过Dunnett′s检验对数据进行单因素方差分析,当p<0.05时,即表示有显著性差异.
3 结果(Results) 3.1 形态学指标的变化稀有鮈鲫的形态学指标变化见表 2.28 d的BaP暴露并未引起条件因子和性腺指数的显著性改变,但抑制了稀有鮈鲫的生长(体长和体重)(p<0.05).与对照组相比,3.0 μg · L-1的BaP暴露显著升高了雌雄鱼的脑指数和雄鱼的肝脏指数(p<0.05).
| 表 2 稀有鮈鲫暴露于不同浓度的BaP中28 d后体质系数的变化 Table 2 Somatic indices of rare minnow after exposure to BaP(0、0.1、0.3、1.0、3.0 μg · L-1)for 28 d |
BaP暴露显著改变了稀有鮈鲫体内性激素的水平并干扰了雌鱼体内性激素的平衡(图 1).3.0 μg · L-1 BaP暴露组的稀有鮈鲫,其雄鱼体内血浆中睾酮的水平显著降低,和对照组相比较下降了46.9%;然而在雌鱼体内,3.0 μg · L-1 BaP暴露组,血浆中睾酮的含量则显著升高1.62倍(图 1a).暴露于3.0 μg · L-1 BaP的稀有鮈鲫,雌雄鱼体内的雌二醇水平都显著下降,与对照组相比,分别下降了43.7%和35.1%,其他低浓度处理组则没有影响(图 1b).T/E2是性激素异常的敏感指示指标,BaP暴露对雄鱼体内T/E2比值并无影响,但3.0 μg · L-1的BaP引起了雌鱼体内T/E2的增加(3.21倍)(图 1c).
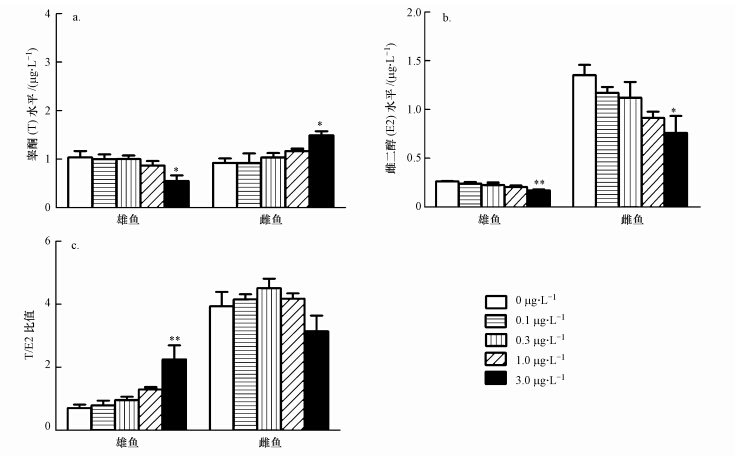 |
| 图 1 稀有鮈鲫成鱼暴露于不同浓度BaP 28 d血浆中睾酮(T)(a)、雌二醇(b)(E2)水平和T/E2比例(c)的变化 Fig. 1 Effects on serum testosterone(T)(a),17β-estradiol(E2)levels(b) and T/E2 ratio(c)in rare minnows after exposure to 0、0.1、0.3、1.0 and 3.0 μg · L-1 of BaP for 28 d |
基因表达结果表明,BaP暴露影响了雌雄鱼HPG轴和肝脏中相关基因的表达.与对照组相比,雌雄鱼Cyp19b的表达在最高剂量组显著下调.在雄鱼中,BaP暴露对性腺中Cyp19a的表达量没有影响,但却显著上调了Cyp17的表达,在0.3、1.0和3.0 μg · L-1 BaP暴露组分别上调了2.97、4.62和6.92倍,并呈现出剂量-效应关系(表 3).在雌鱼中,1.0和3.0 μg · L-1 BaP暴露组,Cyp19a的表达量分别上调了1.82和2.73倍(表 3).
在雄鱼肝脏中,VTG表达量在3.0 μg · L-1暴露组显著下调2.56倍,而对雌鱼,1.0和3.0 μg · L-1 BaP暴露则抑制了肝脏VTG的表达(1.58和2.24倍)(表 3).BaP暴露对雌雄鱼肝脏内ERβ均无显著影响,但却抑制了ERα的表达.雌鱼ERα在最高剂量组(3.0 μg · L-1 BaP)下调了1.35倍.对于雄鱼,BaP暴露显著抑制了ERα的表达,在0.3、1.0和3.0 μg · L-1 BaP分别下调了1.56、3.12和3.23倍(表 3).
| 表 3 稀有鮈鲫暴露不同浓度的BaP下28天HPG轴及肝脏中相关基因的表达水平 Table 3 Gene transcription profiles in Chinese rare minnow after exposure to 0,0.1,0.3,1.0,and 3.0 μg · L-1 of BaP for 28 d |
本实验选用稀有鮈鲫来评价BaP的内分泌干扰效应,通过对鱼体内激素水平、HPG轴及肝脏中相关基因定量表达的测定,结果表明,激素含量和基因表达的改变主要发生在较高的暴露剂量(3.0 μg · L-1),而在环境相关剂量的BaP暴露下,并未影响激素含量和基因表达,因此,并没有明显的内分泌干扰效应.
性激素水平的变化是评价生殖内分泌干扰效应的重要指标.本研究中,28 d的BaP暴露导致雌、雄鱼体内雌二醇和睾酮的显著改变.具体表现为:在雌、雄鱼体内,雌二醇的含量显著下降,并呈现出一定的剂量-效应关系;在雄鱼中,睾酮的含量显著下降,但在雌鱼中,与对照组相比睾酮的含量却显著升高,且这些改变都发生在最高的暴露浓度(3.0 μg · L-1).BaP暴露导致性激素水平的改变同样在其他鱼类中观察到,例如,石首鱼经腹腔注射BaP后,其血浆中睾酮和雌二醇的水平显著受到抑制(Thomas,1988).10 μg · L-1的BaP暴露成年底鳉(Fundulus heteroclitus)28 d,明显降低了雄鱼体内睾酮的水平和雌鱼体内雌二醇的水平,破坏了性激素的平衡(Booc et al.,2014).短时间(96 h)更高浓度的BaP(100 μg · L-1)暴露同样引起青鳉血浆中雌二醇水平的降低(Kim et al.,2014).而本实验,我们发现暴露在3.0 μg · L-1的剂量下,即可改变性激素含量,说明与其他鱼类相比,稀有鮈鲫对于BaP的影响较为敏感,因此,可成为评价BaP引起的内分泌干扰效应的良好模式鱼类.
在类固醇激素合成过程中,一系列酶类如Cyp17、3β-HSD、17β-HSD和Cyp19发挥重要作用,因而编码这些酶类的基因表达的改变可能与血浆中类固醇激素(如睾酮和雌二醇)的水平有关(Omura et al.,1995).为了探讨BaP对稀有鮈鲫造成内分泌干扰效应的可能机制,本研究检测了HPG轴及肝脏中与性激素合成相关的关键基因的表达水平.结果表明,雌雄鱼脑中Cyp19b基因表达在3.0 μg · L-1 BaP暴露组显著受到抑制,而Cyp19b基因编码的芳香化酶催化雄激素(睾酮)转化为雌激素(雌二醇),因此,抑制该基因的表达,可能抑制由睾酮向雌二醇的转化,导致血浆中雌二醇水平下降.在斑马鱼幼鱼中,BaP显著抑制E2诱导的Cyp19b 基因表达(Cheshenko et al.,2007),同样,Dong等(2008)研究表明,10 μg · L-1 BaP暴露显著抑制成年底鳉下丘脑和垂体中Cyp19b的基因表达.因此,我们推测BaP暴露导致血浆中E2水平的下降可能与Cyp19b基因表达受到抑制有关.然而,在雌鱼卵巢中,Cyp19a基因表达量显著上调,这种上调可能是机体对雌二醇水平下降的一种补偿机制.Cyp17基因编码的蛋白在类固醇合成途径中催化脱氢表雄酮和雄烯二酮的合成,为睾酮的合成提供前体(Hanukoglu,1992).在稀有鮈鲫雄鱼的精巢中,Cyp17基因表达量的显著上调,这种上调可能与雄鱼血浆中性激素水平的降低有关.然而,5.5 μg · L-1的BaP暴露斑马鱼56 d后,Cyp17表达无明显变化(Hoffmann et al.,2006),这可能是因为在不同的浓度和暴露时间下,不同鱼类对同一污染物有着不同的响应.
在鱼类中,卵黄蛋白原(VTG)是卵子发生,卵子成熟及卵黄合成中必不可少的营养物质,是雌激素效应敏感的生物标志物,其基因的表达受雌激素调控.体外研究表明,BaP可显著抑制鲫鱼肝细胞中己烯雌酚诱导的VTG蛋白和mRNA 的表达,呈明显的抗雌激素效应(梁勇等,2004).在本研究中,雌、雄稀有鮈鲫肝脏中VTG转录水平受到抑制,同样表明BaP对稀有鮈鲫产生了抗雌激素效应,与先前的报道一致.研究结果表明,VTG的生成是通过ERα来介导的(Marlatt et al.,2008).在本研究中,我们同样观察到雌、雄鱼肝脏中ERα表达不同程度的下降.结合以上结果,我们推测BaP暴露引起的雌二醇水平的下降引发了肝脏中ERα表达量的降低,进而导致了VTG表达的下降,该结果从另一方面反映出了BaP的抗雌激素效应.而BaP暴露引起雌二醇水平下降的可能机制是BaP激活了细胞内P4501A 酶系统,从而促进了雌激素的代谢.
5 结论(Conclusions)较高剂量BaP暴露显著改变了血浆中性激素的水平,同时引起HPG轴及肝脏中与类固醇激素合成相关关键基因表达的改变.而低剂量暴露并没有引起激素或者基因表达的改变,因此,我们可以推测,长江上游水体中BaP单独存在下并不会对三峡库区上游水体区域的鱼类产生内分泌干扰效应及繁殖毒性.考虑到长江上游水体中共同存在着BaP与其他有毒物质,因而需要长期的环境监测和进一步的研究来探讨有毒物质共存条件下对长江上游珍稀鱼类的影响.
| [1] | Ankley G T, Jensen K M, Kahl M D, et al. 2007. Ketoconazole in the fathead minnow (Pimephales promelas): Reproductive toxicity and biological compensation [J]. Environmental Toxicology and Chemistry, 26(6): 1214-1223 |
| [2] | Archibong A E, Ramesh A, Inyang F, et al. 2012. Endocrine disruptive actions of inhaled benzo(a)pyrene on ovarian function and fetal survival in fisher F-344 adult rats [J]. Reproductive Toxicology, 34(4): 635-643 |
| [3] | Booc F, Thornton C, Lister A, et al. 2014. Benzo pyrene effects on reproductive endpoints in Fundulus heteroclitus [J]. Toxicological Sciences, 140(1): 73-82 |
| [4] | Borman S M, Christian P J, Sipes I G, et al. 2000. Ovotoxicity in female Fischer rats and B6 mice induced by low-dose exposure to three polycyclic aromatic hydrocarbons: comparison through calculation of an ovotoxic index [J]. Toxicology and Applied Pharmacology, 167(3): 191-198 |
| [5] | Boström C E, Gerde P, Hanberg A, et al. 2002. Cancer risk assessment, indicators, and guidelines for polycyclic aromatic hydrocarbons in the ambient air [J]. Environmental Health Perspectives, 110(Suppl 3): 451-488 |
| [6] | 曹文宣,王剑伟.2003.稀有鮈鲫—一种新的鱼类实验动物[J]. 实验动物科学与管理, 20(S1): 96-99 |
| [7] | Cao Z H, Wang Y Q, Ma Y M, et al. 2005. Occurrence and distribution of polycyclic aromatic hydrocarbons in reclaimed water and surface water of Tianjin, China [J]. Journal of Hazardous Materials, 122(1/2): 51-59 |
| [8] | Cheshenko K, Brion F, Page Y L, et al. 2007. Expression of zebra fish aromatase cyp19a and cyp19b genes in response to the ligands of estrogen receptor and aryl hydrocarbon receptor [J]. Toxicological Sciences, 96(2): 255-267 |
| [9] | Cui Z H, Liu J Y, Li P, et al. 2009. Biomonitoring of detoxifying activity as measured by CYP1A1 induction in Yangtze and Jialing Rivers in Chongqing city in China [J]. Journal of Toxicology and Environmental Health (Part A: Current Issues), 72 (11/12): 782-788 |
| [10] | Dong W, Wang L, Thornton C, et al. 2008. Benzo(a)pyrene decreases brain and ovarian aromatase mRNA expression in Fundulus heteroclitus [J]. Aquatic Toxicology, 88(4): 289-300 |
| [11] | Feng C L, Xia X H, Shen Z Y, et al. 2007. Distribution and sources of polycyclic aromatic hydrocarbons in Wuhan section of the Yangtze River, China [J]. Environmental Monitoring and Assessment, 133(1/3): 447-458 |
| [12] | 郭志顺, 罗财红, 张卫东, 等. 2006. 三峡重庆库区PAHs污染研究[J]. 四川大学学报, 43(6): 1337-1340 |
| [13] | Hanukoglu I, 1992. Steroidogenic enzymes: structure, function, and role in regulation of steroid hormone biosynthesis [J]. The Journal of Steroid Biochemistry and Molecular Biology, 43(8): 779-804 |
| [14] | Hoffmann J L, Oris J T. 2006. Altered gene expression: a mechanism for reproductive toxicity in zebrafish exposed to benzo pyrene [J]. Aquatic Toxicology, 78(4): 332-340 |
| [15] | Inyang F, Ramesh A, Kopsombut P, et al. 2003. Disruption of testicular steroidogenesis and epididymal function by inhaled benzo(a)pyrene [J]. Reproductive Toxicology, 17(5): 527-537 |
| [16] | Kim B -M, Rhee J -S, Jeong C -B, et al. 2014. Effects of benzo pyrene on whole cytochrome P450-involved molecular responses in the marine medaka Oryzias melastigma [J]. Aquatic Toxicology, 152: 232-243 |
| [17] | 梁勇, 黄港住, 徐盈, 等. 2004. 2, 3, 7, 8-四氯代二苯并二英(TCDD)和苯并芘(B P)对原代培养鲫鱼肝细胞中卵黄蛋白原诱导的影响[J].科学通报, 49(16): 1605-1610 |
| [18] | Marlatt V L, Martyniuk C J, Zhang D, et al. 2008. Auto-regulation of estrogen receptor subtypes and gene expression profiling of 17β-estradiol action in the neuroendocrine axis of male goldfish [J]. Molecular and Cellular Endocrinology, 283(1/2): 38-48 |
| [19] | Omura T, Morohashi K. 1995. Gene regulation of steroidogenesis [J]. The Journal of Steroid Biochemistry and Molecular Biology, 53(1/6): 19-25 |
| [20] | Thomas P. 1988. Reproductive endocrine function in female Atlantic croaker exposed to pollutants [J]. Marine Environmental Research, 24(1/4): 179-184 |
| [21] | Wang X F, Yang Y J, Zhang L P, et al. 2013. Endocrine disruption by di-(2-ethylhexyl)-phthalate in Chinese rare minnow (Gobiocypris rarus) [J]. Environmental Toxicology and Chemistry, 32(8): 1846-1854 |
| [22] | Wu J G, Huang J H, Han X G, et al. 2004. The Three Gorges Dam: an ecological perspective [J]. Frontiers in Ecology and the Environment, 2(5): 241-248 |
| [23] | Zenzes M T. 2000. Smoking and reproduction: gene damage to human gametes and embryos [J]. Human Reproduction Update, 6(2): 122-131 |
| [24] | Zha J M, Sun L W, Zhou Y Q, et al. 2008. Assessment of 17α-ethinylestradiol effects and underlying mechanisms in a continuous, multigeneration exposure of the Chinese rare minnow (Gobiocypris rarus) [J]. Toxicology and Applied Pharmacology, 226(3): 298-308 |
| [25] | Zheng R H, Wang C G, Zuo Z H, et al. 2006. Combined effect of tributyltin and benzo pyrene on the levels of sex hormone and vitellogenin in female Sebastiscus marmoratus [J]. Journal of Environmental Sciences, 18(2): 359-363 |
| [26] | Zhou J L, Maskaoui K. 2003. Distribution of polycyclic aromatic hydrocarbons in water and surface sediments from Daya Bay, China [J]. Environmental Pollution, 121(2): 269-281 |
 2015, Vol. 35
2015, Vol. 35


