2. 华南理工大学化学与化工学院, 广州 510006
2. School of Chemistry and Chemical Engineering, South China University of Technology, Guangzhou 510006
光催化技术是一种在能源和环境领域有着重要应用前景的“绿色”技术,而光催化材料是此技术的核心,常见的半导体材料有TiO2(Fujishima et al., 1972;Khan et al., 2002;Roy et al., 2011)、WO3(Su et al., 2010;Su et al., 2011)、ZnO(Ko et al., 2011)和CdS(Peng et al., 2001;Wang et al., 2010)等.由于TiO2具有化学性质稳定、无毒、成本低、可在常温常压下进行催化反应且不产生二次污染等优点,因而被广泛研究.TiO2纳米管具有较大的比表面积、孔体积,可以迅速传导电子,有效抑制电子空穴的结合率,从而表现出更高的光催化性能和光电转化效率.但TiO2 作为一种宽带半导体(锐钛矿型,带隙能Eg=3.2 eV),只有在波长小于387 nm的紫外区下才能激发其催化活性,这一波段的光占整个太阳光光谱尚不足5%,但可以通过复合或掺杂其它元素扩大其光谱响应范围,进而提高其光催化性能和光电转化效率.Asahi等(2001)证明在N、C、S、P、F这几种非金属元素中,N最能提高TiO2在可见光区的催化活性,因为N 2p态与O 2p态混合,可以使带隙变窄.在N掺杂的基础上,多元素的共掺杂(如N-F(Pelaez et al., 2009)、N-S(Parida et al., 2010)、C-N(Wang et al., 2011;Dai et al., 2012)等比单元素掺杂更能提高TiO2在可见光区的响应.除了提高TiO2在可见光区的催化活性外,也可以运用PEC(光电化学)的方法,降低光生电子和空穴的复合率,从而提高光电转化效率,PEC体系已经被广泛地运用在如下几个方面:太阳能电池(Nakade et al., 2005;Peng et al., 2013)、产氢(Wolcott et al., 2009; van de Krol et al., 2011)、二氧化碳还原(Cole et al., 2010;Peng et al., 2013)、去除水体污染物(Zhao et al., 2006; Zhang et al., 2007)等.
面对日益严峻的能源和环境问题,本研究拟利用PEC方法,以实现同时水解产氢和降解甲基橙.氢气是一种清洁能源,具有燃烧热值高、资源丰富和无二次污染等优点,自从1972年Fujishima发现TiO2半导体电极进行光电化学反应可使水分子分解为氧气及氢气的现象以来(Fujishima et al., 1972),应用不同材料进行光电化学分解水产氢的研究成为全世界关注的焦点.在光电化学产氢系统内,光电转化效率及光电极的稳定性是产氢的关键点,而TiO2具有良好的光电转化效率、化学及光学稳定性高等特点,是一种最常被应用在光电化学产氢研究的材料.甲基橙是纺织染料中的代表性污染物之一,由于印染废水具有水量大、色度高、成分复杂、可生化性差等特点,一直是废水处理的难点.染料分子中大量苯环的存在和现在染料的良好稳定性,使得传统的生物方法在脱色和降解方面的效果并不显著(Hachem et al., 2001).因此,本研究应用阳极氧化法和超声辅助沉积法合成碳氮共掺杂二氧化钛纳米管阵列(C,N-TNAs),并将FESEM、XRD、XPS、UV-vis用于C,N-TNAs理化性质、结构特征、光学特性的表征测试.同时,在PEC体系中,C,N-TNAs作为工作电极,Pt片和SCE(Saturated Calomel Electrode,饱和甘汞电极)分别作为辅助和参比电极,以甲基橙作为目标污染物测试C,N-TNAs的催化氧化性能,并在不同的pH条件下对甲基橙催化降解效率进行探讨,在阴极部分,用气相色谱测量其产氢量.最后,提出在PEC体系中C,N-TNAs实现同时氧化甲基橙和产氢的机理.
2 材料与方法(Materials and methods) 2.1 实验材料氟化氢(HF)、甲基橙(Methyl Orange,MO)购于Sigma-Aldrich公司,Ti foils(厚0.25 mm,纯度99.5%)购于Fisher公司,氢氧化钠(NaOH)、硫酸(H2SO4)购自成都科龙化工试剂厂,以上试剂为分析纯,去离子水由华南理工大学自制.
2.2 C,N-TNAs电极的制备将裁剪好的钛片按顺序分别放入蒸馏水、丙酮、蒸馏水中超声清洗,清洗时间为15 min,最后置于空气中干燥.制备时采用量程为0~60 V 的可调式直流稳压稳流电源(ITECH,IT6720,0~5 A,0~60 V),钛片作为阳极,铂片作为阴极,以质量分数0.25%的 HF作电解液于室温、20 V电压下恒电位阳极氧化30 min,取出样品立即用大量去离子水冲洗,干燥待用.将上述制备好的样品置于20 mg · L-1的尿素中,超声辅助沉积后放置一段时间,取出后置于马弗炉中,450 ℃煅烧180 min,得到碳氮共掺杂二氧化钛纳米管阵列(C,N-TNAs);再用导电银胶等把铜线和C,N-TNAs粘连,得到C,N-TNAs电极.
与此同时,将清洗、阳极氧化后的材料在450 ℃下煅烧180 min,得到锐钛矿的二氧化钛纳米管阵列,再用导电银胶等把铜线TNAs粘连,得到TNAs电极,作为对照实验.
2.3 材料表征C,N-TNAs和TNAs样品的表面形态采用FESEM(Nova NanoSEM 430 FEI,USA)进行分析,晶相采用X-射线衍射仪(XRD,Rigaku D/max-2500)检测,以Cu Kα为放射源(λ=0.15418 nm),其操作条件为:40 kV,100 mA,30 MPa,扫描速度2° · min-1,扫描范围1°~10°,衍射数据记录时间间隔(步长)为0.01° ·步-1.光吸收特性采用UV-vis(UV2401/2,Shimadu,Japan)分析,表面元素性质采用XPS(PHI-1600型电子能谱仪)分析,以MgKα(1253.6 eV)作为激发光源,功率为300 W,以C1s(284.98 eV)作为校正电荷.
2.4 甲基橙的光电催化降解在PEC体系中,以C,N-TNAs、Pt片和SCE分别为工作、辅助和参比电极,光源采用100 W低压 汞灯,汞灯置于石英冷阱中,两层管壁间接入循环冷却水,以保证过程中温度的基本稳定.在自制的H型反应器(图 1)内加入 300 mL的甲基橙(5 mg · L-1)溶液及0.1 mol · L-1的NaCl溶液作为电解液.整个反应中,每10 min采样1次,将所采的样过滤后进行吸光度测试,以紫外可见分光光度计(Shimadzu,UV-1750)分析降解效果.
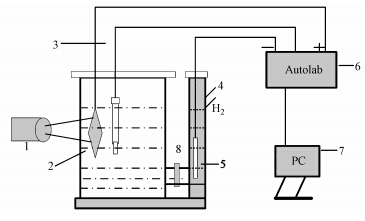 |
| 图 1 三电极体系示意图(1.灯源:低压汞灯,2.工作电极:TNAs,3.参比电极:SCE,4.气体出口,5.铂电极,6.电化学工作站:Autolab,7.PC控制终端,8.阳离子交换膜) Fig. 1 Schematic diagram of photoelectrochemical experiment system(1.Light source: Hg lamp; 2. Worting electrode: TNAs; 3. Reference electrode: SCE; 4. Gas coutlet; 5. Counter eletrode: Pt; 6. Electrode chemical working station: Autolab; 7. PC controhler; 8. Anion exchange membrame) |
用气相色谱(Agilent 7820A)检测氢气的含量,色谱条件:5A分子筛为色谱柱,氮气为载气,TCD为检测器.
3 结果与讨论(Results and discussion) 3.1 材料表征图 2为经表面预处理的钛板在w(HF)=0.25%的水溶液中,控制电压20 V,阳极氧化30 mim后,制得的TiO2纳米管阵列膜的SEM 图.从图 2a可以看出,TiO2膜层表面呈现纳米管阵列排布,纳米管管径在100 nm左右;从侧面图(右上角子图)可以看出,TiO2纳米管管径尺寸基本一致,上端开口,底部封闭,膜层厚度(TiO2纳米管长度)为300~400 nm.TiO2膜层底部是一层薄而致密的阻挡层,从而构成纳米管阵列膜层/阻挡层/基体钛3层结构.从图 2b可以看出,表面C,N-TNAs膜具有不连续的纳米管状结构特征,管径约为90~100 nm,与未经尿素浸泡、直接热处理得到的未掺杂氮的TiO2纳米管阵列相比,两者的形貌相似,说明该纳米TiO2管状结构稳定,虽经尿素长时间浸泡也不会影响它的阵列结构.
 |
| 图 2 场发射扫描电镜图(a.TNAs,b.C,N-TNAs) Fig. 2 FESEM spectra of TNAs(a) and C,N-TNAs(b) |
TNAs和C,N-TNAs的XRD分析结果如图 3所示.由图可知,在2θ为20°~80°范围内出现了明显的(100)、(110)、(200)和(210)晶面的特征衍射峰,TNAs和C,N-TNAs的X 射线衍射图与标准卡JCPDS 2121272和JCPDS 2921360 对比可知,25.151°、37.199°、47.182°和54.108°处为锐钛矿的特征衍射峰,这正是TiO2锐钛矿相特征衍射峰.由此可见,TiO2纳米管中TiO2主要形态为锐钛矿型,在450 ℃煅烧的温度下,并没有出现金红石相.从图 3中还可知,该峰是相当的尖锐,可说明该材料的结晶度良好.同时,运用Scherrer公式计算得到TNAs和C,N-TNAs的晶粒尺寸分别为27.3 nm和32.3 nm,相对较小的晶粒尺寸表明锐钛矿相有更好的光催化活性(孙奉玉等,1998),这跟Wang等(2010)用溶液法合成C-N-TiO2的结果类似.
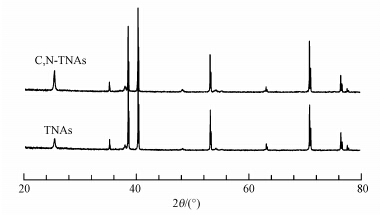 |
| 图 3 TNAs和C,N-TNAs X射线衍射图 Fig. 3 XRD patterns of TNAs and C,N-TNAs |
图 4显示的是C,N-TNAs和TNAs的紫外可见光谱图.从图中可见,无论纯TNAs电极或者复合TNAs 电极对紫外光都有吸收.经过掺杂之后,相对于未掺杂的电极在紫外区域的吸收明显增强.与纯 TiO2纳米管相比,掺杂纳米管在 200~400 nm 波长处出现了一个吸收平台,这表明复合纳米管可以被部分可见光激发,从而获得更高的光电转化效率.此外,通过如下Tauc公式(公式(1)、(2)),可以作图计算出C,N-TNAs和TNAs的带隙分别为2.7 eV和3.2 eV,通过碳氮的掺杂,可以明显提高TNAs在可见光部分的光活性,从而增强其光催化活性.
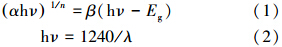
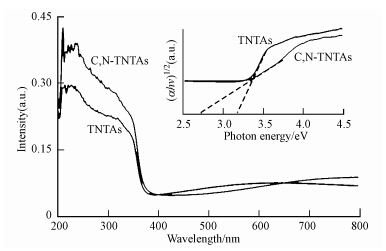 |
| 图 4 TNAs和C,N-TNAs紫外可见光谱图 Fig. 4 UV-vis spectra of TNAs and C,N-TNAs |
C,N-TNAs的XPS表征结果包括Ti 2p、O 1s和N 1s,具体如图 5所示.从Ti 2p图可知,459.5 eV(Ti 2p3/2)和465.3 eV(Ti 2p1/2)处的峰表明Ti是以+4价态存在的,证明Ti被氧化成了+4价的形态,结合XRD分析可知,此形态为TiO2锐钛矿相.如N 1s 图所示,在400.2 eV处出现一个明显的峰,可以归因于Ti—O—N键,而在396.5 eV处出现的肩峰则是N—Ti—O 键(Ou et al., 2011),N1s的出现也证实了N元素已经成功地掺杂到TNAs的结构中,其中,N的质量分数为0.48%(表 1).本方法合成的C,N-TNAs呈现黄色,与其他学者(Irie et al., 2003;Peng et al., 2010;Ou et al., 2011)所做的研究相似,这有利于对可见光部分的吸收.此外,在O 1s图中在528.5~531.6 eV处出现的峰可能是O与Ti、C或者N键接所造成的;另外,在二氧化钛纳米管阵列的表面也可能形成碳酸盐物种(Chen et al., 2007).综合以上分析,碳和氮已经掺杂到了二氧化钛纳米管阵列中.
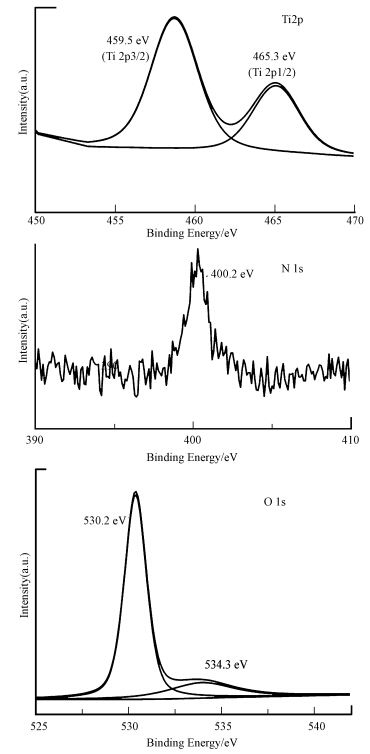 |
| 图 5 C,N-TNAs的XPS 谱图 Fig. 5 XPS spectra of C,N-TNAs |
| 表 1 C,N-TNAs的XPS分析的元素含量 Table 1 Element content results of XPS analysis for C,N-TNAs |
在不同pH值下,甲基橙的降解率如图 6所示,其中,甲基橙起始浓度为5 mg · L-1,以100 W低压汞灯作为光源.由图可知,开灯反应60 min后,甲基橙基本降解完全.pH=4时,光电催化氧化10 min后甲基橙的降解率就达到了91%,15 min时就基本降解完全,其速率常数达到了2.3×10-3 s-1,远大于pH=7(1.5×10-3 s-1)和pH=10(0.8×10-3 s-1)时的速率常数.通过比较可以得出,在pH=4和7时,C,N-TNAs对甲基橙的降解率明显大于pH=10时.可见,pH值对甲基橙的降解效率的影响比较大.方世杰等(2001)及李明玉等(2009)利用TiO2作为光催化剂降解甲基橙的实验也证实了在酸性条件下甲基橙的降解速率比在碱性条件下较佳.
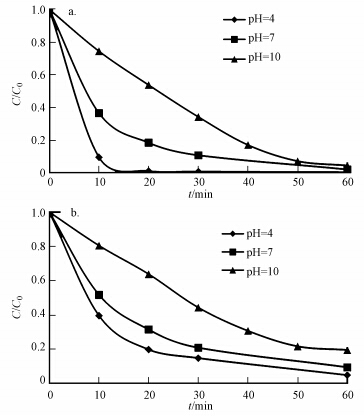 |
| 图 6 不同pH下甲基橙的光电催化降解情况(a.C,N-TNAs,b.TNAs) Fig. 6 Degradation of MO by photoelectrochemical method at different pHs(a.C,N-TNAs,b.TNAs) |
此外,本研究还测试了不同pH条件下C,N-TNAs和TNAs对甲基橙溶液的降解效率.实验中甲基橙起始浓度为5 mg · L-1,以100 W低压汞灯作为光源,得到了材料在pH=4、7和10条件下去除率随时间的变化曲线.通过比较可知,在相同的条件下,C,N-TNAs对甲基橙的降解效率都优于TNAs(表 2,3),这是因为碳氮的掺杂提高了材料对光的吸收效率,从而具有较高的光电利用效率.
| 表 2 不同pH条件下甲基橙的C,N-TNAs光电催化降解的准一级动力学速率常数 Table 2 Pseudo-first-order rates of MO degradation(kobs)of PEC under different pH |
| 表 3 不同pH条件下甲基橙的TNAs光电催化降解的准一级动力学速率常数 Table 3 Pseudo-first-order rates of MO degradation(kobs)of PEC under different pH |
此实验表明,在同样的实验条件下,C,N-TNAs的催化降解效率明显比TNAs高.这是因为随着碳氮的引入,增加了缺陷数量,从而提高反应活性(Chao et al., 2004).同时由于金属离子的可交换性,可提高表面的吸附性能,从而改善其催化性能.此外,本研究的光催化反应为异相反应(Heterogeneous Reaction),即液相中的染料与固体材料接触时,才会发生降解反应,因此,吸附在C,N-TNAs上的染料分子会最先被降解.
3.3 催化剂的产氢效率自从日本学者Fujishima等(1972)发现光照TiO2电极可以使水分解产氢这一现象以来,极大地推动了光催化产氢研究的迅速发展.但对钛基催化剂来说,由于电子和空穴的复合导致了较低的产氢效率,对钛基催化剂的改性修饰(Pt负载、非金属元素的掺杂等)可以提高产氢效率(Kudo et al., 2009).由图 7可知,C,N-TNAs的产氢效率明显高于TNAs,其产氢速率达到了0.95 mmol · h-1,是TNAs的1.46倍,明显高于钛基催化剂(0.006~0.568 mmol · h-1)(Kudo et al., 2009).这是因为在PEC体系中,外加的电场可以使电子和空穴有效分离,降低电子和空穴的复合效率,从而提高产氢效率.
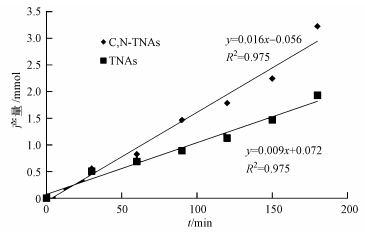 |
| 图 7 C,N-TNAs和TNAs的时间-产氢关系图 Fig. 7 Plots of time vs hydrogen production using C,N-TNAs and TNAs |
由于二氧化钛属于半导体,半导体的能带结构由填满电子的低能价带(Valence B and ,VB)和空的高能导带(Conduction B and ,CB)构成,价带和导带之间存在禁带.半导体的禁带宽度一般在 3.0 eV 以下.当能量大于或等于禁带的光(hν≥Eg)照射到半导体时,处于价带的电子就可跃迁到导带上,即产生电子-空穴对.纳米级的TiO2在紫外光的照射下,由于吸收了光能而产生电子空穴对.在阳极部分,这些空穴对会迅速迁移至表面,并激活其表面附着的H2O与O2而产生氢氧自由基(·OH),在阴极部分,在外加电场的作用下,产生的电子传递到阴极,与H+结合,产生H2,其机理方程式如下:
阳极:
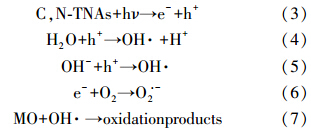
阴极:
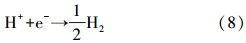
C,N-TNAs和TNAs对甲基橙的光电催化降解实验的结果表明,在相同的实验条件下,C,N-TNAs对甲基的橙降解效率优于TNAs,主要的原因可以归纳为以下两点:①由于碳氮的掺杂,可以在二氧化钛的价带边上形成C 2p和N 2p的局域态(Serpone,2006),在光的照射下,可以使电子从价带跃升到导带,而留在价带上的h+可以和水结合,或者和水解离出的OH-生成OH ·,再对甲基橙进行氧化;②二氧化钛纳米管阵列的表面可能形成碳酸盐物种,充当了光敏剂(Yang et al., 2007),在光的作用下被激发,产生的电子注入到二氧化钛的导带,电子随后与表面吸附的氧结合,形成O· -2,可以对甲基橙进行氧化,与此同时,h+可以和水结合,或者和水解离出的OH-生成OH ·,再对甲基橙进行氧化.此外,由于碳氮的掺杂,缩短了带隙的宽度,从而提高了材料对光的吸收效率,从而具有较高的光电利用效率,最终导致降解效率的提高.
通过对实验结果的分析可知,C,N-TNAs和TNAs对甲基橙的光电催化降解都表现为在酸性条件下甲基橙的降解速率比在碱性条件下较佳.原因如下:TiO2的等电位点为6.70(Aliabadi et al.,2011),在酸性条件下(pH <pHpzc),TiO2表面带正电荷,在碱性条件(pH <pHpzc)下带负电荷;另一方面,甲基橙存在醌式结构和偶氮结构,其pKa=3.47(Trabelsi et al., 2013),在pH>pKa条件下,甲基橙发生脱质子反应,当3.47<pH<6.70时,醌式结构的甲基橙会吸附在二氧化钛表面,pH大于6.7时,则会排斥;与此同时,随着pH的增高,羟基自由基主要通过吸附在二氧化钛表面上的羟基负离子俘获光生空穴而产生,其产生的羟基自由基也会相应的增加;在低pH 值条件下,羟基自由基是通过氢质子与被吸附在二氧化钛表面上的氧俘获,相继发生一系列反应.因此,虽然甲基橙的光催化高的降解率在高pH和低pH区都可能出现,但在低pH值出现时更为有利,其最佳pH为3.47<pH<5.29.本研究发现,醌式结构比偶氮结构更容易氧化降解,这与其他研究的结果一致(Wang et al., 2011,Saleh et al., 2012).
4 结论(Conclusions)本研究以阳极氧化法结合超声辅助沉积法合成碳氮共掺杂二氧化钛纳米管阵列,并对该材料进行表征及光电化学催化实验.XPS结果表明,碳氮成功地掺入到了二氧化钛纳米管阵列中;XRD分析结果表明,C,N-TNAs主要的晶相为锐钛矿相;FESEM结果显示,碳氮元素的掺杂并没有改变二氧化钛纳米管阵列规整有序的管阵列结构;UV-vis表明,碳氮的掺杂可以提高光的吸收效率.以上表征结果表明,碳氮成功地掺入到了二氧化钛纳米管阵列中,并未破坏其多孔有序的结构,而且比二氧化钛纳米管阵列具有更高的光催化活性,二氧化钛纳米管阵列掺杂了碳氮,可明显提高其光催化活性.在光电催化降解甲基橙的实验当中,酸性溶液条件下,二氧化钛纳米管阵列的催化氧化效率较高,其速率常数为2.3×10-3 s-1(pH=4),同时也具有较高的产氢速率(0.95 mmol · h-1),所以,该实验体系在光电催化降解污水中的有机污染物同时产氢方面有应用前景.
| [1] | Aliabadi M, Sagharigar T. 2011. Photocatalytic removal of rhodamine b from aqueous solutions using TiO2 nanocatalyst [J]. Journal of Applied Environmental and Biological Sciences, 1(12): 620-626 |
| [2] | Asahi R, Morikawa, T, Ohwaki T,et al. 2001. Visible-light photocatalysis in nitrogen-doped titanium oxides [J]. Science, 293(5528): 269-271 |
| [3] | Chao M C, Lin H P, Mou C Y,et al. 2004. Synthesis of nano-sized mesoporous silicas with metal incorporation [J]. Catalysis Today, 97(1): 81-87 |
| [4] | Chen C, Bai H,ChangC L. 2007. Effect of plasma processing gas composition on the nitrogen-doping status and visible light photocatalysis of TiO2 [J]. The Journal of Physical Chemistry C, 111(42): 15228-15235 |
| [5] | Cole E B, Lakkaraju P S, Rampulla D M, et al. 2010. Using a one-electron shuttle for the multielectron reduction of CO2 to methanol: kinetic, mechanistic, and structural insights [J]. Journal of the American Chemical Society, 132(33): 11539-11551 |
| [6] | Dai G P, Liu S Q, LiangY, et al. 2012. A simple preparation of carbon and nitrogen co-doped nanoscaled TiO2 with exposed {001} facets for enhanced visible-light photocatalytic activity [J]. Journal of Molecular Catalysis (A: Chemical), 368-369: 38-42 |
| [7] | 方世杰, 徐明霞, 黄卫友, 等. 2001. 纳米 TiO2光催化降解甲基橙 [J]. 硅酸盐学报, 29(5): 439-442 |
| [8] | Fujishima A, Honda K. 1972. Electrochemical photolysis of water at a semiconductor electrode [J]. Nature, 238(5358): 37-38 |
| [9] | Hachem C, Bocquillon F, Zahraa O,et al. 2001. Decolourization of textile industry wastewater by the photocatalytic degradation process [J]. Dyes and Pigments, 49(2): 117-125 |
| [10] | Irie H, WatanabeY, Hashimoto K. 2003. Nitrogen-concentration dependence on photocatalytic activity of TiO2-xNx powders [J]. The Journal of Physical Chemistry B, 107(23): 5483-5486 |
| [11] | Khan S U, Al-Shahry M,InglerJr W B. 2002. Efficient photochemical water splitting by a chemically modified n-TiO2 [J]. Science, 297(5590): 2243-2245 |
| [12] | Ko S H, Lee D, Kang H W,et al. 2011. Nanoforest of hydrothermally grown hierarchical ZnO nanowires for a high efficiency dye-sensitized solar cell [J]. Nano Letters, 11(2): 666-671 |
| [13] | Kudo A,Miseki Y. 2009. Heterogeneous photocatalyst materials for water splitting [J]. Chemical Society Reviews, 38(1): 253-278 |
| [14] | 李明玉, 尚薇, 王心乐, 等. 2009. 光电化学协同催化降解甲基橙的研究 [J]. 中国环境科学, 29(5): 512-517 |
| [15] | Nakade S, Kanzaki T, Kambe S, et al. 2005. Investigation of cation-induced degradation of dye-sensitized solar cells for a new strategy to long-term stability [J]. Langmuir,21(24): 11414-11417 |
| [16] | Ou H H, Lo S L,Liao C H. 2011. N-doped TiO2 prepared from microwave-assisted titanate nanotubes (NaxH2-xTi3O7): the effect of microwave irradiation during TNT synthesis on the visible light photoactivity of N-doped TiO2 [J]. The Journal of Physical Chemistry C, 115(10): 4000-4007 |
| [17] | Parida K M, Sahu N, Tripathi A K,et al. 2010. Gold promoted S, N-doped TiO2: an efficient catalyst for CO adsorption and oxidation [J]. Environmental Science & Technology, 44(11): 4155-4160 |
| [18] | Pelaez M, de la Cruz A A, Stathatos E,et al. 2009. Visible light-activated N-F-codoped TiO2 nanoparticles for the photocatalytic degradation of microcystin-LR in water [J]. Catalysis Today,144(1/2): 19-25 |
| [19] | Peng Y P, Lo S L, Ou F H,et al. 2010. Microwave-assisted hydrothermal synthesis of N-doped titanate nanotubes for visible-light-responsive photocatalysis [J]. Journal of Hazardous Materials, 183(1/3): 754-758 |
| [20] | Peng Y P, Yeh Y T, Wang P Y,et al. 2013. A solar cell driven electrochemical process for the concurrent reduction of carbon dioxide and degradation of azo dye in dilute KHCO3electrolyte [J]. Separation and Purification Technology, 117: 3-11 |
| [21] | Peng Z A,Peng X G. 2001. Formation of high-quality CdTe, CdSe, and CdS nanocrystals using CdO as precursor [J]. Journal of the American Chemical Society, 123(1): 183-184 |
| [22] | Roy P,Berger S, Schmuki P. 2011. TiO2 nanotubes: synthesis and applications [J]. Angewandte Chemie International Edition, 50(13): 2904-2939 |
| [23] | Saleh T A,Gupta V K. 2012. Photo-catalyzed degradation of hazardous dye methyl orange by use of a composite catalyst consisting of multi-walled carbon nanotubes and titanium dioxide [J]. Journal of Colloid and Interface Science,371(1): 101-106 |
| [24] | Serpone N. 2006. Is the band gap of pristine TiO2narrowed by anion- and cation-doping of titanium dioxide in second-generation photocatalysts? [J]. The Journal of Physical Chemistry B, 110(48): 24287-24293 |
| [25] | Su J Z, Feng X J, Sloppy J D,et al. 2010. Vertically aligned WO3 nanowire arrays grown directly on transparent conducting oxide coated glass: synthesis and photoelectrochemical properties [J]. Nano Letters, 11(1): 203-208 |
| [26] | Su J Z, Guo L J, Bao N Z,et al. 2011. Nanostructured WO3/BiVO4 heterojunction films for efficient photoelectrochemical water splitting [J]. Nano Letters, 11(5): 1928-1933 |
| [27] | 孙奉玉,吴鸣,李文钊, 等. 1998. 二氧化钛的尺寸与光催化活性的关系 [J]. 催化学报, 19(3): 229-233 |
| [28] | Trabelsi H, Khdhraoui M, Hentati O,et al. 2013. Titanium dioxide mediated photo-degradation of methyl orange by ultraviolet light [J]. Toxicological & Environmental Chemistry, 95(4): 543-558 |
| [29] | van de Krol R,Grätzel M. 2011. Photoelectrochemical hydrogen production [M]. New York: Springer |
| [30] | Wang G M, Yang X Y, Qian F, et al. 2010. Double-sided CdS and CdSe quantum dot co-sensitized ZnO nanowire arrays for photoelectrochemical hydrogen generation [J]. Nano Letters, 10(3): 1088-1092 |
| [31] | Wang J P, Huang B B, Wang Z Y, et al. 2011a. Synthesis and characterization of C, N-codoped TiO2 nanotubes/nanorods with visible-light activity [J]. Rare Metals, 30(S1): 161-165 |
| [32] | Wang S Q, Liu Q L,Zhu A M. 2011b. Preparation of multisensitive poly (N-isopropylacrylamide-co-acrylic acid)/TiO2 composites for degradation of methyl orange [J]. European Polymer Journal, 47(5): 1168-1175 |
| [33] | Wolcott A, Smith W A, Kuykendall T R, et al. 2009. Photoelectrochemical study of nanostructured ZnO thin films for hydrogen generation from water splitting [J]. Advanced Functional Materials, 19(12): 1849-1856 |
| [34] | Yang X X, Cao C D, Hohn K,et al. 2007. Highly visible-light active C- and V-doped TiO2 for degradation of acetaldehyde [J].Journal of Catalysis, 252(2): 296-302 |
| [35] | Zhang Z H, Yuan Y, Shi G Y, et al. 2007. Photoelectrocatalytic activity of highly ordered TiO2 nanotube arrays electrode for azo dye degradation [J]. Environmental Science & Technology, 41(17): 6259-6263 |
| [36] | Zhao X,Zhu Y F. 2006. Synergetic degradation of rhodamine B at a porous ZnWO4 film electrode by combined electro-oxidation and photocatalysis [J]. Environmental Science & Technology, 40(10): 3367-3372 |
 2015, Vol. 35
2015, Vol. 35


