溶解性有机物(dissolved organic matter,DOM)是指水中能通过0.45 μm 滤膜并在后续处理过程中不因蒸发而损失的那部分有机物(Aiken et al., 2011).它是一个复杂的体系,无明确的化学结构,其成分主要有酸类,醇类,醛类,小分子的蛋白质及氨基酸等,DOM是消毒副产物的主要前体物质(魏群山等,2010),同时也是影响水体质量的最主要的有机物部分,影响着污水处理效果和饮用水生产质量(Wenk et al., 2011).一直以来没有恰当的方法对DOM进行完全的逐一分析,近年发展起来的 XAD树脂吸附分级法为研究溶解性有机物不同组分的特性提供了一种有效手段(Labanowski and Feuillade, 2011).
光降解作用对水环境中污染物的归趋具有显著影响(Valencia et al., 2012).在东北地区,每年冰封期长达150多天,冰层最厚可达1.2 m,许多深度较浅的水体发生“连底冻”(李晶等,2009).冰封期水体表面巨大的冰层无疑是污染物的一个贮库.相对于流动性的大气和水体,污染物在冰体内部的物理迁移过程、常规的化学反应以及微生物作用相对较弱,而光化学作用却表现出特别的重要性(康春莉等,2008).目前以冰体作为污染物光化学反应媒介的研究虽然相对较少,但从不同方面仍然有成果报道.Kang等进行了在NO-2存在条件下对冰相中氯苯酚的光转化动力学与机理的研究(Kang et al., 2009).薛洪海等研究了模拟太阳光作用下间甲酚在冰相中的光转化规律(薛洪海等,2011).Rowl and 等考察了杀虫剂在冰相中的光化学行为( Rowland et al., 2011).然而冰体中DOM的光降解作用却未见文献报道.本研究以沈阳市细河河水为研究对象,考察了天然太阳辐射作用下冰体中各DOM组分的光化学降解特性.
2 材料与方法(Materials and methords) 2.1 试验水质分析本研究中的水样采自沈阳市细河.细河是流经沈阳市的一条河流,是浑河的一条主要支流.其北起沈阳市铁西新区卫工明渠南端,向西南流经铁西区、于洪区和辽中县,最终汇入浑河.所采集水样的水质情况见表 1.
| 表 1 细河河水的水质情况 Table 1 Water quality data for the Xihe River waters |
水样经过0.45μm滤膜过滤后,依次通过串联的XAD-8和XAD-4树脂柱,按DOM在不同树脂上的吸附特性将其分为疏水性有机酸(HPO-A)、疏水性中性有机物(HPO-N)、过渡亲水性有机酸(TPI-A)、过渡亲水性中性有机物(TPI-N)和亲水性有机物(HPI)共5种组分(Jiang et al., 2010).
2.3 光降解试验光降解试验在2013年12月进行.采用用超纯水溶解(稀释)或蒸发浓缩的方法调节各DOM组分样品DOC=5.0 mg · L-1,并用盐酸(0.1 mol · L-1)和NaOH溶液(0.1 mol · L-1)调节各DOM组分样品pH=7.0,然后将5种DOM组分样品和未分级的DOM样品分别装入6批(每批7支)具塞石英比色管(定制规格:内径×高度×壁厚=28 mm×380 mm×2 mm)中,敞口放于冰箱中(-30 ℃)冻结成冰.然后将所有样品加塞置于楼顶,南北朝向摆放,石英管与楼顶平面呈45度角,实验期内天气晴朗,每日光照时间8:00—16:00,其他时间取回放于-15 ℃冰箱中保存.光照时的气温-12~-23 ℃.每批比色管中,6支直接光照,光照时间分别为0 h,16 h,32 h,48 h,64 h和80 h,另1支用铝箔包裹后光照80 h.光降解试验结束后的样品取回于室温25 ℃条件下融化,测量其溶解性有机碳(Dissolved organic carbon,DOC)、紫外-可见吸收光谱、三维荧光光谱和三卤甲烷生成势(Trihalomethane formation potential,THMFP).
2.4 DOCDOC采用Shimadou TOC-5000(日本岛津公司)测定.
2.5 紫外-可见吸收光谱调节水样pH=7.0,然后将水样置于1 cm石英比色皿中,用紫外-可见分光光度计(Cary 50,美国Varian公司)进行紫外-可见扫描,扫描范围为190~900 nm,用超纯水作空白.
2.6 三维荧光光谱三维荧光光谱用CARY Eclipse荧光分光光度计(美国Varian公司)测定.测定荧光光谱时,先根据已测得的DOC值,将各待测水样DOC用超纯水稀释至2.0 mg · L-1.用光程为1 cm的石英荧光比色皿盛装样品.激发和发射狭缝宽度均为5 nm,扫描速度为1200 nm · min-1,三维荧光光谱图的激发波长扫描范围为220~400 nm,发射波长扫描范围为280~550 nm,扫描间隔为1 nm.
2.7 THMFP取100 mL水样于具反口胶塞的玻璃瓶中,用0.1 mol · L-1的NaOH溶液或0.1 mol · L-1的HCl调节样品pH=7.0.加入2 mL磷酸盐缓冲溶液,并根据确定的水样耗氯量(耗氯量按公式[Cl2] =(3×[DOC])+(7.5×[NH4+])计算)(柳清等,2010),加入次氯酸钠使用液.在20 ℃的培养箱中避光反应72 h,反应结束后取20 mL水样,加入2 mL的甲基叔丁基醚(MTBE)和10 g Na2SO4,剧烈振荡至Na2SO4全部溶解,静止分层.待两相分层后移取1 μL有机相注入CP-3800气相色谱仪(美国Varian公司)进行测定.
3 结果与讨论(Results and discussion) 3.1 DOC在光降解试验中各DOM组分的初始浓度均为DOC=5.0 mg · L-1.经80 h光照后,HPO-A,HPO-N,TPI-A,TPI-N和HPI以及DOM(未分级)的DOC分别如图 1所示,这5种组分的DOC去除率分别为42.3%,33.9%,13.2%,14.6%和HPI 35.7%.整体DOM(未分级)的DOC去除率为31.7%.而用铝箔包裹的避光对照组经80 h光照后,各组分的DOC减少量均小于0.01 mg · L-1,考虑到仪器误差的影响,认为本次试验中,光降解是使各DOM组分DOC减小的唯一原因.在光降解试验的前64 h,五种DOM组分以及整体DOM按DOC的大小可排序为HPO-A<HPI<整体DOM<HPO-N<TPI-N和TPI-A.可见相对于其它DOM组分,TPI-N和TPI-A是不容易被光降解的,HPO-A则最容易被光降解掉,其次是HPI也较容易被光降解,HPO-N的可光降解性处于中间水平.HPO-A、HPO-N、TPI-A、TPI-N和HPI在这80 h内的平均DOC光降解速率分别为:0.03、0.02、0.01、0.01、0.02 mg · L-1 · h-1,整体DOM的为0.02 mg · L-1 · h-1,最大降解速率出现在HPO-A光照0~16 h内,为0.06 mg · L-1 · h-1.这些实验结果说明在太阳辐射作用下,冰体中的5种DOM组分均会发生光降解,其中HPO-A的光降解程度最高.另外,除HPO-N外,其它样品的DOC去除速度都表现为由快变慢,这可能是因为样品中含有溶解氧,O2能够捕获光照过程中产生的水合电子e-aq,形成超氧阴离子自由基(O2-.),进而生成过氧化氢(H2O2)(Andrew et al., 2013),而H2O2是羟基自由基(· OH)的前驱物质,它可通过直接光解或者(类)Fenton反应生成 · OH,· OH具有极强的氧化性,可以促进有机物的降解(Gomis et al., 2014).但是,随着光反应的进行,溶解氧基本被消耗完,光降解速度变慢.
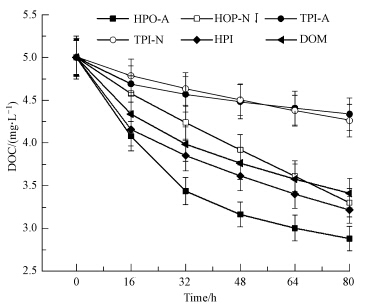 |
| 图 1 DOM及其组分的DOC随光照时间的变化 Fig.1 DOC of DOM and its components as a function of solar irradiation time |
范晓明等(2012)用250、500、700 W · m-2氙灯照射水中的DOM,72 h后,DOC去除率分别为8.28%、15.30%、25.01%,楼涛(2005)用太阳光模拟器作为光源,研究了Suwannee河腐殖酸在水中的降解特性,结果显示经过70 h模拟太阳光照射后,DOC去除率为26.4%,均小于本研究中整体DOM的DOC去除率(31.7%).这可能是因为虽然其介质(水)的温度高于本研究中介质(冰)的温度,升高温度能加剧分子内原子的振动,从而使化学键更容易断裂(Drastík et al., 2013),但是由于本研究中所用光源为太阳光,并且样品直接接受光照,而不是位于水浴池的水面以下(5~10 mm)接受光照,加之本研究中的光照时间(80 h)长于其光照时间(72 h和70 h),导致本研究中DOC的去除率高于其他研究中的DOC去除率.薛洪海(2012)用20 W紫外杀菌灯(主波长253.7 nm)作为光源,研究了六六六在水、雪、冰中的光降解规律,结果显示光照24 h后,水、雪、冰中的六六六的光转化程度分别为88.0%、99.9%、77.8%.
3.2 紫外-可见吸收光谱由于DOM组分结构复杂,多种官能团相互干扰,其紫外-可见吸收光谱均无明显特征吸收峰.实验结果显示DOM的5种组分的紫外-可见吸收光谱的走势十分相似,变化规律基本相同,因此这里仅将不同光照时间的HPO-A的紫外-可见吸收光谱图列于文中,如图 2所示.在220~350 nm范围内,DOM的组分经不同光照时间的样品的吸光度差别较明显.
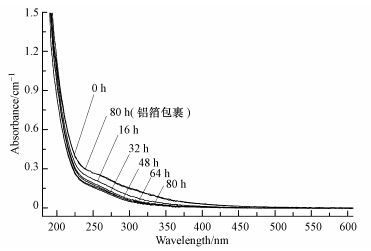 |
| 图 2 不同光照时间的HPO-A的紫外-可见吸收光谱图 Fig.2 UV/Vis absorption spectra of DOM fractions with different solar irradiation time |
UV-254是指在波长254 nm处的单位比色皿光程下的紫外吸光度.其值能够反映所测样品中腐殖质类大分子有机物以及含C C双键和C O双键的芳香族化合物的多少(Valencia et al., 2013).水中DOM成分非常复杂,分子量变化大,其中一些有机物,如腐殖质类的分子量从5×102~5×105变化,UV-254不仅可以反映这一类有机物,而且与总有机碳(TOC)、溶解性有机碳(DOC)以及三卤甲烷生成势(THMFP)等具有很好的相关性(Lamsal et al., 2011).因此本研究重点考察了各样品的UV-254随光照时间的变化.
虽然5种组分的初始DOC值均为5.0 mg · L-1(图 1),但它们的初始UV-254值却并不相同.如图 3所示,HPO-A、HPO-N、TPI-A、TPI-N和HPI的初始UV-254分别为0.10、0.06、0.06、0.08、0.03 cm-1.由于UV-254与物质所含的芳香环数量有关,由此可以推断HPO-A含有较多的芳香环、共轭双键结构,而HPI的UV-254最低,说明HPI所含的类似芳香环这样的电子共轭体系机构较少.据相关研究,HPI主要是由氨基酸等小分子有机物组成(Fuentes et al., 2006;楼涛,2005).HPO-A、HPO-N和HPI的UV-254在前32 h下降较快,各自下降量分别占其80 h内总下降量的74.3%、86.8%、84.4%;32 h以后下降速度骤减,特别是HPI和HPO-N,32 h以后的UV-254值下降很慢,HPO-N甚至有保持不变的趋势.TPI-N的UV-254下降速度在0~16 h内最大,16 h以后下降速度变慢,前16 h内的下降量占80 h内总下降量的69.1%.TPI-A在80 h内的UV-254下降速度几乎不变.这可能是因为DOM的光降解机理:一是初始不依赖于其它物质的直接裂解羰基类基团(属于直接光降解过程);二是光化学氧化过程(Liu et al., 2015).光照开始阶段光能直接裂解DOM中羰基类基团,使得UV-254下降较快,而到后期羰基类基团已经大量减少,直接裂解作用变弱,UV-254下降速度变慢.光照80 h后,整体DOM、HPO-A、HPO-N、TPI-A、TPI-N和HPI的UV-254分别为0.03、0.06、0.04、0.03、0.04、0.01 cm-1,UV-254去除率分别为48.2%、43.4%、44.15%、45.9%、55.0%和58.8%.避光的各样品吸光度均维持在初始水平±0.005 cm-1范围内,表明光降解是DOM及其各组分的UV-254值下降的最主要原因,在太阳辐射作用下,冰体中具有芳香烃结构的DOM产生了有效的分解和转化.
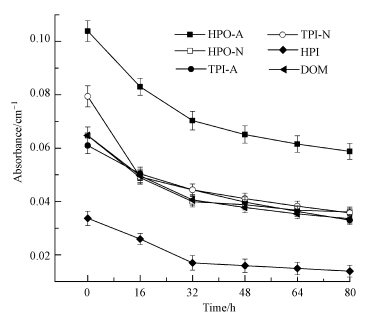 |
| 图 3 DOM及其组分的UV-254随光照时间的变化 Fig.3 UV-254 of DOM and its components as a function of solar irradiation time |
虽然UV-254在表征DOM方面有众多的优点,但其值容易受样品中生色基团浓度的影响,在反映不同浓度DOM样品芳香构化程度方面存有局限性,因此我们引入SUVA,即单位浓度DOC的紫外吸收值,其计算公式为SUVA=(UV-254/DOC)×100.SUVA可以反映水中有机物的芳香度,以及不饱和双键或芳香环有机物的相对含量等(Zhou et al., 2011).
从图 4可以看出,DOM组分按初始SUVA大小可排序为HPO-A>TPI-N>HPO-N>TPI-A>HPI,说明在这5种组分中,HPO-A的芳香性最高,而HPI的芳香性最低.HPO-A的SUVA随光照时间变化不大,基本维持初始水平不变,表明光降解作用对HPO-A中芳香性物质和非芳香性物质的去除率接近.TPI-A、TPI-N和HPI的SUVA在光降解试验中表现出不同程度的降低,说明光降解作用对这3种组分中非芳香性物质的去除率高于芳香性物质.HPO-N的最小SUVA出现在光照32 h后,其值为0.94 L · m-1 · mg-1,与初始水平(1.29 L · m-1 · mg-1)相比,降低了27.1%.此后SUVA开始增大,光照80 h后的SUVA为1.09 L · m-1 · mg-1,与初始水平相比降低了15.5%.0~80 h光照条件下HPO-A,HPO-N,TPI-A,TPI-N和HPI的SUVA降低率可排序为TPI-N(47.2%)>TPI-A(37.7%)>HPI(35.8%)>HPO-N(15.5%)>HPO-A(1.9%).整体DOM的SUVA降低率为24.1%.
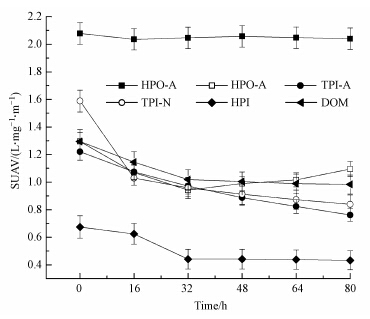 |
| 图 4 DOM组分的SUVA随光照时间的变化 Fig.4 SUVA of DOM components as a function of solar irradiation time |
三维荧光光谱能够获得激发波长和发射波长同时变化时的荧光强度信息,包含了DOM的全部指纹,能够揭示有机物的分类及其含量信息,并且可对多组分复杂体系中荧光光谱重叠的对象进行光谱识别和表征(Baghoth et al., 2011).根据Chen等的研究(Chen et al., 2003),可将所得三维荧光谱图分为5个荧光区域:Ⅰ区(Ex/Em=220~250 nm/280~330 nm)为色氨酸、酪氨酸和苯丙氨酸等类芳香族蛋白质(Ⅰ)荧光区域;II区(Ex/Em=220~250 nm/330~380 nm)为类芳香族蛋白质(Ⅱ)荧光区域;Ⅲ区(Ex/Em=220~250 nm/380~480 nm)为类富里酸物质荧光区域;Ⅳ区(Ex/Em=250~280 nm/290~380 nm)为类溶解性微生物代谢产物荧光区域;Ⅴ区(Ex/Em=>250 nm/380~480 nm)为类腐殖酸物质荧光区域.
用铝箔包裹的避光对照组经80 h光照后,各组分的荧光光谱图与0 h时的光谱图相同.光照0、16、48、80 h的样品的荧光光谱如图 5所示,可以看出,各荧光峰的强度均发生了变化.说明光照使DOM组分中荧光物质的含量发生了变化.
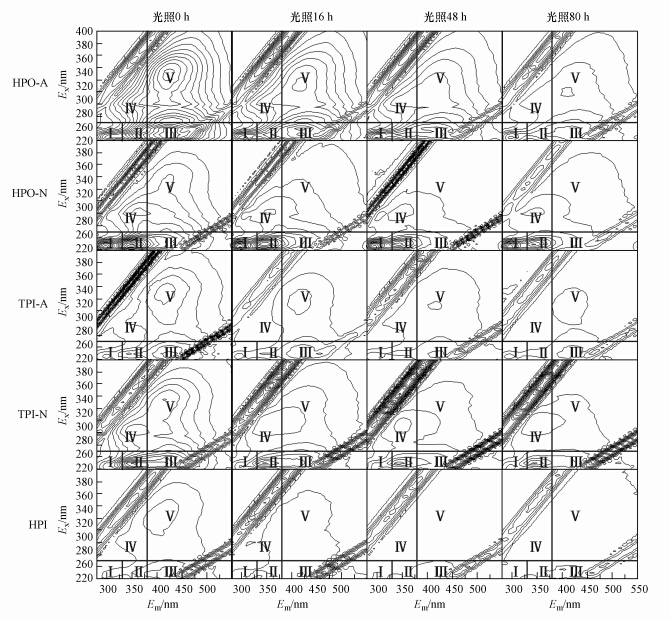 |
| 图 5 不同光照时间的DOM组分的三维荧光光谱图 Fig.5 Three-dimensional fluorescence spectra of DOM components with different solar irradiation time |
在HPO-A的荧光光谱图上有3个显著的荧光峰,分别是类腐殖酸荧光峰、类富里酸荧光峰、类芳香族蛋白质(Ⅰ)荧光峰,类富里酸荧光峰表现为“肩峰”形式,而类芳香族蛋白质(Ⅱ)荧光峰和类溶解性微生物代谢产物荧光峰不明显.光照使类芳香族蛋白质(Ⅰ)荧光物质先增加后减少,最大荧光强度出现在光照32 h的样品中,与0 h相比,增高22.9%,荧光强度最小值出现在光照80 h的样品中,与初0 h相比降低22.8%;类富里酸荧光物质和类腐殖酸荧光物质的荧光强度均随光照时间的增加而降低,与0 h相比,类富里酸荧光物质在16、48、80 h分别降低28.7%、50.6%、58.%,类腐殖酸荧光物质分别降低30.0%、48.5%、53.4%.
在HPO-N的荧光光谱图上,类芳香族蛋白质(Ⅰ)荧光峰、类芳香族蛋白质(Ⅱ)荧光峰和类溶解性微生物代谢产物荧光峰都很显著,类富里酸和类腐殖酸荧光峰不明显.与其他4种DOM组分相比,HPO-N含类芳香族蛋白质(Ⅰ)荧光物质和类芳香族蛋白质(Ⅱ)荧光物质含量最高.光照使类芳香族蛋白质(Ⅰ)荧光物质先增加后减少,最大荧光强度出现在光照16 h的样品中,与0 h相比,增高3.0%,最小荧光强度出现在光照80 h的样品中,与0 h相比减少8.2%;类芳香族蛋白质(Ⅱ)荧光物质和类微生物代谢产物荧光物质的荧光强度均随光照时间的增加而降低,与0 h相比,类芳香族蛋白质(Ⅰ)荧光物质在16、48、80 h内分别降低23.0%、41.1%、45.5%,类微生物代谢产物分别降低32.4%、44.0%、47.6%.
在TPI-A 的荧光光谱图上没有观察到类溶解性微生物代谢产物荧光峰,而类富里酸荧光峰、类腐殖酸荧光峰以及类芳香族蛋白质(Ⅰ)荧光峰比较明显,而且这4个荧光峰的强度相近.光照使类芳香族蛋白质(Ⅰ)荧光物质先减少后增加,最小荧光强度出现在光照32 h的样品中,与初始水平相比,减小42.9%,类富里酸荧光物质和类腐殖酸荧光物质的荧光强度均随光照时间的增加而降低,与0 h相比,类富里酸荧光物质在16 h、48 h、80 h内分别降低43.6%、62.5%、65.6%,类腐殖酸荧光物质分别降低48.9%、63.8%、65.0%.
在TPI-N的荧光光谱图上,类芳香族蛋白质(Ⅰ)荧光峰、类芳香族蛋白质(Ⅱ)荧光峰和类溶解性微生物代谢产物荧光峰都很显著,类富里酸荧光峰和类腐殖酸荧光峰不明显.随着光照时间的增加,类芳香族蛋白质(Ⅰ)荧光物质、类芳香族蛋白质(Ⅱ)荧光物质和类溶解性微生物代谢产物荧光物质均表现为先减少后增加,并且这3种荧光物质的最小荧光强度都出现在光照32 h的样品中,与0 h相比,分别减小33.7%、41.0%、34.3%.
在HPI的荧光光谱图上,类腐殖酸荧光峰和类富里酸荧光峰显著,类芳香族蛋白质(Ⅰ)荧光峰和类溶解性微生物代谢产物荧光峰虽然强度较小,但峰形明显.最为特殊的是类芳香族蛋白质(Ⅱ)荧光峰,该区域荧光峰呈凹陷状,表现为对此类物质的“缺失”,由此可见.分级操作使得类芳香族蛋白质(Ⅱ)都被吸附在树脂柱中,导致直接流出的HPI组分中不含有或极少含有此类物质.随着光照时间的增加,类芳香族蛋白质(Ⅰ)荧光物质和类溶解性微生物代谢产物荧光物质都表现出波动性的变化,最大荧光强度都出现在光照0 h的样品中,最小荧光强度都出现在光照16 h的样品中,与0 h相比分别减小34.2%和65.4%;类富里酸荧光物质和类腐殖酸荧光物质的荧光强度均随光照时间的增加而降低,与0 h相比,类富里酸荧光物质在16、48、80 h内分别降低43.3%、59.6%、63.7%,类腐殖酸物质分别37.1%、54.5%、66.9%.
3.4 卤代活性THMFP是指水样中的有机物质在加氯量足够的条件下生成的4种三卤甲烷(Trihalomethanes,THMs)(三氯甲烷、一溴二氯甲烷、二溴一氯甲烷和三溴甲烷)的总量,水样中THMs前体物的含量通常用THMFP来表征(Kim,2009; Sun et al., 2009).但由于THMFP在很大程度上受到水样DOC浓度的影响,因此,通常用单位浓度的DOC水样的THMFP,即三卤甲烷生成活性(Specific Trihalomethane Formation Potential,STHMFP)来表征DOM与氯反应生成三卤甲烷的能力(Abouleish and Wells, 2012).
DOM组分的THMFP和STHMFP随光照时间的变化情况如图 6所示.光照时间的增加使各组分的THMFP发生变化,而用铝箔包裹的避光对照组经80 h光照后,各组分的THMFP与初始值几乎相同,说明光照是引起DOM组分的THMFP变化的原因.
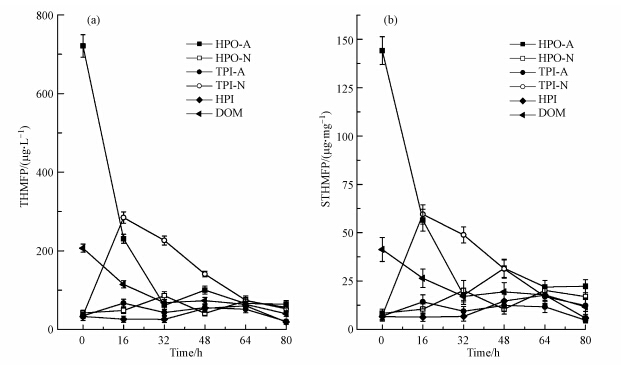 |
| 图 6 DOM及其组分的THMFP(a)和STHMFP(b)随光照时间的变化情况 Fig.6 THMFP(a) and STHMFP(b)of DOM and its components as a function of solar irradiation time |
HPO-A在光降解试验中的THMFP初始值(0 h)为720.0 μg · L-1,远高于其他4种组分(33.6~41.8 μg · L-1),是整体DOM(206.8 μg · L-1)的3.5倍.5种DOM组分随光照时间的变化趋势并不相同.HPO-A的THMFP随光照时间的变化趋势为减小-增大-减小,最大值为720.0 μg · L-1,出现在光照0 h.最小值为61.0 μg · L-1,出现在光照32 h,与0 h相比,减少91.6%.HPO-N的THMFP随光照时间的变化趋势为增大-减小-增大-减小,最大值为85.6 μg · L-1,出现在光照32 h,与0 h(41.8 μg · L-1)相比,增加104.9%.最小值为40.9 μg · L-1,出现在光照48 h,与0 h相比,减少2.1%.
TPI-A的THMFP随光照时间的变化趋势为增大-减小-增大-减小,最大值为67.0 μg · L-1,出现在光照16 h,与0 h(34.7 μg · L-1)相比增加93.0%.最小值为20.4 μg · L-1,出现在光照80 h,与0 h相比,减少41.1%.TPI-N的THMFP随光照时间的变化趋势为减小-增大-减小,最小值为37.0 μg · L-1,出现在光照0 h,最大值为284.6 μg · L-1,出现在光照16 h,与0 h相比,增加668.9%.HPI的THMFP随光照时间的变化趋势为减小-增大-减小,最大值为60.2 μg · L-1,出现在光照64 h,与0 h(33.6 μg · L-1)相比增加78.9%.最小值为18.6 μg · L-1,出现在光照80 h,与0 h相比,减少44.7%.光照80 h使HPO-A、TPI-A和HPI的THMFP分别减少91.1%、41.2%和44.7%,使HPO-N和TPI-N的THMFP分别增加33.9%和41.6%.整体DOM的THMFP变化趋势整体呈下降趋势,光照80 h后减少80.9%.由实验结果来看,在冰体中5种DOM组分的光降解过程中,既发生THMs前体物的去除,也发生THMs前体物的生成.总的来说,光降解使HPO-A中THMs前体物的量减少,使TPI-N中THMs前体物的量增加,而其他3种组分中THMs前体物的量的变化与光照时间有关.
从图 6b可以看出,HPO-A的STHMFP远高于其他4种组分,这说明HPO-A是生成三卤甲烷的主要组分.光照使HPO-A的STHMFP显著降低,光照80 h后其降幅达到84.6%;HPO-N的STHMFP随光照时间的增加表现为波动上升,光照80 h后增加了102.9%;TPI-N的STHMFP随光照时间的变化趋势为先上升后下降,最大值为最小值的6.6倍,但整体来看,光照80 h后STHMFP仅升高了2.3%;整体DOM的STHMFP随光照时间下降,光照80 h后降幅达72.0%;相比之下,TPI-A和HPI的STHMFP变化较平稳,表现为微小幅度的上升.
4 结论(Conclusion)1)太阳辐射作用下,冰体中的5种DOM组分均会发生光降解,其中HPO-A的光降解程度最高.
2)在太阳辐射作用下,冰体DOM中芳香烃含量显著下降.光照80 h后,HPO-A、HPO-N、TPI-A、TPI-N和HPI的UV-254去除率分别为43.4%、44.15%、45.9%、55.0%和58.8%.
3)光降解作用对冰体中的荧光物质具有显著的去除效果.除了HPO-A中的类芳香族蛋白质荧光物质(Ⅰ)之外,其它DOM组分中的各类荧光物质的光降解程度均高于以DOC表征的整体有机物.光降解对DOM组分中类富里酸荧光物质和类腐殖酸荧光物质的去除效果优于类溶解性微生物代谢产物荧光物质和类芳香族蛋白质荧光物质.
4)在冰体中DOM组分的光降解过程中,既发生THMs前体物的去除,也发生THMs前体物的生成.光降解使HPO-A中THMs前体物的量减少,使TPI-N中THMs前体物的量增加,而其他三种组分中THMs前体物的量的变化与光照时间有关.
| [1] | Abouleish M Y Z, Wells M J M. 2012. Trihalomethane formation potential of aquatic and terrestrial fulvic and humic acids:examining correlation between specific trihalomethane formation potential and specific ultraviolet absorbance[J]. Environmental Chemistry, 9(5):450-461 |
| [2] | Aiken G R, Hsu-Kim H, Ryan J N. 2011. Influence of dissolved organic matter on the environmental fate of metals, nanoparticles, and colloids[J]. Environmental Science & Technology, 45(8):3196-3201 |
| [3] | Andrew A A, Del Vecchio R, Subramaniam A, et al. 2013. Chromophoric dissolved organic matter (CDOM) in the Equatorial Atlantic Ocean:optical properties and their relation to CDOM structure and source[J]. Marine Chemistry, 148:33-43 |
| [4] | Baghoth S A, Sharma S K, Amy G L. 2011. Tracking natural organic matter (NOM) in a drinking water treatment plant using fluorescence excitation-emission matrices and PARAFAC[J]. Water Research, 45(2):797-809 |
| [5] | Chen W, Westerhoff P, Leenheer J A, et al. 2003. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 37(24):5701-5710 |
| [6] | Drastík M, Novák F, Kučerík J. 2013. Origin of heat-induced structural changes in dissolved organic matter[J]. Chemosphere, 90(2):789-795 |
| [7] | 范晓明, 李先国, 唐旭利, 等. 2012. 水体中 DOM 的光解影响因素研究[J]. 海洋学报, 34(5):191-196 |
| [8] | Fuentes M, González-Gaitano G, García-Mina J M, et al. 2006. The usefulness of UV-visible and fluorescence spectroscopies to study the chemical nature of humic substances from soils and composts[J]. Organic Geochemistry, 37(12):1949-1959 |
| [9] | Gomis J, Prevot A B, Montoneri E, et al. 2014. Waste sourced bio-based substances for solar-driven wastewater remediation:Photodegradation of emerging pollutants[J]. Chemical Engineering Journal, 235:236-243 |
| [10] | Jiang J Q, Zhao Q L, Wei L L, et al. 2010. Extracellular biological organic matters in microbial fuel cell using sewage sludge as fuel[J]. Water Research, 44(7):2163-2170 |
| [11] | Kang C L, Gao H J, Guo P, et al. 2009. Kinetics and mechanism of para-chlorophenol photoconversion with the presence of nitrite in ice[J]. Journal of Hazardous Materials, 170(1):163-168 |
| [12] | 康春莉, 高红杰, 郭平, 等. 2008. 雪冰中有机污染物的研究进展[J]. 科学技术与工程, 8(2):468-472 |
| [13] | Kim J. 2009. Fate of THMs and HAAs in low TOC surface water[J]. Environmental Research, 109(2):158-165 |
| [14] | Labanowski J, Feuillade G. 2011. Dissolved organic matter:Precautions for the study of hydrophilic substances using XAD resins[J]. Water Research, 45(1):315-327 |
| [15] | Lamsal R, Walsh M E, Gagnon G A. 2011. Comparison of advanced oxidation processes for the removal of natural organic matter[J]. Water Research, 45(10):3263-3269 |
| [16] | 李晶, 马云, 周浩, 等. 2009. 扎龙湿地冰封期水环境特征初步研究[J]. 环境科学与管理, 34(9):128-130; 135 |
| [17] | Liu N, Sijak S, Zheng M, et al. 2015. Aquatic photolysis of florfenicol and thiamphenicol under direct UV irradiation, UV/H2O2 and UV/Fe (II) processes[J]. Chemical Engineering Journal, 260:826-834 |
| [18] | 柳清, 张丽萍, 刘文君, 等. 2010. umu试验研究饮用水氯和氯胺消毒过程中遗传毒性的变化以及消毒条件的影响[J]. 环境科学, 31(1):93-98 |
| [19] | 楼涛. 2005. 溶解有机物的光化学过程模拟及其对环境污染物结合性质的影响研究. 青岛:中国海洋大学. 3-11 |
| [20] | Rowland G A, Bausch A R, Grannas A M. 2011. Photochemical processing of aldrin and dieldrin in frozen aqueous solutions under arctic field conditions[J]. Environmental Pollution, 159(5):1076-1084 |
| [21] | Sun Y X, Wu Q Y, Hu H Y, et al. 2009. Effects of operating conditions on THMs and HAAs formation during wastewater chlorination[J]. Journal of Hazardous Materials, 168(2/3):1290-1295 |
| [22] | Valencia S, Marín J, Velásquez J, et al. 2012. Study of pH effects on the evolution of properties of brown-water natural organic matter as revealed by size-exclusion chromatography during photocatalytic degradation[J]. Water Research, 46(4):1198-1206 |
| [23] | Valencia S, Marín J M, Restrepo G, et al. 2013. Application of excitation-emission fluorescence matrices and UV/Vis absorption to monitoring the photocatalytic degradation of commercial humic acid[J]. Science of the Total Environment, 442:207-214 |
| [24] | 魏群山, 罗专溪, 陈强, 等. 2010. 天然水体溶解性有机物(DOM)分级组分对典型城市源污染的荧光响应[J]. 环境科学研究, 23(10):1229-1235 |
| [25] | Wenk J, von Gunten U, Canonica S. 2011. Effect of dissolved organic matter on the transformation of contaminants induced by excited triplet states and the hydroxyl radical[J]. Environmental Science & Technology, 45(4):1334-1340 |
| [26] | 薛洪海, 李林璘, 康春莉, 等. 2011. 模拟太阳光作用下间甲酚的水相和冰相光转化研究[J]. 环境化学, 30(8):1505-1508 |
| [27] | 薛洪海. 2012. 六六六在水、冰和雪中的光化学行为. 长春:吉林大学. 25-91 |
| [28] | Zhou T, Lim T T, Chin S S, et al. 2011. Treatment of organics in reverse osmosis concentrate from a municipal wastewater reclamation plant:feasibility test of advanced oxidation processes with/without pretreatment[J]. Chemical Engineering Journal, 166(3):932-939 |
 2015, Vol. 35
2015, Vol. 35


