2. 工业聚集区污染控制与生态修复教育部重点实验室, 广州 510006
2. The Key Lab of Pollution Control and Ecosystem Restoration in Industry Clusters, Ministry of Education, Guangzhou 510006
溴代阻燃剂(brominated flame retardants,BFRs)已被广泛应用于工业和商业产品中(陈海等,2011),多溴联苯醚(polybrominated diphenyl ethers,PBDEs)是使用最为广泛的溴代阻燃剂,工业生产的PBDEs 混合物主要包括3种:五溴代(penta-BDE)、八溴代(octa-BDE)和十溴代(deca-BDE)(Tian et al., 2011).近年来,随着人们越来越关注PBDEs对环境和人体健康的不利影响,多种溴代阻燃剂已被禁止生产(Venier et al., 2012).如:penta-和octa-BDE混合物中四溴代(tetra-BDE)至七溴代(hepta-BDE)联苯醚由于具有持久性、生物累积性、毒性等不利效应,2004年被欧盟禁止生产和使用,2009年又被纳入《斯德哥尔摩公约》(Möller et al., 2012).大量研究表明,PBDEs已在全球范围内的大气、水体、沉积物、生物体和人体中(Lee et al., 2004; Wu et al., 2008; Guo et al., 2008; Hites,2004; 张亮等,2011; 陈社军等,2005)被广泛检出,并且全球很多区域PBDEs的污染水平呈指数增长(Luross et al., 2002).PBDEs污染已对生态环境和人体健康构成了较大的潜在危害.
PBDEs为添加型阻燃剂,其与聚合物是机械混合,并不形成化学键,因此易于脱离聚合物而进入环境(Christensen et al., 2002).含有PBDEs 的电子废物,在资源化过程中极易释放出大量的PBDEs.大量研究对我国广东汕头、清远和浙江台州等粗放电子物资源化处置集中区域的PBDEs污染进行了报道,结果表明这些电子废物拆解和粗放处置地是我国PBDEs污染的高风险区.Leung等(2007)报道了广东贵屿表层土以及垃圾焚烧残余中的PBDEs含量高达33000~97400 ng·g-1(dw);Gao等(2011)报道了清远电子废物污染场地PBDEs 平均为3230 ng·g-1(dw),并估算清远拆解地土壤中PBDEs 残留为13.4 t;陈涛等(2011)报道了台州电子污染场地 ∑PBDEs 在33.2~2190 ng·g-1(dw)之间.然而,对这些污染区土壤的研究多集中在电子废物粗放处置地整体污染特征,而大气环境变化对土壤中PBDEs的自然降解过程影响的研究很少.
近年来全球大气污染严重,导致大气环境中的O3、CO2、SO2及其他有害气体的浓度快速上升,出现全球性的气候变暖.其次,臭氧逐渐耗竭的现象也引起了人们极大的关注,臭氧层的破坏将使过量的紫外线辐射到达地面;据报道,珠三角多个城市臭氧超标,臭氧8 h均值达180~225 μg·m-3(杨辉,2012),珠三角首要污染物为臭氧(黄熙灯,2014).另外,近年酸雨发生频率及酸雨分布区域保持稳定,但部分地区酸雨强度加大,华南酸雨区的珠江三角洲地区污染加重(Guo et al., 2011).近年来,有关臭氧化法修复土壤有机污染物的研究反映出该方法的不少优越性.如Nelson和Borwn(1994)在实验室中不同的通气时间使土壤中的PAHs,有机氯农药或多氯联苯、THP、TCE及DCE降解了35%~90%,现场实验的降解率为50%~90%.结果表明臭氧对于PAHs类挥发性弱、毒性大、难生物降解的污染物能够达到比较理想的修复效果.
因此,本研究选取模拟电子垃圾拆解区污染水平的BDE-209污染土壤为研究对象,分析PBDEs在大气臭氧浓度升高,光照(紫外光和自然光)、温度和pH等条件变化情况下的自然降解特征及规律,并对其降解产物进行探讨.以期为电子废物处置地PBDEs 污染风险的分类管理和场地土壤修复提供参考.
2 材料与方法(Materials and methods) 2.1 实验试剂及仪器PBDE混标(8种组分)标准样品:BDE-28、BDE-47、BDE-99、BDE-100、BDE-153、BDE-154、BDE-183和BDE-209,购自AccuSt and ards(美国);GC-MS检测出纯度分别为:99.3%、100%、99.2%、100%、99.3%、100%、100%和98.3%.工业用十溴二苯醚阻燃剂,BDE-209纯度为98%,购自Aladdin-阿拉丁试剂(上海)有限公司.所用试剂(二氯甲烷、正己烷和丙酮)均经过二次重蒸.硅胶(粒径为0.150~0.180 mm)和中性氧化铝(粒径为0.075~0.150 mm)分别用甲醇、二氯甲烷超声清洗30 min,于通风橱干燥后在180 ℃下活化12 h,再加入3% 超纯水去活后置于干燥器内备用.处理后的硅胶分别加入浓硫酸(硅胶和浓硫酸的质量比为100:44)和1 mol·L-1 的NaOH溶液(硅胶和NaOH溶液的质量比为100:30),涡旋振荡混匀后,获得酸性硅胶和碱性硅胶,于密闭容器内用正己烷浸没保存备用.无水硫酸钠置于马弗炉中450 ℃ 烘烤4 h 后储存于干燥器中备用.所有玻璃器皿经重铬酸钾浓硫酸洗涤、自来水和超纯水洗净.
仪器包括: Agilent 7890A GC-EI/5795C MSD 气相色谱质谱仪(美国安捷伦公司);KQ5200DE型数控超声波清洗器;RE-52A 旋转蒸发仪(上海亚荣生化仪器厂);SHZ-D(Ⅲ)循环水式真空泵;MTN-2800W 型氮气浓缩装置(天津奥特赛恩斯仪器有限公司);TDL-5-A 旋转离心机(上海安亭科学仪器厂);30 cm×1.0 cm玻璃层析柱.
2.2 供试土壤与材料由于污染场地土样中PBDEs含量不均匀,不利于实验研究,所以本次研究依据珠三角电子垃圾拆解区土壤中PBDEs的平均污染水平自配污染土壤,空白土壤采自华南理工大学环境与能源学院外围(23°02′47″ N,113°24′08″ E)绿地表层0~20 cm土壤.去除土壤中碎石等杂物,自然条件下风干,得到实验用土壤(沙子粒径为1.0~2.0 mm,过20目筛,含水率5%).采用十溴二苯醚阻燃剂配制污染土壤.实验用土样BDE-209污染浓度均为1 μg·g-1.根据实验设计称取1 mg BDE-209阻燃剂,以1 L正己烷(PBDEs未检出)溶解后加入1 kg土壤中,搅拌器搅拌混合24 h后,于棕色瓶密封并翻转振荡24 h,自然条件下培养2 d,使得土壤吸附BDE-209基本达到平衡(傅海辉,2012),放置通风橱挥发,过夜,密封保存于棕色瓶中备用.除温度实验外,其余实验均在25 ℃常温下进行;除pH实验外,其余实验土壤原始pH值为7.58;除光照实验外,其余实验均在避光条件下进行.所有实验均为单一环境因子变化实验,无双因子变化交叉实验.
2.3 样品前处理称取1.0 g土壤样品,用60 mL 正己烷-丙酮(1:1,V/V)超声提取30 min,提取液旋转浓缩至1~2 mL并用正己烷置换溶剂,备用.湿法装填多层硅胶层析柱(6 cm 的中性氧化铝、2 cm 中性硅胶、5 cm 碱性硅胶、2 cm 中性硅胶、8 cm 酸性硅胶和2 cm 无水硫酸钠);用10 mL正己烷预淋洗,上样,用60 mL 二氯甲烷-正己烷(1:1,V/V)淋洗硅胶柱,接收洗脱液. 将洗脱液旋转浓缩至1~2 mL,转移至进样瓶中,用柔和N2吹干,正己烷置换溶剂,定容至1 mL,待仪器分析.
2.4 仪器分析样品分析采用Agilent 7890A GC-EI/5795C MSD,色谱柱为HP-5MS(30 m × 0.25 mm i. d.× 0.25 μm),初始温度100 ℃,保持1 min,以20 ℃·min-1升温至210 ℃,然后以4 ℃·min-1升温至250 ℃,最后以2 ℃·min-1升温至290 ℃保持5 min.进样口温度280 ℃,四级杆和离子源温度分别为230 ℃和150 ℃;以高纯氦气为载气,载气流量为1.0 mL·min-1;进样量5 μL,不分流进样.MSD在全扫描模式下扫描范围为50~900 m/z,PBDEs的定量分析在选择离子检测模式(SIM)下完成,数据采集在溶剂延迟5 min后开始.
2.5 质量控制及质量保证对于PBDEs的检测分析,在本研究中,采用方法空白、溶剂空白和加标空白,空白样品中无目标污染物检测出.在仪器分析过程中,每5个样品进一个方法空白,用以监控分析过程中的背景值,每15个样品进一个PBDEs标准样品,监测仪器的稳定性和确定保留时间.每个样品进行平行样3次,所有平行样之间的数据差异小于35%.仪器的检出限定义为3倍信噪比,对于土壤样品(1.0 g),三溴~七溴联苯醚的检出限为1.3~30 ng·g-1.为验证实验方法的回收率,空白土壤样品上添加定量的PBDE混标(8种组分)标准溶液进行回收率验证,回收率为85%~110%.本研究中所有数据均进行了回收率校正.
2.6 实验设计与方法 2.6.1 臭氧实验臭氧实验分为低浓度、高浓度两个系列,在两个不同尺寸的反应器中进行.低浓度臭氧实验以华南地区大气污染平均臭氧浓度为依据,将制备好的污染土壤装入氧反应器(150 mm × 100 mm i. d.)内,通入0.3 mg·L-1的臭氧,气体流速为100 mL·min-2.反应器共运行256 h,分别在通气2、4、8、16、32、64、128和256 h时在不同的土壤深度(1~3、4~6、7~9、10~12和13~15 cm)取样.
在高浓度臭氧实验中,为研究污染土壤中PBDEs的臭氧氧化最佳降解效果,将制备好的污染土壤装入氧反应器(150 mm × 40 mm i. d.)内,臭氧浓度分别设置为1、3、5、7.5和10 mg·L-1,气体流速为100 mL·min-2.反应器均运行2 h,反应结束后在不同的土壤深度(1~3、4~6、7~9、10~12和13~15 cm)取样.
2.6.2 光照实验光照实验分为紫外光照、太阳光照两个系列,分别在实验室紫外光照箱内和户外太阳光照射下完成.紫外光照箱由16 W的紫外灯管和滤光片组成,紫外光波长范围为300~400 nm(Shih and Wang, 2009),光照强度为1.0 mW·cm-2.将制备好的污染土壤放入照射箱内,分别在持续光照0、2、4、8、16、32、64、128和256 h时取样.
太阳光照实验在华南理工大学环境与能源学院顶楼(23°02′47″ N,113°24′08″ E)露天阳台进行,光照时间为2014年2月24日至4月15日,此期间来自太阳光的光强范围为0~1.0 mW·cm-2,相应的在太阳光照累计0、2、4、8、16、32、64、128和256 h时取样.
2.6.3 温度和pH实验温度实验分为高温、低温两组,以华南地区夏季地面最高温度(Chen and Guo, 2012)和年平均温度(Ding et al., 2011)为依据,恒温箱分别设置为40 ℃和25 ℃.两组实验均在反应1、2、3、4、5、12、18、24和30 d时取样.
pH实验分为酸性、弱酸性、弱碱性3组,称取一定量的土壤样品放入25 ℃的恒温箱内,土壤样品的pH值分别设置为2.0、5.0和9.0(Guo et al., 2011).3组实验均在反应1、2、3、4、5、12、18、24和30 d时取样.
3 结果(Results) 3.1 臭氧对土壤中PBDEs自然降解过程的影响通入0.3 mg·L-1的臭氧对土壤中PBDEs自然降解过程的影响结果见图 1,可知,低浓度的臭氧对PBDEs的自然降解有促进作用.通入臭氧气体后,低溴态产物迅速生成.在1~3 cm的表层土壤中,通入256 h的臭氧后,随着通气时间的变化(2、4、8、16、32、64、128和256 h)降解产物PBDEs(BDE-28、BDE-47、BDE-99、BDE-100、BDE-153、BDE-154和BDE-183)总生成量依次为99%、82%、64%、45%、24%、23%、19%和17%.通气时间逐渐延长,降解产物的积累量慢慢减少,5个不同深度土壤中PBDEs的降解过程均遵循此规律.在同一个时间段,例如2 h内,从表层到深层5个不同深度土壤中BDE-209的降解产物生成量分别为99%、94%、71%、62%和53%.随着土壤深度的加深,降解产物的生成量也逐渐下降,相同时间段内降解产物的分布均体现此特征.
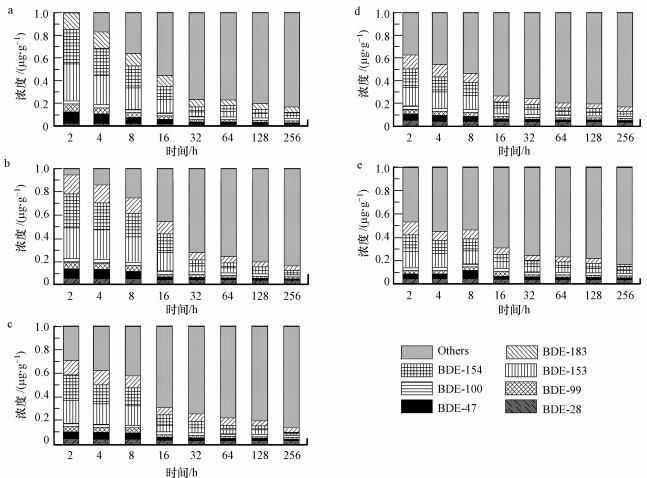 |
| 图 1 0.3 mg·L-1臭氧对不同深度土壤中BDE-209降解产物浓度分布的影响(土壤深度a:1~3 cm、b:4~6 cm、c:7~9 cm、d:10~12 cm、e:13~15 cm) Fig.1 Concentrations of degradation products of BDE-209 from BDE-183 to BDE-28 under 0.3 mg·L-1 ozone in the soil depths of 1~3(a),4~6(b),7~9(c),10~12(d) and 13~15 cm(e) |
臭氧浓度的升高对土壤中PBDEs自然降解过程的影响见图 2,相比于0.3 mg·L-1的低浓度臭氧,高浓度的臭氧在2 h短时间内对PBDEs的降解作用更加显著.通入5个不同浓度水平的高浓度臭氧,在表层土壤中7种降解产物的总量分别为38%、72%、99%、92%和59%,当臭氧浓度为5 mg·L-1时表层降解产物积累量最大.但由图 2a可知,臭氧浓度为10 mg·L-1时,5个不同深度土壤中降解产物所占百分比分别为38%、54%、78%、92%和99%,深层土壤中产物积累量最大;臭氧浓度为7.5 mg·L-1(图 2b)时同样遵循此规律.当臭氧浓度降至5 mg·L-1后(图 2c ~ 2e)最大产物积累量则出现在表层土壤中,且随土壤深度的加深产物生成量下降.
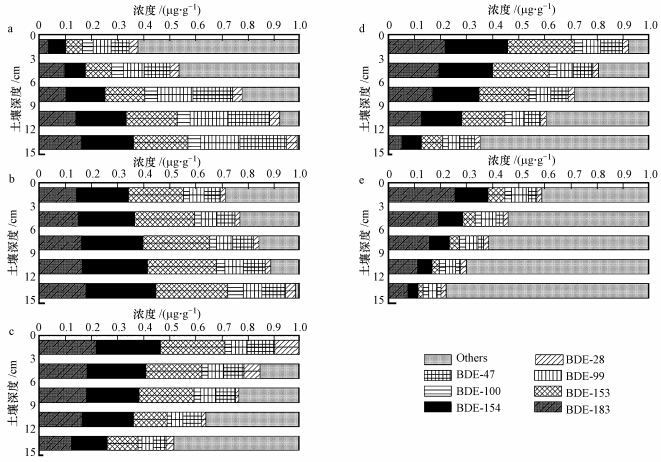 |
| 图 2 1~10 mg·L-1臭氧对不同深度的土壤中BDE-209降解产物浓度分布的影响(臭氧浓度a. 10 mg·L-1、b. 7.5 mg·L-1; c. 5 mg·L-1、d. 3 mg·L-1; e. 1 mg·L-1;通气时间2 h) Fig.2 Concentration of degradation products under five different ozone concentrations,10(a),7.5(b),5(c),3(d) and 1 mg·L-1(e),soil samples were taken from the column at different depths, and each column was run for 2 h |
紫外光与太阳光的光降解对比结果见图 3,可知,紫外光的光降解速率明显大于太阳光,BDE-209在紫外光照条件下迅速降解生成低溴态产物,在光照8 h时降解产物总量已达到82%;而此时太阳光照下的降解速率则明显较为缓慢,产物总量仅为40%.但经过光照64 h后,太阳光照的产物累积达最大值99%,表明此时BDE-209几乎全部降解为低溴联苯醚;此时紫外光与低溴联苯醚的光降解反应成为主导反应,降解产物PBDEs总量逐渐减少.
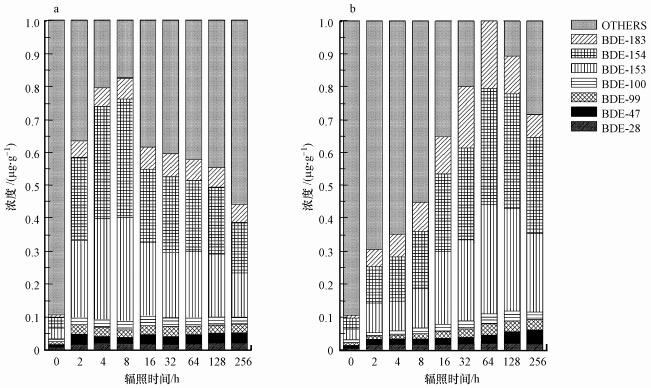 |
| 图 3 1~10 mg·L-1光照条件下土壤中降解产物PBDEs的浓度分布(a. 紫外光照;b. 太阳光照) Fig.3 Concentration of degradation products under indoor UV-lamp irradiation(a) and outdoor solar light irradiation(b) |
温度对土壤中BDE-209降解产物PBDEs的浓度分布影响见图 4.由图 4a可知,BDE-209在25 ℃下的降解速率非常的缓慢,直到第30 d降解产物的总量仅为25%.相比于常温条件,夏季地面高温40 ℃下(图 4b)的降解速率则较高,实验进行到第5 d时产物总量已累积达24%,第18 d达最大值98%,此时BDE-209几乎完全被去除.
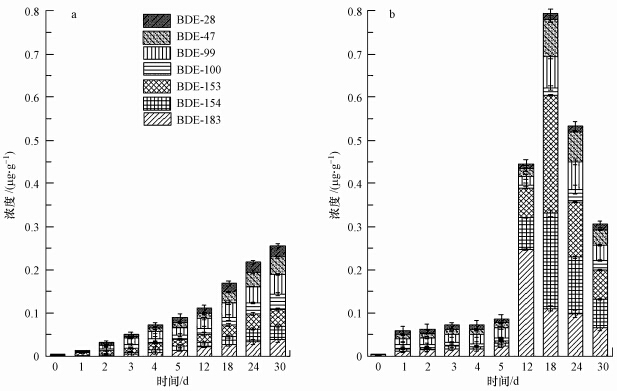 |
| 图 4 1~10 mg·L-1温度对土壤中降解产物PBDEs的浓度分布的影响(a. 25 ℃;b. 40 ℃) Fig.4 Concentration of degradation products during 30 days under the summer average high temperature of 25 ℃(a) and room temperature of 40 ℃(b)treatments |
由图 5可知,土壤pH值也是影响PBDEs自然降解过程的一个重要因素.当pH值约为9.0土壤偏弱碱性时(图 5c),BDE-209的降解速率最快,第1 d降解产物PBDEs的总量就已达最大值接近85%左右;随后产物量逐渐减少,第30 d时PBDEs剩余10%.相较于碱性土壤,在酸性土壤中的降解速率则较为缓慢.尤其是在强酸性土壤中(图 5a),直到第5 d降解产物累积量不足10%,第12 d产物累积量达最大值接近60%.在华南地区最为常见的弱酸性土壤中,即pH值约为5.0时(图 5b),BDE-209降解速度也相对较快,在第5 d降解产物的量达最大值70%左右,随后产物逐渐分解,至第30 d PBDEs总量缩减到18%.综合上图 4a可知,中性土壤中BDE-209的降解速度最慢,不同pH值土壤中BDE-209降解速率大小依次为:pH=7.5<pH=2.0<pH=5.0<pH=9.0.
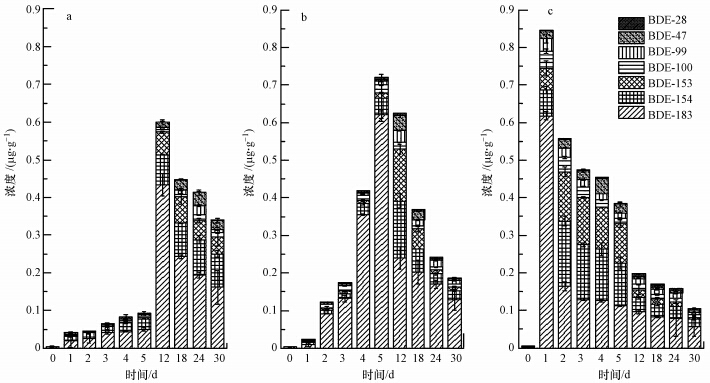 |
| 图 5 pH对土壤中降解产物PBDEs的浓度分布的影响(a. pH=2.0;b. pH=5.0;c. pH=9.0) Fig.5 Concentration of degradation products in the pH value of 2.0(a),5.0(b) and 9.0(c)soil during 30days,under the room temperature |
在通入低浓度臭氧条件下,从图 1a可以看出,虽然PBDEs的去除率随着通气时间的增加而增加,但PBDEs的去除速率却随着臭氧通气时间的增加而减小,分别为每小时8.5%、4.5%、2.4%、1.17%、0.03%、0.024%和0.019%.该现象的产生是由吸附作用和中间产物与BDE-209之间的竞争作用共同导致的.Watts和Dilly(1996)认为,当化学物质被吸附时,其与很多物质如HO·自由基反应的活性会降低.在反应的初期,臭氧很容易接触到土柱中未被吸附的BDE-209,因此反应很快.随着反应的不断进行,土柱中未被吸附的BDE-209越来越少,这时,臭氧就必须与吸附于沙子颗粒表面或者吸附于土壤微孔中的BDE-209反应,反应速度不断减小.本次实验的结果与Choi等(2001)用臭氧氧化在沙子中的菲和苯并花的实验结果相似.另外,臭氧与有机化合物的反应包含着一系列复杂化学反应的.这些反应既包括了臭氧与目标化合物BDE-209的反应也包括了其与中间产物PBDEs的反应.在臭氧与BDE-209的反应过程中,随着臭氧氧化的不断进行,生成的中间产物越来越多,这就导致臭氧与中间产物的反应超过了臭氧与BDE-209的反应成为主要的反应,从而使臭氧去除BDE-209的效率降低.由图 1a~1e可知,随着土壤深度的加深PBDEs去除率逐渐降低,同一时间段内,表层土壤中间产物的量明显高于深层土壤.由臭氧穿透曲线(纪录,2004)可知,随着土壤深度的增加,臭氧在土柱中穿透所需时间增加.这是由于在传输过程中,臭氧溶于土壤水分并与BDE-209及中间产物发生反应,该反应的发生会阻碍臭氧在土柱中的传输.臭氧传输所受阻力的大小与BDE-209的含量有关.整个反应中所发生的传质过程以及化学反应均对臭氧的穿透造成影响(Sung and Huang, 2002; Zhang et al., 2003).这是因为,臭氧在土柱中的传输是通过在孔隙气体中发生的平流扩散以及溶解于包裹在沙粒表面的水中来完成的.溶解后的臭氧再与溶解及吸附于沙粒表面的污染物发生反应(Kim and Choi, 2002).而化学反应的存在能够促进臭氧从气态到液态的传输(Sung and Huang, 2002).该促进程度由两个量来决定,即瞬时反应因子以及Hatta准数(Levenspiel,1999).这两个量都与反应物的含量有关,即反应物含量越高促进程度越大.用单位量的臭氧所去除的PBDEs量来表示臭氧的利用率.对运行两小时土壤深度分别为1~3、4~6、7~9、10~12和13~15 cm的土柱,计算可得到臭氧的利用率分别为0.274、0.26、0.197、0.172和0.147 mg PBDEs·mg 臭氧-1.这表明,随着土壤深度增加,单位量的臭氧所能去除的PBDEs的量在减少,也就是说溶解于水中与PBDEs反应的臭氧的利用率在降低.所以我们得到了图 1中所表示的PBDEs的浓度分布,土壤深度增加,与臭氧反应的PBDEs的总量增加,臭氧在土柱中的传质越快,消耗越多,因此去除率越低.
随着臭氧浓度的增加,臭氧在土柱中穿透所需时间减少.这是由于臭氧浓度的提高使更多的臭氧分子能够溶解于土壤水分中并在传质的过程中与PBDEs发生反应,化学反应的存在能够促进臭氧从气态到液态的传输(Sung and Huang, 2002),因此穿透更快.高浓度的臭氧(图 2)在短时间内迅速降解BDE-209,同时与降解产物PBDEs发生化学反应,正如前面所提到的,整个反应过程既包括了臭氧与BDE-209的反应,也包括了臭氧与中间产物PBDEs的反应.在BDE-209含量较低且去除率达到一定程度时,臭氧与中间产物的反应会逐渐变成主导反应,使相当一部分的臭氧消耗在与中间产物反应的过程中,致使PBDEs总量降低.当臭氧浓度为10 mg·L-1时,臭氧与BDE-209迅速反应,并且表层土壤中臭氧与中间产物的反应成为主导反应,导致中间产物的量也迅速减少;降解速率沿臭氧通气方向逐渐降低,2 h后中间产物在深层土壤中累积量最大.当臭氧浓度较低时,土壤可吸附的臭氧分子相应减少,大部分臭氧气体被表层土壤所利用生成大量中间产物,导致深层土壤中降解产物的量较小.造成差异变化的原因主要是,表层土壤中溶解于水中的臭氧越多,土柱中的气态臭氧越少,这样使气态臭氧在土柱中的空间分别变化越来越大.因此,沿着通气方向,能溶解于水中与污染物发生反应的臭氧越来越少,使土柱中的PBDEs去除率差异变化较大.
从实验结果可以看出,臭氧气体的存在能够促进BDE-209的自然降解,BDE-209降解过程中高溴态产物逐渐生成并与臭氧发生反应,在高溴态产物累积达一定量后其与臭氧的反应成为主导反应,进一步脱溴生成低溴态产物.这一结果说明BDE-209的自然降解过程为渐进脱溴的过程.此外,臭氧浓度越高PBDEs降解速率越大;但随着土壤深度的加深,降解速率逐渐降低.
4.2 光照对土壤中PBDEs自然降解过程影响的特性由图 3可知,在紫外光照条件下土壤中BDE-209产生了明显的降解反应,光照2 h时已有近65%的降解产物生成.土壤中BDE-209的降解主要是由光解作用引起的(有机溴化物的光降解是已知的基本化学反应)(Pierpoint et al., 2003);然而不能排除复杂的土壤混合物中还存在的许多其他的降解途径(Feo et al., 2014).
光照强度是有机物光降解过程中的一个重要参数(Feo et al., 2014; Bezares-Cruz et al., 2004; Lee et al., 2004; Park et al., 2003).紫外光照反应器中为持续的光强,并且强度高于太阳光,因此紫外光的光降解速率高于太阳光.紫外光照8 h后产物已累积生成82%,此后中间产物开始发生光降解逐渐减少;在自然光照条件下的光降解速率相对较慢,中间产物在光照64 h后累积达最大值99%,此时BDE-209几乎完全分解.这与Sderstrm 等(2004)实验结果相符.Lee等(2004)发现有机物双酚A的光降解速率随着紫外光强度的增加而增加.这一实验结果表明,室内虚拟紫外光与室外自然光照是具有可比性的,并且PBDEs的光降解反应在持续和非持续照射的光源下均可产生,因此PBDEs在非持续的太阳光照的情况下也会发生降解.自然光中的紫外光强度随着地理位置和季节的不同发生变化,夏季光强几乎是冬季的10倍(Josefsson,1996),因此PBDEs的自然光降解很可能随着季节和地点的不同发生变化.
BDE-209在光降解的过程中形成中间产物PBDEs.BDE-153和BDE-154是光降解初期生成量最大的降解产物,占产物总量的60%.低溴态的BDEs随后逐渐产生,并在紫外光照8 h和太阳光照64 h产物累积量分别达最大值后开始减少.这一结果表明,BDE-209的光降解过程是逐渐脱溴的过程,有机溴化物吸收紫外线然后逐步进行脱溴(Shih and Wang, 2009).在太阳光照下,PBDEs负载在自然环境介质如土壤、金属氧化物、沉积物等中进行还原脱溴生成低溴态产物(Josefsson,1996; Ahn et al., 2006).由实验结果可知,光降解过程可能是PBDEs在自然环境中的重要降解途径.
4.3 温度和pH对土壤中PBDEs自然降解过程的影响根据以往相关研究显示,自然界中PBDEs的排放和分布过程受环境温度的控制,如高温环境的蒸发和低温环境的冷凝沉降(Wania and Mackay, 1993; Hoff et al., 1996; Melymuk,2012).Ikonomou 等(2002)的研究结果显示,BDE-47在远距离传播过程中具有相对较高的效率,尤其是在夏季温度较高有利于挥发扩散.近期,Ge等(2014)检测到环境中的PBDEs在冬季的含量是夏季的两倍多,并且在许多采样点只有冬季才监测到PBDEs.本次实验结果显示,BDE-209降解生成的低溴态化合物(三溴至七溴)的浓度在模拟夏季高温的条件下较高,降解产物PBDEs浓度与环境温度呈现良好的正相关性.由此可推断,夏季高温有利于PBDEs的降解转化,然而仍需要进一步的研究探索来验证这一结论.
土壤pH实验结果显示,改变土壤的pH值可促进PBDEs的自然降解,在弱碱性土壤中的降解速率最大,这与Kang和Ge(2010)研究的土柱中PAH在不同pH值下的迁移变化结果相似.此类有机物的降解行为与本次研究结果相符,表明碱性土壤有利于PBDEs的自然降解.因此,可以通过改变土壤pH值的控制措施来改善被PBDEs污染的地区的土壤.
5 结论(Conclusions)1)一定浓度的臭氧能促进土壤中PBDEs的自然降解,臭氧浓度越高PBDEs的降解速率越大;但随着土壤深度的加深降解速率逐渐减小.
2)PBDEs的光降解速率随光强的增加而增加,且在持续和非持续照射的光源照射下均可进行光降解,光降解过程可能是PBDEs在自然环境中的重要降解途径.
3)夏季高温有利于PBDEs的自然降解.改变土壤pH值可促进PBDEs的降解,不同pH值的土壤中降解速率的大小依次为: 弱碱性>弱酸性>酸性>中性.
4)PBDEs的降解过程是逐步脱溴的过程.PBDEs的降解反应过程既包括了BDE-209的降解,也包括了中间产物∑7PBDEs的降解.在BDE-209去除率达到一定程度且中间产物逐渐积累到一定量时,中间产物的降解反应会逐渐变成主导反应,致使PBDEs总量逐渐降低.
| [1] | Ahn M Y, Filley T R, Jafvert C T, et al. 2006. Photodegradation of decabromodiphenyl ether adsorbed onto clay minerals, metal oxides, and sediment[J]. Environmental Science & Technology, 40(1):215-220 |
| [2] | Bezares-Cruz J, Jafvert C T, Hua I. 2004. Solar photodecomposition of decabromodiphenyl ether:products and quantum yield[J]. Environmental Science & Technology, 38(15):4149-4156 |
| [3] | Chen J W, Guo Z M. 2012. The summer high temperature climate characteristics and abnormal flow analysis of Fugang county[J]. Guangdong Meteorology, 34:33-34 |
| [4] | 陈海, 孙云娜, 魏东洋. 2011. 溴代阻燃剂的环境危害[J]. 广东化工, 38(8):91-92 |
| [5] | 陈社军, 麦碧娴, 曾永平, 等. 2005. 珠江三角洲及南海北部海域表层沉积物中多溴联苯醚的分布特征[J]. 环境科学学报, 25(9):1265-1271 |
| [6] | 陈涛, 周纯, 牟义军, 等. 2011. 典型电子废物集中处置场地及周边土壤中多溴联苯醚的污染特征[J]. 生态与农村环境学报, 27(3):20-24 |
| [7] | Choi H K, Kim Y Y, Lim H, et al. 2001. Oxidation of polycyclic aromatic hydrocarbons by ozone in the presence of sand[J]. Water Science & Technology, 43, 349-356 |
| [8] | Christensen J H, Glasius M, Pécseli M, et al. 2002. Polybrominated diphenyl ethers (PBDEs) in marine fish and blue mussels from southern Greenland[J]. Chemosphere, 47(6):631-638 |
| [9] | Ding L J, Wang C L, Ling L X. 2011. Spatial-temporal variation characteristics of average temperature in Guangdong[J]. Chinese Journal of Agrometeorology, 32, 500-506 |
| [10] | Feo M L, Gonzalez O, Baron E, et al. 2014. Advanced UV/H2O2 oxidation of deca-bromo diphenyl ether in sediments[J]. Science of the Total Environment, 479/480:17-20 |
| [11] | 傅海辉. 2012. 多溴联苯醚(PBDEs)污染土壤热脱附实验研究[D]. 西安:西北农林科技大学. 23-24 |
| [12] | Gao S T, Hong J W, Yu Z Q, et al. 2011. Polybrominated diphenyl ethers in surface soils from e-waste recycling areas and industrial areas in South China:Concentration levels, congener profile, and inventory[J]. Environmental Toxicology and Chemistry, 30(12):2688-2696 |
| [13] | Ge J, Liu M X, Yun X Y, et al. 2014. Occurrence, distribution and seasonal variations of polychlorinated biphenyls and polybrominated diphenyl ethers in surface waters of the East Lake, China[J]. Chemosphere, 103:256-262 |
| [14] | Guo L L, Qiu Y W, Zhang G, et al. 2008. Levels and bioaccumulation of organochlorine pesticides (OCPs) and polybrominated diphenyl ethers (PBDEs) in fishes from the Pearl River estuary and Daya Bay, South China[J]. Environmental Pollution, 152(3):604-611 |
| [15] | Guo Z X, Wang J, Chai M, et al. 2011. Spatiotemporal variation of soil pH in Guangdong Province of China in past 30 years[J]. Chinese Journal of Applied Ecology, 22(2):425-430 |
| [16] | Hites R A. 2004. Polybrominated diphenyl ethers in the environment and in people:A meta-analysis of concentrations[J]. Environmental Science & Technology, 38(4):945-956 |
| [17] | Hoff R M, Strachan W M J, Sweet C W, et al. 1996. Atmospheric deposition of toxic chemicals to the Great Lakes:A review of data through 1994[J]. Atmospheric Environment, 30(20):3505-3527 |
| [18] | 黄熙灯. 2014. 珠三角首要污染物由PM2.5变臭氧[N]. 信息时报, http://gd.sina.com.cn/news/m/2014-05-20/0908100865.html. |
| [19] | Ikonomou M G, Rayne S, Addison R F. 2002. Exponential Increases of the brominated flame retardants, polybrominated diphenyl ethers, in the Canadian Arctic from 1981 to 2000[J]. Environmental Science & Technology, 36(9):1886-1892 |
| [20] | 纪录. 2004. 原位臭氧化法处理模拟土壤中的多环芳烃[D]. 武汉:武汉大学. 13-16 |
| [21] | Josefsson W. 1996. Five years of solar UV-radiation monitoring in Sweden[R]. SMHI |
| [22] | Kang Y, Ge X L. 2010. Simulation experiments on influences of pH level on the vertical migration of polycyclic aromatic hydrocarbons in soils[J]. Rock and Mineral Analysis, 29(2):123-126 |
| [23] | Kim J, Choi H. 2002. Modeling in situ ozonation for the remediation of nonvolatile PAH-contaminated unsaturated soils[J]. Journal of Contaminant Hydrology, 55(3/4):261-285 |
| [24] | Lee J M, Kim M S, Kim B W. 2004. Photodegradation of bisphenol-A with TiO2 immobilized on the glass tubes including the UV light lamps[J]. Water Research, 38(16):3605-3613 |
| [25] | Lee R G M, Thomas G O, Jones K C. 2004. PBDEs in the atmosphere of three locations in Western Europe[J]. Environmental Science & Technology, 38(3):699-706 |
| [26] | Leung A O W, Luksemburg W J, Wong A S, et al. 2007. Spatial distribution of polybrominated diphenyl ethers and polychlorinated dibenzo-p-dioxins and dibenzofurans in soil and combusted residue at Guiyu, an electronic waste recycling site in Southeast China[J]. Environmengtal Science & Technology, 41(8):2730-2737 |
| [27] | Levenspiel O. 1999. in chemical reaction engineering, third ed[M]. New York:John Wiley & Sons. 523-539 |
| [28] | Luross J M, Alaee M, Sergeant D B, et al. 2002. Spatial distribution of polybrominated diphenyl ethers and polybrominated biphenyls in lake trout from the Laurentian Great Lakes[J]. Chemosphere, 46(5):665-672 |
| [29] | Melymuk L. 2012. Semi-volatile Organic Contaminants in the Urban Atmosphere:Spatial and Seasonal Distributions and Implications for Contaminant Transport[D]. Toronto:University of Toronto. 155 |
| [30] | M ller A, Xie Z Y, Caba A, et al. 2012. Occurrence and air-seawater exchange of brominated flame retardants and Dechlorane plus in the North Sea[J]. Atmospheric Environment, 46:346-353 |
| [31] | Nelson C H, Brown R A. 1994. Adapting ozonation for soil and ground water cleanup[J]. Chemical Engineering Journal, 9(1):EE18-EE25 |
| [32] | Park S E, Joo H, Kang J W. 2003. Photodegradation of methyl tertiary butyl ether (MTBE) vapor with immobilized titanium dioxide[J]. Solar Energy Materials and Solar Cells, 80(1):73-84 |
| [33] | Pierpoint A C, Hapeman C H, Torrents A. 2003. Ozone treatment of soil contaminated with aniline and trifluralin[J]. Chemosphere, 50(8):1025-1034 |
| [34] | Shih Y H, Wang C K. 2009. Photolytic degradation of polybromodiphenyl ethers under UV-lamp and solar irradiations[J]. Journal of Hazardous Materials, 165(1/3):34-38 |
| [35] | S derstr m G, Sellstr m U, de Wit C A, et al. 2004. Photolytic debromination of decabromodiphenyl ether (BDE 209)[J]. Environmental Science & Technology, 38(1):127-132 |
| [36] | Sung M, Huang C P. 2002. In situ removal of 2-chlorophenol from unsaturated soils by ozonation[J]. Environmental Science & Technology, 36(13):2911-2918 |
| [37] | Tian M, Chen S J, Wang J, et al. 2011. Brominated flame retardants in the atmosphere of e-waste and rural sites in southern China:seasonal variation, temperature dependence, and gas-particle partitioning[J]. Environmental Science & Technology, 45(20):8819-8825 |
| [38] | Venier M, Ma Y N, Hites R A. 2012. Bromobenzene flame retardants in the Great Lakes atmosphere[J]. Environmental Science & Technology, 46(16):8653-8660 |
| [39] | Wania F, Mackay D. 1993. Global fractionation and cold condensation of low volatility organochlorine compounds in polar regions[J]. Ambio, 22(1):10-18 |
| [40] | Watts R J, Dilly S E. 1996. Evaluation of iron catalysts for the Fenton-like remediation of diesel-contaminated soils[J]. Journal of Hazardous Materials, 51(1/3):209-224 |
| [41] | Wu J P, Luo X J, Zhang Y, et al. 2008. Bioaccumulation of polybrominated diphenyl ethers (PBDEs) and polychlorinated biphenyls (PCBs) in wild aquatic species from an electronic waste (e-waste) recycling site in South China[J]. Environment International, 34(8):1109-1113 |
| [42] | 杨辉. 2012. 珠三角刚赶走PM2.5污染又陷臭氧污染[N]. 羊城晚报, http://news.ycwb.com/2012-03/28/content_3756133.htm. |
| [43] | Zhang H, Song M H, Huang C P. 2003. One dimensional model of in-situ ozonation for the remediation of phenanthrene-contaminated soil[J]. Jounal of Chemical Engineering of Chinese Universities, 17:466-470 |
| [44] | 张亮, 廖海清, 郭建阳, 等. 2011. 成渝经济区河流表层沉积物中多溴联苯醚的分布特征[J]. 环境科学研究, 24(8):842-849 |
 2015, Vol. 35
2015, Vol. 35


