2. 山西大学环境科学研究所, 太原 030006
2. Institute of Environmental Science, Shanxi University, Taiyuan 030006
大气细颗粒物(PM2.5,即空气动力学直径≤2.5 μm的颗粒)是灰霾天气发生时的首要污染物,由于PM2.5较易吸附空气中的有毒有害物质(如重金属、挥发性有机化合物和多环芳烃等),且可以进入下呼吸道到达肺泡,因而对人体健康产生严重威胁(Perrone et al., 2010;Boublil et al., 2013).流行病学研究表明,灰霾可以增加急性呼吸道疾病、支气管哮喘、心血管系统疾病及皮肤病的发病率,甚至和糖尿病的发生呈正相关(Pui et al., 2014;Goldberg et al., 2001),而这些影响的发生主要与灰霾天气下大气PM2.5浓度增高有关(阚海东等,2002).
近年来,灰霾天气在我国各地时有发生,尤其京津冀、长三角等地有愈演愈烈的趋势,有关灰霾的健康影响及毒理机制正受到越来越多的关注(Gualtieri et al., 2010;Zhang et al., 2008;Lee et al., 2014).基于此,本文以山西省太原市发生严重灰霾天气时采集的大气PM2.5为实验材料,通过体外染毒试验,研究PM2.5对肺泡巨噬细胞(AM)存活率、胞内超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)、丙二醛(MDA)、活性氧(ROS)水平及Ca2+浓度的影响,并观察细胞凋亡程度,旨在从AM氧化损伤和细胞凋亡方面揭示灰霾PM2.5的健康危害效应和毒理机制.
2 材料与方法(Materials and methods) 2.1 主要试剂与仪器主要试剂:RPMI-1640培养基(Thermo Fisher公司),小牛血清(浙江天杭生物有限公司),牛血清蛋白(BSA)、胰蛋白酶、四甲基偶氮唑盐(MTT)(Solarbio公司),二甲基亚砜(DMSO)、考马斯亮蓝-G250(Sigma公司),SOD试剂盒、MDA试剂盒、GSH-Px试剂盒(南京建成公司),活性氧(ROS)检测试剂盒、钙离子荧光探针Fluo-3 AM(碧云天),Annexin V/PI细胞凋亡检测试剂盒(Invitrogen公司).
主要仪器:高速低温离心机(Sigma,Germany)、酶标仪(Bio-rad Model 550)、细胞恒温培养箱(Thermo,美国)、Accuri C6流式细胞仪(BD,美国).
2.2 颗粒物的采集及制备大气PM2.5采样地点位于山西大学环境与资源学院楼顶,距地面约20 m,采样时间为2011年12月30—31日,采样期间气温-8.1~1.2 ℃,相对湿度50.3%~86.8%,能见度0.1~1.0 km,风速0~1级,气溶胶在线检测仪8530(美国TSI仪器公司)测得PM2.5日平均质量浓度为957 μg · m-3,为典型的灰霾天气(曹玲娴等,2014).使用大流量(1.13 m3 · min-1)大气PM2.5采样器(Thermo Andersen)采集样品,采样膜为石英纤维滤膜(Whatman).采样结束后,将载有PM2..5的石英纤维滤膜称重、剪碎后放入Milli-Q超纯水中超声振荡以洗脱颗粒物,收集悬浮液并真空冷冻干燥,低温保存,实验时用0.9%生理盐水配成母液(耿红等,2006a).
2.3 大鼠AM的提取与培养每次实验选取体重为220~250 g的清洁、健康雄性Wistar大鼠3只,每只注射1.2 mL 1%的戊巴比妥钠,待全身麻醉后,腹主动脉放血致死,用灭菌的磷酸盐缓冲液(PBS,pH=7.0)灌洗双肺,将肺泡灌洗液(BLAF)于3000 r · min-1、4 ℃下离心10 min.弃上清液,细胞沉淀用含10%小牛血清的培养液洗涤2次,制成细胞悬浮液.用台盼蓝拒染法计数,稀释细胞浓度为2×106个 · mL-1,分装于细胞培养皿,放于37 ℃、5%CO2培养箱中孵育2 h.弃原培养液,用PBS清洗2次,去除非贴壁细胞和原培养液成分,此时AM纯度可达95%以上.
加入不同浓度的灰霾PM2.5悬浮液染毒,终浓度分别为33、100、300 μg · mL-1,同时设阴性对照组(只加培养液和同量的生理盐水).染毒4 h后,用胰酶消化收集细胞,进行SOD、MDA、GSH-Px、ROS、Ca2+浓度和细胞凋亡的测定.
2.4 AM存活率的测定采用MTT法测定细胞存活率.将浓度为1.5×105个 · mL-1的AM细胞悬浮液加入96孔培养板,每孔添加100 μL,于37 ℃细胞培养箱中培养2 h.之后吸出培养液,添加不同浓度的PM2.5染毒液,同时设置对照组.培养4 h后,吸出染毒液,每孔添加120 μL含MTT的培养液继续培养4 h.然后吸出MTT溶液,用PBS清洗一次后,每孔添加150 μL DMSO,室温下缓慢摇晃至蓝紫色结晶全部溶解,酶标仪490 nm处测定吸光值.
2.5 各指标的测定方法 2.5.1 SOD、GSH-Px、MDA测定采用试剂盒进行测定,按照试剂盒说明进行操作,用酶标仪测量其吸光值,并分别计算出SOD、GSH-Px活性和MDA含量.
2.5.2 ROS测定贴壁2 h后收集AM于2 mL EP管中,PBS清洗1次,按照1∶2500的比例用无血清培养液稀释DCFH-DA(二氯二氢荧光素-乙酰乙酸酯),每管添加DCFH-DA工作液1 mL,37 ℃孵育25 min后,3000 r · min-1离心10 min,PBS清洗3次.然后添加不同浓度灰霾PM2.5染毒液对细胞进行染毒4 h,并且提前30 min对阳性对照管添加Rosup刺激物.4 h后,打匀细胞,过滤(200目),用流式细胞仪检测ROS,检测的荧光强度可反应细胞内ROS水平.
2.5.3 Ca2+浓度的测定染毒4 h后收集AM于2 mL EP管中,PBS清洗3次,按1∶5000的比例用DMSO稀释Fluo-3 AM,每管添加Fluo-3 AM工作液1 mL,37 ℃孵育30 min后,3000 r · min-1离心10 min,PBS再次清洗,最后用1 mL PBS重悬,打匀细胞,每孔添加200 μL于96孔板,用多功能酶标仪进行荧光检测.分别设定激发波长488 nm,发射波长525 nm,测定静息荧光值F,然后加入终浓度为0.1%的Triton-X 100溶液,测得最大荧光值Fmax,再加入0.05 mol · L-1的EDTA溶液,测得最小荧光值Fmin.按下面公式计算Ca2+浓度:
[Ca2+]=Kd ·(F-Fmin)/(Fmax-F)
式中,Kd为荧光剂与结合反应的解离常数,取值为400 nmol · L-1.
2.5.4 细胞凋亡的测定染毒4 h后收集AM于2 mL EP管中,预冷PBS清洗2次,将细胞重悬于100 μL 1×annexin binding-buffer,使浓度稀释为1×106个 · mL -1,每个待测样品分别加入5 μL Annexin V和1 μL PI,避光室温培养15 min,最后添加400 μL 1×annexin binding-buffer,过滤(200目),上流式细胞仪检测,通过二维点图以双参数显示结果.获得的细胞散点图由4个象限组成,散点图左下象限代表活细胞,右上象限代表晚期凋亡细胞,右下象限代表早期凋亡细胞.
2.6 统计方法实验数据以平均值±标准误差(Mean±SD)表示,用Origin 8.0软件进行数据统计分析,采用one-way ANOVA单因素方差分析,并用LSD检验法进行两两比较,p<0.05表示差异有显著性.
3 结果(Results) 3.1 不同浓度PM2.5对AM 存活率的影响实验结果(图 1)表明:随着灰霾PM2.5悬浮液浓度的增大,AM的存活率呈降低趋势,依次降低了3.7%、12.3%和19.9%,但33 μg · mL-1和100 μg · mL-1染毒组与对照组相比,差异不显著,300 μg · mL-1染毒组与对照组相比出现显著差异(p<0.05).
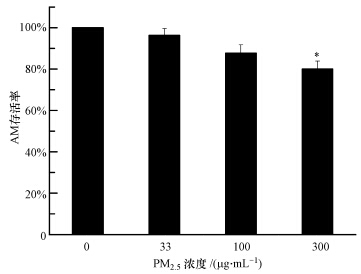 |
| 图 1 灰霾PM2.5对AM存活率的影响(n=5,与对照组相比,*p<0.05) Fig. 1 Effects of haze PM2.5 on the survival rate of AM(n=5,compared to the control,*p<0.05) |
如图 2所示,不同浓度灰霾PM2.5悬浮液处理大鼠AM细胞后,其SOD活性(以prot计)随着染毒浓度的增大而减小,且呈现剂量-效应关系.染毒组SOD活性与对照组相比,分别降低了37%、40.7%、50.2%,各浓度处理组与对照组相比差异显著(p<0.05或p<0.01),但染毒组之间没有显著差异.
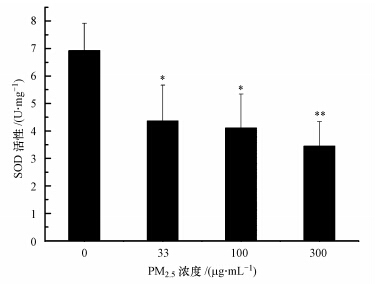 |
| 图 2 灰霾PM2.5对AM中SOD活性的影响(n=5,与对照组相比,*p<0.05,* *p<0.01) Fig. 2 Effects of PM2.5 on the activity of SOD in AM(n=5,compared to the control,*p<0.05,* *p<0.01) |
由图 3可以看出,随着灰霾PM2.5悬浮液浓度的增加,AM中GSH-PX活性(以prot计)呈递减趋势,浓度为33、100 μg · mL-1时,与对照组相比无显著差异,当浓度为300 μg · mL-1时,GSH-Px活性比对照组降低了12.6%,且差异显著(p<0.05),但各染毒组之间GSH-Px活性差异不显著.
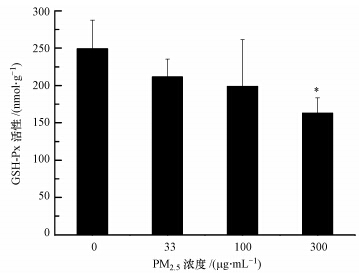 |
| 图 3 灰霾PM2.5对AM中GSH-Px活性的影响(n=5,与对照组相比,*p<0.05) Fig. 3 Effects of haze PM2.5 on the activity of GSH-Px in AM(n=5,compared to the control,*p<0.05) |
由图 4可以看出,各染毒组MDA含量(以prot计)随着灰霾PM2.5悬浮液浓度的增大而显著增加,与对照组相比,3个染毒组MDA含量分别增加了0.55、0.67、3.76倍,差异显著(p<0.05或 p<0.01).300 μg · mL-1染毒组与其他浓度染毒组相比,也具有显著差异(p<0.05),说明高染毒浓度组造成AM严重的脂质过氧化.
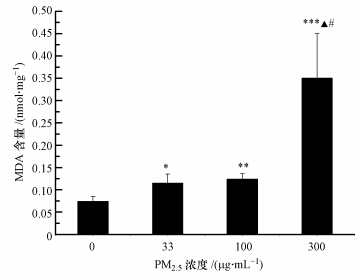 |
| 图 4 灰霾PM2.5对AM中MDA含量的影响(n=5,与对照组相比,*p<0.05,* *p<0.01,* * *p<0.001;与33 μg · mL-1染毒组相比,▲p<0.05;与100 μg · mL-1染毒组相比,#p<0.05) Fig. 4 Effects of haze PM2.5 on the content of MDA in AM(n=5,compared to the control,*p<0.05,* *p<0.01,* * *p<0.001; compared to the treatment of 33 μg · mL-1,▲p<0.05; compared to the treatment of 100 μg · mL-1,#p<0.05) |
如图 5所示,随着灰霾PM2.5染毒浓度的增大,AM内ROS的平均荧光强度逐渐升高,呈剂量-效应关系.浓度为33、100和300 μg · mL-1时,平均荧光强度分别是对照组的1.25、1.51和1.62倍,染毒浓度大于100 μg · mL-1时,与对照相比差异显著(p<0.01或p<0.001).而且300 μg · mL-1染毒组与33 μg · mL-1染毒组相比,也具有显著差异(p<0.05).
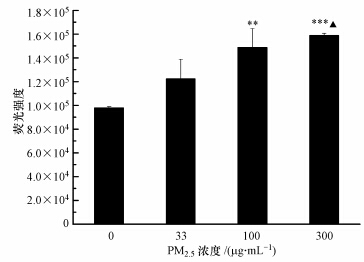 |
| 图 5 灰霾PM2.5对AM中ROS含量的影响(n=5,与对照组相比,* *p<0.01,* * *p<0.001;与33 μg · mL-1染毒组相比,▲p<0.05 ) Fig. 5 Effects of haze PM2.5 on the cellular ROS level(n=5,compared to the control,* *p<0.01,* * *p<0.001; compared to the treatment of 33 μg · mL-1,▲p<0.05) |
如图 6所示,随着灰霾PM2.5悬浮液浓度的增大,胞质内游离Ca2+浓度增加,且存在一定的剂量依赖关系.与对照组相比,染毒浓度为300 μg · mL-1时,出现了极显著差异(p<0.001),而与其它染毒组相比,高浓度染毒组也出现了显著差异(p<0.05).
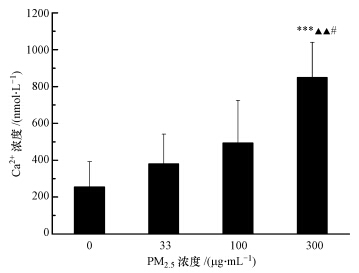 |
| 图 6 灰霾PM2.5对AM中Ca2+浓度的影响(n=5,与对照组相比,* * *p<0.001;与33 μg · mL-1染毒组相比,▲▲p<0.01;与100 μg · mL-1染毒组相比,#p<0.05) Fig. 6 Effects of haze PM2.5 on cellular Ca2+ concentration(n=5,compared to the control,* * *p<0.001; compared to the treatment of 33μg · mL-1,▲▲p<0.01; compared to the treatment of 100 μg · mL-1,#p<0.05) |
从图 7可以看出,对照组与3个染毒组细胞早期凋亡率依次为3.3%、4.2%、4.7%、5.1%,呈升高趋势.5次实验数据统计分析表明(表 1),随着灰霾PM2.5染毒浓度的升高,AM的早期凋亡率也逐渐升高,与对照组相比,当PM2.5处理浓度大于100 μg · mL-1时,差异显著(p<0.05),300 μg · mL-1染毒组与33 μg · mL-1染毒组相比,差异也显著(p<0.05).
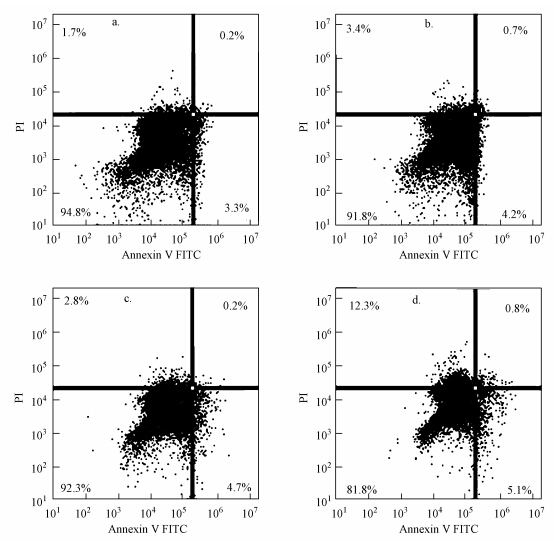 |
| 图 7 流式细胞仪测定AM凋亡图(a.阴性对照组;b.33 μg · mL-1染毒组;c.100 μg · mL-1染毒组;d.300 μg · mL-1染毒组) Fig. 7 The figures of AM apoptosis by FCM(a.control;b.the treatment of 33 μg · mL-1;c.the treatment of 100 μg · mL-1;d.the treatment of 300 μg · mL-1) |
| 表 1 不同浓度的灰霾PM2.5对AM凋亡率的影响 Table 1 Effects of haze PM2.5 on the apoptosis rate of AM |
肺泡巨噬细胞(AM)是呼吸系统重要的免疫防御细胞.当大气PM2.5随着呼吸进入肺泡后,AM发挥吞噬、免疫和分泌作用,对其及时进行清除.但当PM2.5浓度超过一定量后,就会引起AM一系列生理生化指标的变化,甚至发生损伤与凋亡(徐佳等,2008).
本实验结果证实,灰霾PM2.5处理AM后,可以使AM发生氧化损伤和凋亡,并呈现剂量-效应关系,说明灰霾PM2.5浓度越高,对AM的毒性作用越大.在测定各氧化损伤指标中,SOD和GSH-Px是两种重要的抗氧化酶,可以清除体内的超氧阴离子(O2-)、H2O2等活性氧和自由基,其活性大小可以间接反映细胞清除活性氧和自由基的能力(宋姗娟等,2014);MDA是脂质过氧化的最终产物,是细胞受损伤的标志,其本身又会对细胞造成一定伤害,MDA的生成量间接反映细胞受氧化损伤的程度(Geng et al., 2005).当体内活性氧浓度过高时,SOD和GSH-Px活性会下降,MDA含量会上升(徐雯等,2013).本实验发现,大于33 μg · mL-1的灰霾PM2.5即可使MDA含量显著升高(p<0.05),会使AM发生脂质过氧化,随着PM2.5浓度增大,细胞脂质过氧化程度也增大,这与郭翔等(2012)的实验结论一致.同时,灰霾PM2.5可使AM胞内活性氧水平显著提高(特别是高浓度组),进一步说明AM的脂质过氧化极有可能是由ROS增高引起的.这些由灰霾PM2.5诱导产生的ROS一方面可以直接和抗氧化物酶(如SOD、GSH-Px)反应,降低它们的活性(Pamplona et al., 2011),如图 2和图 3所示;另一方面,过量的ROS还可以对细胞的DNA、RNA和蛋白质造成损伤,破坏正常的细胞周期,从而导致细胞的早期凋亡(图 7和表 1),并导致细胞存活率降低(图 1)(Azad et al., 2009).
细胞对外界环境的刺激反应是通过胞质内Ca2+浓度的变化来传递的,氧化应激可导致细胞内游离Ca2+浓度升高,破坏细胞内的钙稳态,引发一系列的不良反应(Grover et al., 2003);同时,胞质内高浓度的Ca2+又会导致更多自由基或ROS产生(Clausen et al., 2013),使细胞受到氧化损伤.本研究中灰霾PM2.5使细胞内Ca2+浓度显著升高,表明细胞内的钙稳态已遭到破坏.高浓度Ca2+和ROS可引发线粒体膜通透性转运孔道开放,使大量凋亡相关蛋白从线粒体膜间隙释放出来(刘健康等,2012),从而诱导AM发生凋亡,该凋亡的发生说明灰霾PM2.5对细胞的损伤很可能是通过过量ROS和Ca2+浓度升高而介导的.
除了作用剂量外,灰霾PM2.5的毒性作用与它所含成分紧密相关(耿红等,2006b;Ghio et al., 2012).本实验所用的灰霾PM2.5的化学成分特征与非霾样品有较大不同(曹玲娴等,2014).灰霾PM2.5中的重金属Pb、As、Hg含量,水溶性阴离子Cl-、SO2-4、NO-3、F-和阳离子K+、Na+含量,以及OC和EC比值均高于非灰霾样品.可见,灰霾发生时,大气PM2.5携带了更多人为污染物质,如Pb、As、Hg元素、二次气溶胶、化石燃料的燃烧产物等.正是由于这些人为污染物的增多使得灰霾PM2.5成分更复杂,对AM的氧化损伤作用可能更强烈.
5 结论(Conclusions)研究表明,太原市冬季灰霾PM2.5导致大鼠肺泡巨噬细胞抗氧化物酶(SOD、GSH-Px)活性降低,ROS含量和Ca2+浓度增加,脂质过氧化水平和早期凋亡率上升,细胞存活率下降.说明冬季灰霾天气下大气细颗粒物可对AM造成氧化损伤,该损伤作用的产生可能与灰霾PM2.5含有的大量二次气溶胶、重金属及煤炭燃烧产物有关.
| [1] | Azad M B,Chen Y,Gibson S B. 2009.Regulation of autophagy by reactive oxygen species (ROS): implications for cancer progression and treatment[J].Antioxidants & Redox Signaling,11(4): 777-790 |
| [2] | Boublil L,Assémat E,Borot M C,et al.2013.Development of a repeated exposure protocol of human bronchial epithelium in vitro to study the long-term effects of atmospheric particles[J].Toxicology in Vitro,27(2): 533-542 |
| [3] | 曹玲娴,耿红,姚晨婷,等.2014.太原市冬季灰霾期间大气细颗粒物化学成分特征[J].中国环境科学,34(4): 837-843 |
| [4] | Clausen A, McClanahan T, Ji S G, et al. 2013. Mechanisms of rapid reactive oxygen species generation in response to cytosolic Ca2+ or Zn2+ loads in cortical neurons[J]. PLoS One, 8(12):e83347. doi: 10.1371/journal.pone.0083347 |
| [5] | 耿红,孟紫强,张全喜.2006a.沙尘暴细颗粒物对大鼠肺泡巨噬细胞膜损伤[J].中国公共卫生,22(2): 144-146 |
| [6] | 耿红,孟紫强,张全喜.2006b.沙尘暴PM2.5水溶和有机成分对巨噬细胞的损伤[J].中国环境科学,26(1): 20-24 |
| [7] | Geng H,Meng Z Q,Zhang Q X.2005.Effects of blowing sand fine particles on plasma membrane permeability and fluidity,and intracellular calcium levels of rat alveolar macrophages [J].Toxicology Letters,157(2): 129-137 |
| [8] | Ghio A J,Carraway M S,Madden M C.2012.Composition of air pollution particles and oxidative stress in cells,tissues,and living systems[J].Journal of Toxicology and Environmental Health,Part B,15(1): 1-21 |
| [9] | Goldberg M S,Burnett R T,Brook J,et al.2001.The association between daily mortality and ambient air particle pollution in Montreal,Quebec.1.Nonaccidental mortality[J].Environmental Research,86(1): 12-25 |
| [10] | Grover A K,Samson S E,Robinson S,et al.2003.Effects of peroxynitrite on sarcoplasmic reticulum Ca2+ pump in pig coronary artery smooth muscle [J].American Journal of Physiology-Cell Physiology,284(2): 294-301 |
| [11] | Gualtieri M,Ørevik J,Holme J,et al.2010.Differences in cytotoxicity versus pro-inflammatory potency of different PM fractions in human epithelial lung cells[J].Toxicology in Vitro,24(1): 29-39 |
| [12] | 郭翔,闫庆倩,赵学彬,等.2012.不同地区大气PM2.5对大鼠肺泡巨噬细胞毒性作用的实验研究[J].环境与健康杂志,29(1): 12-15 |
| [13] | 阚海东,陈秉衡.2002.我国大气颗粒物暴露与人群健康效应的关系[J].环境与健康杂志,19(6): 422-424 |
| [14] | Lee K Y,Wong C K C,Chuang K J,et al.2014.Methionine oxidation in albumin by fine haze particulate matter: Anin vitro and in vivo study[J].Journal of Hazardous Materials,274: 384-391 |
| [15] | 刘健康,王学敏.2012.线粒体医学与健康[M].北京: 科学出版社.82-86 |
| [16] | Pamplona R,Costantini D.2011.Molecular and structural antioxidant defenses against oxidative stress in animals[J].American Journal of Physiology-Regulatory,Integrative and Comparative Physiology,301(4): R843-R863 |
| [17] | Perrone M G,Gualtieri M,Ferrero L,et al.2010.Seasonal variations in chemical composition and in vitro biological effects of fine PM from Milan[J].Chemosphere,78(11): 1368-1377 |
| [18] | Pui D Y H,Chen S C,Zuo Z L.2014.PM2.5 in China: Measurements,sources,visibility and health effects,and mitigation [J].Particuology,13(2): 1-26 |
| [19] | 宋姗娟,魏海英,刘婷,等.2014.菲对肺泡巨噬细胞的毒性作用[J].环境化学,33(4): 551-555 |
| [20] | 徐佳,牛静萍,丁国武,等.2008.兰州市大气细颗粒物对大鼠肺泡巨噬细胞吞噬功能的影响[J].环境与健康杂志,25(3): 243-245 |
| [21] | 徐雯,江俊康,杨北平,等.2013.不同粒径汽车尾气颗粒物对A549细胞毒性作用的比较[J].环境科学学报,33(12): 3407-3412 |
| [22] | Zhang Y X,Schauer J J,Zeng Y H,et al.2008.Characteristics of particulate carbon emissions from real-world Chinese coal combustion[J].Environmental Science & Technology,42(14): 5068-5073 |
 2015, Vol. 35
2015, Vol. 35


