随着我国城市化水平的提高,城市生活垃圾日益增多.目前,我国生活垃圾的处理处置方式主要有卫生填埋、焚烧、堆肥和综合利用等.其中,卫生填埋在国内外垃圾处理方式中所占的比例高达80%,也是我国应用最为广泛的垃圾处理技术(杨帆,2012).然而生活垃圾填埋场会产生大量温室气体,其主要成分为CH4和CO2,分别约占填埋气的30%~70%和20%~50%(Humer et al., 1999;Kallistova et al., 2005;Zamorano et al., 2007),而CH4的温室效应是等质量CO2的25倍(IPCC,2007).据有关资料预测,我国垃圾填埋场的CH4释放量将在10年内达到3.60×108 t(以CO2当量计),占全国甲烷排放量的31%(张相锋等,2010).根据相关资料显示,在未来两百年内CH4排放量仍将快速上升,若不对填埋场进行CH4减排,预计到2030年大气中CH4浓度将达2.34 μL · L-1(李春瑛等,2005).因此,填埋场CH4的减排已经成为全球各地学者及政府关注的焦点.
目前,国内外学者已对垃圾填埋场覆盖层甲烷氧化作了大量研究,主要侧重于好氧甲烷氧化单菌的分离筛选(Hatamoto et al., 2010;王晓丽等,2008)、新型覆盖材料的选择(Wang et al., 2011;杨文静等,2010)及甲烷氧化机理探讨(Wilshusen et al., 2004;华绍烽等,2006)等方面.而对填埋场普遍存在的覆盖土甲烷氧化效果差、覆盖土资源短缺等问题仍缺乏较好的对策.此外,作为一种经济有效的CH4减排方法,高效生物强化剂(甲烷氧化菌)的筛选及施用仍然未得到重视.
甲烷氧化菌是甲基营养菌的一种,它能以CH4为唯一碳源进行生长.目前,有关于甲烷氧化菌纯培养物培养条件的研究较多,刑新会等进行了有关化学物质提高甲烷氧化菌M. trichosporium OB3b生长速度的可能性研究,结果表明,向培养液中添加15 μmol · L-1的柠檬酸盐可大大提高细胞的浓度(3~4倍),并且在第7 d获得最高的细胞浓度,高达0.75 g · L-1(以干细胞计)(Xing et al., 2006).Park等(1991)向M. trichosporium OB3b中加入了10 μmol · L-1的铜离子,其细胞浓度在120 h后可达18 g · L-1(以干细胞计).由前人的研究结果所得,M. trichosporium OB3b和M. capsulatus Bath在相同培养条件下比其他甲烷氧化菌的细胞浓度要大(Taylor et al., 1995;Xing et al., 2006),但与甲烷氧化菌的混合培养物相比,其生长速度仍然较慢,生长性能和抗环境冲击能力也较差(罗明芳等,2007).因此,相比而言,甲烷氧化菌的混合培养物较纯培养物在实际应用中具有更大的优势.研究表明,甲烷氧化菌的混合培养物可在缺氮的废水处理反应器中获得2.94 g · L-1(以干细胞计)的细胞浓度(Smith et al.,1997).在续流式搅拌反应器中,甲烷氧化菌的混合培养物同样能获得3.4 g · L-1(以干细胞计)的细胞浓度,每克CH4可获得0.33 g的生物量(Chang et al., 1997).
目前,有关甲烷氧化菌纯培养物的甲烷氧化能力已被深入研究,并已得出甲烷氧化能力最佳的甲烷氧化菌.然而,针对混合培养物的甲烷氧化能力至今仍未出现较为系统的研究,这给甲烷氧化菌混合培养物的应用带来了障碍.因此,筛选最佳的甲烷氧化菌混合培养物显得尤为重要.针对上述问题,本研究对不同分离源甲烷氧化菌的甲烷氧化能力进行对比,筛选出最佳甲烷氧化菌,并对其在不同填埋期CH4浓度下的甲烷氧化能力进行评估,以期得到适应能力和甲烷氧化能力较强的甲烷氧化菌,并将其制备成菌剂,从而为甲烷氧化混合培养物在填埋场中的应用奠定基础.
2 材料与方法(Materials and methods) 2.1 试验材料 2.1.1 驯化材料的采集及其预处理本研究采用的驯化材料为垃圾填埋场普通覆盖土、矿化垃圾、好氧污泥、西湖北里湖底泥,其依据在于这4个分离源分别来自于3个典型的甲烷排放源(填埋场、污水处理厂和湿地),填埋场普通覆盖土和矿化垃圾因在填埋场中受CH4污染的程度极其不同而将其同时作为甲烷氧化菌的筛分源.
填埋场普通覆盖土和矿化垃圾采自浙江省绍兴市平水大坞岙垃圾填埋场,填埋场普通覆盖土为填埋龄10~15 a填埋区的终场覆盖土,矿化垃圾为覆盖土正下方的陈垃圾.好氧污泥采自杭州七格污水处理厂的好氧池.底泥采自西湖北里湖沉积物.将填埋场普通覆盖土和矿化垃圾用4 mm筛进行筛分,去除大块物质;将好氧污泥和底泥进行适当的脱水,使其不以泥水混合物的形式存在.
2.1.2 气体及试剂CH4气体(99.99%)购于杭州今工特种气体有限公司;Na2HPO4、KH2PO4、乙二胺四醋酸四钠、ZnSO4 · 7H2O等试剂购自杭州汇普试剂有限公司.
2.1.3 试液的配制甲烷氧化菌的培养采用NMS培养基(Hanson et al., 1996),其配方如下(mg · L-1):Na2HPO4 72,KH2PO428,EDTA-4Na · 4H2O 1.0,ZnSO4 · 7H2O 0.07,MnCl2 · 4H2O 0.03,H3BO3 0.30,NaMoO4 · 2H2O 0.03,CoCl2 · 6H2O 0.60,CuCl2 · H2O 0.01,NiCl2 · 6H2O 0.02,FeSO4 · 7H2O 0.5,MgSO4 · 7H2O 200,CaCl2 2H2O 20.0,将pH调至6.8,然后灭菌.
2.2 试验设计 2.2.1 甲烷氧化菌的分离和筛选取4种预处理后的分离源样品各10.0 g于100 mL血清瓶中,放入30 ℃的恒温培养箱中过夜培养(12~14 h)后用橡胶塞将血清瓶密封,采用置换法用注射器从血清瓶中抽出一定量的气体后注入等体积CH4,使其浓度为20%(郑军等,2007).随后放入30 ℃恒温培养箱中培养,培养过程中适时监测血清瓶内CH4浓度,当CH4浓度低于50 ppm时换气1次,并采取前述方法注入相同浓度的CH4气体.将各分离源在CH4氛围下持续驯化2个月,期间每隔1个月测定不同分离源甲烷氧化能力,每组分离源均设定3个平行.驯化结束后,取驯化的分离源各1.0 g于250 mL的锥形瓶中,加入100 mL去离子水,放入摇床中振荡10 min,随后将菌悬液进行常压过滤,取其中3 mL接种于装有已灭菌的30 mL NMS培养基的血清瓶中,用橡胶塞密封;采用置换法,使瓶内CH4浓度达到20%,然后置于30 ℃、180 r · min-1的摇床中培养5~7 d直至培养液混浊,取其中0.4 mL培养液作为种子液接种于新鲜的NMS培养液中,如此重复7次,细胞浓度基本稳定,得到能以CH4为唯一碳源和能源的混合菌群.在第7次传代培养时,试验同时设定不注射CH4的空白作为对照,看其是否为甲烷氧化菌.根据上述试验结果,对比不同分离源所得甲烷氧化菌的甲烷氧化效率,选择甲烷氧化效率最高的菌种作为后续试验的菌种,试验设定3个平行.
2.2.2 甲烷氧化菌应用潜力的探究为了考察所得甲烷氧化菌在实际应用中是否同样具有最高的甲烷氧化能力,本研究将不同分离源的甲烷氧化菌按2.6%(菌体湿重/样品干重)的接种量接种入完全矿化的垃圾(粒径为4 mm)中,将其含水率调节至30%,测定初始及培养4 d后矿化垃圾的甲烷氧化效率.验证2.2.1节中所得甲烷氧化菌是否拥有最高的应用潜力.
为了考察所得甲烷氧化菌在不同填埋期填埋气环境下的甲烷氧化效果,本研究设定了3个CH4浓度(5%、20%、50%)来模拟填埋后期、中期及初期的CH4浓度.移取1 mL 2.2.1节中所得最佳甲烷氧化菌培养液(使用前,菌种测定OD600值)接种于装有100 mL新鲜NMS培养液的盐水瓶中,分别注射不同体积的CH4,使CH4浓度为5%、20%、50%.每隔24 h测定CH4浓度和细胞浓度.试验设定3个平行,每个浓度设置两个空白对照,一个接种菌液但不含CH4,另外一个则不接种菌液但含有CH4.
2.2.3 甲烷氧化菌剂的制备将筛选得到的最佳甲烷氧化菌培养至OD600为0.4~0.6,作为种子进行发酵培养.甲烷氧化菌剂的制备采用容积为20 L的发酵罐进行,发酵接种量为5%,制备条件如下:密闭培养,培养温度为30 ℃,转速为100 r · min-1,pH通过1 mol · L-1的氢氧化钠溶液和1 mol · L-1的盐酸溶液调节在6.9~7.1之间,通气量为1.6 L · min-1(其中CH4与空气的比例为1 ∶ 7(韩冰,2008)).定期取样测定菌液的细胞浓度,所得菌体采用离心法收集,并保存至-80 ℃冰箱中,用于后续的试验.
2.3 分析项目及测定方法CH4氧化速率的测定:试验样品注入CH4之后,每隔2~3 h测定样品中CH4浓度,CH4浓度采用气相色谱法进行测定;然后根据CH4浓度的变化计算CH4氧化速率,气相色谱仪为天美公司的GC-7890II型.测定条件如下:色谱柱柱温120 ℃(5A分子筛填充柱),FID检测器 温度150 ℃,进样口温度 150 ℃,氮气流量25 mL · min-1,氢气流量6 mL · min-1,空气流量600 mL · min-1,进样量1 mL.
细胞浓度的测定:采用Unico 2100可见分光光度计进行测定,以600 nm下测定的吸光度值(OD600)表示.
2.4 数据处理方法数据统计分析采用SPSS 19.0软件,图表绘制采用Origin 8.0软件.
3 结果与讨论(Results and discussion) 3.1 甲烷氧化菌的分离和筛选 3.1.1 分离源的筛选图 1显示了驯化过程中不同分离源的甲烷氧化速率.驯化初期,4种分离源中以好氧污泥的甲烷氧化速率最高,可达1001.65 μg · h-1 · g-1,其次为西湖北里湖底泥(332.98 μg · h-1 · g-1),填埋场普通覆盖土最低,只有22.68 μg · h-1 · g-1.当驯化时间增至30 d,不同分离源样品的甲烷氧化速率得到了大幅度提高,其中,好氧污泥和底泥提升最多,分别提升了414.08和268.74 μg · h-1 · g-1,然而,填埋场普通覆盖土的甲烷氧化速率却仍然较低,只有33.97 μg · h-1 · g-1,较培养初期只增加了11.39 μg · h-1 · g-1.当驯化时间为60 d时,好氧污泥和底泥的甲烷氧化速率同样出现了大幅度的增加,但好氧污泥的增幅大大超过了底泥,其甲烷氧化速率高达2461.29 μg · h-1 · g-1,增幅为1045.56 μg · h-1 · g-1.由此可知,在这4种分离源中,污水处理厂好氧污泥的甲烷氧化能力最高,这为我们重新认识好氧污泥提供了新的视角;填埋场覆盖土甲烷氧化能力最差,这也表明直接利用垃圾填埋场覆盖土的生物氧化能力进行填埋场CH4减排的潜力非常有限,有待于生物强化以提高.
相比而言,污水处理厂的好氧污泥较其他分离源更具人工培养潜力,在2个月的驯化时间里,其甲烷氧化能力的增幅巨大,高达1045.56 μg · h-1 · g-1;其次为西湖北里湖底泥,增幅为639.26 μg · h-1 · g-1,填埋场覆盖土最差,只有63.29 μg · h-1 · g-1.因此,为了高效获得甲烷氧化菌,在后续的筛选试验中,填埋场覆盖土将不予考虑.
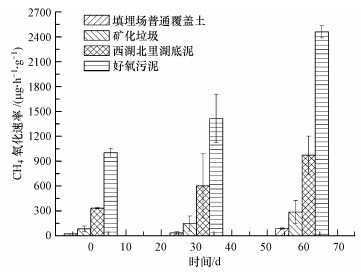 |
| 图 1 驯化过程中不同分离源的甲烷氧化速率 Fig.1 CH4 oxidation rates of different samples during domestication |
不同分离源所得甲烷氧化菌的甲烷氧化率如图 2所示,可见,当培养时间为24 h时,最高甲烷氧化率(34.78%)出现在好氧污泥甲烷氧化菌中,其次为矿化垃圾甲烷氧化菌(14.42%),西湖北里湖底泥甲烷氧化菌的甲烷氧化率最低.当培养时间为48 h时,好氧污泥甲烷氧化菌的甲烷氧化率提升至90.54%,而矿化垃圾甲烷氧化菌却只有68.26%,西湖北里湖底泥则更低,只有18.69%.当培养时间为72 h时,好氧污泥和矿化垃圾甲烷氧化菌的甲烷氧化率都达到了100%,西湖北里湖底泥的只有62.71%.由此可知,从好氧污泥和矿化垃圾中筛分得到的甲烷氧化菌具有较高的甲烷氧化能力,而西湖北里湖底泥中所得的甲烷氧化菌却没有得到相对较高的甲烷氧化能力,且低于矿化垃圾所得甲烷氧化菌,这表明分离源的高甲烷氧化能力并不代表其分离物也具有相同的甲烷氧化能力,其可筛分及培养的能力截然不同.
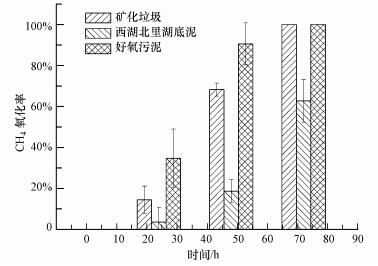 |
| 图 2 不同分离源甲烷氧化菌的甲烷氧化率 Fig.2 CH4 oxidation rates of mixed culture of methanotrophs at different samples |
为了进一步选出最佳甲烷氧化菌,本研究对不同分离源甲烷氧化菌的甲烷氧化能力及生长情况进行了测定.由图 3可知,不同分离源甲烷氧化菌的甲烷氧化能力随培养时间的变化与前面所述现象相同,且好氧污泥甲烷氧化菌可以将CH4高效氧化,这可以从甲烷氧化菌的生长状况及CH4浓度的变化中得到验证.当培养时间为24 h时,好氧污泥甲烷氧化菌的生长最为迅速,细胞浓度(OD600值)由最初的0.028上升至0.189,同时CH4浓度下降了6.41%,而同期的矿化垃圾中甲烷氧化菌的OD600只有0.084,CH4浓度也只下降了2.55%;当培养时间为48 h时,好氧污泥甲烷氧化菌的OD600增至0.267,CH4浓度下降了17.01%,而矿化垃圾甲烷氧化菌的OD600为0.239,CH4浓度下降了12.92%;随着培养时间的延长,好氧污泥甲烷氧化菌因CH4不足而出现了衰亡的现象,此时矿化垃圾甲烷氧化菌的细胞浓度则开始大于好氧污泥甲烷氧化菌.由此可知,好氧污泥甲烷氧化菌生长速度更快,甲烷氧化活性更高,更具有应用潜力.
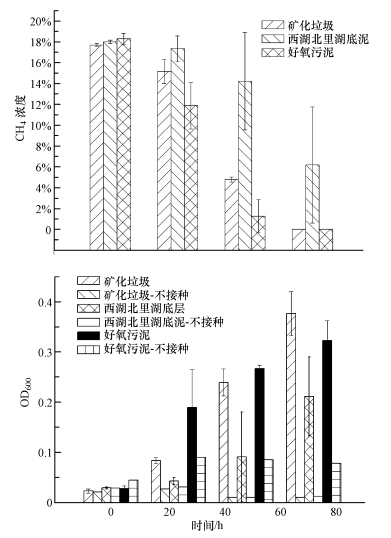 |
| 图 3 不同分离源甲烷氧化菌的甲烷氧化能力及生长状况 Fig.3 CH4 oxidation capacity and growth of mixed culture of methanotrophs at different samples |
好氧污泥甲烷氧化菌之所以甲烷氧化活性更高,有机质含量可能是影响其甲烷氧化活性的原因之一.Kightley等(1995)研究发现,增加土壤有机质含量,可以明显提高甲烷的氧化活性,甲烷最大氧化速率可达166 g(CH4)· m-2(column)· d-1.与对照相比,添加污泥的覆土甲烷氧化能力提高了26%,而添加K2HPO4的覆土甲烷氧化能力变化则不大.好氧污泥的有机质含量较其他分离源要高,故其甲烷氧化活性更高.另外,甲烷氧化菌的富集培养过程是在好氧条件下进行的,与其他分离源相比较而言,好氧污泥更能适应这样的培养条件.综合分析,好氧污泥甲烷氧化菌甲烷氧化活性更高,更具有应用潜力.
3.2 甲烷氧化菌的应用潜力 3.2.1 甲烷氧化菌在覆盖材料中的适应能力接种不同分离源甲烷氧化菌后覆盖材料的甲烷氧化速率如图 4所示,可见,接种好氧污泥甲烷氧化菌的覆盖材料在4 d内即可将浓度20%的CH4完全氧化,而接种其他甲烷氧化菌的均不能氧化完全.此外,接种有好氧污泥甲烷氧化菌的覆盖材料,其甲烷氧化速率高达388.22 μg · h-1 · g-1,而接种矿化垃圾及北里湖底泥甲烷氧化菌的覆盖材料,其甲烷氧化速率分别只有301.05 μg · h-1 · g-1和293.38 μg · h-1 · g-1. 因此,接种好氧污泥甲烷氧化菌能显著提高覆盖材料的甲烷氧化能力,同时其甲烷氧化能力显著高于其他两种(p<0.05).综上,源自好氧污泥的甲烷氧化菌在覆盖层中有最高的适应和应用潜力.
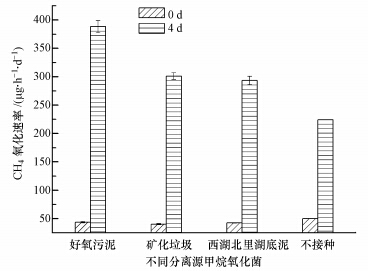 |
| 图 4 接种不同分离源甲烷氧化菌后覆盖材料的甲烷氧化速率 Fig.4 CH4 oxidation rates of l and fill covers inoculated by different mixed culture of methanotrophs |
不同CH4浓度下好氧污泥甲烷氧化菌的甲烷氧化率如图 5所示.该甲烷氧化菌在48 h内即可将5%浓度的CH4氧化完全,在72 h内就可将20%浓度的CH4氧化96%,更可在120 h内将50%浓度的CH4氧化70%.由此可知,无论环境中CH4的浓度高低与否,该甲烷氧化菌都能将其氧化,而纯培养物在培养10 d后,其甲烷氧化率只有64.18%(周生芳等,2008),因此,甲烷氧化速率较纯培养物高得多.
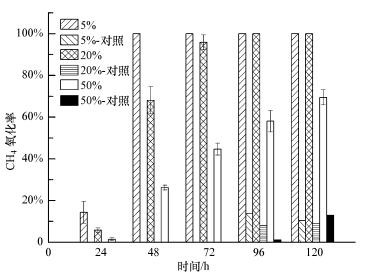 |
| 图 5 不同CH4浓度下好氧污泥甲烷氧化菌的甲烷氧化率 Fig.5 CH4 CH4 oxidation rate of sludge mixed culture of methanotrophs at different CH4 concentrations |
从不同CH4浓度下好氧污泥甲烷氧化菌的甲烷氧化能力及生长状况可知(图 6),在甲烷氧化菌初始细胞浓度(OD600)为0.01的条件下,该甲烷氧化菌在不同CH4浓度下都能很好的生长,并且能拥有较高的甲烷氧化能力.当培养时间为24 h时,不同CH4浓度下甲烷氧化菌的生长速率基本相同,但48 h后,5% CH4浓度下甲烷氧化菌的细胞浓度便达到了最大值(OD600=0.12),且在之后的培养中不再生长,而20%和50% CH4浓度下的甲烷氧化菌仍在生长(OD600=0.26),此时,3种CH4浓度下甲烷氧化菌的甲烷氧化率分别达到了100%、68.02%和26.25%.由此可知,基质(CH4)限制着甲烷氧化菌的生长.当培养时间为72 h时,20%和50% CH4浓度下的甲烷氧化菌细胞浓度增加到了0.36和0.39,且甲烷氧化率也分别增至95.86%和44.68%;96 h后,20% CH4浓度下的甲烷氧化菌也不再生长,而50% CH4浓度下的甲烷氧化混合菌OD600却高达0.49,此时,20% CH4浓度下的CH4已被完全氧化,而50% CH4浓度下的CH4也被氧化了58.06%.由此可以得出,20%的CH4浓度仍限制着甲烷氧化菌的生长,即甲烷氧化菌具有更高的基质负荷需求.当培养时间为120 h时,只有50%CH4浓度下的甲烷氧化菌还在继续生长,且甲烷氧化率也在增加(70%).因此,由上述结果可知,高CH4浓度并不会抑制该甲烷氧化菌的生长及甲烷氧化作用,并且不论在高或低CH4浓度下它都能快速地将CH4氧化完全,这对填埋场CH4的削减而言,更具有适应性.
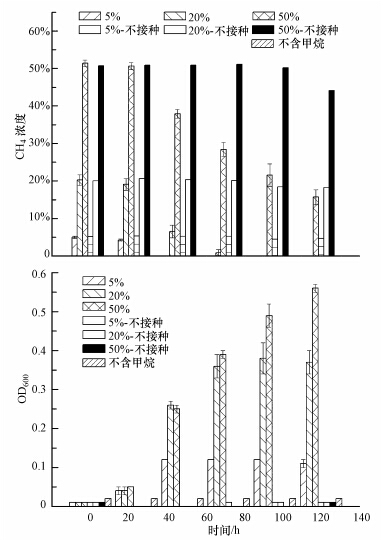 |
| 图 6 不同CH4浓度下好氧污泥甲烷氧化菌的甲烷氧化能力及生长状况 Fig.6 CH4 oxidation capacity and growth of mixed culture of methanotrophs at different CH4 concentrations |
甲烷氧化菌的发酵培养效果如图 7所示,可知,好氧污泥甲烷氧化菌在进行发酵培养时的迟滞期很短,只有24 h,与韩冰所报道的M.trichosporium OB3b的发酵培养相比,迟滞期至少缩短了46 h(Han et al., 2009).此外,该甲烷氧化菌在发酵培养145 h左右时,其细胞浓度就达到了最大值,OD600高达2.917,此后,甲烷氧化菌生长就进入了稳定期.梁洪野(2011)以甲烷为唯一碳源培养Methylosinus trichosporium 3011,生长7 d后,最大生长密度OD600值为0.769,细胞干重为0.2075 g · L-1,最大生长速率为0.0064 h-1,迟滞期为27.613 h.采用甲醇代替甲烷作为甲烷氧化菌的唯一碳源时,当甲醇添加量为0.05%(V/V)时的生长速率为0.0456 h-1,最大生长密度OD600值为1.578,发酵终止后细胞干重为1.026 g · L-1,但迟滞期远高于甲烷条件下培养细胞的迟滞期,为60.4152 h(梁洪野,2011).由此可见,好氧污泥甲烷氧化菌具有生长迟滞期短、生长速率高等特点,这为其后续的工程应用奠定了坚实的基础.
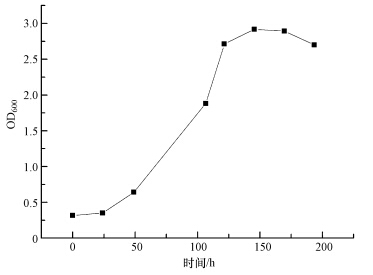 |
| 图 7 不同CH4好氧污泥甲烷氧化菌在发酵培养中的生长状况 Fig.7 CH4 Growth of mixed culture of methanotrophs in sludge in fermentation system |
1)在供试的4种分离源中,污水处理厂好氧污泥的甲烷氧化能力最高,填埋场覆盖土最差.污水处理厂的好氧污泥较其他分离源更具人工培养潜力,甲烷氧化能力的增幅高达1045.56 μg · h-1 · g-1.好氧污泥甲烷氧化菌比其他分离源的生长速度更快,甲烷氧化活性也更高,更具适应和应用潜力.
2)接种源自好氧污泥的甲烷氧化菌较其他两种介质(矿化垃圾和西湖北里湖底泥)更能显著提高覆盖层的甲烷氧化能力(p<0.05),且不受CH4浓度高低的抑制,对填埋场CH4的削减更具有适应性.
3)源自好氧污泥的甲烷氧化菌的生长迟滞期短、生长速率高,有利于其工程应用.
| [1] | Chan g H L, Alvarez-Cohen L. 1997. Two-stage methanotrophic bioreactor for the treatment of chlorinated organic wastewater[J]. Water Research, 31(8): 2026-2036 |
| [2] | 韩冰. 2008. 甲烷氧化菌的微生态解析及其应用基础研究[D]. 北京: 清华大学 |
| [3] | Han B, Su T, Wu H, et al. 2009. Paraffin oil as a "methane vector" for rapid and high cell density cultivation of Methylosinus trichosporium OB3b[J]. Applied Microbiology and Biotechnology, 83(4): 669-677 |
| [4] | Hanson R S, Hanson T E. 1996. Methanotrophic bacteria[J]. Microbiological Reviews, 60(2): 439-471 |
| [5] | Hatamoto M, Koshiyama Y, Kindaichi T, et al. 2010. Enrichment and identification of methane-oxidizing bacteria by using down-flow hanging sponge bioreactors under low methane concentration[J]. Annals of Microbiology, 61(3): 683-687 |
| [6] | 华绍烽, 李树本, 辛嘉英, 等. 2006. 一个II型甲烷氧化菌中甲烷单加氧酶羟基化酶的分离纯化和理化性质[J]. 生物工程学报, 22(6): 1107-1112 |
| [7] | Humer M, Lechner P. 1999. Alternative approach to the elimination of greenhouse gases from old landfills[J]. Waste Management & Research, 17(6): 443-452 |
| [8] | Kallistova A Y, Kevbrina M V, Nekrasova V K, et al. 2005. Methane oxidation in landfill cover soil[J]. Microbiology, 74(5): 608-614 |
| [9] | Kightley D, Nedwell D B, Cooper M. 1995. Capacity for methane oxidation in landfill cover soils measured in laboratory-scale soil microcosms[J]. Applied Environmental Microbiology, 61(2): 592-601 |
| [10] | 李春瑛, 张宝成. 2005. 影响全球气候的温室气体及我国温室气体标准物质的研究现状[J]. 计量与测试技术, 32(4): 34-35 |
| [11] | 梁洪野. 2011. 甲烷氧化菌的高密度培养[D]. 哈尔滨: 哈尔滨商业大学 |
| [12] | 罗明芳, 吴昊, 王磊, 等. 2007. 含有甲烷氧化菌的混合菌群特性研究[J]. 微生物学报, 47(1): 103-109 |
| [13] | Park S, Hanna L, Taylor R T, et al. 1991. Batch cultivation of Methylosinus trichosporium OB3b: I. Production of soluble methane monooxygenase[J]. Biotechnology and Bioengineering, 38(4): 423-433 |
| [14] | Smith L H, McCarty P L. 1997. Laboratory evaluation of a two-stage treatment system for TCE co-metabolism by a methane-oxidizing mixed culture[J]. Biotechnology and Bioengineering, 55(4): 650-659 |
| [15] | Taylor R T, Hanna M L. 1995. Laboratory treatability studies for resting-cell in situ microbial filter bioremediation[A]// Hinchee R E, Fredrickson J, Alleman B C (Eds.).Third International In Situ and On-site Bioreclamation Symposium Book Series: Bioaugmentation for Site Remediation[M]. Columbus: Battelle Press.3: 15-29 |
| [16] | Wang J, Xia F F, Bai Y, et al. 2011. Methane oxidation in landfill waste biocover soil: kinetics and sensitivity to ambient conditions[J]. Waste Management, 31(5): 864-870 |
| [17] | 王晓丽, 于建国. 2008. 一个甲烷氧化菌株的分离、鉴定及其特性研究[J]. 微生物学报, 35(6): 934-938 |
| [18] | Wilshusen J H, Hettiaratchi J P A, De Visscher A, et al. 2004. Methane oxidation and formation of EPS in compost: effect of oxygen concentration[J]. Environmental Pollution, 129(2): 305-314 |
| [19] | Xing X H, Wu H, Luo M F, et al. 2006. Effects of organic chemicals on growth of Methylosinus trichosporium OB3b[J]. Biochemical Engineering Journal, 31(2): 113-117 |
| [20] | 杨帆. 2012. 国内外城市生活垃圾处理技术研究进展[J]. 科学与财富, (5): 95-95 |
| [21] | 杨文静, 张相锋, 董世魁, 等. 2010. 一种新型垃圾填埋场生物覆盖层基质的甲烷氧化动力学研究[J]. 中国沼气, 28(3): 11-14 |
| [22] | Zamorano M, Pérez J I P, Pavés I A, et al. 2007. Study of the energy potential of the biogas produced by an urban waste landfill in Southern Spain[J]. Renewable and Sustainable Energy Reviews, 11(5): 909-922 |
| [23] | 张相锋, 杨文静, 董世魁, 等. 2010. 生物覆盖层基质对垃圾填埋场甲烷氧化的影响[J]. 生态环境学报, 19(1): 72-76 |
| [24] | 郑军, 程红兵, 刘尚俊, 等. 2007. 甲烷利用菌培养条件的优化及其初步应用[J]. 中国生物工程杂志, 72(12): 80-83 |
| [25] | 周生芳, 陶秀祥, 朱红威, 等. 2008. 煤矿土壤甲烷氧化菌的筛选及其培养条件优化的初步研究[J]. 洁净煤技术, 14(4): 98-100 |
 2015, Vol. 35
2015, Vol. 35


