2. 中国科学院烟台海岸带研究所, 中国科学院海岸带环境过程与生态修复重点实验室, 山东省海岸带环境工程技术研究中心, 烟台 264003
2. Key Laboratory of Coastal Environmental Processes and Ecological Remediation, Research Center for Coastal Environment Engineering and Technology of Shandong Province, Yantai Institute of Coastal Zone Research, Chinese Academy of Sciences, Yantai 264003
随着人类活动的不断增加,大量的含磷废水排入水体,造成水体磷浓度上升,水体富营养化程度日益严峻.为了有效控制水体中磷的含量,防止水体富营养化,人们越来越关注人为活动产生的污水中磷的去除.除磷的方法主要有离子交换法(Blaney et al., 2007)、膜分离法(van Voorthuizen et al., 2005)、微生物法(de-Bashan et al., 2004)、人工湿地法(Prochaska et al., 2006)、吸附法(Kang et al., 2003)与结晶法(Donnert et al., 1999)等.其中,吸附法具有高效、迅速、适应性强、易操作及无二次污染等优点,是一种具有较好应用前景的除磷方法(Qu,2008).文献报道的磷吸附剂主要有粉煤灰(Yildiz,2004)、高炉矿渣(Kostura et al., 2005)、赤泥(Lopez et al., 1998)、针铁矿(Chitrakar et al., 2006)、给水处理厂废铝泥(Agyin-Birikorang et al., 2007)、铁氧化物(Zeng et al., 2004)、锰氧化物(Yao et al., 1996)及稀土氧化物(Guo et al., 2011)等,研究重点亦逐渐由传统的炭质类吸附剂、矿物类吸附剂等吸附材料向纳米型金属氧化物吸附剂转变.此外,由于金属复合氧化物比单一氧化物具有更好的吸附性能,合成金属复合氧化物吸附剂越来越受到关注(Zhang et al., 2009).
铈(Ce)是稀土元素中资源量最大、丰度最高的元素,其氧化物对水体中的含氧阴离子具有特异的吸附性能.铈氧化物纳米颗粒(Guo et al., 2011)和铈修饰纤维蛋白(Deng et al., 2012)对水体中的磷具有良好的去除效果,水合氧化铈(Li et al., 2012)、二氧化铈(Feng et al., 2012)、铁铈复合氧化物(Zhang et al., 2005)对水体中的砷具有良好的去除效果.过渡金属锰的氧化物特别是二氧化锰,带有较高的电荷,比表面积大,对水体中磷、砷等阴离子具有较强的吸附作用(Yao et al., 1996).由此预见,铈锰复合氧化物将会对水中的磷及其它阴离子具有较好的去除效果.铈锰氧化物吸附阴离子的研究已有文献报导,如Deng等(2011)合成了铈锰复合氧化物,对氟具有优良的吸附性能;Gupta等(2011; 2012)制备了铈锰纳米颗粒,对水体中的As(V)与As(Ⅲ)均具有较好的吸附效果.然而,到目前为止,利用铈锰复合氧化物吸附去除水中磷的研究未见报道.因此,本文采用共沉淀法制备具有纳米结构的铈锰复合氧化物吸附剂,并对磷在吸附剂表面的吸附行为与机制进行重点研究.
2 材料与方法(Materials and methods) 2.1 实验试剂与仪器试剂:Ce2(SO4)3 · 8H2O、KMnO4、NaOH、HNO3、NaNO3均为分析纯,KH2PO4为优级纯,实验用水均为去离子水.准确称取439.44 mg KH2PO4于1 L容量瓶中,加水至刻线配得100 mg · L-1的磷储备液,实验中根据不同的需要将储备液稀释至不同浓度.
仪器:HZQ-C型空气恒温振荡器,DH-201型电热恒温干燥箱,TU-1810型紫外可见分光光度计,PHS-2F pH计(上海雷磁).
2.2 铈锰复合氧化物的制备铈锰复合氧化物采用共沉淀法制备,以Ce2(SO4)3 · 8H2O和KMnO4为原料,分别配制成溶液,使得Ce2(SO4)3 · 8H2O和KMnO4的物质的量比为3 ∶ 2.向KMnO4溶液中加入一定量的NaOH溶液至整个溶液呈碱性,然后在快速搅拌下把KMnO4溶液逐滴加入Ce2(SO4)3 · 8H2O溶液中,加毕,继续搅拌30~60 min,再静置陈化4 h左右.倾倒出上清液,加等量的去离子水于沉淀物中,搅拌,再用去离子水洗涤固体物3~4次,过滤,55 ℃烘干,研磨密封保存,得到铈锰复合氧化物.
2.3 铈锰复合氧化物的表征用扫描电子显微镜(Gemini1530)来观察吸附剂的表面形貌,用N2吸附-脱附等温线与BET方程结合(比表面和孔径分布分析仪,QuantachromeAsiq)计算吸附剂的比表面积、孔容和BET孔径等参数.X射线衍射仪(Rigaku D/max2500VPC)用于观测吸附剂的X射线衍射图谱.傅氏变换拉曼红外谱仪(Nicolet is10,Thermo SCIENTIFIC)用于观测吸附剂吸附磷前后的红外谱图.Zeta电位分析仪(Nano-ZS90,Malvern)用于分析铈锰复合氧化物吸附磷前后的Zeta电位.
2.4 吸附实验除吸附动力学外,吸附实验均在100 mL规格的聚乙烯塑料瓶中进行.用去离子水配制的含磷溶液总体积为50 mL,背景电解质为0.01 mol · L-1的NaNO3,吸附剂的投加量均为10 mg.在(25±1)℃、转速为170 r · min-1的振荡器中平衡24 h,使用NaOH或HNO3调节pH值.前8 h每2 h调节一次pH,使最终pH稳定在7.0±0.1(pH对吸附的影响除外).吸附完成后样品过0.45 μm醋酸纤维素膜,采用钼锑抗分光光度法测定磷浓度.
2.4.1 吸附等温线在一系列盛有50 mL不同浓度(2、5、10、15、20、30、40、60 mg · L-1)磷溶液的聚乙烯塑料瓶中进行,吸附剂投加量为10 mg,背景电解质为0.01 mol · L-1的NaNO3. 吸附完毕,取样、过膜、测定磷浓度.
2.4.2 吸附动力学在1.5 L磷浓度分别为5.0、10.0 mg · L-1的2种溶液中进行,铈锰复合氧化物投加量为300 mg,背景电解质为0.01 mol · L-1的NaNO3.每隔一定时间(0 min、1 min、5 min、10 min、20 min、40 min、1 h、2 h、4 h、6 h、8 h、12 h、24 h、36 h)取样,过膜后分析溶液中磷浓度.
2.4.3 pH及离子强度对铈锰复合氧化物吸附磷的影响在一系列盛有50 mL浓度为5.0 mg · L-1磷溶液的聚乙烯塑料瓶中投加10 mg吸附剂,分别考察不同pH(3~11)和不同离子强度(0.1、0.01、0.001 mol · L-1 NaNO3)对吸附效果的影响.用HNO3和NaOH调节溶液pH,使pH稳定在不同预定值左右,反应结束后记录下最终pH值,取样过膜后测定磷浓度.
2.4.4 共存阴离子对铈锰复合氧化物吸附磷的影响在一系列盛有50 mL浓度为5.0 mg · L-1磷溶液的聚乙烯塑料瓶中投加10 mg吸附剂,分别考察CO32-、SO2-4、Cl-、SiO32- 4种阴离子在4种不同浓度(0、0.1、1.0、10 mmol · L-1)时对磷吸附效果的影响.
2.4.5 铈锰复合氧化物的再生和重复利用采用吸附脱附循环实验评估铈锰复合氧化物的重复利用性能.吸附实验在盛有1.5 L浓度为10.0 mg · L-1磷溶液的烧杯中进行,吸附剂的投加量为300 mg,背景电解质为0.01 mol · L-1的NaNO3,pH为7.0±0.1. 常温下持续搅拌6 h后取样,过膜后分析溶液中的磷浓度,计算磷吸附量.脱附实验是将负载有磷的铈锰复合氧化物吸附剂加入到100 mL 0.5 mol · L-1的NaOH溶液中,搅拌4 h后固液分离,抽滤、烘干、称量,然后进行下一次的吸附脱附实验,共进行4次循环.
2.5 数据分析 2.5.1 磷吸附量计算铈锰复合氧化物对磷吸附量q(mg · g-1)按式(1)计算:
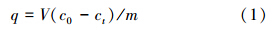
铈锰复合氧化物对磷吸附结果分别用Langmuir模型(2)和Freundlich模型(3)拟合:
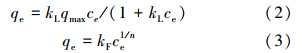
磷吸附动力学分别用准一级模型(4)和准二级模型(5)对吸附数据进行拟合.准一级动力学模型基于假定吸附受扩散步骤控制,吸附速率正比于平衡吸附量与t时刻吸附量的差值(Lagergren,1898).准二级动力学模型基于假定吸附速率受化学吸附机理的控制,该机理涉及到吸附剂与吸附质之间的电子共用或电子转移(Ho et al., 1999).
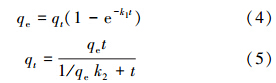
铈锰复合氧化物的扫描电镜照片如图 1所示.可以看到,铈锰复合氧化物是由纳米级的细小颗粒团聚而成,颗粒直径大约为10~20 nm,且具有凸凹不均匀的多孔状结构.铈锰复合氧化物的XRD图谱如图 2所示.可以看出,在28.5°和47.5°出现了两个特征峰,与标准谱图对比发现,这与无定形的水合氧化铈的特征峰衍射峰一致,表明铈锰复合氧化物中的铈氧化物有类似水合氧化铈的无定形结构(Nilchi et al., 2009).此外,图谱中再无其他特征峰,表明该复合氧化物中的锰氧化物可能是以无定形形式存在的.BET分析结果表明,此铈锰复合氧化物的比表面积为157 m2 · g-1.相比而言,二氧化铈的比表面积较低,仅为11.5 m2 · g-1(闫春燕等,2008),说明铈锰复合氧化物具有较高的吸附潜势.对铈锰复合氧化物进行孔结构特性分析,测得孔容为0.28 cm3 · g-1,孔径大约为7.5 nm.Zeta电位分析结果显示,铈锰复合氧化物吸附剂的等电点为6.5.
 |
| 图 1 铈锰复合氧化物的扫描电镜照片 Fig. 1 SEM image of the Ce-Mn binary oxide |
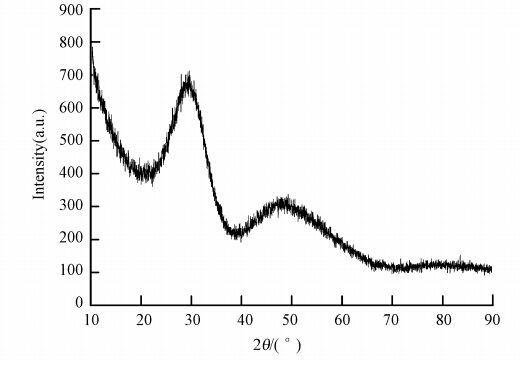 |
| 图 2 铈锰复合氧化物的XRD图 Fig. 2 XRD diffraction pattern of Ce-Mn binary oxide |
铈锰复合氧化物对磷的吸附等温线如图 3所示,在低浓度区,随着磷溶液平衡浓度的增加,铈锰复合氧化物的磷吸附量快速增高,随着磷平衡浓度的进一步增加,磷吸附量逐渐趋于平缓. 该变化趋势表明复合氧化物对磷具有较强的亲和力,且在低平衡浓度下,亦具有较高的吸附容量.分别采用Langmuir方程和Freundlich方程对实验数据进行拟合(表 1).可以发现,Langmuir模型(R2=0.938)较Freundlich模型(R2=0.887)可以更好地描述此吸附过程.按Langmuir模型计算所得的磷最大吸附量为28.6 mg · g-1(pH=7.0),与文献报道的吸附剂相比(表 2),铈锰复合氧化物吸附剂具有较高的吸附容量.
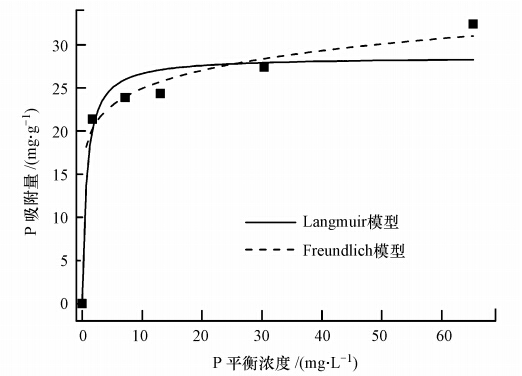 |
| 图 3 铈锰复合氧化物对磷的吸附等温线(溶液体积50 mL,吸附剂投加量200 mg · L-1,pH=7.0±0.1,转速170 r · min-1,T=(25±1)℃,平衡时间24 h) Fig. 3 Adsorption isotherm of phosphate by Ce-Mn binary oxide |
| 表1 Langmuir和Freundlich吸附等温线拟合结果 Table 1 Langmuir and Freundlich isotherms parameters for phosphate adsorption |
| 表2 其它吸附剂对磷的最大吸附容量 Table 2 Maximum phosphate adsorption capacities of some reported adsorbents |
由图 4可知,铈锰复合氧化物对磷的吸附可以明显分为2个阶段:快速阶段(0~2 h)和慢速阶段(2~36 h).在初始阶段,磷吸附速度很快,磷吸附量随时间迅速增加;在第二阶段,随着时间的延长,吸附速率逐渐减小,吸附进入慢速阶段.这是因为在吸附动力学初始阶段,吸附剂外表面吸附位点较多,液相与固表面离子浓度差较大,磷容易扩散到固体表面与之结合,故反应速率较快;随着吸附的进行,吸附位点逐渐饱和,吸附速率逐渐放缓,直至吸附平衡(李国亮等,2012).分别采用准一级和准二级动力学模型对两种不同磷初始浓度的吸附过程进行拟合(表 3).结果显示,准二级动力学模型拟合时可决系数均较高,因此,该吸附过程比较符合准二级动力学模型.由于准二级动力学模型是基于假定吸附速率受化学吸附机理控制的,说明磷在铈锰复合氧化物表面可能发生了化学吸附.
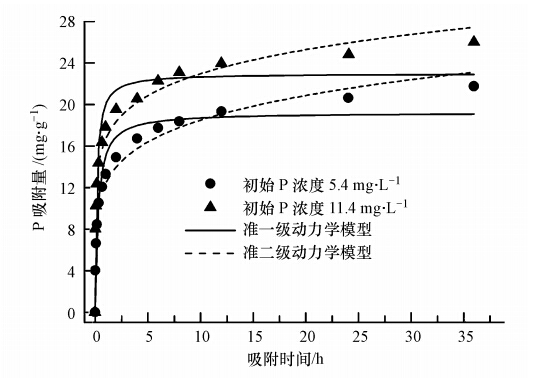 |
| 图 4 吸附时间对铈锰复合氧化物吸附不同初始浓度磷的影响(初始浓度分别为5.4 mg · L-1和11.4 mg · L-1,溶液体积 1.5 L,吸附剂投加量200 mg · L-1,pH=7.0±0.1,转速 170 r · min-1,T=(25±1)℃,平衡时间 36 h) Fig. 4 Effect of contact time on the adsorption capacity of different initial concentrations of phosphate by Ce-Mn binary oxide |
| 表3 铈锰复合氧化物吸附动力学拟合参数 Table 3 Kinetic parameters for the phosphate adsorption by Ce-Mn binary oxide |
由图 5可得,磷的吸附效果受溶液pH影响较大. 在酸性条件下,吸附率最高,随着溶液pH的升高吸附率逐渐下降,特别是在pH高于6.0以后,下降更为显著.主要因为在考察的pH范围内(3~11),H2PO4-和HPO2-4是磷主要的存在形式,较低的pH有助于吸附剂表面的质子化,而质子化的增强可增加吸附剂表面的正电荷,进而增加吸附剂表面与磷离子之间的静电引力,最终导致高的吸附量.在较高的pH条件下,吸附剂表面带负电荷,磷离子和吸附剂表面的静电斥力导致磷的吸附量下降(Zhang et al., 2009).
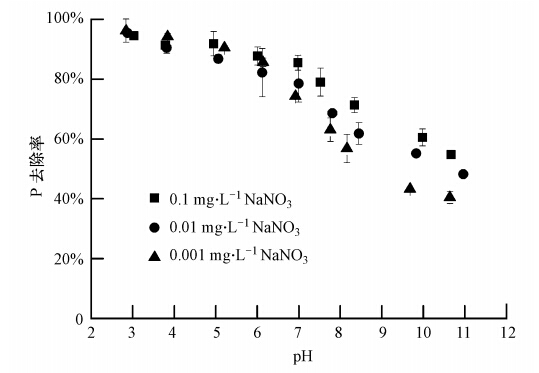 |
| 图 5 pH值及离子强度对铈锰复合氧化物吸附磷的影响(磷初始浓度5 mg · L-1,溶液体积50 mL,吸附剂投加量200 mg · L-1,转速 170 r · min-1,T=(25±1)℃,平衡时间 24 h) Fig. 5 Effect of pH and ionic strength on phosphate adsorption by Ce-Mn binary oxide |
此外,pH在3~6的范围内,NaNO3的浓度从0.001 mol · L-1增加到0.1 mol · L-1,离子强度的变化对磷的吸附几乎没有影响;但当pH>6时,随着离子强度增加磷的吸附量增加.类似的现象也出现在Giesler等(2005)用其他的金属氧化物吸附除磷的研究中.如果随着离子强度的增加阴离子的吸附量降低,说明电解质可以通过静电力形成外层表面络合物;反之如果随着离子强度的增加阴离子的吸附量增加或不变,说明电解质可以通过静电力形成内层表面络合物(McBride,1997).本研究中磷酸根的去除率随着离子强度的增加而增加,因此,可推断出磷在铈锰复合氧化物表面形成了内层表面络合物.
3.2.4 共存阴离子对铈锰复合氧化物吸附磷的影响在天然水体中,通常会存CO32-、SO2-4、Cl-、SiO32-这4种阴离子,它们可能通过竞争吸附影响磷的去除.这4种阴离子在不同浓度下对铈锰复合氧化物吸附磷的影响如图 6所示.显然,SiO32-对磷吸附的影响较为明显,当其浓度由0.1 mmol · L-1增大到10 mmol · L-1,磷去除率显著降低,由96%降至38%;CO32-的存在亦可导致磷去除率降低,但相对SiO32-而言,对磷去除的影响程度较小;而Cl-和SO2-4对磷去除率几乎没有影响.4种离子的影响顺序由大到小依次为:SiO32->CO32->Cl-≥ SO2-4.SiO32-和CO32-对磷去除影响较明显的原因可能是:硅与磷位于元素周期表中同一周期的相邻位置,碳与磷位于对角线位置,硅和碳的阴离子形态与磷酸根非常相似,这样硅和碳的阴离子就会与磷酸根在吸附剂表面的活性位点产生较强的竞争吸附(Li et al., 2014),从而导致磷去除率的显著降低.
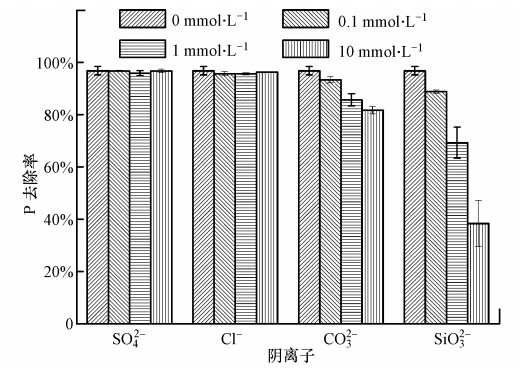 |
| 图 6 共存离子对铈锰复合氧化物吸附磷的影响(磷初始浓度5 mg · L-1,溶液体积50 mL,吸附剂投加量200 mg · L-1,pH=7.0±0.1,转速 170 r · min-1,T=(25±1)℃,平衡时间24 h) Fig. 6 Effect of coexisting anions on phosphate adsorption by Ce-Mn binary oxide |
为了评估已使用过的铈锰复合氧化物吸附剂的重复利用性能,利用不同浓度的NaOH溶液对该复合吸附剂进行脱附再生,初步实验结果表明,0.5 mol · L-1的NaOH溶液脱附效果较好.故本研究采用0.5 mol · L-1的NaOH溶液对吸附磷的铈锰复合氧化物进行脱附再生-再吸附实验,共进行4次循环,其中,第0次循环对应的吸附量是指铈锰复合氧化物吸附剂初次的吸附量,实验结果如图 7所示.可以看出,第1次再生后吸附剂的磷吸附量低于初次吸附量,第2次和第3次再生后磷的吸附量比第1次再生后略有增加,第4次再生后磷的吸附量又略有减少.总之,与新制备的铈锰复合氧化物相比,再生后的吸附剂对磷的吸附效能有所降低,但仍保持了较高的吸附容量,表明制备的铈锰复合氧化物可以通过碱液再生后多次重复使用.
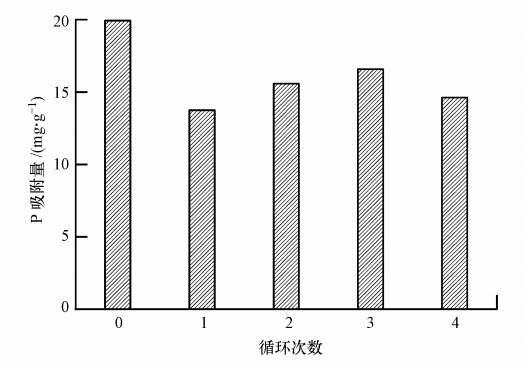 |
| 图 7 铈锰复合氧化物再生循环作用中磷吸附量的变化 Fig. 7 Variation of the phosphate adsorption capacity by the Ce-Mn binary oxide as a function of regeneration cycle |
磷吸附前后铈锰复合氧化物的Zeta电位随pH变化如图 8所示.可以看出,吸附磷之后,铈锰复合氧化物的等电点明显降低了,由吸附前的6.5降到了吸附后的约3.2.研究表明,阴离子的特性吸附可使吸附剂表面带更多负电荷,对阴离子吸附量越大,吸附剂表面净的负电荷越多,从而导致吸附剂的等电点移向低pH值(Hsia et al., 1994).因此,从铈锰复合氧化物吸附磷后等电点的降低可以推断磷的吸附是特性吸附而不仅仅是静电吸附过程(Zhang et al., 2009).
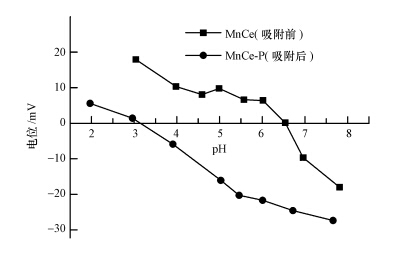 |
| 图 8 铈锰复合氧化物吸附磷前与吸附磷后的Zeta电位(磷初始浓度5 mg · L-1,溶液体积50 mL,吸附剂投加量200 mg · L-1,平衡时间 72 h) Fig. 8 Zeta potential of Ce-Mn binary oxide before and after phosphate adsorption |
铈锰复合氧化物吸附磷前后的红外谱如图 9所示.图 9a是吸附磷前的红外图谱,其中,1633 cm-1的吸收峰是铈锰复合氧化物物理结合水的弯曲振动峰;1497 cm-1处的吸收峰可归属于表面的Ce—OH的弯曲振动(Guo et al., 2011);而1352 cm-1处出现的吸收峰可归属于CO32-的振动吸收,因为该实验是在空气中进行的(Li et al., 2014);1174 cm-1处的吸收峰可属于HSO4-的振动吸收;1112、1045、974 cm-1这3个吸收峰归属于SO2-4的振动吸收(Lefèvre,2004).当铈锰复合氧化物吸附磷后(图 9b,c,d),HSO4-和SO2-4的吸收峰完全消失,同时在1010 cm-1处出现了一个新峰,对应于P—O的不对称伸缩振动(Persson et al., 1996).这表明铈锰复合氧化物表面的硫酸根被磷酸根取代了.反应后,1497 cm-1处的吸收峰变弱,且随着磷浓度的增加而愈加显著,表明吸附剂表面的金属羟基被磷酸根取代了.此外,1352 cm-1处的吸收峰明显减弱,表明部分CO32-可能与磷酸根进行了离子交换.
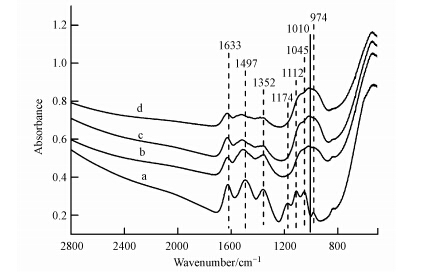 |
| 图 9 铈锰复合氧化物的FTIR图谱(a.与磷反应前,b.与2.5 mg · L-1磷反应后,c.与5.0 mg · L-1磷反应后,d.与10 mg · L-1磷反应后;平衡时间 24 h,pH=7.0±0.1,T=(25±1)℃) Fig. 9 FTIR spectra of Ce-Mn binary oxide |
为确定SO2-4在磷吸附中的作用,测得磷的吸附量和SO2-4的释放之间的关系如图 10所示.从拟合线性方程的斜率可知,每克吸附剂吸附1 mmol · L-1的磷酸根,其表面释放大约0.4 mmol · L-1的SO2-4.由此可推断,在初始磷浓度为2~60 mg · L-1的范围内,铈锰复合氧化物吸附剂每吸附1个单位磷酸根,其中2/5可归因于表面SO2-4与磷酸根之间进行的离子交换作用,其余的3/5主要归于表面金属羟基与之进行的交换.因此,吸附剂表面的SO2-4和磷酸根之间的离子交换在磷吸附过程中起重要作用,但并不是主要去除机制.磷酸根主要是通过取代金属氧化物表面的羟基而被吸附去除的.类似的报道也出现在锆锰复合氧化物吸附砷的研究(Zhang et al., 2013)和施氏矿物吸附砷的研究(Burton et al., 2009)中,这也正好与前面的FTIR分析相吻合.
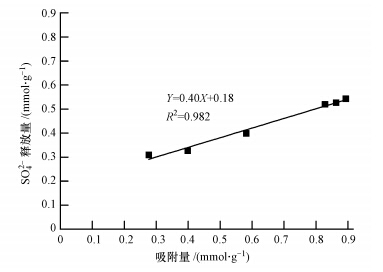 |
| 图 10 磷的吸附量和SO2-4的释放之间的关系(溶液体积50 mL,吸附剂投加量200 mg · L-1,pH=7.0±0.1,转速 170 r · min-1,T=(25±1)℃,平衡时间 4 h) Fig. 10 Relationship between adsorbed phosphate and the amounts of released sulfate |
由离子强度对铈锰复合氧化物吸附磷的影响及Zeta电位和红外谱图的分析结果表明,磷在铈锰复合氧化物(用M-OH表示)的表面上可能发生了内表面络合吸附反应.
当溶液pH在3.0~6.5之间时,H2PO4-是磷存在的主要形态(pKa1=2.12,pKa2=7.20,pKa3=12.36),此时较低的pH有助于吸附剂表面的质子化,而质子化的增强可增加吸附剂表面的正电荷,进而导致吸附剂表面与磷离子之间的静电引力增加,最终导致高的吸附量. 可能发生的反应如下:
M-OH+H+→M-OH+2
M-OH+2+H2PO4-→M-H2PO4+H2O
2M-OH+2+H2PO4-→M2-H2PO+4+2H2O
当溶液pH在6.5~7.2之间时,H2PO4-是磷存在的主要形态.此时吸附剂表面电荷由正变为负,与H2PO4-之间的静电引力变为静电斥力,导致吸附量降低.可能发生的反应如下:
M-O-+H2PO4-→M-HPO4-+OH-
2M-O-+H2PO4-→M2-PO4-+2OH-
当溶液pH在7.2~11.0之间时,HPO2-4是磷存在的主要形态. 此时吸附剂表面的负电荷越积越多,与HPO2-4由静电斥力逐渐增大,导致吸附量进一步降低. 可能发生的反应如下:
M-O-+HPO2-4→M-PO2-4+OH-
2M-O-+HPO2-4+H2O→M2-PO4-+3OH-
1)制备的铈锰复合氧化物由纳米颗粒组成,展示了明显的纳米结构,比表面积为157 m2 · g-1,等电点为6.5.
2)溶液pH对铈锰复合氧化物吸附磷影响较为明显,随着pH的升高,去除率降低;离子强度对磷的吸附影响不大;铈锰复合氧化物对磷有较好的吸附效果,在pH=7时,最大吸附容量达到28.6 mg · g-1;铈锰复合氧化物对磷有较高的吸附速率,吸附符合准二级动力学模型,吸附过程为化学吸附.水中常见阴离子对铈锰复合氧化物吸附磷影响大小顺序为:SiO32-> CO32-> Cl-≥ SO2-4.
3)铈锰复合氧化物对磷的吸附是特性吸附,形成了内层表面络合物,而不仅仅是静电吸附.磷的主要去除机制是磷酸根取代铈锰复合氧化物表面的羟基,此外,磷酸根和复合氧化物表面的SO2-4之间的离子交换在磷的去除过程中也起着较为重要作用.
| [1] | Agyin-Birikorang S, O'Connor G A. 2007. Lability of drinking water treatment residuals (WTR) immobilized phosphorus: Aging and pH effects[J]. Journal of Environmental Quality, 36(4): 1076-1085 |
| [2] | Blaney L M, Cinar S, SenGupta A K. 2007. Hybrid anion exchanger for trace phosphate removal from water and wastewater[J]. Water Research, 41(7): 1603-1613 |
| [3] | Burton E D, Bush R T, Johnston S G, et al. 2009. Sorption of Arsenic(V) and Arsenic(III) to Schwertmannite[J]. Environmental Science & Technology, 43(24): 9202-9207 |
| [4] | Chitrakar R, Tezuka S, Sonoda A, et al. 2006. Phosphate adsorption on synthetic goethite and akaganeite[J]. Journal of Colloid and Interface Science, 298(2): 602-608 |
| [5] | de-Bashan L E, Bashan Y. 2004. Recent advances in removing phosphorus from wastewater and its future use as fertilizer (1997-2003)[J]. Water Research, 38(19): 4222-4246 |
| [6] | Deng H, Yu X L. 2012. Adsorption of fluoride, arsenate and phosphate in aqueous solution by cerium impregnated fibrous protein[J]. Chemical Engineering Journal, 184: 205-212 |
| [7] | Deng S B, Liu H, Zhou W, et al. 2011. Mn-Ce oxide as a high-capacity adsorbent for fluoride removal from water[J]. Journal of Hazardous Materials, 186(2/3): 1360-1366 |
| [8] | Donnert D, Salecker M. 1999. Elimination of phosphorus from waste water by crystallization[J]. Environmental Technology, 20(7): 735-742 |
| [9] | Feng Q Z, Zhang Z Y, Ma Y H, et al. 2012. Adsorption and desorption characteristics of arsenic onto ceria nanoparticles[J]. Nanoscale Research Letters, 7: 84-91 |
| [10] | Giesler R, Andersson T, Lvgren L, et al. 2005. Phosphate sorption in aluminum-and iron-rich humus soils[J]. Soil Science Society of America, 69(1): 77-86 |
| [11] | Guo H C, Li W J, Wang H Y, et al. 2011. A study of phosphate adsorption by different temperature treated hydrous cerium oxides[J]. Rare Metals, 30(1): 58-62 |
| [12] | Gupta K, Bhattacharya S, Nandi D, et al. 2011. Ceria associated manganese oxide nanoparticles: Synthesis, characterization and arsenic(V) sorption behavior[J]. Chemical Engineering Journal, 172(1): 219-229 |
| [13] | Gupta K, Bhattacharya S, Nandi D, et al. 2012. Arsenic(III) sorption on nanostructured cerium incorporated manganese oxide(NCMO): A physical insight into the mechanistic pathway[J]. Journal of Colloid and Interface Science, 377(1): 269-276 |
| [14] | Ho Y S, McKay G. 1999. Pseudo-second order model for sorption processes[J]. Process Biochemistry, 34(5): 451-465 |
| [15] | Hsia T H, Lo S L, Lin C F, et al. 1994. Characterization of arsenate adsorption on hydrous iron oxide using chemical and physical methods[J]. Colloids and Surfaces (A: Physicochemical and Engineering Aspects), 85(1): 1-7 |
| [16] | Kang S K, Choo K H, Lim K H. 2003. Use of iron oxide particles as adsorbents to enhance phosphorus removal from secondary wastewater effluent[J]. Separation Science and Technology, 38(15): 3853-3874 |
| [17] | Kostura B, Kulveitová H, Leško J. 2005. Blast furnace slags as sorbents of phosphate from water solutions[J]. Water Research, 39(9): 1795-1802 |
| [18] | Lagergren S. 1898. Zurtheorie dersogenannten adsorption gelöster stoffe[J]. Kungliga Svenska Vetenskapsakademiens Handlingar, 24(4): 1-39 |
| [19] | Lefèvre G. 2004. In situ Fourier-transform infrared spectroscopy studies of inorganic ions adsorption on metal oxides and hydroxides[J]. Advances in Colloid and Interface Science, 107(2/3): 109-123 |
| [20] | 李国亮, 张高生, 陈静, 等. 2012. 纳米结构Fe3O4/Y2O3磁性颗粒的制备、表征及磷吸附行为研究[J]. 环境科学学报, 32(9): 2167-2175 |
| [21] | Li G L, Gao S, Zhang G S, et al. 2014. Enhanced adsorption of phosphate from aqueous solution by nanostructured iron(III)-copper(II) binary oxides[J]. Chemical Engineering Journal, 235: 124-131 |
| [22] | Li R H, Li Q, Gao S A, et al. 2012. Exceptional arsenic adsorption performance of hydrous cerium oxide nanoparticles: Part A. Adsorption capacity and mechanism[J]. Chemical Engineering Journal, 185-186: 127-135 |
| [23] | Liu H L, Sun X F, Yin C Q, et al. 2008. Removal of phosphate by mesoporous ZrO2[J]. Journal of Hazardous Materials, 151(2/3): 616-622 |
| [24] | Long F, Gong J L, Zeng G M, et al. 2011. Removal of phosphate from aqueous solution by magnetic Fe-Zr binary oxide[J]. Chemical Engineering Journal, 171(2): 1-8 |
| [25] | Lopez E, Soto B, Arias M, et al. 1998. Adsorbent properties of red mud and its use for wastewater treatment[J]. Water Research, 32(4): 1314-1322 |
| [26] | McBride M B. 1997. A critique of Diffuse Double Layer Models applied to colloid and surface chemistry[J]. Clays and Clay Minerals, 45(4): 598-608 |
| [27] | Nilchi A, Yaftian M, Aboulhasanlo G, et al. 2009. Adsorption of selected ions on hydrous cerium oxide[J]. Journal of Radioanalytical and Nuclear Chemistry, 279(1): 65-74 |
| [28] | Persson S, Nilsson N, Sjoberg S. 1996. Structure and bonding of orthophosphate ions at the iron oxide-aqueous interface[J]. Journal of Colloid and Interface Science, 177(1): 263-275 |
| [29] | Prochaska C A, Zouboulis A I. 2006. Removal of phosphates by pilot vertical-flow constructed wetlands using a mixture of sand and dolomite as substrate[J]. Ecological Engineering, 26(3): 293-303 |
| [30] | Qu J H. 2008. Research progress of novel adsorption processes in water purification: A review[J]. Journal of Environmental Sciences, 20(1): 1-13 |
| [31] | van Voorthuizen E M, Zwijnenburg A, Wessling M. 2005. Nutrient removal by NF and RO membranes in a decentralized sanitation system[J]. Water Research, 39(15): 3657-3667 |
| [32] | 闫春燕, 伊文涛, 马培华, 等. 2008. 水合二氧化铈的制备、表征及对硼的吸附研究[J]. 中国稀土学报, 26(3): 302-305 |
| [33] | Yao W S, Millero F J. 1996. Adsorption of phosphate on manganese dioxide in seawater[J]. Environmental Science & Technology, 30(2): 536-541 |
| [34] | Yildiz E. 2004. Phosphate removal from water by fly ash using cross flow microfiltration[J]. Separation and Purification Technology, 35(3): 241-252 |
| [35] | Zeng L, Li X M, Liu J D. 2004. Adsorptive removal of phosphate from aqueous solutions using iron oxide tailings[J]. Water Research, 38(5): 1318-1326 |
| [36] | Zhang G S, Liu H J, Liu R P, et al. 2009. Removal of phosphate from water by a Fe-Mn binary oxide adsorbent[J]. Journal of Colloid and Interface Science, 335(2): 168-174 |
| [37] | Zhang G S, Khorshed A, Chen J P. 2013. Simultaneous removal of arsenate and arsenite by a nanostructured zirconium-manganese binary hydrous oxide: Behavior and mechanism[J]. Journal of Colloid and Interface Science, 397: 137-143 |
| [38] | Zhang Y, Yang M, Dou X M, et al. 2005. Arsenate adsorption on an Fe-Ce bimetal oxide adsorbent: role of surface properties[J]. Environmental Science & Technology, 39(18): 7246-7253 |
 2015, Vol. 35
2015, Vol. 35


