2. 广西华蓝设计(集团)有限公司, 南宁 530011
2. Guangxi Hualan Design and Consulting Group Co. Ltd, Nanning 530011
介质阻挡放电(DBD)等离子技术作为一种高级氧化技术因其处理效率高、操作简便等优点,引起了极大关注(Gao et al.,2013; Tichonovas et al.,2013; Reddy et al.,2013),其原理是高压放电过程中产生高能电子,与H2O和O2发生碰撞,产生· OH、· O、· H、H2O2和O3等活性物质,这些活性物质与有机物反应使其降解.放电过程中由于分子的电离、跃迁会产生一些物理效应,如紫外辐射、超声波、冲击波、局部高温等进一步加速有机物的降解(Gao et al.,2013; Tichonovas et al.,2013; Reddy et al.,2013).但是DBD技术存在紫外光不能充分利用,能源利用率低的缺点(Tang et al.,2013).TiO2是一种在工业上应用最广泛的催化剂,具有良好的紫外光吸收性能,以及化学稳定性高、无毒、低价、可重复利用等优点.在一定波长(λ<385 nm)的光照射下,TiO2表面产生光生电子(e-)、空穴(h+)和· OH,可有效地降解有机污染物(Zhang et al.,2007).Ghezzar等(2009)将等离子技术与TiO2光催化技术结合起来处理染料废水,投加了TiO2后降解95%的污染物所需时间由60 min缩短到30 min,取得了较好的处理效果.但是该体系存在TiO2难分离的问题,为了克服该问题,已有研究将TiO2负载在玻璃微珠(Wang and Chen,2011)和活性炭(Tang et al.,2013)上,其中活性炭是TiO2最理想的载体.活性炭不仅能将污染物和活性物质富集起来,还能将吸附在活性炭表面的O3催化分解成· OH(Zhang et al.,2010a),使污染物快速降解.同时,活性炭在等离子体系中获得原位再生.颗粒活性炭(GAC)具有发达的孔隙结构、良好的吸附性能、机械强度高、易反复再生和造价低等特点常常用于污染物的去除当中(Tang et al.,2013),因此DBD与TiO2-GAC协同处理是集吸附、催化和再生于一体的方法.目前,Tang等(Tang et al.,2013)研究了该协同体系中各种条件因素(放电电压、初始pH、初始电导率等)对污染物降解的影响,但是关于该协同体系的表观动力学基础研究报道甚少.
甲基橙是一种典型的染料废水,具有排放量大、色度高、难生物氧化、毒性大等特点(Huang et al.,2010),因此选取甲基橙为目标污染物,采用DBD协同TiO2-GAC降解甲基橙,考察该体系的协同处理效果,探究各操作条件的影响,并建立协同体系的反应动力学模型.同时,对该协同体系产生的O3和H2O2进行测定分析,并进行TiO2-GAC的重复使用性能及再生效果的研究.研究结果为等离子水处理技术进一步推向工业化应用提供技术支持.
2 材料与方法(Materials and methods) 2.1 主要试剂与仪器试剂:商品TiO2(P25,80%锐钛矿,20%金红石,比表面积50 m2 · g-1,平均粒径20 nm,德国Degussa公司),颗粒活性炭(椰壳基,粒径为1 mm,比表面积为1105 m2 · g-1,河南郑州活性炭厂),甲基橙、硫酸、氢氧化钠、重铬酸钾、硫酸亚铁铵、硫酸亚铁、硫酸汞、硫代硫酸钠、草酸钛钾、碘化钾、可溶性淀粉均为分析纯.
仪器:国华79-1磁力搅拌器、KQ3200DB超声波清洗机、SKGL-1200马弗炉、FA-004分析天平、pHS-25精密pH计、DDSJ-308A电导率仪、722分光光度计、UV2540紫外分光光度计、Milli-Q超纯水机.
2.2 实验装置实验装置如图 1所示.
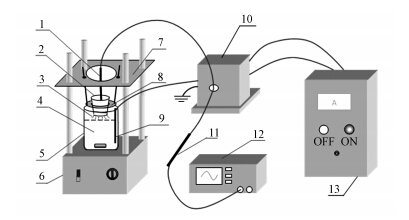 |
| 图 1 介质阻挡放电等离子实验装置(1. 高压电极;2. 陶瓷坩埚;3. 气相放电区域;4. 反应液;5. 玻璃反应器;6. 磁力搅拌器;7.支撑架;8. 陶瓷介质支撑圈;9. 接地电极;10. 变压器;11. 衰减棒;12. 示波器;13. 高频脉冲交流电源) Fig.1 Schematic diagram of dielectric barrier discharge plasma(1. High electric voltage electrode; 2. Ceramic dielectiC-ceramic crucible; 3. Gas phase discharge area; 4. Reaction solution; 5. Glass reactor; 6. Magnetic stirrer; 7. St and ; 8. Ceramic dielectric retaining clip; 9. Ground electrode; 10. Tranformer; 11. Attenuation rod; 12. Oscilloscope; 13. High frequency pusle AC power) |
实验装置如图 1所示.该装置由高频脉冲交流电源、变压器、示波器和反应器组成.其中高频脉冲交流电源的放电参数为:脉冲电压峰-峰值11~14 kV,脉冲宽度22~36 μs,脉冲前沿上升时间21~39 μs和8~13 μs,脉冲频率21~29 kHz;通过高频脉冲电源上的电流表可以直接读出放电时的电源电流,通过示波器(TDS2012)可以读出放电电压;反应器为圆柱形玻璃反应器,直径为9.5 cm,高为12.0 cm,反应液的体积为500 mL;在反应液面上方2~3 mm处放置陶瓷坩埚(容积200 mL)作为放电介质,内装150 mL自来水;变压器输出高压端通过高压线连接至自来水中作为高压电极(阳极),变压器输出接地端通过导线连接到反应液作为接地电极(阴极),当接通高频脉冲电源时,通过介质阻挡放电的方式在气液界面产生等离子.此外,在反应过程中通过磁力搅拌器持续搅拌,使得GAC悬浮于反应液中,并与活性基团充分接触反应.
2.3 实验方法 2.3.1 TiO2-GAC的制备GAC的活化:向GAC中加入去离子水,加热煮沸,弃去去离子水,此过程重复3~4次.然后向GAC中加入体积分数为20%的硝酸溶液,恒温(50 ℃)搅拌2 h;最后用去离子水冲洗GAC,直至冲洗过后的去离子水pH值接近中性,放入烘箱(80 ℃)烘干待用.
TiO2-GAC的制备:称取一定量TiO2,分散于去离子水中,并恒温(50 ℃)加热搅拌20 min,形成乳白色悬浮液;加入一定量活化后的GAC,剧烈搅拌5 min;将所得TiO2悬浮液与GAC的混合物超声2 h;超声结束后,静置一段时间,弃去多余的TiO2悬浮液,在105 ℃条件下烘干,此过程重复2次;将烘干后的样品置于马弗炉中,600 ℃煅烧2 h;取出样品,置于干燥器中冷却待用.
2.3.2 甲基橙降解实验配制一定浓度的甲基橙溶液(500 mL),置于反应器中,并投加一定量的TiO2-GAC,设定反应器的峰值电压,启动反应器,记录反应过程中电流和电压的变化情况,分别在0、5、10、15、20和25 min取样分析,测定甲基橙的浓度及COD,计算甲基橙的降解率、COD去除率和协同强度.其中:
协同强度计算公式(Zhang et al.,2008)为:
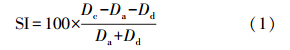
式中,SI为协同强度;Dc为联合处理降解率;Da为单独吸附降解率;Dd单独放电处理的降解率.
2.3.3 溶解O3浓度和H2O2浓度的测定水中溶解O3浓度的测定采用碘量法(Zhang et al.,2010a),H2O2浓度的测定采用草酸钛钾法(Sellers,1980).
2.3.4 重复使用和再生实验重复使用实验:同一份TiO2-GAC样品,多次重复使用,考察其多次重复使用性能,以甲基橙的降解率表示.
再生实验:采用再吸附法(韩严和,2006)评价活性炭的再生效果.
甲基橙在TiO2-GAC上的饱和吸附量计算公式(Narbaitz and Cen,1997):
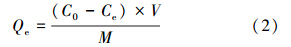
式中,Qe为饱和吸附量(mg · g-1);C0为初始溶液的浓度(mg · L-1);Ce为吸附平衡时溶液的浓度(mg · L-1);V为吸附平衡溶液的体积(L);m为吸附平衡时吸附剂的质量(g).
TiO2-GAC的再生率计算公式(Narbaitz and Cen,1997):
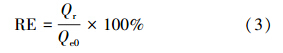
在放电电压为12 kV,甲基橙浓度为100 mg · L-1,溶液体积为500 mL,TiO2-GAC投加量为2 g · L-1,电导率为35 μS · cm-1,pH为6.5时,考察不同体系对甲基橙的降解效果,并比较DBD和DBD+TiO2-GAC体系COD去除率和协同强度,实验结果见图 2和表 1.
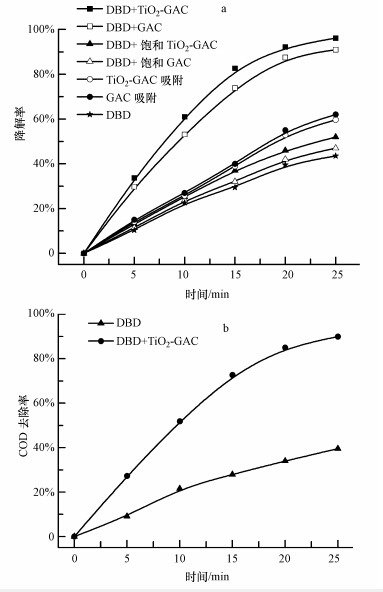 |
| 图 2 DBD与TiO2-GAC协同效果 Fig.2 Synergistic effects of DBD and TiO2-GAC |
| 表 1 DBD与TiO2-GAC降解甲基橙的协同强度 Table 1 Synergy intensities in DBD and TiO2-GAC |
由图 2a可以看出,反应25 min后,单独DBD对甲基橙的降解率为43.5%,而DBD与TiO2-GAC体系对甲基橙的降解率达96.2%,说明TiO2-GAC的引入大大提高了DBD的降解效率.从表 1可以看出,在反应的前15 min,DBD与TiO2-GAC的协同强度为正值,最大可达37.6,主要是由TiO2的光催化以及GAC的吸附、催化作用引起的(Zhang et al.,2010b).由图 2a可知,TiO2-GAC对甲基橙的吸附率小于GAC,分别为59.6%和62.0%,但DBD协同TiO2-GAC体系对甲基橙的降解率比DBD协同GAC体系提高了5%;将吸附饱和的TiO2-GAC和GAC分别投加到DBD中,饱和TiO2-GAC协同DBD体系对甲基橙的降解效果比饱和GAC协同DBD体系提高了约5%,以上两点共同说明了TiO2在DBD协同TiO2-GAC体系中起到了积极作用.这种积极作用主要是通过TiO2光催化反应实现的,因为等离子在放电的过程中产生大量的紫外光,负载在GAC上的TiO2受到紫外光的激发,产生具有强氧化性的空穴和强还原性的电子(Tang et al.,2013),空穴和电子直接或间接与甲基橙作用,促进甲基橙的降解.此外,还发现DBD协同GAC体系、DBD协同饱和GAC体系与单独DBD体系相比,对甲基橙的降解率分别提高了32.1%和2.5%(图 2a),说明除了GAC的吸附作用外,还可能是GAC的催化效应,GAC 能加速 O3分解成· OH(Zhang et al.,2010a),增加了处理效率.随着反应时间的延长,协同强度逐渐减小,反应15 min以后,协同强度为负值.可能这是由于大多数甲基橙分子在前15 min已经被分解,与· OH自由基的反应概率降低.然而这时期,· OH 自由基可能与副产物反应,进一步把它们矿化成 H2O和CO2.此外,GAC和TiO2-GAC对甲基橙的吸附率分别为62%和59.6%,掺杂TiO2后,GAC的吸附能力减弱,但变化不明显,说明TiO2-GAC保持了原GAC较好的吸附能力.
从图 2b可以看出,DBD协同TiO2-GAC体系对COD的去除率达90%,而单独的DBD对COD的去除率只有39.6%,也体现了协同体系有较好的矿化效果.在等离子体系中起氧化作用的主要是O3和· OH,O3的氧化作用生成的副产物多为有机酸或醛,这些产物不能被O3进一步氧化(Grabowski et al.,2007),而· OH可以无选择性地氧化甲基橙或副产物(Gao et al.,2013),将其矿化为CO2和H2O.协同体系体现出较好的矿化效果,说明在TiO2-GAC的催化作用下该体系能够产生更多的· OH,并作用于甲基橙及副产物,提高了COD的去除率.
3.2 动力学研究 3.2.1 反应动力学模型的建立DBD协同TiO2-GAC体系降解甲基橙的过程十分复杂,它涉及到放电物理过程、等离子体中的粒子碰撞过程和自由基化学反应等过程,因此其化学动力学的研究不只是研究自由基化学反应动力学,同时还应结合包含表征放电状态参数的放电物理模型.最常见的研究方法是利用实验动力学数据确定动力学方程.该方法主要特征是忽略具体的放电物理细节和放电过程中的各种反应途径,将放电等离子体化学反应器当作“黑箱”问题来进行处理,仅考虑模型的输入与输出问题和描述反应条件的宏观参数.因此,该体系的反应动力学方程可以按照一般的化学反应动力学方法来研究(程虎,2007).
本研究通过对放电电压、初始pH、初始电导率、甲基橙浓度、TiO2-GAC 投加量对甲基橙浓度(Ct)时间(t)关系的影响,且研究表明通过三次多项式(Y=A+B1X+B2X2+B3X3)能够较好地拟合体系浓度和反应时间的关系(王华柱,2011),并采用初始浓度法,通过t=0时该方程对t的倒数得到初始反应速率r0(见表 2),从而建立DBD协同TiO2-GAC体系降解甲基橙的表观反应动力学模型.
| 表 2 不同操作条件对初始反应速率的影响 Table 2 Effects of various operating conditions on initial rate by DBD and TiO2-GAC |
在甲基橙初始浓度为100 mg · L-1,溶液体积为500 mL,TiO2-GAC投加量为2 g · L-1,初始电导率35 μS · cm-1,初始pH为6.5时,研究放电电压对甲基橙降解的影响.实验结果如图 3所示.
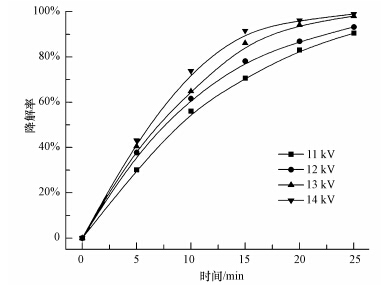 |
| 图 3 不同放电电压对甲基橙降解的影响 Fig.3 Effect of peak voltage on degradation of methyl orange |
由图 3可知,随着放电电压的升高,甲基橙的降解率升高.同时,由表 2可知,初始反应速率也升高.主要是因为电压升高,向反应器中注入的能量增多,电场强度变强,提高了自由电子的能量和速度,产生更多的活性物质,活性物质与甲基橙的接触、碰撞和反应的机率提高,致使更多的甲基橙被氧化降解(Hernández-Leal et al.,2011).此外,电压升高,等离子体系中的物理效应增强,更多的紫外光激发TiO2产生电子和空穴,直接或间接地与甲基橙反应,进而提高降解效率.
3.2.3 初始pH值的影响在放电电压为12 kV,甲基橙初始浓度为100 mg · L-1,溶液体积为500 mL,TiO2-GAC投加量为2 g · L-1,考察初始pH对甲基橙降解的影响.由于调节溶液 pH 值会增加溶液电导率,因此在调节 pH 值时同时调节电导率,以保证实验条件的一致性,消除因溶液电导率不同而造成处理效果的差异.实验结果如图 4所示.
由图 4和表 2可知,溶液初始pH值为2时降解率最高,降解率为96.55%,而pH为10时降解率最低,降解率为78.93%,pH由2变化到10,初始反应速率由9.5 mg · L-1 · min-1迅速降到5.9 mg · L-1 · min-1,与Wang等人(Wang and Chen,2011)有关脉冲放电体系中溶液初始pH值对染料废水脱色效果影响的研究结果一致.一方面,O3在不同的pH的条件下作用于有机物的机理不同.一般认为,酸性或中性条件下反应遵循直接O3氧化作用机理,在碱性条件下遵循自由基作用机理(Irmak et al.,2005).pH值升高,OH-浓度增加,促进了O3的分解,加速了· OH的生成,但是在碱性条件下甲基橙的降解过程中产生的CO2以CO2-3形式存在,CO2-3是· OH的猝灭剂,与· OH反应速率常数达4.2×108 L · mol-1 · s-1(曲险峰等,2007),因此在碱性条件下,虽然O3分解速度加快,但在很短的时间内分解产生的· OH很快淬灭,导致降解率降低.另一方面,起主要氧化作用的· OH在酸性条件比碱性条件下氧化能力强(Hao et al.,2007).因此,在酸性条件下更有利于反应的进行.
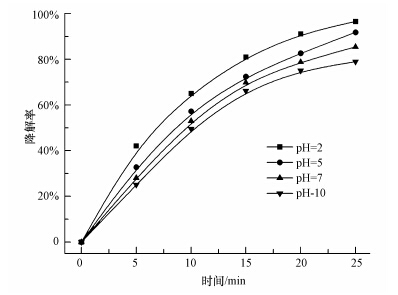 |
| 图 4 不同pH对甲基橙降解的影响 Fig.4 Effect of pH on degradation of methyl orange |
在放电电压为12 kV,甲基橙初始浓度为100 mg · L-1,溶液体积为500 mL,TiO2-GAC投加量为2 g · L-1,初始pH 为6.5时,考察初始电导率对甲基橙降解的影响,实验结果见图 5.从图 5和表 2可以看出,随着溶液初始电导率的增加,甲基橙的降解率和初始反应速率减小,但变化不显著,与高丽红等(2012)的研究结果一致.在DBD体系中,加入TiO2-GAC后,可充分利用体系中产生的O3和紫外光.但随着电导率的增加,水溶液中的电场力降低,减少了高能电子的数量,使放电产生的流光变短,活性物种的产率下降,导致降解率逐渐降低(Zhang et al.,2010c).同时,电导率的增加,导致O3在水中的溶解度降低(Sunka,2001),不利于协同体系催化作用的进行.
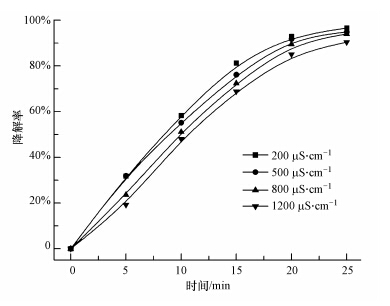 |
| 图 5 不同初始电导率对甲基橙降解的影响 Fig.5 Effect of initial solution conductivity on degradation of methyl orange |
在放电电压为12 kV,溶液体积为500 mL,TiO2-GAC投加量为2 g · L-1,初始电导率为27~65 μS · cm-1,溶液初始pH为6.3~7.1时,考察初始浓度对甲基橙降解的影响,实验结果见图 6.
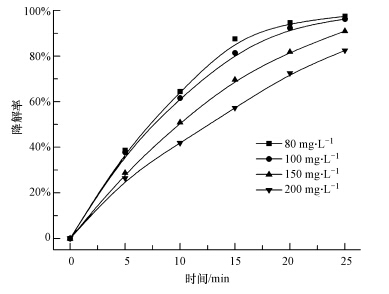 |
| 图 6 初始浓度对甲基橙降解的影响 Fig.6 Effect of initial concentration on degradation of methyl orange |
由图 6可知,随着甲基橙初始浓度的增加,甲基橙的降解率逐渐降低,是因为在稳定的放电过程中,协同体系产生的活性物质的量维持在一定的水平(Jiang et al.,2012),活性物质不仅与甲基橙反应,还与反应过程中生成的副产物反应.当甲基橙浓度增加时,单位体积内的甲基橙分子数增加,生成的副产物也增加,副产物与甲基橙竞争反应更激烈,因此甲基橙初始浓度升高时降解率降低.然而,甲基橙浓度升高,初始反应速率逐渐增大,甲基橙初始浓度从80 mg · L-1增加到200 mg · L-1时,初始反应速率由6.8 mg · L-1 · min-1增加到10.9 mg · L-1 · min-1,是因为甲基橙浓度增大,甲基橙分子与活性物质的碰撞次数增大,从而提高了活性物质的利用率,因此初始反应速率呈上升的趋势.
3.2.6 TiO2-GAC投加量的影响在放电电压为12 kV,甲基橙初始浓度为100 mg · L-1,溶液体积为500 mL,初始电导率35 μS · cm-1,初始pH为6.5时,考察TiO2-GAC投加量对甲基橙降解的影响,实验结果如图 7所示.
从图 7中可以看出,随着投加量的增加甲基橙的降解率逐渐增加,但当投加量超过2 g · L-1时,甲基橙降解率的增加减缓.从表 2也可以看出,TiO2-GAC投加量从1 g · L-1增加到2 g · L-1时,初始反应速率迅速从4.8 mg · L-1 · min-1增至8.3 mg · L-1 · min-1,可能是由于催化剂的增加,吸附在催化剂表面的污染物较多,从而实现了污染物的富集,同时协同体系产生的· OH、O3等物质也在GAC表面聚集,减少了活性物质与污染物分子的扩散距离,实现了甲基橙的快速高效降解.但当TiO2-GAC投加量大于2.0 g · L-1时,甲基橙的降解率变化不明显,可能是因为投加量过多,阻碍了等离子通道的产生和光辐射的穿透,不能充分利用紫外光激发TiO2产生更多的活性物质(周志刚,2005).
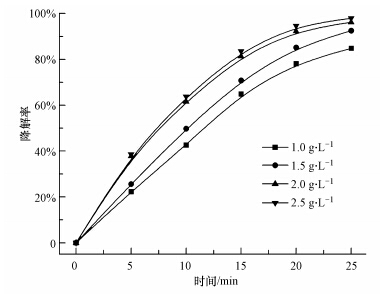 |
| 图 7 不同TiO2-GAC投加量对甲基橙降解的影响 Fig.7 Effect of TiO2-GAC concentrations on degradation of methyl orange |
假定t时刻体系中放电电压为U,氢氧根离子浓度为H,电导率为D,甲基橙的浓度为C,GAC-TiO2投加量为G,该体系降解甲基橙的表观动力学方程为(程虎,2007):
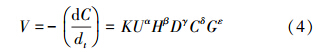
式中,α、β、λ、δ、ε分别为放电电压、氢氧根离子、电导率、TiO2-GAC投加量和甲基橙浓度的反应级数,K是总反应速率常数.
对上式两边取对数,如下所示:
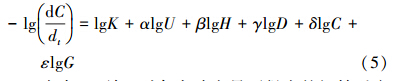
由表 2可知,对各实验变量下得出的初始反应速率(r0)与变量CB做lgr0(y)-lgCB(x)方程拟合(R2均在0.995以上),得到放电电压、氢氧根离子浓度、电导率、甲基橙浓度和TiO2-GAC投加量的反应级数分别为:α=1.304,β=-0.027,λ= -0.099,δ=0.484,ε=0.689.因此,反应总级数为2.352.
由各实验变量下的lgr0(y)-lgCB(x)方程,还得到以下关系:
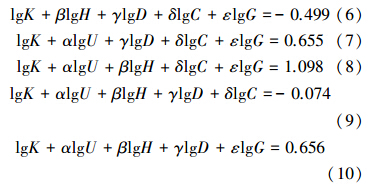
将式(6)至式(10)相加得:
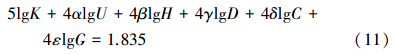
将放电电压U=12 kV,氢氧根离子浓度H=10-7.5 mol · L-1,电导率D=35 μS · cm-1,甲基橙初始浓度C=100 mg · L-1,TiO2-GAC投加量G=2 g · L-1,α= 1.304,β=-0.027,λ=-0.099,δ=0.484,ε=0.689代入式(11)中,经计算K=1.83×10-2;将以上结果代入式(4),得到协同体系降解甲基橙的表观反应动力学方程为:
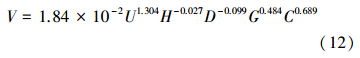
在放电电压为12 kV,反应液为去离子水,体积为500 mL,TiO2-GAC投加量为2 g · L-1,测定投加TiO2-GAC前后反应过程中O3、H2O2的浓度,实验结果分别如图 8所示.
从图 8可以看出,DBD协同TiO2-GAC体系比单独DBD体系生成的O3的量小,而生成的H2O2的量的趋势正好相反.这是因为在DBD体系中投加了TiO2-GAC,GAC催化O3转化成· OH,使该体系生成更多的双氧水.同时,等离子体系中产生的紫外光激发TiO2产生空穴和电子,O3俘获电子,生成O· -3,经过一系列的自由基反应后,最终生成· OH,也使得协同体系的H2O2的量增多(Hao et al.,2007),故该协同体系体现出了较好的协同效果.此外,DBD和DBD+TiO2-GAC体系反应10 min后都有下降的趋势,可能是协同体系在降解甲基橙的过程中溶液的电导率逐渐增大,导致了O3在水中的溶解度变小(Sunka,2001).
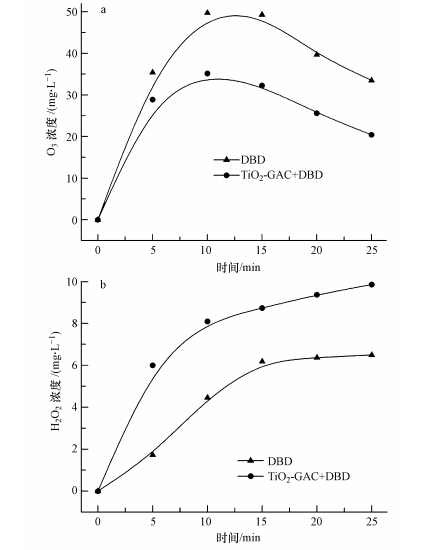 |
| 图 8 DBD、DBD+TiO2-GAC体系产生臭氧、过氧化氢的量 Fig.8 The amount of dissolved ozone and hydrogen peroxide produced in DBD,DBD and TiO2-GAC system |
在DBD与TiO2-GAC联合使用过程中,TiO2-GAC作为催化剂,不但要具备较高的催化活性,而且也要有较长的使用寿命,这决定了DBD与TiO2-GAC联合处理的应用前景.为了考察TiO2-GAC在协同处理过程中的使用寿命,研究了同一份TiO2-GAC随使用次数的变化情况.5次循环降解甲基橙的效果如图 9所示.
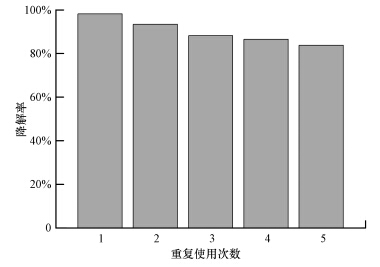 |
| 图 9 TiO2-GAC的重复使用性能 Fig.9 Repeat performance of TiO2-GAC |
从图 9看出,5次循环使用后甲基橙的降解率都会维持在83%以上,均高于单独DBD体系中甲基橙的降解率,因此,TiO2-GAC具有良好的重复使用性能.
分别测定原TiO2-GAC和协同处理5个循环后的TiO2-GAC的饱和吸附量,实验结果分别为143.7 mg · g-1和115.0 mg · g-1,即TiO2-GAC的再生率为80%,可见DBD体系对TiO2-GAC有较好的再生效果.
4 结论(Conclusions)1)DBD与TiO2-GAC协同处理甲基橙,表现出明显的协同效应,协同强度最大可达37.6,反应25 min后,甲基橙的降解率为96.2%,COD的去除率为90%.
2)DBD与TiO2-GAC协同体系降解甲基橙的过程符合表观反应动力学模型,模型值与实验值吻合良好,其表观反应动力学方程为V=1.83×10-2U1.304H-0.027D-0.099G0.484C0.689,反应总级数为2.352.
3)DBD与TiO2-GAC协同体系的O3浓度降低,而H2O2的浓度升高,说明TiO2-GAC起到了很好的催化作用;
4)TiO2-GAC经5次循环使用后,甲基橙的降解率都会维持在83%以上;TiO2-GAC在DBD中获得了原位再生,再生率达80%.
| [1] | 程虎. 2007. 气液两相体放电化学动力学的初步研究[D]. 武汉: 华中科技大学 |
| [2] | 高丽红, 喻泽斌, 黄俊. 2012. 高频脉冲介质阻挡放电去除水中17β-雌二醇 [J]. 环境工程学报, 6(12): 4475-4480 |
| [3] | Gao L H, Sun L, Wan S G, et al. 2013. Degradation kinetics and mechanism of emerging contaminants in water by dielectric barrier discharge non-thermal plasma: The case of 17β-Estradiol [J]. Chemical Engineering Journal, 228: 790-798 |
| [4] | Ghezzar M R, Abdelmalek F, Belhadj M, et al. 2009. Enhancement of the bleaching and degradation of textile wastewaters by Gliding arc discharge plasma in the presence of TiO2 catalyst [J]. Journal of Hazardous Materials, 164(2/3): 1266-1274 |
| [5] | Grabowski L R, van Veldhuizen E M, Pemen A J M, et al. 2007. Breakdown of methylene blue and methyl orange by pulsed corona discharge [J]. Plasma Sources Science & Technology, 16(2): 226-232 |
| [6] | 韩严和. 2006. 电增强活性炭纤维吸附水中部分有机物的研究[D]. 大连: 大连理工大学 |
| [7] | Hao X L, Zhou M H, Lei L C. 2007. Non-thermal plasma-induced photocatalytic degradation of 4-chlorophenol in water [J]. Journal of Hazardous Materials, 141(3): 475-482 |
| [8] | Hernández-Leal L, Temmink H, Zeeman G, et al. 2011. Removal of micropollutants from aerobically treated grey water via ozone and activated carbon [J]. Water Research, 45(9): 2887-2896 |
| [9] | Huang F M, Chen L, Wang H L, et al. 2010. Analysis of the degradation mechanism of methylene blue by atmospheric pressure dielectric barrier discharge plasma [J]. Chemical Engineering Journal, 162(1): 250-256 |
| [10] | Irmak S, Erbatur O, Akgerman A. 2005. Degradation of 17 β-estradiol and bisphenol A in aqueous medium by using ozone and ozone/UV techniques [J]. Journal of Hazardous Materials, 126(1/3): 54-62 |
| [11] | Jiang B, Zheng J T, Liu Q, et al. 2012. Degradation of azo dye using non-thermal plasma advanced oxidation process in a circulatory airtight reactor system [J]. Chemical Engineering Journal, 204-206: 32-39 |
| [12] | Narbaitz R M, Cen J. 1997. Alternative methods for determining the percentage regeneration of activated carbon [J]. Water Research, 31(10): 2532-2542 |
| [13] | 曲险峰, 郑经堂, 何小超, 等. 2007. ACF催化臭氧化降解苯酚的反应参数影响[J]. 化工进展, 26(9): 1283-1287 |
| [14] | Reddy P M K, Raju B R, Karuppiah J, et al. 2013. Degradation and mineralization of methylene blue by dielectric barrier discharge non-thermal plasma reactor [J]. Chemical Engineering Journal, 217: 41-47 |
| [15] | Sellers R M. 1980. Spectrophotometric determination of hydrogen peroxide using potassium titanium (IV) oxalate [J]. Analyst, 105(1255): 950-954 |
| [16] | Sunka P. 2001. Pulse electrical discharges in water and their applications [J]. Physics of Plasmas, 8(5): 2587-2594 |
| [17] | Tang S F, Lu N, Li J, et al. 2013. Improved phenol decomposition and simultaneous regeneration of granular activated carbon by the addition of a titanium dioxide catalyst under a dielectric barrier discharge plasma [J]. Carbon, 53: 380-390 |
| [18] | Tichonovas M, Krugly E, Racys V, et al. 2013. Degradation of various textile dyes as wastewater pollutants under dielectric barrier discharge plasma treatment [J]. Chemical Engineering Journal, 229: 9-19 |
| [19] | Wang H J, Chen X Y. 2011. Kinetic analysis and energy efficiency of phenol degradation in a plasma-photocatalysis system [J]. Journal of Hazardous Materials, 186(2/3): 1888-1892 |
| [20] | 王华柱. 2011. 脉冲放电协同TiO2处理染料废水的数值模拟研究[D]. 赣州: 江西理工大学 |
| [21] | Zhang Y J, Zhou J L, Ning B Q. 2007. Photodegradation of estrone and 17 β-estradiol in water [J]. Water Research, 41(1): 19-26 |
| [22] | Zhang Y Z, Zheng J T, Qu X F, et al. 2008. Design of a novel non-equilibrium plasma-based water treatment reactor [J]. Chemosphere, 70(8): 1518-1524 |
| [23] | Zhang Y Z, Sun B Y, Deng S H, et al. 2010a. Methyl orange degradation by pulsed discharge in the presence of activated carbon fibers [J]. Chemical Engineering Journal, 159(1/3): 47-52 |
| [24] | Zhang Y Z, Xiong X Y, Han Y, et al. 2010b. Application of titanium dioxide-loaded activated carbon fiber in a pulsed discharge reactor for degradation of methyl orange [J]. Chemical Engineering Journal, 162(3): 1045-1049 |
| [25] | Zhang Y Z, Deng S H, Sun B Y, et al. 2010c. Preparation of TiO2-loaded activated carbon fiber hybrids and application in a pulsed discharge reactor for decomposition of methyl orange [J]. Journal of Colloid and Interface Science, 347(2): 260-266 |
| [26] | 周志刚. 2005. 高压脉冲放电/TiO2协同处理染料废水的实验研究[D]. 大连: 大连理工大学 |
 2015, Vol. 35
2015, Vol. 35


