白腐真菌处理染料废水是一种新兴的有效技术(Vanhullea et al., 2008).白腐真菌产生的胞外木质素降解酶主要包括木质素过氧化酶(Lignin peroxidase,Lip)、锰过氧化酶(Manganase peroxidase,MnP)和漆酶(Laccase,Lac),被认为是降解木质素和染料等污染物的特殊酶系(Spadaro et al., 1992).这些酶具有非特异性、无需底物诱导的特殊性能,对许多结构不同、高度稳定、难降解的高分子有机物质,包括不同结构的多种染料具有广谱的降解能力;通过白腐真菌所分泌的这些特殊的降解酶系或其他机制可以将各种人工合成的染料彻底降解为CO2和H2O(李慧蓉,1996).直接湖蓝5B是一种广泛使用的双偶氮染料.研究发现,含偶氮染料的废水具有耐光性、耐生物降解性、抗掉色性和抗氧化性,以及能在水体中稳定存在等特点,而且偶氮染料的前体及其中间产物芳香胺具有致癌性,因此,偶氮染料废水处理的研究成为热点(Yin et al., 2007).
平菇(Pleurotus ostreatus)是一种常见的白腐菌,其分泌的木质素降解酶主要包括漆酶和锰过氧化物酶,但不分泌木质素过氧化物酶(Poxdnyakova et al., 2006).有关白腐真菌对偶氮染料的脱色研究国内外已有较多的报道(Khan et al., 2013; Murugesan et al., 2009; Pandey et al., 2013; Papadopoulou et al., 2013; Pointing et al., 2000),酵母菌对偶氮染料脱色的研究也有少量的报道(Jadhav et al., 2007; Yang et al., 2008; 阮晓东等,2009),但有关白腐真菌和酵母菌混菌发酵,以及用预适应培养的菌种接种对发酵体系的木质素降解酶活性和对染料的脱色作用的研究还鲜见报道.因此,本文以稻草和豆渣为平菇深层培养的碳、氮源,研究平菇分别和酿酒酵母、产朊假丝酵母和热带假丝酵母混菌培养,以及用不同浓度直接湖蓝5B预培养的菌种接种对发酵体系分泌的木质素降解酶活性和直接湖蓝5B脱色率的影响,旨在探索低培养成本和高效降解的白腐真菌处理偶氮废水的新方法.
2 材料与方法(Materials and methods) 2.1 实验材料 2.1.1 实验菌种平菇(Pleurotus ostreatus)AF-1为本实验室分离保藏.酿酒酵母(Saccharomyces cerevisiae)CGMCC 2.118、产朊假丝酵母(C and ida utilis)AS2.281和热带假丝酵母(C and ida tropicalis)AS 2.587均购自中国农业科学院.
2.1.2 实验材料及试剂稻草秸秆(当年产)取自芜湖郊区,粉碎备用.马铃薯和豆渣购于农贸市场,豆渣烘干粉碎备用.麦芽购自芜湖大江啤酒厂.葡萄糖、磷酸二氢钾、硫酸镁、直接湖蓝5B、愈创木酚、醋酸钠、邻联甲苯胺、琥珀酸钠、酒石酸钠、亚甲基蓝等均为国产分析纯.
2.1.3 主要培养基平菇斜面培养基:PDA.平菇液体菌种培养基:葡萄糖2%、蛋白胨0.2%、MgSO4 · 7H2O 0.05%、CaCl2 0.01%、KH2PO4 0.05%,pH自然.平菇液体发酵基础培养基:稻草粉3%、豆渣粉1%、MgSO4 0.05%、KH2PO4 0.05%,pH自然.酵母菌麦芽汁液体培养基的制备:麦芽(打碎)∶ 蒸馏水=1 ∶ 6(质量比),63.5 ℃恒温水浴加热1.5 h,再68.5 ℃恒温水浴加热1.5 h,水浴加热期间用玻璃棒不断搅拌,10层纱布过滤,取滤液,pH自然.酵母菌斜面培养基:麦芽汁琼脂固体培养基.所有培养基均121 ℃灭菌20 min.
2.2 实验方法 2.2.1 染料溶液的配制蒸馏水配制成直接湖蓝5B浓度为5 g · L-1的母液,再添加不同量到各培养基中,得到所需浓度.研究发现,直接湖蓝5B浓度为100 mg · L-1时,平菇对直接湖蓝5B脱色效果最好,故后面脱色率研究选用的染料浓度为100 mg · L-1.
2.2.2 菌种制备及深层培养方法深层培养均采用500 mL三角烧瓶,装液体培养基150 mL.平菇液体菌种制备:在液体菌种培养基中接入PDA斜面菌种,25 ℃、130 r · min-1振荡培养6 d,再以10%(V/V)接种量转接到液体菌种培养基,25 ℃、130 r · min-1振荡培养3 d成为平菇二级液体菌种.酵母菌液体菌种制备:酵母菌斜面菌种接种至麦芽汁液体培养基中,28 ℃、130 r · min-1摇床振荡培养18 h.
发酵试验均采用平菇液体发酵基础培养基,平菇菌种采用二级液体菌种,平菇和酵母菌液体菌种接种量均为10%(V/V).混菌发酵时,酵母菌菌种在平菇接种1 d后接入,25 ℃、130 r · min-1振荡培养.
2.2.3 菌丝体产量的测定发酵10 d后,培养液经80目筛过滤,把菌球上未过滤掉的稻草粉用蒸馏水冲洗干净,然后置于100 ℃烘箱中烘至恒重,电子天平称重.
2.2.4 粗酶液的制备在无菌条件下,每隔48 h移取5 mL菌液,3000 r · min-1离心15 min后取上层清液,即为粗酶液.
2.2.5 木质素酶活性的检测漆酶(Lac)活性测定参考文献方法(朱陶等,2002):定义为在600 nm处每分钟引起OD值增加0.1单位为1个酶活力单位(U).锰过氧化物酶(MnP)活性测定参照文献方法(Arora et al., 2001):定义为在波长465 nm处每分钟引起OD值增加0.01单位为一个酶活单位(U).
2.2.6 脱色率的检测无菌条件下,每隔48 h取菌液5 mL,4000 r · min-1离心10 min取上清液,测上清液在600 nm(直接湖蓝5B最大吸收波长)处吸光度为A;同理,测得不加菌种的含同浓度直接湖蓝5B的培养基上清液的吸光度为A0(排除了培养料对染料吸附的影响).按朗伯特-比耳定律计算染料脱色率η:
η=(A0- A)/A0×100%
2.6 数据处理每种处理均设3个重复,数据用SPSS13.0软件进行单因素方差分析,结果取平均值±标准误.
3 结果与分析(Results and analysis) 3.1 不同浓度直接湖蓝5B对平菇菌丝体产量的影响以稻草为主要基质的培养基中,不同浓度的直接湖蓝5B对平菇深层培养菌丝体产量的影响见图 1.与对照相比,100~400 mg · L-1的直接湖蓝5B对平菇菌丝体产量有显著的促进作用,染料浓度为200 mg · L-1时最高,菌丝体干重达29.4 g · L-1,比对照高出12.7 g · L-1;直接湖蓝5B浓度为800 mg · L-1时,则显著抑制了菌丝体的产量,菌丝体干重为10.3 g · L-1,比对照少6.4 g · L-1.
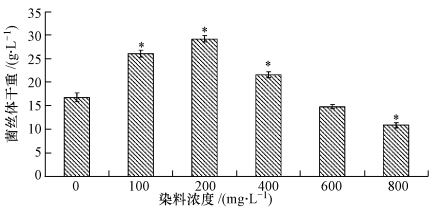 |
| 图 1 不同浓度直接湖蓝5B对平菇菌体产量的影响(*表示与对照相比具有显著性差异,p<0.05) Fig. 1 Effects of direct sky blue 5B at different concentrations on the dry weight of P. ostreatus mycelia(*indicates significantly different from the controls,p<0.05) |
平菇深层培养对不同浓度(100、150、200、300、400 mg · L-1)直接湖蓝5B的脱色效果见图 2.染料浓度越高,脱色率越低.随着发酵时间的延长,脱色效果越好;在发酵的第10 d,直接湖蓝5B浓度为100 mg · L-1时,脱色率可达到85.9%,而染料浓度为400 mg · L-1时,脱色率仅为68.4%.
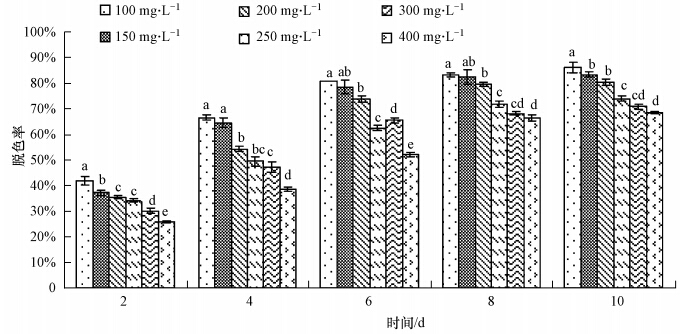 |
| 图 2 平菇对不同浓度直接湖蓝5B的脱色率(同列不同字母间表示差异显著,p<0.05) Fig. 2 Decolorization rate of different concentrations of direct sky blue 5B by P. ostreatus (Different letters indicate significant difference in the same column,p<0.05) |
以平菇单菌发酵为对照,平菇分别与酿酒酵母、产朊假丝酵母和热带假丝酵母混菌发酵漆酶和锰过氧化物酶的活性见图 3.随着发酵时间的延长,漆酶、锰过氧化物酶活性逐渐提高,在第8 d酶活达到峰值,到第10 d两种酶的活性有了显著下降.与对照相比,平菇分别与酿酒酵母和产朊假丝酵母混菌发酵,体系中漆酶活性有显著提高,在发酵第8 d,活性分别达到578 U · L-1和630 U · L-1,分别高出对照组129 U · L-1和181 U · L-1.3种酵母与平菇混菌发酵均可显著提高发酵体系中的锰过氧化物酶活性,其中,与产朊假丝酵母混菌时促进效果最好,第8 d其活性达到380 U · L-1,较对照提高了177 U · L-1.
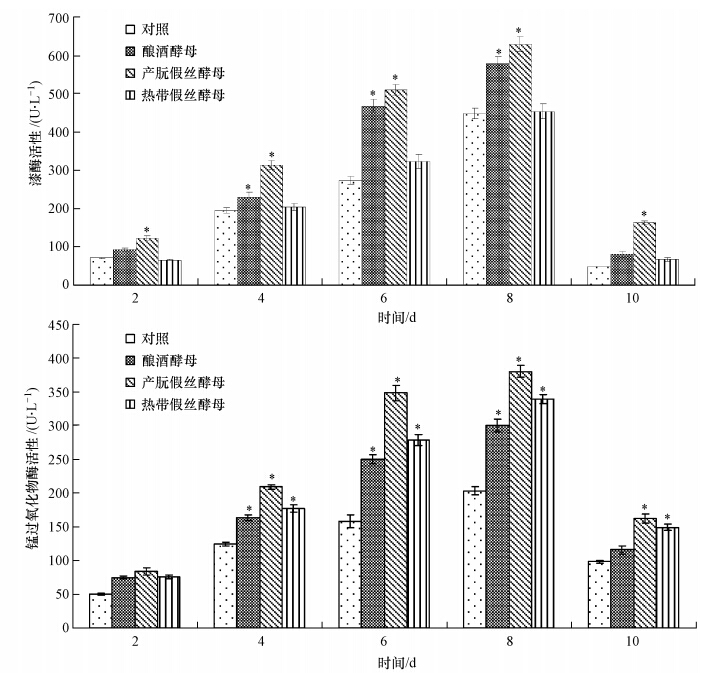 |
| 图 3 平菇和3种酵母菌混菌培养发酵体系漆酶和锰过氧化物酶的活性(*表示与对照相比具有显著性差异,p<0.05,下同) Fig. 3 Lac and MnP activity in the mixed-strain fermentation system of P. ostreatus and three yeasts(* indicates significantly different from the controls,p<0.05,the same below) |
将平菇一级液体菌种分别接种到含50~400 mg · L-1直接湖蓝5B溶液的液体菌种培养基中培养3 d后,再接入到基础发酵培养基中,以不含染料的菌种培养基培养的平菇菌种接种为对照,发酵体系中漆酶和锰过氧化物酶的活性见图 4.用50~200 mg · L-1染料预培养的菌种接种,漆酶活性有显著的提高,其中,预培养的染料浓度为50 mg · L-1时,第8 d漆酶的活性最高,达到616 U · L-1,比对照高出165 U · L-1.50 mg · L-1和100 mg · L-1染料预培养后的菌种接种可显著提高锰过氧化物酶的活性,100 mg · L-1的促进作用最大,其最高活性为282 U · L-1,较对照提高了77 U · L-1.而200~400 mg · L-1染料预培养菌种对锰过氧化物酶的活性影响不显著.
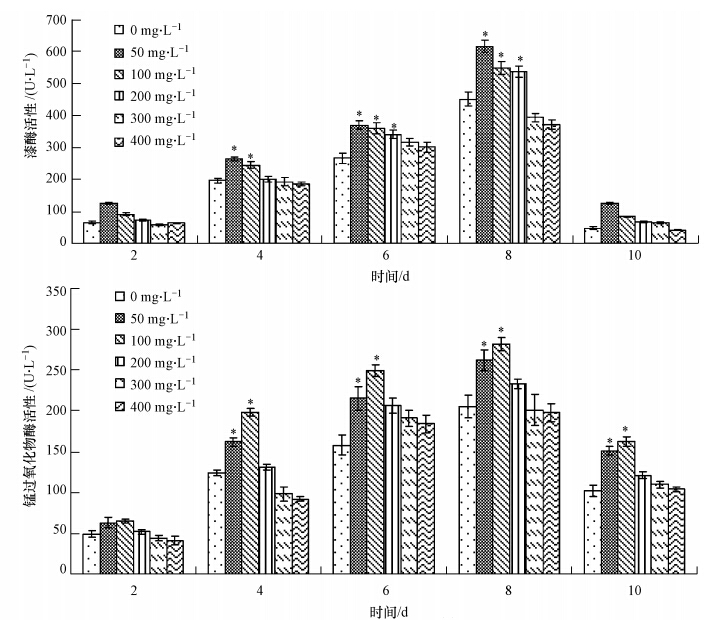 |
| 图 4 不同浓度直接湖蓝5B预适应培养后的平菇菌种对平菇分泌漆酶和锰过氧化物酶的影响 Fig. 4 Effects of pre-adaption P. ostreatus inocula cultured with different concentrations of direct sky blue 5B on the Lac and MnP activity of P. ostreatus |
前面的研究表明,平菇对100 mg · L-1的直接湖蓝5B的脱色效果最好,故以下试验选用直接湖蓝5B的浓度均为100 mg · L-1.平菇深层培养1 d后分别接入酿酒酵母、产朊假丝酵母和热带假丝酵母,以没有接入酵母菌的为对照,发酵体系对直接湖蓝5B脱色率的影响见图 5.3种酵母菌与平菇混菌发酵均显著提高了发酵体系对直接湖蓝5B的脱色率.在平菇培养的第2 d,也就是酵母菌培养的24 h,酿酒酵母和产朊假丝酵母即显著促进了直接湖蓝5B的脱色率,第6~10 d热带假丝酵母也显著提高了直接湖蓝5B的脱色率.平菇与3种酵母混菌发酵对染料的脱色率均超过90%;与产朊假丝酵母混菌发酵时促进效果最好,第10 d脱色率高达96.3%,比对照高出14.2%,而产朊假丝酵母对发酵体系漆酶和锰过氧化物酶活性的促进作用也最高,提示漆酶和锰过氧化物酶的活性与直接湖蓝5B的脱色率可能呈正相关关系.
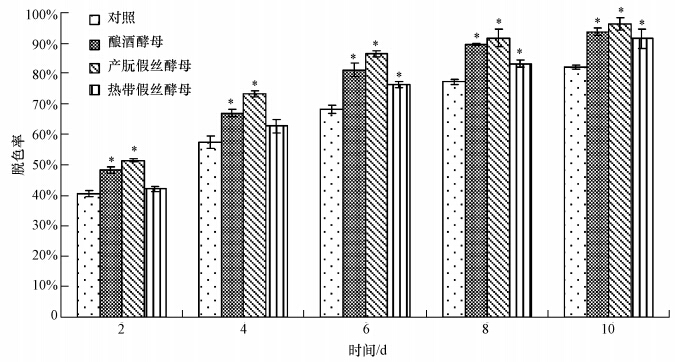 |
| 图 5 平菇和3种酵母菌混菌培养发酵体系中直接湖蓝5B染料的脱色率 Fig. 5 Decolorization rate of direct sky blue5B in the mixed-strain fermentation system of P. ostreatus and three yeasts |
用不同浓度(100、150、200、300、400 mg · L-1)直接湖蓝5B预培养的平菇液体菌种接种对直接湖蓝5B脱色率的影响见图 6.与对照相比,用50 mg · L-1和100 mg · L-1的染料预培养的菌种接种,平菇对直接湖蓝5B脱色率有显著的提高,其最高脱色率分别为92.6%和88.4%,较对照分别提高了9.5%和6.3%.分析发酵体系木质素降解酶活性和染料脱色率之间的关系,同样可以看出,漆酶和锰过氧化物酶的活性与直接湖蓝5B的脱色率基本呈正相关关系.
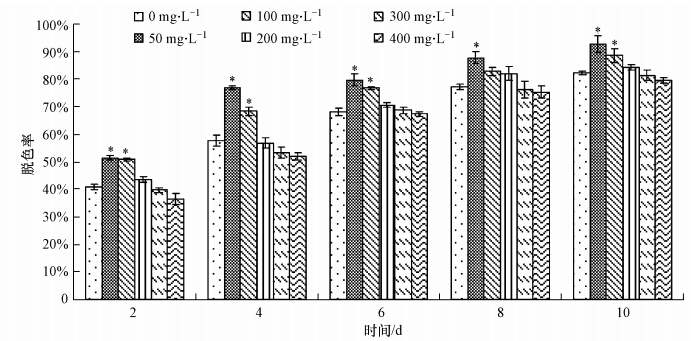 |
| 图 6 不同浓度直接湖蓝5B预适应培养的平菇菌种接种后对直接湖蓝5B脱色率的影响 Fig. 6 Effects of pre-adaption P. ostreatus inocula cultured with different concentrations of direct sky blue 5B on the decolorization rate of direct sky blue 5B |
20世纪80年代《Science》首次报道了白腐真菌黄孢原毛平革菌(Phanerochaete chrysosporium)能向胞外分泌降解木质素的酶,使降解木质素的研究取得重大进展(Tien et al., 1983).白腐真菌因为其极强的降解能力、广谱的降解范围,以及低廉的营养要求、竞争的优势和固液基质的适应性使其在处理染料废水的应用中具有经济、高效实用等多项优势(高大文等,2005).
由于被降解的染料不需进入细胞内代谢,白腐真菌菌体本身不易受到染料的侵害.本研究中,100~400 mg · L-1的直接湖蓝5B对平菇菌丝体生长有显著的促进作用,而800 mg · L-1时则有显著的抑制作用.偶氮染料作为含碳和氮的化合物,白腐真菌可能以其作为碳源或氮源,促进微生物生长;而且随着培养时间的延长,菌体进入次生代谢阶段,分泌木质素胞外酶对染料进行降解,降低了培养液的染料浓度,进而减轻其对菌丝的毒害作用;但发酵体系中酶的活性有限,当环境中染料达到一定的高浓度时,对菌体有毒害作用,会抑制其生长.有关偶氮染料对白腐真菌生长的影响还少见报道,其对生长的影响特别是促进生长的机理还有待于进一步研究.
白腐真菌初生阶段几乎不产生胞外酶,木质素降解酶是在次生代谢阶段产生的,菌丝体的生长与酶的释放在时间上的先后使其在染料废水的处理中需要保证足够的水力停留时间,这给利用白腐真菌实现对工业废水的连续脱色造成了工艺上的困难.当然,菌丝体生长阶段对染料的吸附,而后又在酶释放阶段对其降解,这种机制水平上的协调,又恰好能够克服上述技术问题(李慧蓉,2005).本研究中,平菇在以稻草为主要培养基质的培养基中深层培养2 d后,就进入对数期后的生长,开始分泌漆酶和锰过氧化物酶,在培养的第2 d对染料就有一定的脱色率;深层培养第4~8 d,漆酶和锰过氧化物酶一直保持着较高的活性.有研究表明,玉米秸秆木质纤维素降解液的加入对白腐真菌产木质素酶具有很大的诱导促进作用,不仅可长时间保持酶活,也可缩短其达到酶活峰值的时间;农作物秸秆如稻草液体培养基比土豆液体培养基中木质素降解酶系酶活力高很多,其原因可能是秸秆中的纤维素和半纤维素等物质为白腐真菌的生长提供了营养源,促其快速生长,白腐真菌降解秸秆后生成的小分子片段能诱导其分泌木质素降解酶,菌株不断降解秸秆从而不断促其分泌木质素降解酶(张晓昱等,2004).也有研究表明,一些木质素类降解物能够帮助激发白腐真菌产生木质素降解过氧化物酶(Singh et al., 2008).因此,以稻草等秸秆类作为白腐真菌的主要营养基质,不仅可以节约培养成本,而且可以缩短白腐真菌产木质素降解酶的时间,提高酶产量.
有关pH、温度、CO2、氮源、金属离子、搅拌、染料结构等因素对白腐真菌对偶氮染料脱色的影响已有一些报道(Khan et al., 2013).但关于白腐真菌与酵母菌混菌发酵对脱色效果的影响还未见报道.平菇与产朊假丝酵母混菌固态发酵玉米秸秆,与平菇单菌发酵相比,平菇菌丝生长快,发酵周期缩短1/3(汪建中等,2011).在白腐真菌与酵母菌混菌发酵农作物秸秆的体系中,白腐真菌降解秸秆等的纤维素,为酵母菌的生长提供了碳源,而酵母菌通过消耗还原糖的方式,解除了还原糖对纤维素降解酶的抑制,从而促进了纤维素降解成小分子物质以被白腐真菌和酵母菌利用.已有研究表明,酵母菌能分泌木质素降解酶,对染料也有脱色作用.Yang等(2005)在筛选偶氮染料活性黑5降解菌时,在多形德巴利酵母(Debaryomyces polymorphus)和热带假丝酵母培养体系中检测到锰过氧化物酶的存在.多形德巴利酵母和热带假丝酵母能够对100 mg · L-1活性黑5进行完全的脱色,而脱色作用是由锰过氧化物酶催化的(Yang et al., 2003;2008).酿酒酵母能够对偶氮染料甲基红进行很好的脱色,培养基中检测到漆酶的活性,当然还有其他酶,如偶氮还原酶等(Jadhav et al., 2007).而Villas-Bôas等(2002)在利用苹果渣固态培养产朊假丝酵母时,也在培养液中检测到了较高水平的锰过氧化物酶.本研究中,与平菇单菌发酵相比,平菇和酵母菌混菌发酵,显著提高了发酵体系中木质素降解酶的活性,且显著提高对直接湖蓝5B的脱色率.混菌发酵体系中,两种菌均能分泌木质素降解酶,较平菇单菌发酵酶活性要高;另一方面,酵母菌在生长代谢过程中形成了多种B族维生素和生长因子等,这些物质可能有助于白腐真菌的生长,从而增强了培养体系中锰过氧化物酶和漆酶的活性(杨艳红等,2003).课题组先前的研究也表明,白腐真菌与酵母菌混菌发酵可以提高发酵体系中木质素降解酶活性(Ke et al., 2011;汪建中等,2011),进而增强了平菇降解木质素的能力,而木质素的降解可以使稻草纤维素暴露,进一步促进了平菇对纤维素的降解,从而为平菇和酵母菌的生长提供更多的碳源,因此,平菇和酵母菌混菌培养是一种互惠互利的共生关系.分析漆酶和锰过氧化物酶活性与染料脱色率间的关系可以看出,平菇单菌及平菇与酵母菌混菌培养对直接湖蓝5B的脱色可能是其分泌的漆酶和锰过氧化物酶作用的结果.但Lucas等(2006)的研究表明,橄榄假丝酵母(C and ida oleophila)能够对200 mg · L-1活性黑5进行完全的脱色,但脱色发生在对数生长期,未检测到漆酶和锰过氧化物酶的活性,说明不同酵母菌对染料脱色,可能其作用的酶种类不尽相同.
虽然白腐真菌分泌的染料降解酶系是在营养条件限制的情况下次生代谢过程中产生的,与被降解对象的关系并非酶与底物的一一对应关系,而是与一类乃至多类底物的关系,这也是白腐真菌技术适用于降解复杂的混合染料废水的理论基础,即降解酶系基本上是组成酶.Martins等(2002)提出了一种提高白腐真菌染料降解能力的新思路,即将菌置于含有某种结构的染料的预适应培养基中培养获得接种物,结果发现,降解体系中某些结构的染料的生物降解一定程度上依赖于预适应培养基中的染料结构,即染料的降解能力可能被诱导.Yang等(2005)的研究也表明,MnP可以被Reactive Black 5所诱导,而且Reactive Black 5是多形德巴利酵母产生MnP的必要条件.本研究表明,平菇液体菌种在含50、100、200 mg · L-1直接湖蓝5B的培养基中培养,显著提高了Lac和MnP活性,即染料诱导了酶的活性,进而提高了对染料的脱色率;但200 mg · L-1染料预培养的菌种并未提高平菇对染料的脱色率,可能是因为液体菌种中含有染料,增加了发酵体系的实际染料浓度,造成酶活性与脱色率间部分的不相关性.较高浓度的染料,如300 mg · L-1和400 mg · L-1直接湖蓝5B预培养的菌种则未提高Lac和MnP活性,其机理还有待于研究.
5 结论(Conclusions)1)以稻草为主要营养基质的液体培养基中,低浓度的直接湖蓝5B可显著提高平菇菌丝体产量,而高浓度的染料对菌丝体的生长有显著抑制作用.
2)与平菇单菌发酵相比,平菇分别与酿酒酵母和产朊假丝酵母混菌培养,可显著提高发酵体系漆酶的活性;平菇分别与酿酒酵母、产朊假丝酵母和热带假丝酵母混菌培养,可显著提高发酵体系锰过氧化物酶的活性和对直接湖蓝5B的脱色率.用低浓度的直接湖蓝5B预适应培养的平菇菌种亦可显著提高发酵体系漆酶和锰过氧化物酶的活性和对直接湖蓝5B的脱色率.平菇与产朊假丝酵母混菌培养时对染料的脱色率最高,达96.3%.
3)漆酶、锰过氧化物酶活性与脱色率间基本呈正相关关系.
| [1] | Arora D S,Gill P K.2001.Effects of various media and supplements on laccase production by some white rot fungi[J].Bioresource Technology,77(1): 89-91 |
| [2] | 高大文,文湘华,钱易.2005.应用白腐真菌降解染料的研究现状及发展趋势[J].哈尔滨工业大学学报,37(9): 1200-1204 |
| [3] | Jadhav J P,Parshetti G K,Kalme S D,et al.2007.Decolourization of azo dye methyl red by Saccharomyces cerevisiae MTCC 463[J].Chemosphere,68(2): 394-400 |
| [4] | Ke L X,Wu Q,Zhang D Q.2011.Bioconversion of rape straw into a nutritionally enriched substrate by Ganoderma lucidum and yeast[J].African Journal of Biotechnology,10(29): 5648-5653 |
| [5] | Khan R,Bhawana P,Fulekar M H.2013.Microbial decolorization and degradation of synthetic dyes: a review[J].Reviews in Environmental Science and Bio/Technology,12(1): 75-97 |
| [6] | 李慧蓉.1996.白腐真菌的研究进展[J].环境科学进展,4(6): 69-77 |
| [7] | 李慧蓉.2005.白腐真菌生物学和生物技术[M].北京:化学工业出版社.140 |
| [8] | Lucas M S,Amaral C,Sampaio A,et al.2006.Biodegradation of the diazo dye Reactive Black 5 by a wild isolate of Candida oleophila[J].Enzyme and Microbial Technology,39(1): 51-55 |
| [9] | Martins M A M,Queiroz M J,Silvestre A J D,et al.2002.Relationship of chemical structures of textile dyes on the pre-adaptation medium and the potentialities of their biodegradation by Phanerochaete chrysosporium[J].Research in Microbiology,153(6): 361-368 |
| [10] | Murugesan K,Kim Y M,Jeon J R,et al.2009.Effect of metal ions on reactive dye decolorization by laccase from Ganoderma lucidum[J].Journal of Hazardous Materials,168(1): 523-529 |
| [11] | Pandey P,Singh R P,Singh K N,et al.2013.Evaluation of the individuality of white rot macro fungus for the decolorization of synthetic dye[J].Environmental Science and Pollution Research,20(1): 238-249 |
| [12] | Papadopoulou K,Kalagona I M,Philippoussis A,et al.2013.Optimization of fungal decolorization of azo and anthraquinone dyes via Box-Behnken design[J].International Biodeterioration & Biodegradation,77: 31-38 |
| [13] | Pointing S B,Bucher V V C,Vrijmoed L L P,2000.Dye decolorization by sub-tropical basidiomycetous fungi and the effect of metals on decolorizing ability[J].World Journal of Microbiology & Biotechnology,16(2): 199-205 |
| [14] | Poxdnyakova N N,Rodakiewicz-Nowak J,Turkovskaya O V,et al.2006.Oxidative degradation of polyaromatic hydrocarbons catalyzed by blue laccase from Pleurotus ostreatus D1 in the presence of synthetic mediators[J].Enzyme and Microbial Technology,39(6): 1242-1249 |
| [15] | 阮晓东,张惠文,王振宇,等.2009.红酵母 YR-1对偶氮染料酸性红B的脱色研究[J].水处理技术,35(12): 38-43 |
| [16] | Singh D,Chen S L.2008.The white-rot fungus Phanerochaete chrysosporium: conditions for the production of lignin-degrading enzymes[J].Applied Microbiology and Biotechnology,81(3): 399-417 |
| [17] | Spadaro J T,Gold M H,Renganathan V.1992.Degradation of azo dyes by the lignini-degrading fungus Phanerochaete chrysosporium[J].Applied and Environmental Microbiology,58(8): 2397-2401 |
| [18] | Tien M,Kirk T K.1983.Ligin-degrading enzyme from the hymenomycete Phanerochaete chrysosporium[J].Science,221: 661-663 |
| [19] | Vanhullea S,Enauda E,Trovasleta M,et al.2008.Coupling occurs before breakdown during biotransformation of Acid Blue 62 by white rot fungi[J].Chemosphere,70(6): 1097-1107 |
| [20] | Villas-Bôas S G,Esposito E,de Mendona M M.2002.Novel lignocellulolytic ability of Candida utilis during solid-substrate cultivation on apple pomace[J].World Journal of Microbiology and Biotechnology,18(6): 541-545 |
| [21] | 汪建中,柯丽霞.2011.混菌发酵玉米秸秆基质蛋白质含量及木质素酶活性的研究[J].食品与发酵工业,37(5): 157-162 |
| [22] | Yang Q X,Yang M,Pritsch K,et al.2003.Decolorization of synthetic dyes and production of manganese-dependent peroxidase by new fungal isolates[J].Biotechnology Letters,25(9): 709-713 |
| [23] | Yang Q X,Yediler A,Yang M,et al.2005.Decolorization of an azo dye,Reactive Black 5 and MnP production by yeast isolate: Debaryomyces polymorphus[J].Biochemical Engineering Journal,24(3): 249-253 |
| [24] | Yang Q X,Tao L X,Yang M,et al.2008.Effects of glucose on the de-colorization of Reactive Black 5 by yeast isolates[J].Journal of Environmental Sciences,20(1): 105-108 |
| [25] | 杨艳红,王伯初,时兰春,等.2003.复合微生物制剂的综合利用研究进展[J].重庆大学学报 (自然科学版),26(6): 81-85 |
| [26] | Yin L X,Liebscher J.2007.Carbon-carbon coupling reactions catalyzed by heterogeneous palladium catalysts[J].Chemical Reviews,107(1): 133-173 |
| [27] | 张晓昱,尹艳丽,王宏勋.2004.玉米秸秆降解液对白腐菌降解染料的影响[J].武汉大学学报(理学版),50(S2): 122-126 |
| [28] | 朱陶,赵永芳.2002.粗毛栓菌漆酶的分离纯化及部分性质研究[J].武汉大学学报(理学版),48(2): 209-212 |
 2015, Vol. 35
2015, Vol. 35


