2. 桂林理工大学环境科学与工程学院, 桂林 541004;
3. 江西俊鑫环境科技有限责任公司, 上饶 334000
2. School of Environmental Science and Engineering, Guilin University of Technology, Guilin 541004;
3. Jiangxi Junxin Environmental Technology Co. Ltd., Shangrao 334000
壬基酚聚氧乙烯醚(NPEO)由于价格优势和可调的亲水亲油平衡值(HLB)在多种工业行业中得到广泛应用.随着分子中环氧乙烷(EO)加成数的增加,NPEO从亲油(加成数1~3)向亲水性(加成数7以上)变化,可制备成乳化剂、润湿剂、洗涤剂、增溶剂等不同用途的印染助剂(刘玉婷等,2010),成为印染行业中不可或缺的一种添加剂.NPEO由NP和环氧乙烷聚合生成,进入环境后通过多种途径转化成NP、NP(1~3)EO和NP(1~3)EC,这些物质由于具有一定的雌激素效应,会对水体生物产生一定的影响(吴伟等,2003a;2003b;Servos,1999;Dussault et al., 2005).因此,各国环境机构及行业机构纷纷限定了其在各类产品中的使用(章杰,2012).
生活污水和天然水体中NPEO的去除和降解一直是相关研究的主体(Bennie,1999;Maguire,1999;Terzic et al., 2005),而厌氧、好氧环境下NPEO的微生物降解途径则是研究的核心(Hayashi et al., 2005;Jonkers et al., 2001;Luppi et al., 2007).作为水体中NPEO的另一个重要来源——工业废水,NPEO的分布和去除则一直缺乏相应的研究.工业废水中NPEO如何降解?其恶劣水质对NPEO微生物降解的影响如何?现有工业废水处理工艺在NPEO去除过程中效果怎样?本研究试图通过这些问题的回答,就如何控制工业废水NP污染提出建议.
牛仔布生产过程中,除了使用到的印染助剂需要添加NPEO外,特有的漂洗过程也大量使用添加了NPEO的高效复配洗涤剂,其排放的废水中NP和NPEO浓度远大于其他印染废水.因此,研究该类废水中NPEO在常规印染废水处理流程下的转化具有更重要的实际意义.基于此,本文通过静态和动态连续降解实验,揭示壬基酚聚氧乙烯醚(NPEO)在碱性牛仔布印染废水中的去除规律.
2 实验部分(Experiments) 2.1 模拟牛仔布印染废水牛仔布混合废水来自生产过程中的多个环节,其中,浆染、印染和漂洗废水排放量较大,丝光工艺水量最小.由于靛蓝和硫化黑染料使用过程需要加碱,浆染、印染排水pH一般较高,丝光工艺排水碱性更强.因此,尽管漂洗废水量大且接近中性,但废水混合后的pH值通常会大于11.本实验原水模拟牛仔布印染混合废水,平均COD为600~700 mg · L-1,由蔗糖(0.64 g · L-1)和其他营养成分组成,硫化黑和靛蓝两种染料投加量分别为0.13 g · L-1和0.032 g · L-1,通过添加氢氧化钠(约0.034 g · L-1)保持废水pH值在9~11之间;另外,还添加保险粉(Na2S2O4,0.038 g · L-1)、小苏打(NaHCO3,0.08 g · L-1)、硫化钠(Na2S,0.13 g · L-1)等印染加工过程中常用的助剂.实验用NPEO采用工业级TX-10,投加量为6.25~12.5 mg · L-1.
2.2 实验过程实验分3个阶段:①第一阶段批式实验,考查厌氧环境不同pH条件下,NPEO的降解产物和降解效率;②第二阶段批式实验,考查好氧环境不同pH条件下,NPEO的降解产物和降解效率;③第三阶段模拟印染废水处理工艺,考查连续处理中NPEO的降解产物和降解效率.
第一阶段批式实验采用6个30 L容器,分为3组,每组2个.各组pH值通过投加氢氧化钠分别设定为9.0、9.6和10.2.驯化时植入6 L生活污水处理厂剩余污泥和20 L人工印染配水,每隔2~3 h加氢氧化钠以维持初始pH值,每日厌氧搅拌处理8 h,静置后撇除处理水,次日投入原水重复实验,直至系统COD处理效果稳定完成驯化.采样阶段系统按原方案继续运行,每天分别在反应6 h和8 h后采样,连续6~8 d.水样200 mL,投加甲醇和硫酸抑制微生物反应,置于低温冰箱冷藏保存,次日进行目标物测定.
第二阶段所用装置及驯化和采样过程与第一阶段类似.除搅拌器外,装置增加曝气设备以维持混合液中溶解氧浓度为4 mg · L-1,原水pH值设定为4.5、7.5和9.6.采样时间为反应后3、6及8 h.
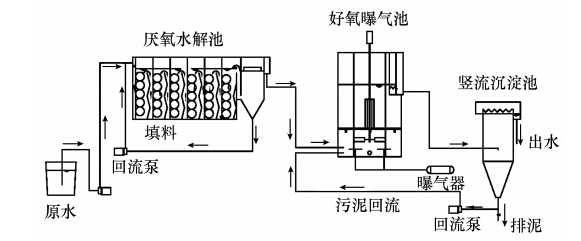 |
| 图 1 连续处理装置流程图 Fig. 1 scheme of continuous treating process for denim wastewater |
第三阶段连续实验在平行的两套模拟设备中进行,设备配置相同(图 1).水解酸化池采用厌氧折板反应器,池底保留污泥层,水流上升段增设填料,驯化后填料上附着污泥.活性污泥曝气池单元出水经竖流沉淀池泥水分离后排出,沉淀污泥经蠕动泵回到曝气池前端,剩余污泥据累积量不定期排出.进水碱性设定pH值11,其他成分同前两阶段配水,各段水力停留时间如下:厌氧水解段9.6 h,好氧曝气段12.7 h,沉淀段3.84 h.采样点设置在原水进水点、水解酸化出水口和末端出水口.经过一个多月驯化,出水常规指标达到印染排水水质要求,此后连续采样检测7 d.
2.3 检测方法参考文献(Ding et al., 1998;Lu et al., 2007)中的提取方法,以Lian等(2009)的方法为基础,用HLB固相萃取柱对废水中的目标污染物进行提取和浓缩.
为全面了解NPEO的主要降解产物,对固相萃取获得的样品中NPEO总量、NP及NP(1~3)EO和NP(1~3)EC三类物质进行检测.NPEO总量检测参考文献(Lu et al., 2007;Goel et al., 2003;陈曦等,2008)的方法,采用ZORBAX Eclipse XDB C-18反相色谱柱进行分析;流动相采用甲醇/水,流速1.0 mL · min-1,柱温23 ℃;进样量10 μL;紫外检测,波长 225 nm.NP及NP(1~3)EO检测方法参考Lian等(2009)的方法,用4-n-NP为内标,BSTFA和TMCS衍生后送GCMS检测.选择性离子模式检测,检测离子如下: 4-n-NP:179;NP:221、179、193;NP1EO:251、265;NP2EO:295、309;NP3EO:281、267.NP(1~3)EC的检测参考文献中(Ding et al., 1998;Lu et al., 2007)的方法,用正丙醇/乙酰氯对NP(1~3)EC进行衍生,GC-MS检测.
2.4 材料与仪器配水所用氢氧化钠、小苏打、保险粉等使用分析纯药剂,NPEO采用市售工业级TX-10(NPEO含量>98%),检测药剂二氯甲烷、正丙醇等采用色谱级,标准产品NP、NP(1~3)EO、NP(1~3)EC,4-n-NPEO购自德国Dr. Ehrenstorfer 公司.CODCr测定采用哈希DR1010快速测定仪;溶解氧测定采用哈希HQ30d溶解氧仪;pH值检测使用WTW手持式PH/溶解氧/电导率测试仪(Multi 3400i),实验开展前及实验过程中不定期校准.
HLB固相小柱(6 mL,500 mg)购于Waters公司,MTN-2800D氮吹仪,玻璃纤维滤膜(0.7 μm,Whatman GF/F,UK)在450 ℃马弗炉中烘4 h.气相色谱质谱仪为安捷伦6890N/5975B GC-MS(Santa Clara,CA,USA).载气氦气,纯度>99.999%;NCI所用反应气体为甲烷气,纯度>99.999%.数据分析采用安捷伦数据分析软件MSD ChemStation D.03.00.611.
3 结果(Results) 3.1 厌氧环境下印染废水中NPEO的降解 3.1.1 厌氧环境不同pH下印染废水中NPEO的降解图 2显示了厌氧批式实验中,不同pH值(9.0、9.6和10.2)不同反应时间下印染废水降解产物的分布情况.图 2结果表明,雌激素效应突出的NP及短链NPEO总量,随着反应pH值的升高平均值从500 μg · L-1经700 μg · L-1升高到900 μg · L-1.具体到各物质,除NP的浓度和比例随pH的升高略有降低外,NP1EO与NP2EO的浓度随pH的增大增加明显,NP3EO浓度有少量增加.
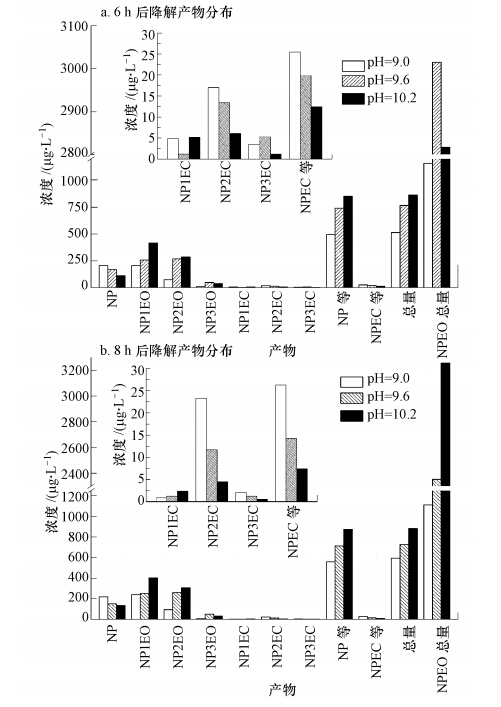 |
| 图 2 批式厌氧反应不同取样时间各pH条件下印染废水中NPEO降解产物分布(NP等:NP及NP(1~3)EO 4种物质浓度和;NPEC等:NP(1~3)EC 3种物质浓度和;总量:NP等+NPEC等;NPEO总量:长链NPEO及部分短链NPEO) Fig. 2 The distribution of anaerobic biodegradation products of NPEO in denim wastewater |
在污染物浓度随反应时间变化方面,比较图 2a和2b发现,NP、NP(1~3)EO 4种物质的浓度随时间变化很小,两个取样时段上的浓度差异在10 μg · L-1以内.图 3结果显示,NPEO总量的去除率差异也同样不明显,3种环境下两个反应时段上的差异很难辨识.图 3还显示,与NPEO去除率不同,COD去除率变化明显,不仅不同pH值间的去除率差距很大,在不同取样时间上,8 h样品的COD去除率普遍高出6 h样品10%.从图 3还可以看出,NPEO总量去除率平均高出COD去除率10%.
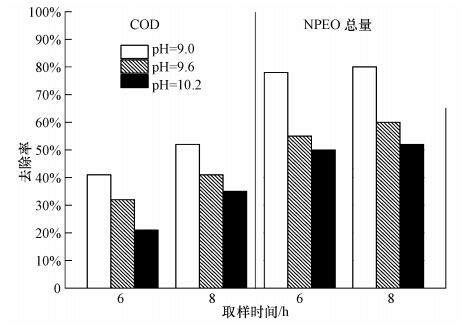 |
| 图 3 静态厌氧反应不同取样时间COD、NPEO去除率 Fig. 3 the removal ratio of COD and NPEO in the anaerobic batch reactor |
图 4显示了相同pH不同反应时间下,NP及各NP(1~3)EO占NP及NP(1~3)EO总量的比例.尽管COD随反应时间改变发生了较大变化,但NP等4种产物各自所占的比例没有发生明显的变化,反应时间的延长没有改变4种物质水相中的分布比例.
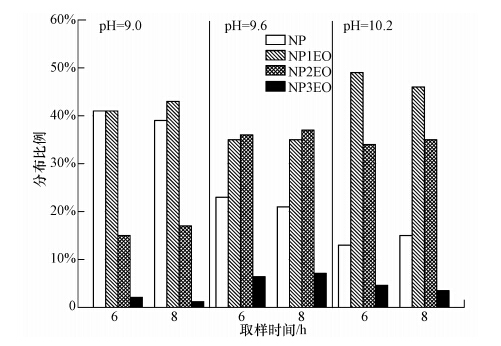 |
| 图 4 静态厌氧反应中NP及d-NPEO分布比例 Fig. 4 the distribution rate of NP and short-chain NPEO in the anaerobic reactor |
图 2显示,批式厌氧反应中,不同pH条件下的NP(1~3)EC浓度都处于较低的水平,pH=9.0(相对更接近中性)时NP(1~3)EC浓度最高,但浓度处于较低的25 μg · L-1左右.这表明厌氧条件下,NPEO的降解产物不是NPEC,但不同条件下的浓度变化也表明,厌氧环境下存在NP(1~3)EC的产生途径.因此,随着反应条件向中性变化,氧化电位升高,出现了NP(1~3)EC浓度增长的现象.
3.1.3 厌氧连续实验中的NP等污染物图 5显示了连续实验两个平行装置中,厌氧单元中NP、NP(1~3)EO和NP(1~3)EC的出水浓度,同期的COD与NPEO总量去除率见图 6.图 5、图 6表明,两装置处理效果的平行性很高,各物质的浓度或去除比例都非常相近.连续实验进水pH值大于11,其厌氧水解段COD与NPEO的平均去除率分别为31%和35%,效果与pH=10.2的批式实验结果相似.与批式实验不同的是,连续厌氧水解出水的NP及NP(1~3)EO浓度更大,两装置4种产物的总量分别达到了4634 μg · L-1和5400 μg · L-1,与pH=10.2时批式实验对应的最大浓度(900 μg · L-1)对比,增加了近6倍.产物分布上,连续实验结果与碱性环境下批式实验的结果相同,出水中NP1EO浓度依然最大,NP2EO其次,NP和NP3EO较低,两者的差异体现在连续实验中,NP和NP(1~3)EO的分布较批式实验更趋均匀.
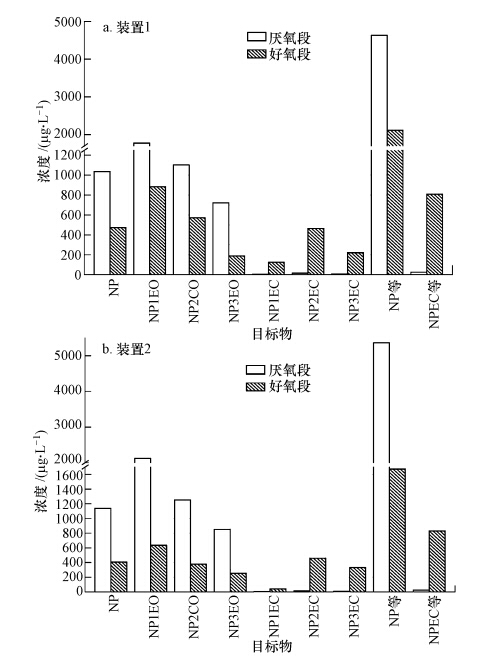 |
| 图 5 动态连续装置厌氧、好氧段出水中目标物浓度分布(*NP等:NP及短链NPEO总量; NPEC等:短链NPEC总量) Fig. 5 the effluent distribution of target chemicals from anaerobic and aerobic unit in the continuous treating processes |
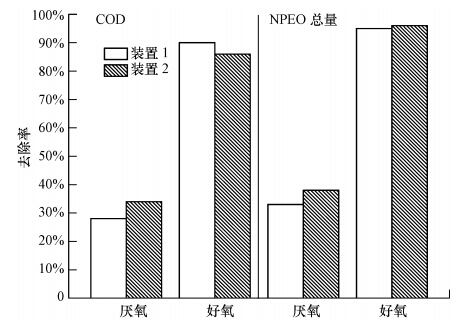 |
| 图 6 连续装置厌氧、好氧段COD、NPEO去除率 Fig. 6 The removal ratio of NP and NPEO from the anaerobic and aerobic unit in the continuous treating processes |
图 7显示了批式好氧反应中,不同pH环境、不同取样时段NPEC、NPEO等的浓度.图 7表明,NP(1~3)EC在酸性条件时浓度最高,累积浓度超过200 μg · L-1,显然,酸性环境中游离质子数量的增加对NPEC浓度形成了影响.图 7还表明,反应后NP及NP(1~3)EO的浓度低于NP(1~3)EC,但两者数量级别相同,特别是在中性与碱性环境下,两类物质的浓度更趋接近.与批式厌氧实验结果对比,好氧反应后NP及NP(1~3)EO浓度远低于厌氧反应后对应物质的浓度,NP(1~3)EC的浓度则有明显增加.
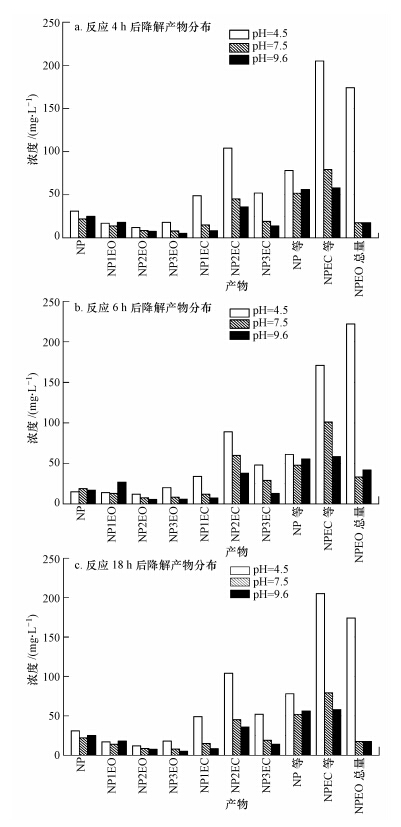 |
| 图 7 静态好氧实验不同取样时间各pH条件下印染废水中NPEO降解产物分布(NP等:NP及NP(1~3)EO总量; NPEC等:NP(1~3)EC总量; NPEO总量: 长链NPEO及部分短链NPEO) Fig. 7 The distribution of aerobic biodegradation products of NPEO in denim wastewater |
图 8显示了批式实验好氧环境下COD的去除效率,结果表明,4、6 h样品中COD去除率小于10%,远低于8 h样品中超过90%的结果.这主要是因为COD检测流程中采用静置沉淀,没有过滤废水,前两个时段样品沉淀时间不足,导致样品中细小污泥没有完全分离,从而影响了检测结果.与COD不同,由于NPEO检测包括过滤步骤,样品中NPEO检测去除了未沉淀污泥的影响,在所有取样时间上都表现了较高的去除率(大于85%,剩余浓度低于350 μg · L-1,图 9).
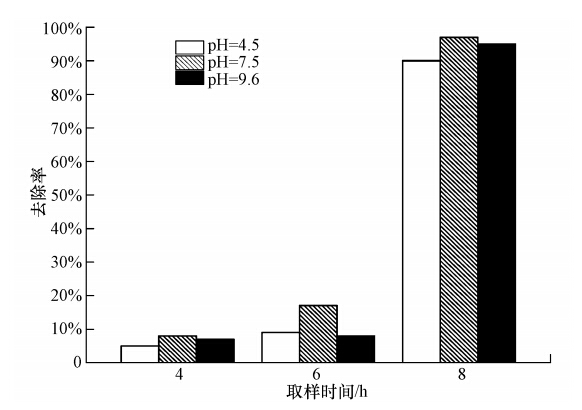 |
| 图 8 静态好氧实验不同取样时间不同pH环境下COD去除率 Fig. 8 the removal ratio of COD in the batch aerobic experiment |
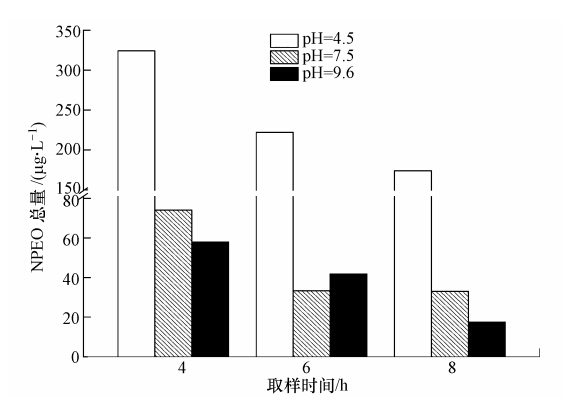 |
| 图 9 静态好氧实验不同取样时间不同pH环境下NPEO总量 Fig. 9 the concentration of NPEOs in the batch aerobic experiment |
对比图 7不同时间点上NPEO及NP(1~3)EC的浓度变化,可以看到,经过6 h反应,NP及NP(1~3)EO的含量逐渐减少,个别样品(主要在酸性和中性条件下)的NP(1~3)EC浓度出现上升.该结果表明,好氧条件下NP(1~3)EO得到有效去除,而NP(1~3)EC则可能因为酸性氧化电位增高从而浓度增加.
3.2.2 连续好氧反应中NPEO的降解好氧连续阶段进水取自连续实验水解酸化段,NP(1~3)EO浓度较批式实验进水高,进水pH值也从厌氧段进水时的11降到厌氧出水时的9.6左右.图 6展示了NPEO在连续好氧条件下的转化率,结果显示,NPEO的总平均去除率始终保持在93%以上,略高于COD的平均去除率.图 5展示了好氧段进出水NP、NP(1~3)EO和NP(1~3)EO等的分布情况.图 5和图 6表明,连续好氧反应与批式好氧实验结果存在众多不同:NP及NP(1~3)EO出水浓度在300~600 μg · L-1间,比进水3000~4000 μg · L-1的高浓度低,但较批式好氧出水20~60 μg · L-1的浓度高;NP(1~3)EC浓度则从进水的10~40 μg · L-1增加到出水的800 μg · L-1以上,对比批式好氧实验,增加明显.
4 讨论(Discussion) 4.1 厌氧环境下印染废水中NPEO的降解厌氧环境下的批式实验结果表明,NPEO的降解和COD降解一样,受废水pH影响明显,中性水质条件下有近80%的去除率,碱性条件下只能达到50%左右.结果还表明,随碱性增加,产物中NP比例减小,而NP1EO和NP2EO等短链NPEO浓度及比例有一定增长.
厌氧环境下,无论是批式还是连续实验,NP(1~3)EC的浓度都很低,这表明NP(1~3)EC的确不是厌氧环境下的产物,但批式实验中,随碱性减小NP(1~3)EC浓度增加的结果说明在该环境中依然存在NP(1~3)EC产生的途径.
NP和NP(1~3)EO在批式和连续实验中的结果差距较大,连续实验出水中NP和NP(1~3)EO浓度总计能达到4000~5000 μg · L-1,而批式实验只能达到500~1000 μg · L-1.不同的污泥培养方式、驯化时间是形成该差异的最大原因,批式实验中每日留固定量污泥为微生物接种,抛弃多余污泥,污泥泥龄较短,而连续式折板厌氧反应器中,底部是污泥床,廊道内是经过较长时间培养,在软性填料上附着生长的污泥,连续系统不进行主动污泥排除,脱落的污泥随水流到下一个处理单元,该运行方式使得连续系统中污泥的泥龄更长,能将更多的NPEO转化成NP及NP(1~3)EO,形成两种厌氧出水的浓度差异.
不同pH条件,批式厌氧实验中,约50%~80%的NPEO得到去除,去除的NPEO或降解成其他非NPEO类物质,或吸附在污泥上,或被微生物同化、矿化.以上3种途径中,矿化方面,虽然有学者(Tanghe et al., 2000)发现,NP2EO可以在某些环境下直接将苯环断链,但厌氧微生物矿化有机物速率较低.对应长链NPEO,Salanitro等(1995)发现,NP9EO在低浓度下可降解生成CO2和甲烷;Chang等(2005)的实验表明,NPEO和NP可以在厌氧条件下通过苯环断裂降解,生成CO2和甲烷;Naylor等(2006)用含14C的NPEO进行降解,发现最终40%苯环的14C转化成了CO2,苯环断链发生在短链NPEO中.上述研究都表明,NPEO的厌氧矿化效率不高,同时还需具备厌氧甲烷菌存在的条件,这在碱性很强的印染废水中一般并不存在.降解方面,NPEO检测到的产物主要通过EO链断裂产生,如Wagener等(1988)提出,微生物攻击EO长链末端,末端的OH基团转移到次末端,最终使整个分子脱除一个半缩醛,使得EO链变短;此外,还有EO链在中间断裂的过程(Gu et al., 2008).但不论哪种方式,NPEO或生成NP及短链NPEO,或转化成NPEC,或向更短链的NPEO逐个转化,这些产物中只有NPEC不是NPEO类物质,但由前面讨论已知,NPEC不是厌氧环境下的主要产物,因此,降解不是厌氧条件下NPEO去除的主要途径.排除以上两种途径可知,去除的NPEO主要被厌氧污泥吸附,批式实验中通过剩余污泥排出系统,而连续实验中则被污泥上的微生物逐渐转化成更多的NP及短链NPEO,形成出水中NP及短链NPEO高浓度的结果.
4.2 好氧反应印染废水中NPEO的降解尽管批式好氧条件下NPEO获得了80%以上的总去除率,实验检测到的NP(1~3)EC和NP(1~3)EO浓度普遍很低,一般在100~200 μg · L-1,两类物质在中性和碱性条件下的浓度更是保持在同一低浓度水平,两类物质的增长量远不足以平衡已去除的NPEO总量.连续实验中,两类物质的增长数量更多,但对应NPEO 80%以上的总去除率,其总量仍不足以平衡已去除部分,因此,水相中去除的NPEO或转化成了其他类物质,或通过其他路径从水相中去除.
批式好氧进水NP及NP(1~3)EO浓度不大,反应后出水中该类物质浓度在20 μg · L-1左右,连续好氧反应器进水NP及NP(1~3)EO浓度大(3000~4000 μg · L-1),出水中NP及NP(1~3)EO浓度高(600~2000 μg · L-1).这两个结果表明好氧反应器出水中NP及NP(1~3)EO浓度与该物质的进水浓度有关:连续好氧反应器中好氧菌降解NP及NP(1~3)EO的能力有限(55%~66%去除率),高浓度的进水NP及NP(1~3)EO将会造成出水NP及NP(1~3)EO浓度较大的结果.另外,连续反应器随着NP(1~3)EO的大幅度降低,出水NP(1~3)EC浓度也有了相当的增长,而批式实验中进水NP(1~3)EO的低浓度对应出水NP(1~3)EC的低浓度.依据已有研究中NPEO氧化生成对应NPEC的理论,两个实验中好氧出水中NP(1~3)EC来源于NP(1~3)EO氧化的可能性较大.因此,在同样的氧化条件下,长链NPEO也存在向对应长链NPEC转化的可能.当长链NPEO转化成对应的长链NPEC后,长链NPEO从水相中消失.NPEO从水相中消失的途径还存在同化及污泥吸附的方式,本研究中因缺少对污泥中NPEO的检测,对此暂无法获得准确判定.
综合静态和动态好氧连续实验的结果,印染废水中的NPEO在好氧曝气过程中能较快地去除,或转化成非NPEO类降解产物(对应NPEC),或发生苯环断链或矿化,或吸附在好氧污泥上.从实验中短链NPEO向短链NPEC的转化看(22%~35%左右的转化率),系统转化NPEO生成NPEC方式的效率不高,需要依靠其他方式,NPEO总量才能获得较高的去除率,吸附或矿化都是水相中NPEO去除的可能途径.最终液相中残留的NP类物质主要是链长不等的NPEC,连续实验好氧出水中的NP及NP(1~3)EO是前段连续厌氧水解过程的残留,如果厌氧出水中短链NPEO含量大,好氧出水中该类物质的含量也大,短链NPEC的含量因NPEO转化有所增长.
5 结论(Conclusions)通过模拟碱性牛仔布印染废水中的静态和动态连续实验发现,连续的厌氧和好氧处理工艺不仅能有效净化含大量硫化染料和靛蓝染料的碱性牛仔布印染废水,也能有效去除废水中的NPEO类污染物,获得90%以上的去除效率.静态实验表明,印染废水pH值对NPEO厌氧处理结果影响明显,pH=10.2条件下,系统所产生的NP及NP(1~3)EO比中性条件下的产生量大.污泥更换慢、污泥龄长的连续厌氧水解池,其出水中NP及NP(1~3)EO含量明显增加.好氧反应中,印染废水中的大部分NPEO能在较短的时间里从水相中去除.好氧批式实验和连续实验都表明,好氧曝气出水中的NP及NP(1~3)EO为进水中未被降解去除的部分,出水中的NP(1~3)EC来自对应NP(1~3)EO转化的可能最大.综合实验结果得到以下认识:厌氧反应器中印染废水中NPEO主要通过吸附方式从水相中去除,如果厌氧污泥泥龄较长,NPEO则可能转化成大量的NP及短链NPEO,进入到好氧反应器中.进入到后续好氧工艺的NPEO通常能以很高的效率从水相中去除,但碱性环境下NP及短链NPEO的去除率不高,部分还可能转化成短链NPEC.去除的NPEO可转化成对应的NPEC,也可能同化或吸附在好氧污泥上,多种途径的共同作用使NPEO总量获得了较高的去除率.从工程实践角度看,控制处理后出水中NP及短链NPEO类物质浓度的重要环节是控制好氧段进水中NP及短链NPEO浓度,因此,减少厌氧水解过程中NP及短链NPEO产生量是工艺运行的关键,适当排除厌氧污泥,控制污泥泥龄,是控制系统最终出水中NP及短链NPEO浓度的可行方法.
| [1] | Bennie D T.1999.Review of the environmental occurrence of alkylphenols and alkylphenol ethoxylates[J].Water Quality Research Journal of Canada,34(1): 79-122 |
| [2] | Chang B V,Chiang F,Yuan S Y.2005.Anaerobic degradation of nonylphenol in sludge[J].Chemosphere,59(10): 1415-1420 |
| [3] | 陈曦,郝瑞霞,姚宁,等.2008.反相高效液相色谱法测定污水中壬基酚聚氧乙烯醚总量[J].环境工程学报,2(4): 455-460 |
| [4] | Ding W H,Tzing S H.1998.Analysis of nonylphenol polyethoxylates and their degradation products in river water and sewage effluent by gas chromatography-ion trap (tandem) mass spectrometry with electron impact and chemical ionization[J].Journal of Chromatography A,824(1): 79-90 |
| [5] | Dussault È B,Sherry J P,Lee H B,et al.2005.In vivo estrogenicity of nonylphenol and its ethoxylates in the Canadian environment[J].Human and Ecological Risk Assessment,11(2): 353-364 |
| [6] | Goel A,Müller M B,Sharma M,et al.2003.Biodegradation of nonylphenol ethoxylate surfactants in biofilm reactors[J].Acta Hydrochimica et Hydrobiologica,31(2): 108-119 |
| [7] | Gu X,Zhang Y,Zhang J,et al.2008.Degradation behaviors of nonylphenol ethoxylates by isolated bacteria using improved isolation method[J].Journal of Environmental Sciences,20(9): 1025-1027 |
| [8] | Hayashi S,Saito S,Kim J H,et al.2005.Aerobic biodegradation behavior of nonylphenol polyethoxylates and their metabolites in the presence of organic matter[J].Environmental Science & Technology,39(15): 5626-5633 |
| [9] | Jonkers N,Knepper T P,De Voogt P.2001.Aerobic biodegradation studies of nonylphenol ethoxylates in river water using liquid chromatography-electrospray tandem mass spectrometry[J].Environmental Science & Technology,35(2): 335-340 |
| [10] | Lian J,Liu J X,Wei Y S.2009.Fate of nonylphenol polyethoxylates and their metabolites in four Beijing wastewater treatment plants[J].Science of the Total Environment,407(14): 4261-4268 |
| [11] | 刘玉婷,郑寿荣.2010.烷基酚聚氧乙烯醚应用在纺织品中对环境的影响[J].中国资源综合利用,28(2): 22-25 |
| [12] | Lu J,Jin Q,He Y L,et al.2007.Biodegradation of nonylphenol polyethoxylates under Fe(III)-reducing conditions[J].Chemosphere,69(7): 1047-1054 |
| [13] | Luppi L I,Hardmeier I,Babay P A,et al.2007.Anaerobic nonylphenol ethoxylate degradation coupled to nitrate reduction in a modified biodegradability batch test[J].Chemosphere,68(11): 2136-2143 |
| [14] | Maguire R J.1999.Review of the persistence of nonylphenol and nonylphenol ethoxylates in aquatic environments[J].Water Quality Research Journal of Canada,34(1): 37-78 |
| [15] | Naylor C G,Staples C A,Klecka G M,et al.2006.Biodegradation of ring-labeled nonylphenol ethoxylate[J].Archives of Environmental Contamination and Toxicology,51(1): 11-20 |
| [16] | Salanitro J P,Diaz L A.1995.Anaerobic biodegradability testing of surfactants[J].Chemosphere,30(5): 813-830 |
| [17] | Servos M R.1999.Review of the aquatic toxicity,estrogenic responses and bioaccumulation of alkylphenols and alkylphenol polyethoxylates[J].Water Quality Research Journal of Canada,34(1): 123-177 |
| [18] | Tanghe T,Dhooge W,Verstraete W.2000.Formation of the metabolic intermediate 2,4,4-trimethyl-2-pentanol during incubation of a shape Sphingomonas sp.strain with the xeno-estrogenic octylphenol[J].Biodegradation,11(1): 11-19 |
| [19] | Terzic S,Matosic M,Ahel M,et al.2005.Elimination of aromatic surfactants from municipal wastewaters: comparison of conventional activated sludge treatment and membrane biological reactor[J].Water Science and Technology,51(6/7): 447-453 |
| [20] | Wagener S,Schink B.1988.Fermentative degradation of nonionic surfactants and polyethylene glycol by enrichment cultures and by pure cultures of homoacetogenic and propionate-forming bacteria[J].Applied and Environmental Microbiology,54(2): 561-565 |
| [21] | 吴伟,瞿建宏,陈家长,等.2003a.壬基酚聚氧乙烯醚及其降解产物对水生生物的毒理效应[J].湛江海洋大学学报,23(6): 39-44 |
| [22] | 吴伟,吴滟,瞿建宏.2003b.壬基酚聚氧乙烯醚降解前后的激素效应和诱变活性[J].中国环境科学,23(5): 470-474 |
| [23] | 章杰.2012.从"壬基酚"事件看我国纺织印染助剂的安全性问题[J].印染助剂,29(3): 1-8 |
 2015, Vol. 35
2015, Vol. 35


