2. 四川省土壤环境保护重点实验室, 成都 611130
2. Key Laboratory of Soil Environment Protection of Sichuan Province, Chengdu 611130
随着城市化、工业化进程的推进,土壤重金属污染日益严重(崔德杰和张玉龙,2004).锌作为动植物生长所必须的微量元素,在适量条件下对植物生长具有一定的促进作用,但当其含量超过50 mg · kg-1时,会使植物中毒,从而通过食物链危害人类健康(王俊等,2009).同时,由于土壤锌污染具有隐蔽性、积累性和不可逆转性,其修复治理存在难度大、成本高、周期长等问题(董彬,2012).因此,锌污染土壤的修复研究已成为重金属污染土壤治理方向的重要课题之一(朱清清等,2011).迄今,锌污染土壤的治理修复途径包括固化稳定化(郝汉舟等,2011)、植物修复(Salt et al., 1995)、电动修复(Acar and Alshawabkeh, 1993)和土壤淋洗(Peng et al., 2009)等.其中,土壤淋洗技术凭借其简单、有效、可操作性强和修复效率高等优势,成为了主要的土壤重金属污染修复技术之一,在国内外均有成功的工程应用(Mann,1999).
土壤淋洗技术的关键在于选择高效、环境友好和成本低廉的淋洗剂.目前,修复锌污染土壤的淋洗剂主要有酸(Makino et al., 2006;Elliott and Shastri, 1999)、盐溶液(Kou et al., 2006)、人工螯合剂(孙小峰等,2006;Zou et al., 2009)和生物表面活性剂(李光德等,2009)等.无机酸、盐等淋洗剂具有使用成本较低,去除效果好与作用速度快等优点.刘磊等(2010)研究表明,2 mol · L-1 HCl可以去除污染土壤中98.00%的锌,但其使用同时也会造成土壤结构破坏、肥力流失等问题;由于乙二胺四乙酸(EDTA)等人工螯合剂在环境中降解性差的特点,其淋洗后的残留物质易造成土壤二次污染,并带来土壤养分的流失(丁竹红等,2009);鼠李糖脂、surfactin(莎梵婷)、皂角苷等生物表面活性剂具有活性高、毒性低、可生物降解等特点(朱清清等,2010).Hong等(2002)研究了皂角苷对污染土壤中锌的去除作用,去除率达到了85%.Mulligan and Wang(2006)用鼠李糖脂振荡淋洗土壤中的锌,最大去除率达到了37.1%.但由于现阶段部分生物表面活性剂生产成本较高且无法对土壤中残渣态重金属产生较好的去除效果,因此在实际应用中受到一定限制(雷国建等,2013).
综上所述,国内外关于锌污染土壤淋洗剂的研究主要集中于高去除率及淋洗后的生态效应上.因此,筛选出高效、环境友好型和成本低廉的淋洗剂尤为重要.本研究前期从10余种生物材料中初步筛选出洋铁酸模(Rumex patientia)、淡竹叶(Herba Loophatheri)、油菜花(Blassika kapestris)、枫杨(Pterocarya stenoptera)4种生物质材料(其生物量分别可达1.93、1.7、1.81、3.4 t · hm-2),采用其水浸提液作为淋洗剂对锌污染土壤进行淋洗修复.通过探索淋洗浓度、pH和淋洗时间对锌淋洗去除的影响,以期为锌污染土壤的实际修复研究工作提供科学合理的依据.
2 材料与方法(Materials and methods) 2.1 供试土壤土壤的采集.供试无污染水稻土采自温江区惠和村农田,采样深度0~20 cm.样品经自然风干后,剔除其中的碎石及杂草,磨碎过2 mm的尼龙筛,混匀,备用.土壤的基本理化性质见表 1.
| 表1 供试土壤基本理化性质 Table 1 Physical-chemical characteristics of the contaminated soil |
污染土壤制备.向过2 mm筛后的土壤中加入一定浓度的ZnSO4 · 7H2O溶液,于室温下振荡48 h后,离心去除游离态锌,剩余土壤保持含水量为田间最大持水量的60%左右,自然状态下平衡钝化反应180 d,期间每隔7 d左右搅拌1次,保证土壤污染均匀.经消煮测得污染土壤中Zn的浓度为975.37 mg · kg-1.
2.2 实验方法 2.2.1 淋洗剂的制备将洋铁酸模、淡竹叶、油菜花、枫杨4种植物清洗干净置于烘箱内在50 ℃下烘干,研磨成粉;各称取洋铁酸模、淡竹叶、油菜花、枫杨4种植物粉末75 g置于白色塑料瓶中,加入1500 mL去离子水,在25 ℃、200 r · min-1下恒温振荡12 h,静置1 h,过滤得浓度均为5%的4种植物浸提液作为淋洗剂,备用.
2.2.2 淋洗液浓度对锌去除率的影响实验称取5.00 g污染土壤样品于一系列白色塑料瓶中,分别加入浓度为1%、2%、3%、4%、5%的4种生物质淋洗液50.00 mL,pH用1%的HNO3或NaOH调节为5.0,在25 ℃、200 r · min-1条件下恒温振荡2 h.随后将淋洗液用0.45 μm微孔滤膜过滤,滤液中的锌含量用火焰原子吸收分光光度法测定,并计算锌的淋洗率.各处理重复3次.
2.2.3 淋洗液pH值对锌去除率的影响实验称取5.00 g污染土壤样品于一系列白色塑料瓶中,分别加入浓度为2%的4种淋洗液50 mL,pH用1%的HNO3或NaOH调节为3、5、7、9、11,在25 ℃、200 r · min-1条件下恒温振荡2 h.随后将淋洗液用0.45 μm微孔滤膜过滤,滤液中的锌含量用火焰原子吸收分光光度法测定,计算锌的淋洗率.各处理重复3次.
2.2.4 淋洗时间对锌去除率的影响实验称取5.00 g污染土壤样品于一系列白色塑料瓶中,分别加入浓度为2%的4种淋洗液50 mL,pH用1%的HNO3或NaOH调节为5.0,在25 ℃、200 r · min-1条件下恒温振荡0.5 h、1 h、2 h、4 h、8 h.随后将淋洗液用0.45 μm微孔滤膜过滤,滤液中的锌含量用火焰原子吸收分光光度法测定,计算锌的淋洗率.各处理重复3次.
2.3 锌含量测定采用火焰原子吸收分光光度法(AAS,WFX-110型,北京北分瑞利分析仪器公司)在波长213.9 nm,通带0.2 nm的条件下测定土壤锌全量、淋洗后滤液中锌含量.
3 结果与讨论(Results and discussion) 3.1 淋洗液浓度对锌去除率的影响在土样中加入不同浓度的4种淋洗液进行振荡淋洗实验,本文针对4种淋洗液设置了1%、2%、3%、4%和5% 5个梯度的浓度,结果如图 1所示.从图 1可知,随着淋洗液浓度的提升,4种淋洗剂对锌的淋洗率均呈上升趋势.当淋洗液浓度值小于4%时,枫杨、洋铁酸模、油菜花3种淋洗液对锌的淋洗率随浓度升高而明显提高,当浓度大于4%时,淋洗率略有下降或趋于稳定.因此,4%为最适浓度,并达到最佳淋洗率,依次为49.32%、48.33%、49.82%.淡竹叶淋洗液对锌的淋洗率随着浓度的提升呈较为缓慢的升高趋势,当浓度为4%时,淋洗率为33.69%,浓度为5%时,淋洗率为35%,提升并不显著(p>0.05).因此,4%为最适浓度.统计分析表明,浓度小于4%时,各浓度的淋洗剂对锌淋洗率的差异均达显著性水平(p<0.05),但4%和5%的4种淋洗液对锌的淋洗率差异不显著(p>0.05),因此,4%即为4种淋洗剂对锌淋洗的最适浓度.
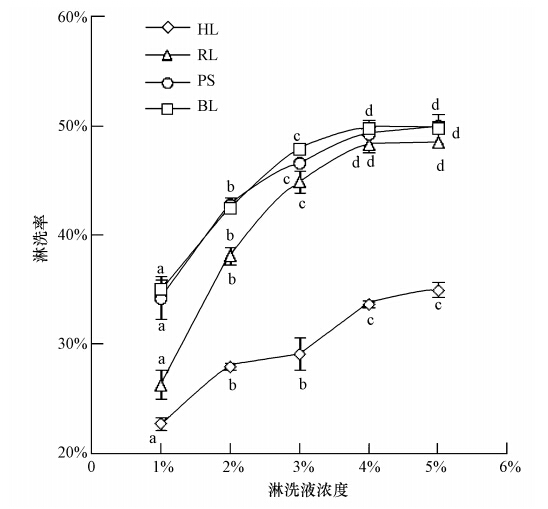 |
| 图 1 淋洗液浓度对锌淋洗率的影响(注:HL(淡竹叶)、RL(洋铁酸模)、PS(枫杨)、BL(油菜花); a、b、c、d、e代表各个数据间差异的显著性,下同) Fig. 1 Effect of leacheate concentration on removal rate of Zn |
本研究所选取的4种生物质材料均为植物,利用4种植物水浸提液作为淋洗剂修复锌污染土壤均取得较好的效果,其原因可能包含两个方面,一是由于淋洗剂的分子结构中含有羟基、羧基等酸性基团,在淋洗过程中解离出H+,从而促进锌从土壤中的解吸(Pacwa-Plociniczak et al., 2011).例如通过淋洗振荡,易龙生等(2013)研究发现,当柠檬酸、酒石酸的浓度为0.6 mol · L-1时,对锌的去除率分别为44.16%及36.4%;另一方面是由于分子中含有羧基、羰基等某些活性基团,其与土壤液相中的锌离子发生络合作用,从而降低土壤对锌的吸附作用.平安等(2011)研究表明,鼠李糖脂、皂素等表面活性剂由于含有较多的螯合基团—COOH、—OH、—C O以及络合官能团等,对土壤中的锌有一定的吸附作用.
3.2 淋洗液pH对锌去除率的影响pH值是影响淋洗液对锌去除效果的一个重要影响因素(曹心德等,2011).本实验研究的pH范围在3.0~11.0,如图 2所示,4种淋洗液对锌的淋洗率均与溶液的pH有关.
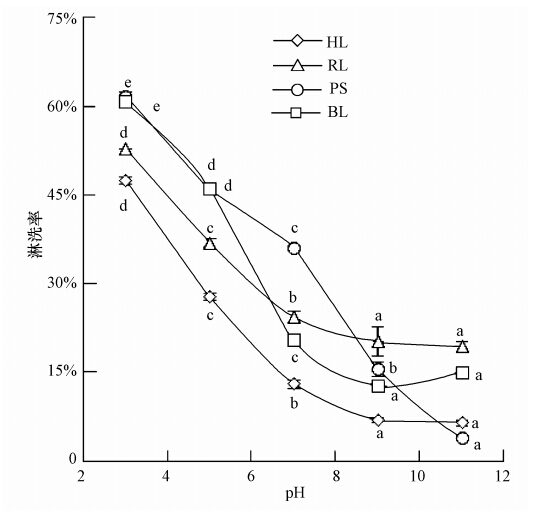 |
| 图 2 淋洗液 pH对锌淋洗率的影响(注:HL(淡竹叶)、RL(洋铁酸模)、PS(枫杨)、BL(油菜花); a、b、c、d、e代表各个数据间差异的显著性) Fig. 2 Effect of leacheate pH on removal rate of Zn |
研究结果表明,随着pH的增大,4种淋洗液对锌的淋洗率均明显降低.当pH小于7.0时,洋铁酸模、淡竹叶、油菜花对锌的淋洗率随着pH的上升而明显降低;当pH大于7.0时,这3种淋洗液对锌的淋洗率变化均逐渐趋于平缓.造成这种现象的原因可能是由于,随着pH的升高,溶液中的H+逐渐减少,锌离子的活性逐渐降低,从而抑制了土壤中锌的解吸,且在pH大于7.0时,不受溶液中OH-含量的影响.郭晓方等(2011)研究表明,不同pH的混合螯合剂对土壤中的锌去除率不同,pH为5和7的淋洗率比pH为9的淋洗率高,说明随着pH提高,有效态重金属含量降低.枫杨对锌的淋洗液随着pH的上升而持续降低,且pH在7.0~11.0范围内所受影响更大,淋洗率下降幅度更为明显.这可能是由于在碱性环境下,淋洗剂中的活性功能团被抑制,土壤液相中的锌直接转化为氢氧化物结合态而沉降下来.Brown和Elliott(1992)的研究结果也表明,在酸性条件下,Pb的去除率略有增加,在中性或碱性条件下,去除率有所降低,主要是由于Pb形成了Pb(OH)3沉淀.在保证较高淋洗率的前提下,考虑过酸性的环境会对土壤结构造成破坏,因此,pH为5左右时最优.
3.3 淋洗时间对锌去除率的影响多数研究表明,淋洗时间越长,淋洗剂与土壤中重金属的反应越彻底,淋洗效果相对较好.但由于不同淋洗剂与土壤重金属的反应平衡时间各有差异(梁金利等,2012),本文针对上述4种淋洗材料分别设置了0.5 h、1 h、2 h、4 h和8 h等5个淋洗时间,探究其在不同淋洗时间内对锌的淋洗效果.
研究结果如图 3 所示,随着淋洗时间的增加,4种淋洗液对锌的淋洗效果均较好,去除能力依次为:油菜花>枫杨>洋铁酸模>淡竹叶.其中,淡竹叶、洋铁酸模、枫杨3种淋洗液对锌的淋洗率随着时间的延长呈缓慢上升趋势.淋洗时间为2 h时,淋洗率依次为32%、42.41%、42.90%;淋洗时间为8 h时,淋洗率分别为34.82%、43.53%、46.25%.由于提升效果并不明显,因此时间为2 h时即可达到较为理想的淋洗效果.油菜花淋洗液对锌的淋洗率随着时间的延长呈现先升高后下降的趋势,并在2 h时达到最大淋洗率49.84%.统计分析表明,2 h的淋洗率与0.5 h、4 h、8 h时的淋洗率均具有显著性差异(p<0.05).因此,2 h即为4种淋洗剂对锌的最佳淋洗时间.
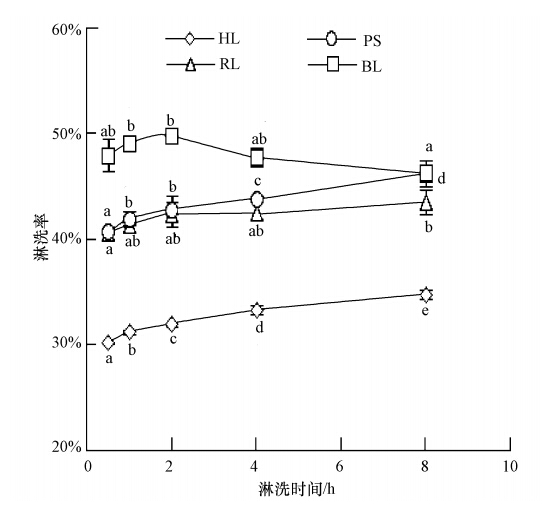 |
| 图 3 淋洗时间对锌淋洗率的影响(注:HL(淡竹叶)、RL(洋铁酸模)、PS(枫杨)、BL(油菜花); a、b、c、d、e代表各个数据间差异的显著性) Fig. 3 Effect of contact time on removal rate of Zn |
吸附在土壤中的重金属在淋洗过程中首先必须被溶解或解析,后逐渐扩散到溶液中,因此反应初期淋洗率缓慢增加,随着反应的进行逐渐趋于平衡(Li et al., 2012).淋洗过程中重金属的去除可以分为短期及长期淋洗两个过程,短期淋洗的是溶液游离态锌,长期淋洗为土壤结合物中难溶态锌(Kirpichtchikova et al., 2006).Bermond和Ghestem(2001)研究表明,随着时间的延长,淋洗过程分为两个部分,初期快速而有效,后期逐渐缓慢或降低.Liu等(2012)使用西瓜皮作为吸附剂去除废水中的锌,研究发现在反应初期较反应后期的去除效率高.造成这种现象的原因可能是相对于离子交换作用及无机沉积物溶解,螯合作用需要更长的时间;也可能是由于淋洗剂的分子量相对较大,进入土壤基质时相对困难(Gheju et al., 2011).
4 结论(Conclusions)1)洋铁酸模、淡竹叶、油菜花、枫杨4种植物的水浸提液作为淋洗剂时,对锌污染土壤有较好的淋洗效果.其中,油菜花与枫杨的效果相近且淋洗率高,洋铁酸模、淡竹叶的效果次之.锌去除率随着淋洗液浓度的增加而上升,且受淋洗液pH值的影响.在pH 5.0、浓度为4%的条件下,4种淋洗剂对锌的淋洗率分别为48.33%、33.69%、49.82%、49.32%,达到最佳淋洗效果.
2)酸度是影响淋洗剂对锌去除效果的一个重要因素.酸度越高,淋洗剂对锌的去除率也越高,但是较高酸度对土壤有一定的破坏力,因此,pH为5.0时,即可达到较好的去除效果.
3)在25 ℃、200 r · min-1的恒温振荡条件下,当浓度与pH固定不变时,振荡时间的长短对锌的去除率无较大影响,不是主要的影响因素.
| [1] | Acar Y B, Alshawabkeh A N. 1993. Principles of electrokinetic remediation [J]. Environmental Science & Technology, 27(13): 2638-2647 |
| [2] | Bermond A, Ghestem J P. 2001. Kinetic study of trace metal EDTA-desorption from contaminated soils// Selim H, Sparks D L. Heavy metals release in soils[M]. Hofida: CRC Press. 131-147 |
| [3] | Brown G A, Elliott H A. 1992. Influence of electrolytes on EDTA extraction of Pb from polluted soil [J]. Water, Air, and Soil Pollution, 62(1/2): 157-165 |
| [4] | 曹心德, 魏晓欣, 代革联, 等. 2011. 土壤重金属复合污染及其化学钝化修复技术研究进展[J]. 环境工程学报, 5(7): 1441-1453 |
| [5] | 崔德杰, 张玉龙. 2004. 土壤重金属污染现状与修复技术研究进展[J]. 土壤通报, 35(3): 366-370 |
| [6] | 丁竹红, 胡忻, 尹大强. 2009. 螯合剂在重金属污染土壤修复中应用研究进展[J]. 生态环境学报, 18(2): 777-782 |
| [7] | 董彬. 2012. 中国土壤重金属污染修复研究展望[J]. 生态科学, 31(6): 683-687 |
| [8] | Elliott H A, Shastri N L. 1999. Extractive decontamination of metal-polluted soils using oxalate [J]. Water, Air, and Soil Pollution, 110(3/4): 335-346 |
| [9] | Gheju M, Pode R, Manea F. 2011. Comparative heavy metal chemical extraction from anaerobically digested biosolids [J]. Hydrometallurgy, 108(1/2): 115-121 |
| [10] | 郭晓方, 卫泽斌, 许田芬, 等. 2011. 不同pH值混合螯合剂对土壤重金属淋洗及植物提取的影响[J]. 农业工程学报, 27(7): 96-100 |
| [11] | 郝汉舟, 陈同斌, 靳孟贵, 等. 2011. 重金属污染土壤稳定/固化修复技术研究进展[J]. 应用生态学报, 22(3): 816-824 |
| [12] | Hong K J, Tokunaga S, Kajiuchi T. 2002. Evaluation of remediation process with plant-derived biosurfactant for recovery of heavy metals from contaminated soils [J]. Chemosphere, 49(4): 379-387 |
| [13] | Kirpichtchikova T A, Manceau A, Spadini L, et al. 2006. Speciation and solubility of heavy metals in contaminated soil using X-ray microfluorescence, EXAFS spectroscopy, chemical extraction, and thermodynamic modeling [J]. Geochimica et Cosmochimica Acta, 70(9): 2163-2190 |
| [14] | Kou S, Lai M S, Lin C W. 2006. Influence of solution acidity and CaCl2 concentration on the removal of heavy metals from metal-contaminated rice soils [J]. Environmental Pollution, 144(3): 918-925 |
| [15] | 雷国建, 陈志良, 刘千钧, 等. 2013. 生物表面活性剂及其在重金属污染土壤淋洗中的应用[J]. 土壤通报, 44(6): 1508-1511 |
| [16] | 李光德, 张中文, 敬佩, 等. 2009. 茶皂素对潮土重金属污染的淋洗修复作用[J]. 农业工程学报, 25(10): 231-235 |
| [17] | Li Y S, Hu X J, Song X Y, et al. 2012. Remediation of cadmium-contaminated soil by extraction with para-sulphonato-thiacalix [4] arene, a novel supramolecular receptor [J]. Environmental Pollution, 167: 93-100 |
| [18] | 梁金利, 蔡焕兴, 段雪梅, 等. 2012. 有机酸土柱淋洗法修复重金属污染土壤[J]. 环境工程学报, 6(9): 3339-3343 |
| [19] | Liu C, Ngo H H, Guo W S. 2012. Watermelon rind: agro-waste or superior biosorbent? [J]. Applied Biochemistry and Biotechnology, 167(6): 1699-1715 |
| [20] | 刘磊, 胡少平, 陈英旭, 等. 2010. 淋洗法修复化工厂遗留地重金属污染土壤的可行性[J]. 应用生态学报, 21(6): 1537-1541 |
| [21] | Makino T, Sugahara K, Sakurai Y, et al. 2006. Remediation of cadmium contamination in paddy soils by washing with chemicals: Selection of washing chemicals [J]. Environmental Pollution, 144(1): 2-10 |
| [22] | Mann J M. 1999. Full-scale and pilot-scale soil washing [J]. Journal of Hazardous Materials, 66(1/2): 119-136 |
| [23] | Mulligan C N, Wang S. 2006. Remediation of a heavy metal-contaminated soil by a rhamnolipid foam [J]. Engineering Geology, 85(1/2): 75-81 |
| [24] | Pacwa-Plociniczak M, Paza G A, Piotrowska-Seget Z, et al. 2011. Environmental applications of biosurfactants: recent advances [J]. International Journal of Molecular Sciences, 12(1): 633-654 |
| [25] | Peng J F, Song Y H, Yuan P, et al. 2009. The remediation of heavy metals contaminated sediment [J]. Journal of Hazardous Materials, 161(2/3): 633-640 |
| [26] | 平安, 魏忠义, 李培军, 等. 2011. 有机酸与表面活性剂联合作用对土壤重金属的浸提效果研究[J]. 生态环境学报, 20(6/7): 1152-1157 |
| [27] | Salt D E, Blaylock M, Kumar N P B A, et al. 1995. Phytoremediation: a novel strategy for the removal of toxic metals from the environment using plants [J]. Nature Biotechnology, 13(5): 468-474 |
| [28] | 孙小峰, 吴龙华, 骆永明. 2006. 有机修复剂在重金属污染土壤修复中的应用[J]. 应用生态学报, 17(6): 1123-1128 |
| [29] | 王俊, 郭颖, 吴蕊, 等. 2009. 不同种植年限和施肥量对日光温室土壤锌累积的影响[J]. 农业环境科学学报, 28(1): 89-94 |
| [30] | 易龙生, 王文燕, 陶冶, 等. 2013. 有机酸对污染土壤重金属的淋洗效果研究[J]. 农业环境科学学报, 32(4): 701-707 |
| [31] | 朱清清, 邵超英, 张琢, 等. 2010. 生物表面活性剂皂角苷增效去除土壤中重金属的研究[J]. 环境科学学报, 30(12): 2491-2498 |
| [32] | 朱清清, 邵超英, 侯书雅, 等. 2011. 烷基糖苷对土壤中重金属的去除研究[J]. 环境科学与技术, 34(8): 120-123; 155 |
| [33] | Zou Z L, Qiu R L, Zhang W H, et al. 2009. The study of operating variables in soil washing with EDTA [J]. Environmental Pollution, 157(1): 229-236 |
 2015, Vol. 35
2015, Vol. 35


