2. 辽宁省环境监测实验中心, 沈阳 110161;
3. 辽宁省生物炭工程技术研究中心, 沈阳 110866
2. Liaoning Environmental Monitoring and Experiment Center, Shenyang 110161;
3. Biochar Engineering Technology Research Center of Liaoning Province, Shenyang 110866
土壤是环境的重要介质,无论以何种方式使用农药,都会直接或间接进入土壤环境,因此,各国土壤中有机氯农药都有不同程度的检出(Wang et al., 2005;Li et al., 2006;Tao et al., 2007).2,4-D(2,4-Dichlorophenoxyacetic Acid)主要作为除草剂、保鲜剂、植物生长调节剂而进入环境,残留于土壤中的2,4-D会发生水解、光解和微生物降解,但由于其本身的迁移性、生物毒性和土壤特性而导致的地表水和地下水污染也有所报道(Leonard,1990; Hall et al., 1993;耿志明等,2007).农药在土壤中的吸附和迁移随着土壤理化性质、气候条件、微生物环境适应性和土壤改良剂性质而改变.
生物炭是生物有机材料在缺氧及低氧环境中经热裂解后的固体产物,大多为粉状颗粒.将生物炭作为土壤添加剂在增加土壤碳汇的同时,还在改善土壤理化性质、提高土壤肥力、降低土壤重金属、农药污染中表现出巨大潜力(田超等,2009;Jones et al., 2011;Lou et al., 2011).生物炭和与其性质相似的活性炭相比,具有成本较低、持续时间长等优点,因此,近年来围绕生物炭对土壤中污染物的吸附行为研究也越来越受到人们的重视.但到目前为止,有关生物炭在土壤中的很多作用机制还不明确,在土壤环境因素对生物炭作用效果的影响及土壤中长期的定位试验等方面还应加强研究.
因此,本文以玉米芯为原料,采用辽宁省生物炭工程技术研究中心研制的炭化炉和亚高温缺氧干馏技术制备生物炭,研究施入不同质量生物炭的土壤对2,4-D的吸附行为,以及土壤环境因素对生物炭吸附效果的影响,探讨生物炭对土壤中有机氯农药的吸附规律和机理,以期为污染土壤的修复和防治提供参考依据.
2 材料与方法(Materials and methods) 2.1 供试材料供试土壤为粘壤质棕壤,2013年6月采自沈阳农业大学北部实验基地0~20 cm未受污染表层土壤(未检出2,4-D),将采集的土壤样本风干、磨细、过2 mm筛,用于培养试验和分析.该土壤理化性质见表 1.
| 表 1 供试土壤理化性质 Table 1 Physical and chemical properties of soil |
供试生物炭由玉米芯为试验原材料,采用辽宁省生物炭工程技术研究中心专利炭化炉(专利号200710086505.4)和亚高温缺氧干馏技术制备.制炭温度约为600 ℃(陈温福等,2011),其理化性质见表 2.
| 表 2 供试玉米芯生物炭理化性质 Table 2 Physical and chemical properties of biochar |
2,4-D购自国药集团,配制成100 mg · L-1的储备液,保存于4 ℃冰箱中待用.二氯甲烷、氯化钠、无水硫酸钠、磷酸等均为分析纯,购自国药集团;甲醇为色谱/光谱纯(Fisher,美国).
2.2 主要仪器设备Autosorb-1型比表面积测定仪(Quantachrome,美国),Superscan 550扫描电镜(Shimadzu,日本),高效液相色谱仪(Agilent 1100,带可变波长检测器),WD-35旋转浓缩仪(瑞士,BuCHI),恒温振荡器(江苏太仓仪器设备厂),台式离心机(无锡瑞江分析仪器有限公司).
2.3 吸附试验 2.3.1 等温吸附试验试验考查了2,4-D在施入生物炭土壤中的等温吸附,采用Langmuir(式(1))、Freundlich(式(2))、Redlich-Peterson(式(3))3种等温吸附模型对实验数据进行拟合.
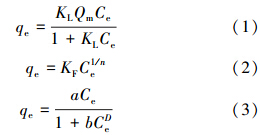
式中,qe为平衡吸附量(μg · g-1),Ce为2,4-D平衡浓度(mg · L-1),Qm为最大吸附量理论值(μg · g-1),KL(L · mg-1)、KF(mg · g-1 ·(L · mg-1)1/n)、a、b、D分别为Langmuir、Freundlich和Redlich-Peterson拟合方程常数.
称取5.0 g土壤(生物炭质量分数分别为0、0.1%、0.3%、0.5%),置于总体积为250 mL 的锥形瓶中,加入50 mL不同浓度(0.1~10 mg · L-1)的2,4-D溶液(介质为0.01 mol · L-1的CaCl2),用聚四氟乙烯密封塞密封,于室温((25±2)℃)下在旋转式振荡器上振荡60 h.然后在5000 r · min-1下离心30 min,测定上清液中的2,4-D浓度,计算吸附量,每处理重复3次.吸附试验在密封避光条件下进行,同时设置不加吸附剂和不加农药的对照.
溶液中2,4-D采用高效液相色谱法进行分析,分析条件:色谱柱为C18 柱(250 mm×4.6 mm,5 μm);流动相为甲醇 ∶ 水(60 ∶ 40,V/V),流速1.0 mL · min-1;进样量20 μL;检测波长 248 nm;外标法进行定量.
2.3.2 吸附动力学研究本文引入Lagergre一级动力学方程(4)和伪二级动力学方程(5)来研究生物炭吸附土壤中2,4-D的反应速率,并探讨其吸附机制.
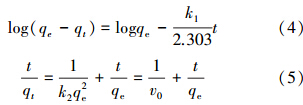
式中,qe为平衡吸附量(μg · g-1),qt为t时的吸附量(μg · g-1),k1、k2(g · μg-1 · h-1)分别为一级和二级动力学吸附速率常数,v0为初始吸附速率(μg · h-1 · g-1).
2.3.3 2,4-D在土壤中吸附形式的研究本文引入土壤吸附系数和吸附自由能来研究2,4-D在施入生物炭的土壤中的吸附程度与机制,吸附系数和吸附自由能的计算公式如下:
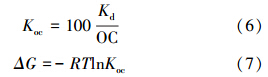
式中,Koc为土壤有机碳吸附系数;OC为土壤或沉积物种有机碳的百分比,由于试验是在实验室条件下的平衡吸附试验,反应时间有限,因而忽略生物炭对土壤有机质含量的长期影响,即OC值取供试自然土壤的有机质含量(1.55%);Kd为吸附方程回归计算得出的吸附常数;ΔG为吸附自由能变化量(kJ · mol-1);R为摩尔气体常数,数值为8.31 J · mol-1 · K-1;T为热力学温度(K).
2.4 温度、pH的影响保持土壤中生物炭质量分数为0.5%,用0.1%NaOH和0.1%H2SO4调整溶液pH值分别为1.6、2.4、3.1、4.4、6.6、7.9,调整水浴温度分别为20、25、30、35、40 ℃,分别研究pH值、温度对2,4-D在土壤中吸附的影响.
3 结果与讨论(Results and discussion) 3.1 生物炭微观形态和比表面积的表征图 1为玉米芯炭化前后的扫描电镜图.由图 1可以看出,玉米芯在炭化部分组织相互密集地连接在一起,且原有生物质结构消失,主要留有多孔炭架结构,轮廓清晰,孔隙结构非常丰富.这种丰富的孔隙结构特征对生物炭在农业上的应用具有重要意义.
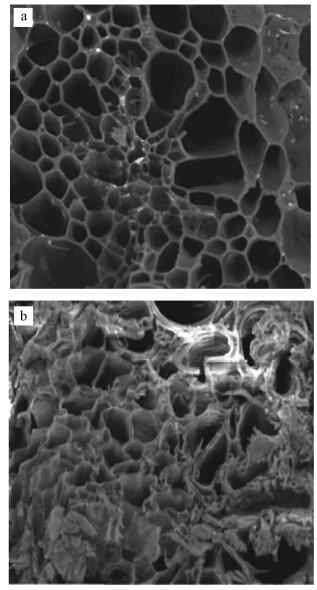 |
| 图 1 玉米芯炭化前后扫描电镜图(a.炭化前,b.炭化后) Fig. 1 SEM image of the maize cob(a)before and (b)after charring |
将制备的生物炭在真空烘箱中下干燥24 h,用Autosorb-1型比表面积测定仪以BET法测定其比表面积并进行孔容与孔径分析,结果如表 3所示.由表 3可知,玉米芯在炭化后的总孔体积、微孔体积和平均孔径都显著变大,比表面积从炭化前的76.7 m2 · g-1增加到410.5 m2 · g-1,提高了近5倍.这可能与供试生物质本身的物质结构组成、疏密结构及生产过程条件控制有关.
| 表 3 生物炭炭化前后孔容、孔径和比表面积 Table 3 Aperture and specific area characterization of biochar before and after charring |
根据吸附试验数据,以吸附平衡时溶液中2,4-D的浓度为横坐标,土壤对2,4-D的吸附量为纵坐标,绘制等温吸附曲线,结果如图 2所示,等温吸附拟合结果见表 4.从图 2中可以看出,在平衡浓度0~10 mg · L-1的范围内,土壤中添加生物炭的量越高,对2,4-D的吸附能力越强.2,4-D在施入生物炭土壤中的吸附可用Freundlich方程和Redlich-Peterson方程较好地拟合.同时,2,4-D在土壤中的吸附与Langmuir方程的拟合程度也随着生物炭投加量的增多而逐渐增强.由于Langmuir方程是基于吸附剂表面均匀的假设,这一结果说明随着土壤中生物炭的增加,生物炭提供了更多均匀的吸附点位.在未添加生物炭的条件下,土壤对2,4-D的吸附作用较差,最大吸附量Qm为20.83 μg · g-1,吸附作用主要由土壤中的有机质所主导.随着生物炭的投入,3种等温吸附方程中表示吸附强度的常数(KL、Qm、Kf、a、b)都变化明显.生物炭质量分数增加到0.5%时,最大饱和吸附量Qm和吸附常数KF分别达到了58.82 μg · g-1和32.76,生物炭对土壤中2,4-D的吸附逐渐起主导作用.此外,Freundlich方程中表示线性的常数n随着生物炭的增加出现下降的趋势,这可能由于生物炭独特而复杂的理化性质使得2,4-D在土壤中的吸附变得错综复杂,吸附过程受到多种作用机制驱动(Yu et al., 2009).
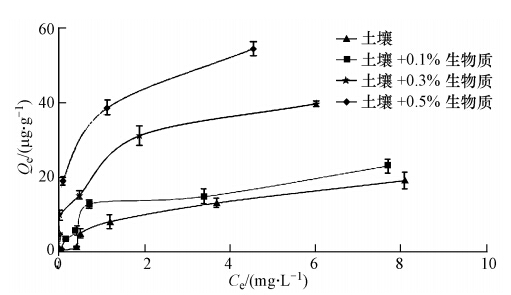 |
| 图 2 2,4-D在不同生物炭施入量土壤中的等温吸附曲线(25℃) Fig. 2 Adsorption isotherms for 2,4-D spiked soil with biochar(25℃) |
| 表 4 2,4-D在施入生物炭土壤中的等温吸附拟合结果 Table 4 Isotherm models fitting to adsorption data of 2,4-D |
有机污染物在土壤中的吸附过程受多种吸附机制的影响,如疏水性吸附、离子交换和配位交换等,而分子态有机物在土壤中吸附作用的强弱主要由土壤有机质含量的高低决定(李克斌等,2003).随着生物炭的施入,2,4-D在土壤中的吸附更多地表现为在生物炭表面上的积累和汇集过程,即土壤对2,4-D的吸附作用由生物炭所主导.3种生物炭处理土壤和对照土壤吸附2,4-D自由能的变化列于表 5.
| 表 5 四种土壤吸附2,4-D自由能的变化 Table 5 Changes of free energy of 2,4-D adsorption in soils |
土壤吸附自由能的变化是土壤吸附性能的重要参考指标,从其数值变化的大小可以推断出土壤对有机物吸附的程度与机制.ΔG小于40 kJ · mol-1时,物理吸附占主导,反之为化学吸附占主导.由表 5可知,生物炭处理土壤的Kd、Koc和吸附自由能变化的绝对值都明显高于对照土壤.其中,3种生物炭处理土壤的Koc分别为自然土壤的1.97、5.51和8.31倍,但吸附自由的变化均小于40 kJ · mol-1,说明施入生物炭的土壤对2,4-D的吸附仍然是以物理吸附为主.值得注意的是,随着生物炭施入量的增加,吸附自由能变化呈现出升高的趋势,说明化学吸附的强度也随着生物炭的增加而增强,这可能与未完全炭化的生物炭表面一些含氧、磷、硫、氮的官能团与2,4-D分子形成一些特定的配合物有关(张鹏等,2012).
一般来说,生物炭对有机污染物的吸附机制主要包括分配作用和表面吸附作用,同时也包括其它一些微观吸附机制.分配作用主要表现为等温吸附曲线呈线性弱的溶质吸收和非竞争吸附.在未添加生物炭的土壤中,2,4-D等温吸附曲线的线性较明显,根据Chiou(2002)提出的线性分配理论,非离子有机物吸附到土壤是有机物分配到有机质中,而与表面积无关.随着生物炭施入量的增加,吸附试验中出现了大量的非线性吸附现象,而表面吸附作用的提出在一定程度上解释了这种现象.表面吸附是产生于分子和原子间微弱的物理吸附作用或化学吸附作用,使某些分子粘着在吸附剂表面的一个过程.如果吸附剂与吸附质之间是通过范德华力而发生的吸附作用,通常称之为物理吸附;吸附剂与吸附质之间是由于化学键(如氢键、配位键和π键等)产生化学作用而引起的吸附,称为化学吸附.本试验中采用的生物炭由玉米芯经高温热解制备而成,除具备较大的比表面积和含碳比外,还包括羧基、酚羟基、酸酐等多种基团,有机物或离子与这些官能团之间可能形成稳定的化学键,从而导致不可逆吸附.如典型的π键作用产生的化学吸附,生物炭的基本特征是具有高度芳香性,富含π电子,可作为电子供体与其它接触的电子受体物质发生π-π电子作用.2,4-D含有芳香π电子,即能与高度芳香化的生物炭形成π-π键,通过π电子供体-受体特殊作用吸附在生物炭表面(李力等,2011;Keiluweit et al., 2009).吸附机制对生物炭的非线性吸附起着重要的作用,在一定程度上弥补了分配机制的局限性.
3.4 2,4-D在施入生物炭土壤中的吸附动力学研究Xing等(1997)提出的有机质扩散理论认为,一些吸附剂由“玻璃态”和“橡胶态”两个区域构成,吸附行为与“玻璃态”和“橡胶态”高分子化合物的吸附行为类似,吸附质在致密的“玻璃态”区域上的吸附速度与不均匀的“橡胶态”区域相比吸附速度慢.土壤对快速吸附质的吸附主要是由于土壤矿质颗粒表面吸附或扩散进入“橡胶态”区域,而对慢速吸附质的吸附则主要是由于附着在吸附剂表面的吸附质缓慢扩散到土壤有机质缝隙中和“玻璃态”区域内部的微孔中.供试生物炭是一种致密结构的多孔性物质,比表面积为410 m2 · g-1,远大于土壤比表面积.土壤中添加生物炭后的微孔数量和表面积显著增大,增加了土壤中“玻璃态”结构区域体积,增强了土壤对2,4-D的吸附作用;同时,表面吸附作用发生后,由于生物炭微孔中有多余的可吸附位点,2,4-D可继续缓慢扩散到其微孔内部,表现为“玻璃态”区域中的慢吸附作用增强.
采用一级动力学模型和准二级动力学模型对试验数据进行拟合,结果见图 3.由图 3可知,对照土壤和添加生物炭的土壤对2,4-D的吸附量均随平衡时间的延长而逐渐增大.吸附初始阶段,添加生物炭的土壤与对照土壤相比,具有较快的吸附速率;至24 h后,各土壤对2,4-D的吸附量随平衡时间的延长趋于平缓,基本达到吸附平衡状态.
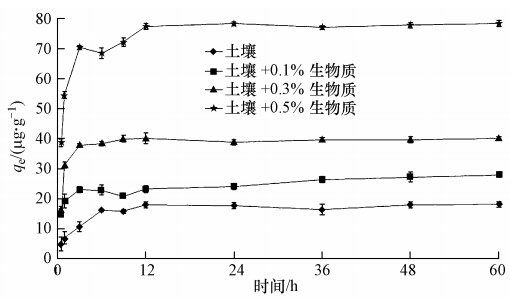 |
| 图 3 2,4-D在添加生物炭土壤中的吸附动力学 Fig. 3 Adsorption kinetic of 2,4-D on the soils amended with biochar |
一级动力学、伪二级动力学速率方程的拟合结果见表 6.由表 6可知,伪二级动力学速率方程对土壤吸附2,4-D的动力学过程拟合效果较好(R2>0.9966),明显优于一级动力学速率模型,吸附速率v0随着生物炭投加量的增加呈现出明显上升趋势.
| 表 6 不同生物炭添加量土壤对2,4-D吸附的一级动力学和伪二级动力学参数 Table 6 Kinetic parameters of the pseudo-first-order and pseudo-second-order model for 2,4-D adsorption on the soils |
一般来说,多孔吸附剂的吸附过程分为3个阶段.第一阶段被称为外扩散阶段,在这一时期溶液中的吸附质从溶液中被吸附到吸附剂表面,吸附初期土壤表面的吸附位点较多,2,4-D容易与之结合,且固液界面的浓度差较大,驱动力也较大,更容易克服吸附质在液相和固相之间的传递阻力,从而使得吸附反应速率较快;第二阶段为粒内扩散阶段,这期间吸附质从吸附剂表面进一步向内部吸附点位扩散,随着吸附时间的延长,吸附剂表面的吸附位点逐渐饱和,固液界面的浓度梯度逐渐降低,吸附速率也随之降低(陈华林等,2004);在最后阶段,吸附质被吸附剂的活性点位所吸附,这一部分吸附发生很快,通常可以忽略不计.由于第一阶段通常发生很快,几乎可在数分钟内就达到平衡,因而酚类化合物在吸附剂上的吸附可能主要是由第二阶段控制.
值得注意的是,吸附试验是模拟短期效应实验,吸附平衡后即停止实验,即未考察生物炭的施入对土壤有机碳含量的影响.然而由于长期的水土作用和土壤中微生物的活动,土壤中施入生物炭会提高土壤有机质含量:一方面,生物炭的施入会使土壤中原有有机碳的矿化量减少,生物炭本身还可以缓慢地分解为有机碳,促进土壤腐殖质的形成;另一方面,生物炭会吸附土壤中的有机分子,通过表面催化作用推动有机分子的团聚,形成土壤有机质.而在大田实验和长期效应实验中,随着时间的推移,生物炭施入土壤后会发生老化并影响土壤有机质含量,具体的吸附机理等仍然有待进一步探讨.
3.5 pH对施入生物炭土壤吸附2,4-D的影响2,4-D作为一种弱酸性有机酸,在溶液中存在如下的电离平衡:
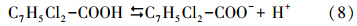
土壤pH的改变会影响2,4-D分子形态的比例,进而影响2,4-D在土壤中吸附作用的强度.实验用0.1%NaOH和0.1%H2SO4调整溶液pH值分别为1.6、2.4、3.1、4.4、6.6、7.9,引入Freundlich方程算出不同条件下的Kd和土壤有机碳吸附系数Koc,并讨论其与pH的关系.
由表 7可以看出,2,4-D在土壤变化pH情况下的等温吸附用Freundlich方程拟合结果仍然较好,R2均大于0.95.pH影响2,4-D在施入生物炭土壤中的吸附,随着pH值的升高,吸附常数Kd和Koc呈现出先升高后降低的趋势,在pH=3.1左右出现最高点.这可能是由于2,4-D在pH值较低时主要以分子形态存在于溶液中,pH越低,分子形态所占的比重越大,参与生物炭吸附过程的量越多;而当pH值持续降低时,生物炭表面会富集大量的H+从而对2,4-D分子产生竞争吸附.当溶液pH值超过6.7,KOC值急剧下降,更多的2,4-D电离为离子态,土壤对2,4-D的吸附量降低,同时生物炭表面聚集的大量负电荷也阻碍了其对2,4-D的吸附.
| 表 7 不同pH下2,4-D等温吸附的拟合结果 Table 7 Freundlich models fitting to adsorption data of 2,4-D under different pH values |
实验通过调整水浴温度分别为20、25、30、35、40 ℃,考察了生物炭质量分数为0.5%的土壤对2,4-D的吸附情况.由图 4可知,从20 ℃到40 ℃,Koc随着反应温度的升高而明显升高,温度超过30 ℃时,Koc急剧上升,说明温度对施入生物炭土壤的有机碳吸附系数影响显著.温度的升高除了通过加速分子热运动而提高生物炭对2,4-D的物理吸附速率外,还为反应过程提供了更多的能量,促进了生物炭表面官能团与有机物之间稳定化学键的形成,从而提高了吸附效果.
 |
| 图 4 2,4-D吸附过程Koc随温度的变化情况 Fig. 4 Effect of reaction temperature on Koc value in 2,4-D adsorption |
1)以施入玉米芯生物炭的土壤为研究对象,发现2,4-D在其中的吸附用Freundlich方程和Redlich-Peterson方程都可以较好地拟合,R2均大于0.95;2,4-D在土壤中的吸附用Langmuir方程拟合的效果也随着生物炭投加量的增多而逐渐增强.与对照土壤相比,最大吸附量理论值从20.83 μg · g-1升高到58.82 μg · g-1.
2)对有机碳吸附系数Koc和2,4-D吸附时自由能变化的研究表明,生物炭对2,4-D的吸附仍然是物理吸附为主,但随着生物炭施入量的增加,吸附自由能变化呈现出升高的趋势,说明化学吸附的强度也随着生物炭的增加而增强.
3)吸附动力学研究表明,伪二级动力学速率方程对土壤吸附 2,4-D的吸附过程拟合效果较好(R2>0.9966),明显优于一级动力学速率模型,吸附速率v0随着生物炭投加量的增加呈现出明显上升的趋势.
4)不同环境因素对土壤中2,4-D吸附的影响结果表明,随着pH值的升高,吸附常数Kd和Koc呈现出先升高后降低的趋势,在pH=3.1左右出现最高点,但过低的pH会使生物炭表面富集大量的H+从而对2,4-D分子产生竞争吸附;温度对2,4-D吸附过程的影响也很显著,具体表现为随着温度的升高,土壤对2,4-D的吸附量和吸附速率v0呈现出明显上升的趋势,吸附量从20 ℃时的74.0 μg · g-1升高到40 ℃时的91.3 μg · g-1,提高了25.5%;初始吸附速率也从20 ℃时的5993.3 μg · h-1 · g-1增加到40 ℃时的8772.4 μg · h-1 · g-1.
| [1] | 陈华林,张建英,陈英旭,等.2004.五氯酚在沉积物中的吸附解吸迟滞行为[J].环境科学学报,24(1):27-32 |
| [2] | 陈温福,张明伟,孟军,等.2011.生物炭应用技术研究[J].中国工程科学,13(2):83-89 |
| [3] | Chiou C T.2002.Partition and Adsorption of Organic Contaminants in Environmental Systems[M].Hoboken,New Jersey,USA: Wiley-Interscience.274 |
| [4] | 耿志明,陈明,王冉,等.2007.高效液相色谱法测定柑橘中2,4-二氯苯氧乙酸残留[J].江苏农业学报,23(1):67-70 |
| [5] | Hall J C,Vandeynze T D,Struger J,et al.1993.Enzyme immunoassay based survey of precipitation and surface water for the presence of atrazine,metolachlor and 2,4-D [J].Journal of Environmental Science and Health,Part B: Pesticides,Food Contaminants,and Agricultural Wastes,28(5): 577-598 |
| [6] | Jones D L,Edwards-Jones G,Murphy D V.2011.Biochar mediated alterations in herbicide breakdown and leaching in soil[J].Soil Biology and Biochemistry,43(4): 804-813 |
| [7] | Keiluweit M,Kleber M.2009.Molecular-level interactions in soils and sediments: The role of aromaticπ-systems[J].Environmental Science & Technology,43(10): 3421-3429 |
| [8] | Leonard R A.1990.Movement of Pesticides into Surface Waters//Cheng H H.Pesticides in the Soil Environment: Processes,Impacts,and Modeling[M]. Madison:Soil Science Society of America. 303-349 |
| [9] | Li J,Zhang G,Qi S H,et al.2006.Concentrations,enantiomeric compositions,and sources of HCH,DDT and chlordane in soils from the Pearl River Delta,South China[J].Science of the Total Environment,372(1): 215-224 |
| [10] | 李克斌,刘维屏,周瑛,等.2003.灭草松在土壤中吸附的支配因素[J].环境科学,24(1): 126-130 |
| [11] | 李力,刘娅,陆宇超,等.2011.生物炭的环境效应及其应用的研究进展[J].环境化学,30(8): 1411-1421 |
| [12] | 刘广良,戴树桂,钱芸.2000.农药涕灭威在土壤中的不可逆吸附行为[J].环境科学学报,20(5): 597-602 |
| [13] | Lou L P,Wu B B,Wang L N,et al.2011.Sorption and ecotoxicity of pentachlorophenol polluted sediment amended with rice-straw derived biochar[J].Bioresource Technology,102(5): 4036-4041 |
| [14] | Tao S,Li B G,He X C,et al.2007.Spatial and temporal variations and possible sources of dichlorodiphenyltrichloroethane (DDT) and its metabolites in rivers in Tianjin,China[J].Chemosphere,68(1): 10-16 |
| [15] | 田超,王米道,司友斌.2009.外源木炭对异丙隆在土壤中吸附-解吸的影响[J].中国农业科学,42(11): 3956-3963 |
| [16] | Wang T Y,Lu Y L,Zhang H,et al.2005.Contamination of persistent organic pollutants (POPs) and relevant management in China[J].Environment International,31(6): 813-821 |
| [17] | Xing B S,Pignatello J J.1997.Dual-mode sorption of low-polarity compounds in glassy poly(Vinyl Chloride) and soil organic matter[J].Environmental Science & Technology,31(3): 792-799 |
| [18] | Yu X Y,Ying G G,Kookana R S.2009.Reduced plant uptake of pesticides with biochar additions to soil[J].Chemosphere,76(5): 665-671 |
| [19] | 张鹏,武健羽,李力,等.2012.猪粪制备的生物炭对西维因的吸附与催化水解作用[J].农业环境科学学报,31(2): 416-421 |
 2015, Vol. 35
2015, Vol. 35


