药物及个人护理品(PPCPs)在污水处理厂中的不完全降解和持续排放,使它在天然水体中的含量不断累积,虽然半衰期不长,但是个人和畜牧业大量地使用,导致PPCPs形成假持续性现象(Ternes et al., 2002,2004; Richardson et al.,2005). 近年来很多PPCPs在天然水体中已经被证实具有相当高的浓度水平(Dębska et al., 2004; Halling-Sørensen et al.,1998; Ternes.,1998; Kolpin et al., 2002),而其中非甾体抗炎药在水体中更是频繁的被检出,作为一类新兴污染物,其在水体中的归趋、生态风险评估也日益得到人们的关注(Kosma et al., 2014; 周海东等,2007).
MEF是一种常见的非甾体抗炎药,化学名N-2,3-二甲苯基邻氨基苯甲酸,俗名扑湿痛,其能抑制环氧化酶,临床上具有解热镇痛和抗炎作用(国家药典委员会等,2010),在欧盟列出的优先污染物中属于第三类化合物(Drzyzga,2003). 很多学者证实,MEF在传统污水处理厂中不能有效的去除(Soulet et al., 2002; Hilton and Thomas,2003). 在地表水中,MEF常被检测出来,是少数环境浓度比预测的无效应浓度大的化合物之一,分别为0.44 μg · L-1和0.428 μg · L-1(Jones et al., 2002; Tauxe et al.,2005). 目前,有关MEF在污水处理厂的残留量、处理效果以及其在天然水体中的生态风险已有文献报道,而关于MEF在水体中环境行为方面的研究则较少.
光降解是水环境中PPCPs降解的重要途径,而水体中大量的共存物会影响非甾体药物的光解(Daughton and Ternes.,1999; Smital et al., 2004; Kim et al., 2007). 特别是氮肥的大量使用,导致天然水体中存在较高浓度的无机氮,这些无机氮随水体pE值的变化而以不同形态存在,其中NO3-、NO2-具有光化学活性,受光照射可以产生羟基自由基和氮氧自由基等活性中间体,进而促进污染物的降解(Zhang et al., 2011; Wang et al., 2012; Chen et al., 2008). 研究水体中无机氮对非甾体药物光解行为的影响,对于更好了解MEF在水环境中的归趋具有重要的意义.
2 材料与方法(Materials and methods) 2.1 试剂甲芬那酸,纯度>98.0%,TCI试剂公司;乙腈,色谱纯,美国ACS恩科化学;硫酸铵、氢氧化钠、硫酸、硝酸钠、亚硝酸钠、异丙醇均为分析纯,成都科试.
2.2 实验方法将0.1 g MEF溶于200 mL乙腈中,配制浓度为0.5 g · L-1的MEF母液. 准确移取1 mL MEF母液于250 mL容量瓶中,用高纯氮吹干乙腈,在剩余MEF的容量瓶中分别加入不同浓度的硝酸钠溶液,用超纯水定溶(Smart2 Pure超纯水/纯水一体化系统,德国TKA),使容量瓶中MEF的浓度为2 mg · L-1,NO3-的浓度分别为0、0.01、0.1、0.2和1 mmol · L-1. 用1% NaOH和H2SO4调溶液pH至中性,摇匀后,移取25 mL溶液至50 mL石英管中,置于XPA-7旋转光化学反应器内(图 1,南京胥江机电厂),控制反应器温度为(25 ± 1)℃,用1 kW汞灯照射(南京胥江机电厂),每隔5 min取样1次,用HPLC测定MEF浓度.每个时间点的样品至少设3个重复,取平均值. 含有NO2-和NH+4的MEF溶液的配制和光解方法同上.
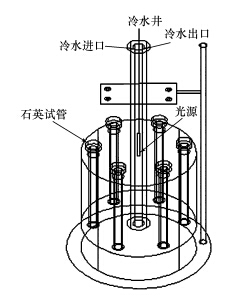 |
| 图 1 旋转光化学反应器 Fig.1 Scheme of rotational photochemical reactor |
高效液相色谱仪(LC-20AT,SHIMADZU),色谱条件:流动相是乙腈-纯水(50 ∶ 50,体积比);色谱柱(VP-ODS,SHIMADZU);检测器为光电二极管阵列检测器(SPD-M20A),检测波长为219 nm,流速为1 mL · min-1,进样量10 μL,柱温30 ℃.紫外分光光度计(UV-2100,北京瑞利).
2.4 pE值及R· OH的计算pE值用于衡量溶液接收或迁移电子的能力(pE=-lge,e为电子活度). NO2-和NH+4以及NO3-和NO2-的反应如式(1)和式(3)所示,并依式(2)和式(4)计算出相应的pE值(Manahan,1984),实验设定水体中的总氮浓度为0.1 mmol · L-1,通过添加不同浓度比例的无机氮来模拟水中pE值的变化,理论促进率是由不同形态氮单独存在时的光解促进率相加得出.
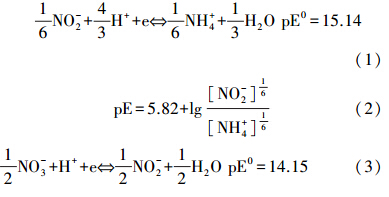
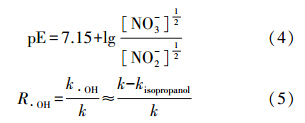
由表 1可见,添加不同浓度NO3-时,MEF的光解较好地符合一级反应动力学. NO3-会促进MEF的光解,NO3-浓度从0.01 mmol · L-1增至1 mmol · L-1,MEF光解速率从0.0104 min-1增至0.1689 min-1(图 2). 这是由于NO3-光解产生O· -2,而O· -2迅速和水反应,生成它本身的共轭酸· OH,· OH是一种强烈的氧化剂(氧化能力分别比H2O2、O3、Cl2高1.58、1.35、2.05倍),参与氧化降解MEF(式(6)~(8))(Zafiriou O C and True, 1979; Blough and Zepp.,1995; Mark et al.,1996; Plumb et al., 1992).
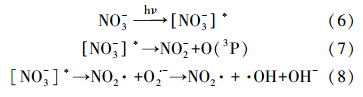
| 表 1 不同形态N对MEF光降解影响的动力学方程及相关常数 Table 1 Photodegradation rate constants of MEF with different forms of nitrogen |
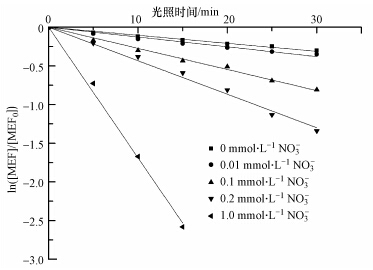 |
| 图 2 不同NO3-浓度对MEF光降解的影响 Fig.2 Effect of NO3- concentration on the MEF photodegradation under ultraviolet light |
为了探究NO3-对MEF的光解影响机制,将进一步检测· OH的生成. 一般认为,在水体中加入某种· OH捕获剂后,目标污染物的光解受到抑制,则证明在光解过程中存在· OH. 异丙醇作为典型的· OH清除剂,其与· OH反应速率常数为1.9×1010 L · mol-1 · s-1(Buxton et al., 1988). 在本实验中,采用异丙醇探究· OH的生成.
如图 3所示,加入50 mmol · L-1异丙醇的MEF溶液与单独MEF溶液的光解速率基本保持一致,分别为0.0115min-1和0.0104min-1,由此推测,MEF单独发生光解时没有产生· OH.
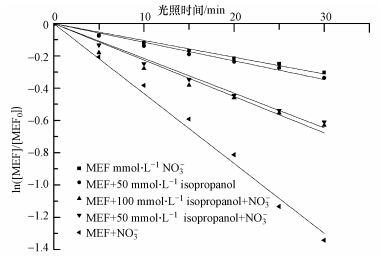 |
| 图 3 羟基自由基的检测(cNO3-=0.2 mmol · L-1,cMEF=2mg · L-1) Fig.3 Determination of the hydroxyl radical(cNO3-=0.2 mmol · L-1,cMEF=2mg · L-1) |
在0.2 mmol · L-1NO3-存在下加入异丙醇,显著抑制MEF的光解,主要原因是异丙醇对· OH的猝灭引起MEF的光解速率变小,实验证实在NO3-存在下,光解产生了· OH并参与促进MEF的降解,通过计算R· OH为54.3%. 值得注意,实验中分别用50 mmol · L-1和100 mmol · L-1异丙醇进行猝灭反应,结果无明显差异,表明添加50 mmol · L-1异丙醇足以猝灭实验中产生的· OH,但从图中发现,在NO3-存在下加入异丙醇,MEF的光解速率依然比单独MEF溶液的光解速率快. 初步推测,一方面NO3-对MEF的光解促进作用不只由· OH引起;另一方面MEF与· OH的二级反应速率常数KM接近异丙醇与· OH的反应速率常数,从而通过竞争反应MEF的光解速率依然比空白时的光解速率快. 实验中产生的其他自由基以及KM有待进一步的确定.
3.2 NO2-对MEF光降解的影响添加不同浓度NO2-,MEF的光解较好的符合准一级反应动力学(表 1),NO2-促进了MEF的降解(图 4),浓度为0.01、0.1、1.0 mmol · L-1时,其光降解速率常数分别为0.0133、0.0417、0.0504 min-1. NO2-光解产生具有强氧化性的自由基可以促进MEF的降解(式(9)). 同时实验发现,低浓度(c<0.1 mmol · L-1)时对MEF的光解促进率比NO3-大,较高浓度时则相反,这可能与NO2-在较高浓度时有部分NO2-与· OH发生猝灭反应相关(式(10))(Oliver et al., 1979). 本实验进一步探究NO2-对MEF光解的影响机制,在0.1 mmol · L-1NO2-存在下添加50 mmol · L-1异丙醇,显著抑制MEF的降解,其光解速率从0.0417 min-1减至0.0182 min-1,得出R· OH为47.9%,实验表明在NO2-存在下,MEF的光解遵循· OH降解机制.
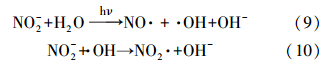
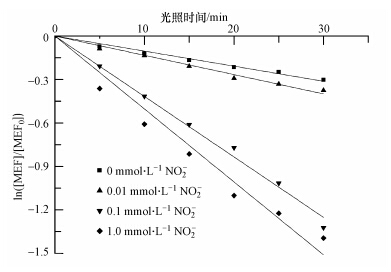 |
| 图 4 不同NO2-浓度对MEF光解的影响 Fig.4 Effect of NO2- concentration on the MEF photodegradation under ultraviolet light |
有文献报道由于NO3-和NO2-会与药物竞争吸收光量子,从而抑制药物在水体中的光解(李超等,2009; 马杜娟,2013). 而本实验中,NO3-和NO2- 均促进了MEF的光解,从图 5中可以看出,虽然NO3-和NO2- 在紫外可见光谱图内和MEF的谱图有重叠,但两者通过竞争吸光引起的抑制行为在MEF的光降解中并没有起主要作用. 而相反,由NO3-和NO2- 产生的ROS引起的间接反应在MEF光降解中起主导作用,这也与许多学者的研究吻合(Aydin,2014; 孟翠等,2011).
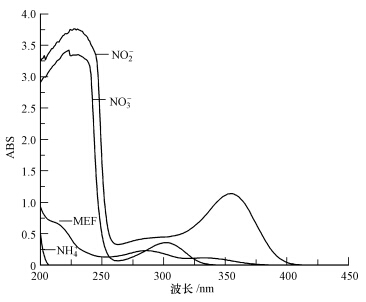 |
| 图 5 MEF、NO3-、NO2-和NH+4紫外可见光谱图 Fig.5 UV-Vis spectra of MEF,NO3-,NO2- and NH+4 |
从图 6中可以看出,NH+4对MEF光解影响不大,NH+4浓度从0.01 mmol · L-1增加到1 mmol · L-1,MEF的光解半衰期无明显变化. 这是由于NH+4在紫外可见光范围内没有光吸收,既不会通过竞争光子来抑制MEF的光解(图 5),也不会产生ROS来促进其光解.
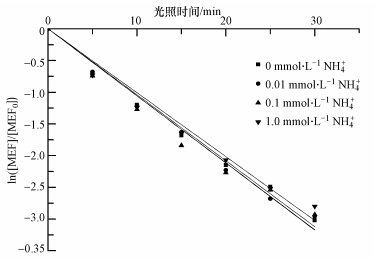 |
| 图 6 不同NH+4浓度对MEF光解的影响 Fig.6 Effect of NH+4 concentration on the MEF photodegradation under ultraviolet light |
实验表明,pE值从4.82增至6.50时,MEF的光解促进率逐渐增大;pE值从6.50增至8.15时,MEF 的光解促进率逐渐下降,其对MEF的促进作用不是简单的叠加关系(表 2).
| 表 2 不同pE值时无机氮对MEF光降解的影响 Table 2 Photolytic effect of MEF under different pE values |
当pE值小于5时,水体中的氮形态主要以NH+4存在,前面研究证实,NH+4对MEF的光解影响不大,在此pE值下促进率无明显变化;当pE值从4.82升到6.50时,水体中NH+4浓度减小,NO2-浓度增大,随着NO2-浓度的增大MEF的光解促进率也随之增大,实际促进率从1.92%增至300.96%,这个阶段的pE值对MEF的光解主要表现为NO2-的影响;当pE值从6.50升至8.15时,水体中NO2-浓度减小,NO3-浓度增大,前面的研究证实,低浓度(c<0.1 mmol · L-1)时NO2-对MEF光解促进作用比NO3-明显,所以这阶段MEF的光解促进率呈下降趋势. 对比实际促进率和理论促进率发现,当NO2-和NO3-共存时,两者对MEF的光解促进率小于两种离子单独存在时的促进率之和,这是因为在NO2-和NO3-共存时,光解产生了· OH并促进MEF的降解,但同时有部分NO2-与自身以及NO3-所产生的· OH发生猝灭反应(式(10)),由此说明两者对MEF的光解存在拮抗作用.
4 结论(Conclusions)1)紫外光照下,MEF的光解符合一级动力学规律.
2)NO3-与NO2-均促进MEF的降解,而且随着NO3-和NO2-浓度的增加,其促进作用逐渐增强. 这主要由于NO3-和NO2-在紫外光照下能产生ROS来促进MEF的光解. 并且低浓度(c<0.1 mmol · L-1)时NO2-对MEF的光解促作用比NO3-大,较高浓度时相反.
3)在NO3-和NO2-存在下添加适量异丙醇,显著抑制MEF的光解,表明NO3-、NO2-光解产生的· OH能促进MEF的降解.
4)NH+4对MEF的光解基本无影响,是由于NH+4在紫外可见光范围内没有光吸收,既不会通过竞争吸光来抑制MEF光解,也不会产生ROS来促进其光解.
5)模拟水体pE值发生变化时,无机氮对MEF光解的影响表明,当NO2-和NH+4共存时,对MEF的光解主要表现为NO2-的影响;当NO2-和NO3-共存时,两者对MEF的光解存在拮抗作用.
| [1] | Aydin E. 2014. Photolysis of naproxen under UV light:Effect of natural organic matter and nitrate to transformation product formation[J]. CLEAN-Soil, Air, Water, doi:10.1002/clen.201300601 |
| [2] | Blough N V, Zepp R G. 1995. Active oxygen in chemistry[M]. Glasgow:Blackie Academic & Professional. 280-333 |
| [3] | Buxton G V, Green stock C L, Helman W P, et al. 1988. Critical review of rate constants for reactions of hydrated electrons, hydrogen atoms and hydroxyl radicals (·OH·/O·-) in aqueous solution[J]. Journal of Physical and Chemical Reference Data, 17(2):513-886 |
| [4] | Chen Y, Hu C, Qu J H, et al. 2008. Photodegradation of tetracycline and formation of reactive oxygen species in aqueous tetracycline solution under simulated sunlight irradiation[J]. Journal of Photochemistry and Photobiology (A:Chemistry), 197(1):81-87 |
| [5] | Daughton C G, Ternes T A. 1999. Pharmaceuticals and personal care products in the environment:agents of subtle change[J]. Environmental Health Perspectives, 107(Suppl 6):907-938 |
| [6] | Dębska J, Kot-Wasik A, Namie s ' nik J. 2004. Fate and analysis of pharmaceutical residues in the aquatic environment[J]. Critical Reviews in Analytical Chemistry, 34(1):51-67 |
| [7] | Drzyzga O. 2003. Diphenylamine and derivatives in the environment:a review[J]. Chemosphere, 53(8):809-818 |
| [8] | 国家药典委员会. 2010. 中华人民共和国药典[M]. 北京:中国医药科技出版社. 139-140 |
| [9] | Halling-Sørensen B, Nielsen S N, Lanzky P F, et al. 1998. Occurrence, fate and effects of pharmaceutical substances in the environment-a review[J]. Chemosphere, 36(2):357-393 |
| [10] | Hilton M J, Thomas K V. 2003. Determination of selected human pharmaceutical compounds in effluent and surface water samples by high-performance liquid chromatography-electrospray tandem mass spectrometry[J]. Journal of Chromatography A, 1015(1/2):129-141 |
| [11] | Jones O A H, Voulvoulis N, Lester J N. 2002. Aquatic environmental assessment of the top 25 English prescription pharmaceuticals[J]. Water Research, 36(20):5013-5022 |
| [12] | Kim Y, Choi K, Jung J Y, et al. 2007. Aquatic toxicity of acetaminophen, carbamazepine, cimetidine, diltiazem and six major sulfonamides, and their potential ecological risks in Korea[J]. Environment International, 33(3):370-375 |
| [13] | Kolpin D W, Furlong E T, Meyer M T, et al. 2002. Pharmaceuticals, hormones, and other organic wastewater contaminants in U. S. streams, 1999-2000:a national reconnaissance[J]. Environmental Science and Technology, 36(6):1202-1211 |
| [14] | Kosma C I, Lambropoulou D A, Albanis T A. 2014. Investigation of PPCPs in wastewater treatment plants in Greece:Occurrence, removal and environmental risk assessment[J]. Science of the Total Environment, 466-467:421-438 |
| [15] | 李超, 谢国红, 刘国光, 等. 2009. 不同形态氮转化对啶虫脒在水溶液中光解的影响[J]. 环境科学学报, 29(9):1918-1922 |
| [16] | 马杜娟. 2013. 水环境中萘普生光化学降解行为研究[D]. 广州:广东工业大学. 51-53 |
| [17] | Manahan S E. 1984. Environmental Chemistry (4th ed)[M]. Boston:Willard Grant Press |
| [18] | Mark G, Korth H G, Schuchmann H P, et al. 1996. The photochemistry of aqueous nitrate ion revisited[J]. Journal of Photochemistry and Photobiology (A:Chemistry), 101(2/3):89-103 |
| [19] | 孟翠, 季跃飞, 曾超, 等. 2011. 防晒剂对氨基苯甲酸在硝酸根溶液中的光解研究[J]. 环境科学, 32(9):2549-2553 |
| [20] | Plumb R C, Edwards J O, Herman M A. 1992. Problem of concurrent measurements of peroxonitrite and nitrite contents[J]. The Analyst, 117(10):1639-1641 |
| [21] | Richardson B J, Lam P K S, Martin M. 2005. Emerging chemicals of concern:Pharmaceuticals and personal care products (PPCPs) in Asia, with particular reference to Southern China[J]. Marine Pollution Bulletin, 50(9):913-920 |
| [22] | Smital T, Luckenbach T, Sauerborn R, et al. 2004. Emerging contaminants-pesticides, PPCPs, microbial degradation products and natural substances as inhibitors of multixenobiotic Defense in aquatic organisms[J]. Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis, 552(1/2):101-117 |
| [23] | Soulet B, Tauxe A, Tarradellas J. 2002. Analysis of acidic drugs in Swiss wastewaters[J]. International Journal of Environmental Analytical Chemistry, 82(10):659-667 |
| [24] | Tauxe-Wuersch A, De Alencastro L F, Grandjean D, et al. 2005. Occurrence of several acidic drugs in sewage treatment plants in Switzerland and risk assessment[J]. Water Research, 39(9):1761-1772 |
| [25] | Ternes T A. 1998. Occurrence of drugs in German sewage treatment plants and rivers[J]. Water Research, 32(11):3245-3260 |
| [26] | Ternes T A, Meisenheimer M, McDowell D, et al. 2002. Removal of pharmaceuticals during drinking water treatment[J]. Environment Science & Technology, 36(17):3855-3863 |
| [27] | Ternes T A, Joss A, Siegrist H. 2004. Peer Reviewed:scrutinizing pharmaceuticals and personal care products in wastewater treatment[J]. Environmental Science and Technology, 38(20):392A-399A |
| [28] | Wang G, Liu G G, Liu H J, et al. 2012. Photodegradation of salicylic acid in aquatic environment:Effect of different forms of nitrogen[J]. Science of the Total Environment, 435-436:573-577 |
| [29] | Zafiriou O C, True M B. 1979. Nitrite photolysis in seawater by sunlight[J]. Marine Chemistry, 8(1):9-32 |
| [30] | Zhang N, Liu G G, Liu H J, et al. 2011. Diclofenac photodegradation under simulated sunlight:Effect of different forms of nitrogen and Kinetics[J]. Journal of Hazardous Materials, 192(1):411-418 |
| [31] | 周海东, 黄霞, 文湘华. 2007. 城市污水中有关新型微污染物PPCPs归趋研究的进展[J]. 环境工程学报, 1(12):1-9 |
 2015, Vol. 35
2015, Vol. 35


