2. 中国科学院大学, 北京 100049;
3. 河北工程大学, 邯郸 056038;
4. 中国矿业大学, 北京 100083
2. University of Chinese Academy of Sciences, Beijing 100049;
3. Hebei University of Engineering, Handan 056038;
4. China University of Mining & Technology, Beijing 100083
磷作为淡水生态系统中初级生产力的限制因素,不仅是水生生物生长发育所必需的重要营养元素,也是导致水体富营养化的主要限制因素之一(陈宜瑜,1995;Correll,1998).滨海湿地位于陆地生态系统和海洋生态系统的过渡地带,对营养元素磷具有较强的过滤和截留作用,是磷输送累积和再生的重要场所(刘景双,2006).湿地土壤作为湿地生态系统中磷的主要储存场所,对磷的生物地球化学循环有重要的作用:一方面湿地土壤自身可以直接吸附和固定外源磷素,另一方面则可以通过为动植物及微生物提供适应的生境吸收利用磷.因此,了解湿地土壤磷形态特征对揭示磷素固定机制、探讨湿地磷循环过程及其对全球变化的响应具有重要意义(Delgado-Baquerizo et al., 2013).
湿地土壤中的磷以多种形态存在.按磷的结合态可分为可交换态磷、铁铝结合态磷、钙结合态磷及闭蓄态磷等;按照其成键类型,可分为磷酸单酯、磷酸二酯、焦磷酸、多聚磷酸、膦酸盐等.相应地,研究土壤磷组成也有多种方法(Worsfold et al., 2005),最常用的是SMT连续提取法,该方法是欧洲标准测试测量组织在改进的Williams法(Williams et al., 1967)的基础上,最终形成的淡水沉积物磷形态连续提取方法(Ruban et al., 2001),具有操作简便、试剂易得、各形态之间干扰少的优点,适合研究磷的形态来源(黄清辉等,2006).SMT法是通过使用酸碱等不同性质的化学提取剂依次提取出土壤中的铁铝结合态磷、钙结合态磷、无机磷及有机磷,从而达到分离的目的.然而SMT法只能得到有机磷总量,不能获取其组成信息,无法深入认识有机磷.液相核磁共振技术(31P-NMR)作为分析环境样品中有机磷的重要手段,具有前处理相对简单、有机磷组分分析完全等优点(钱轶超等,2010;白秀玲等,2011),并且已成功分析出环境样品中的磷酸单酯、磷脂、DNA、膦酸盐、焦磷酸盐、多聚磷酸盐等多种成分及其含量(Cade-Menun,2005;Turner et al., 2005),是目前研究有机磷最为有效的方法.
环渤海地区作为中国三大工业聚集区之一,人口密度大、经济发展快,GDP占全国的25%左右,因此,环境污染也相对严重(Gao et al., 2014);同时,环渤海区域由于40多条河流向其输入大量的淡水和泥沙,形成了广阔的三角洲湿地及滩涂湿地.滨海湿地作为重要的生态屏障,通过土壤吸附和沉淀、植物吸收、微生物固定、泥炭增长等作用,截留净化了大量的氮磷等营养物,成为净化近岸海域水环境的关键区域和重要的生态功能单元(Nichols,1983;Pant et al., 2001).环渤海滨海湿地主要位于渤海西岸的冀鲁平原和北岸的下辽河平原及各河流的两岸,是我国滨海湿地分布最集中的地理区域,湿地规模较大,利用前景可观.因此,本研究以渤海典型滨海湿地为研究对象,利用SMT分级方法结合液相31P-NMR技术,研究湿地土壤中磷的形态特征及其组分之间的含量差异,以期为深入认识磷在滨海湿地系统中的持留特征和转化规律提供支持.
2 材料与方法(Materials and methods) 2.1 样品采集研究区域位于环渤海地区,属于暖温带大陆性半湿润季风气候,该区有海岸线约3000 km,是我国滨海湿地分布最集中的地理区域.其中,沼泽及沼泽化草甸湿地3452 km2,河口及三角洲湿地1172 km2及河滩沼泽2120 km2(赵玉灵等,2007).区域内包括辽宁省、河北省、山东省、北京市、天津市内的多座城市,分布有辽河、滦河、海河、独流减河、潮白河、黄河等河流及较多的湖泊和人工水库,水位季节变化明显,湿地资源丰富.
本次样品主要取自典型滨海湿地,分别是位于辽宁的辽河湿地、天津的七里海湿地、北大港湿地、河北的南大港湿地及山东的黄河三角洲湿地.采样点沿海岸线布设(图 1),即在每个湿地垂向海岸线的中部位置,并根据湿地沿海岸线的长度大小沿海岸线布设了数量不同的采样点.其中,辽河湿地有3个采样点(1、2、3),七里海、北大港湿地各一个采样点(4、5),南大港湿地两个采样点(6、7),以及黄河三角洲湿地采样点8、9.
样品采集于2013年9月进行,土壤样品利用彼得森自重力采泥器采集,采集土壤表层约5 cm的样品,为了取得代表性的样品,样点布设时,根据目标湿地实际情况每个样点同时设置3~5个子样点,每个子样点间间距不小于200 m.样品采集后现场充分混匀,采用隔氧保存法装入可密封的聚乙烯塑料袋中并于冷藏箱低于4 ℃密封保存.运回实验室后,将土壤样品冷冻,并使用LGJ10冷冻干燥机干燥48 h,研磨过100目筛后,四分法取土壤样品密封低温保存待用(金相灿等,1990).
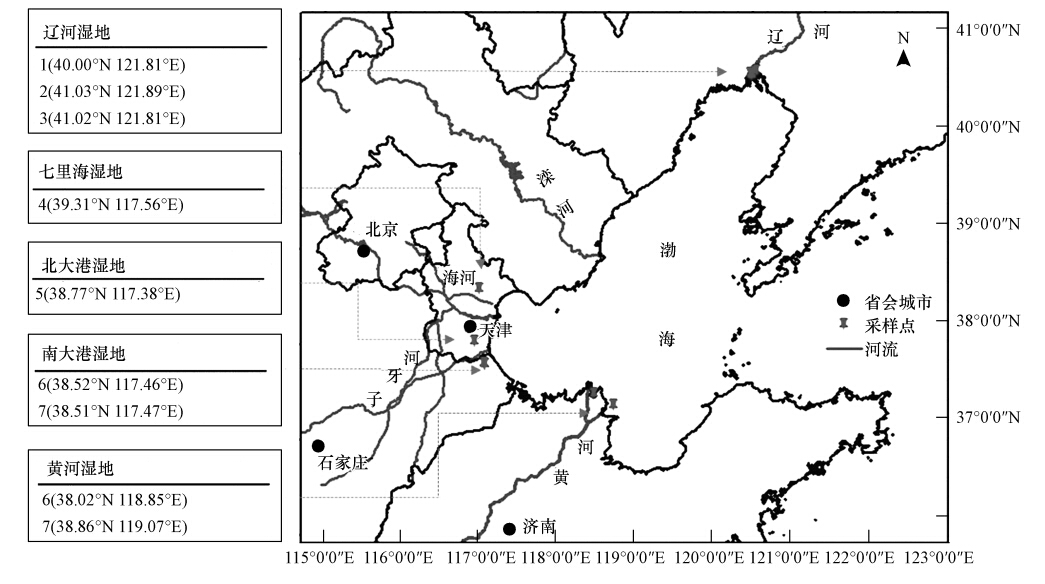 |
| 图 1 环渤海典型湿地土壤取样点位置 Fig. 1 Distribution of the sampling sites in coastal wetl and soils surrounding Bohai Sea |
称取20~30 mg过100目筛土壤样品,利用Vario EL Ⅲ型元素分析仪分析其中的TC与TN.土壤pH采用pH计电测法测定,土壤与水的比例为1∶2.5;有机质采用LOI烧失法测定,取0.5 g样品在马弗炉中550 ℃灼烧5 h以上,获得土壤的烧失量来近似反映土壤的有机质含量(Heiri et al., 2001).
2.3 土壤磷SMT分级采用改进的SMT分级法,OP含量根据差减法得到.通过使用不同性质的提取剂HCl、NaOH提取,将土壤磷分为无机磷(IP)、有机磷(OP)、NaOH提取态磷(NaOH-P,主要为Fe/Al/Mn-P)、HCl提取态磷(HCl-P,主要为Ca-P)及3.5 mol · L-1 HCl提取磷(TP)(图 2).每个提取步骤后,使用离心机离心15 min,分离固液相,各种形态提取液的磷均根据《水与废水监测分析方法(第四版)》采用钼锑抗分光光度法测定上清液磷的含量.
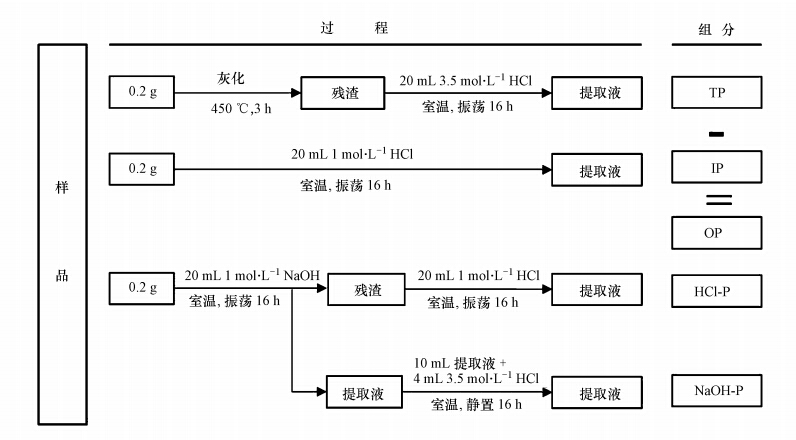 |
| 图 2 SMT分级法 Fig. 2 SMT harmonized protocol |
TP测定:准确称量0.2 g过100目筛土壤样品于坩埚中,在马弗炉中450 ℃灰化3 h,温度降到室温后将样品转移到离心管中,加入20 mL 3.5 mol · L-1 HCl(HCl可直接加到坩埚中以减少转移粉末产生的损失),旋紧盖后水平放置于摇床中,在恒温20 ℃振速250 r · min-1条件下振荡16 h.振荡结束后使用美国BECKMAN Allegra X-22离心机在2000 RCF条件下离心15 min,离心后过滤,弃去残渣,上清液适当稀释,使用钼锑抗分光光度法测量吸光度,得到TP.
IP与OP测定:测定IP时,准确称取0.2 g样品于离心管中,直接加入20 mL 1 mol · L-1 HCl,振荡16 h,振荡结束后在2000 RCF条件下离心15 min,过滤,比色法测定上清液磷含量.将TP与IP含量相减得到OP.
NaOH-P与HCl-P测定:准确称取0.2 g土壤样品于离心管中,加入20 mL 1 mol · L-1 NaOH,振荡16 h,以保证充分的混合.振荡结束后在2000 RCF条件下离心15 min,过滤后保留残渣.取10 mL过滤后的上清液于新离心管中,加入4 mL3.5 mol · L-1 HCl,剧烈摇晃20 s后静置16 h.静置后在200 RCF条件下离心15 min,过滤后测定上清液的P含量得到NaOH-P.残渣则使用12 mL 1 mol · L-1 NaCl清洗,剧烈摇晃5 min后,再在2000 RCF条件下离心15 min,小心弃掉上清液,重复清洗两次.清洗后在离心管残渣中加入20 mL 1 mol · L-1 HCl,2000RCF条件下离心15 min,比色法测定上清液的P,得到HCl-P.
2.4 土壤OP提取与液相31P-NMR分析本研究中选择目前在土壤有机磷方面应用相对广泛的提取剂比例m(土壤)∶ V(提取剂)=1 ∶ 10,提取时间16 h(Turner et al., 2005).准确称取3 g过100目筛土壤样品于冷冻离心管中,加入30 mL 0.25 mol · L-1 NaOH和50 mmol · L-1 EDTA的混合溶液,旋紧盖后水平放置于摇床中,在恒温20 ℃振速250 r · min-1条件下振荡16 h,振荡结束后使用美国BECKMAN Avanti J-26XP冷冻离心机在4 ℃、8000 r · min-1条件下离心40 min,过滤后取上清液.取适量提取液稀释后使用钼锑抗分光光度法分析TP.剩余提取液利用冷冻干燥机冷干至粉末状,冷藏待用.
称取冷冻干燥粉末300 mg用于31P-NMR分析.取300 mg冷冻干燥粉末重新溶于0.1 mL 10 mol · L-1 NaOH和0.6 mL D2O的混合溶液,室温下超声振荡30 min,超声完毕后样品静止平衡5 min;之后在14000 r · min-1条件下高速离心15 min,将离心获得的上清液转移至核磁共振管中上机检测,获得图谱.核磁共振仪选用瑞士BRUKER公司的BRUKERAV400,采用BRUKER标准腔5 mm的BBO探头,31P谱的脉冲P1=12.00 usec,脉冲功率PL1=3.00 dB,31P的共振频率为129.534Hz,循环延迟dl=3.6 s,扫描20000次左右,测定温度为20 ℃(Zhang et al., 2013;张文强等,2013).对图谱进行解析,所有31P化学位移均参照85%的正磷酸盐,根据参照文献中主要磷形态峰值的位移确定其组成,分别为:正磷酸盐(Ortho-P: 6~7 ppm)、磷酸单酯(Mono-P: 4~6 ppm)、磷脂(Lipid-P: 1~3 ppm)、DNA磷(DNA-P: 0 ppm)、焦磷酸盐(Pyro-P: -3.5~-4.5 ppm)及膦酸盐(Phon-P: 18~20 ppm)(Cade-Menun,2005;Turner et al., 2005).最后对沉积物有机磷不同组分图谱进行积分,计算沉积物中不同组分有机磷的含量.
3 结果与讨论(Results and discussion) 3.1 湿地土壤理化性质渤海湾典型滨海湿地土壤总磷、有机质等基本理化指标在不同湿地间变化较大.湿地土壤呈偏碱性,总磷在410.35~691.57 mg · kg-1之间,9个采样点的平均值为569.26 mg · kg-1,且各点差异较大.由于湿地初级生产力较高,土壤有机质,C/N比高于一般沉积物.
湿地土壤的基本理化性质见表 1.土壤pH保持在8左右,平均值为8.25,属于偏碱性.总有机质通过LOI来反映,范围在1.8~10.3 g · kg-1之间,平均含量为5.5 g · kg-1,且pH低的土壤有机质含量较高;TC含量较一般河流土壤高,主要由于湿地较高的初级生产力,含量在1.23%~5.15%之间,平均值为2.47%;TN含量在0.04%~0.41%之间,平均含量为0.17%;TS含量在0.02%~0.98%之间,平均含量为0.2%;其中,5号采样点北大港湿地土壤的有机质含量最高为10.3 g · kg-1,腐殖酸含量较高,因此,pH最低,同时其TC、TN含量也为最大值,说明该点有丰富的有机质,且有很高的初级生产力.9号点东营湿地处于油田分布区,受干扰大,土壤较贫瘠,植被丰度较低,有机质含量低.
| 表1 土壤基本理化性质 Table 1 Physiochemical properties of soils |
碳氮元素比是用来区分土壤有机质来源的常用方法.水生生物的C/N比值为6~9,陆生高等植物的C/N比为14~23,甚至高达30(Meyers,1994).由于湿地高等植物多,渤海湿地表层土壤C/N比值远高于一般河流土壤,其值在11.12~42.76之间,平均值为17.62.其中,采样点9东营湿地较高的C/N比,可能是由于外源污染物的输入造成的.由于离海岸带较近,环渤海湿地所在地区的土壤类型基本都为盐碱土,土壤沉积层次明显,颜色灰棕至黄棕色,植物优势种主要是芦苇,植被种类差异性较小,在不同湿地间丰度差异较大;此外还有少量的三棱草、香蒲、菖蒲、蒿草、金鱼藻等植物.黄河湿地9号点有少量的盐蓬植物,盐碱化较严重,土壤有机质也较低.
湿地土壤总磷平均值为569.26 mg · kg-1,根据第二次全国土壤普查资料,其值高于全国土壤磷平均含量500 mg · kg-1,湿地土壤磷含量相对较高的原因是沉积物的自然累积,大量湿地植物死后腐败分解,释放了大量的氮磷.此外,渤海湿地土壤总磷平均值略低于长江口崇明东滩湿地沉积物总磷(465.78~824.95 mg · kg-1),且远低于三江平原沼泽湿地,其磷含量在2000 mg · kg-1左右(于君宝等,2010).渤海湿地磷含量低于其他湿地的原因一方面与土壤种类有关,其土壤类型主要都为滨海盐土,有机质相对较低;另一方面也与海河流域河流闸坝众多有关,湿地上游河流闸坝众多,河流流动不连续,截留了部分磷,使得入海口湿地土壤磷含量偏低.
环渤海不同湿地间磷含量差别较大一方面与表层土壤本身有关,虽然样点所在区域都是滨海盐土,但其植被丰度有差异,表层土壤有机质也不同,而植物腐败积累是表层土壤磷的主要来源之一,因此,植被腐烂造成的磷积累也不同;其次,由于湿地特殊的结构,表层土壤磷形态与湿地水质情况是密不可分的,水中的氮磷等营养物质会不断在沉积物土壤中富集,土壤中的氮磷也会不断地释放到上覆水中,因此,水质的差别直接影响了土壤的磷含量.由于滨海湿地都位于河流入海口附近,主要流经河流携带了大量的污染物进入湿地,使得N、P等营养物质在湿地表层土壤中累积,各湿地间有机质、氮、磷等差异较大.
3.2 SMT分级分析土壤磷组成SMT分级方法分析所得湿地土壤磷组成结果见图 3,总体而言,湿地土壤中磷以无机磷为主,其中,HCl-P是无机磷的主要组成成分.无机磷占总磷含量的66%以上,土壤磷的主要组成部分为HCl-P,占47%~83%,其次为有机磷,所占比例为8%~34%,NaOH-P所占比例最小,为5%~22%.其中,Ca-P是HCl-P的一个主要存在形态,通常认为在一般环境下,Ca-P较难被分解参与短时期的P循环,释放风险较小;而NaOH-P主要为铁、铝、锰结合态磷,这类磷常被认为是内源P释放的主要来源,在不同pH、氧化还原条件下会导致其释放.
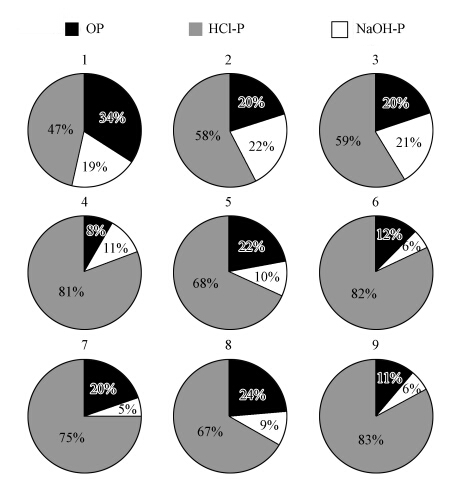 |
| 图 3 各样点SMT分级所得不同结合态磷所占比例 Fig. 3 Proportion of various phosphorus fractions in soils by SMT protocol |
不同湿地土壤磷组成与含量变化差异较大.从图 3中可看出,辽河湿地(样地1、2、3)土壤中的HCl-P比例在所有采样点中最小,而NaOH-P所占比例是最大的,达到20%左右,说明辽河湿地土壤磷相比其他样点有较大的释放风险.有机磷主要来源于外源输入,采样点1存在异常高的有机磷比例(34%),主要是因为湿地附近有蟹类养殖,水产养殖导致营养盐浓度升高(Zhang et al., 2008).同样的,采样点5天津北大港湿地有机磷含量较高也与周围的水产养殖有关,同时独流减河对其输入的污染物也会使得有机磷含量相对较高.采样点4七里海湿地的有机磷比例最低,只有8%,而HCl-P比例较高,可能是由于样点位于水库附近,水质较好,主要是不易释放的Ca-P(HCl-P的主要成分).采样点6、7南大港湿地各形态磷含量组成比例相差较大,7号点有机磷相对较高,主要由于采样点7水量很少,植被茂盛,有机磷含量高.位于黄河入海口附近的采样点8、9东营湿地磷含量组成区别较大,8号点有机磷比例较高,达到24%,HCl-P含量较低,相比之下,9号点有机磷、NaOH-P含量都很低,主要由于采样点位于油田附近,湿地退化较严重(刘志杰等,2012),生物可利用磷较少.
湿地土壤中磷的分布规律与滨海湿地独特的理化特征有关.滨海湿地土壤无机磷以Ca-P为主,这可能与滨海土壤成土类型及海水倒灌等的影响有关(肖笃宁等,2003),海水倒灌等引起的土壤理化性质的变化(盐碱变化、氧化还原电位变化、土壤空隙结构变化等)会对磷,尤其是有机磷造成影响.同时,在受水产养殖污染的湿地,土壤无机磷Fe/Al结合态磷含量明显高于普通湿地;此外,湿地土壤中有机磷所占比例较大,在植物茂盛和受水产养殖污染的样点,土壤有机质丰富,有机磷含量普遍较高.
3.3 液相31P-NMR分析土壤有机磷形态湿地土壤样品的核磁共振图谱见图 4.利用31P-NMR技术在NaOH-EDTA提取液中共检测到6类磷化合物,分别为正磷酸盐(Ortho-P)、磷酸单酯(Mono-P)、磷脂(Lipid-P)、DNA磷(DNA-P)、焦磷酸盐(Pyro-P)及膦酸盐(Phon-P).
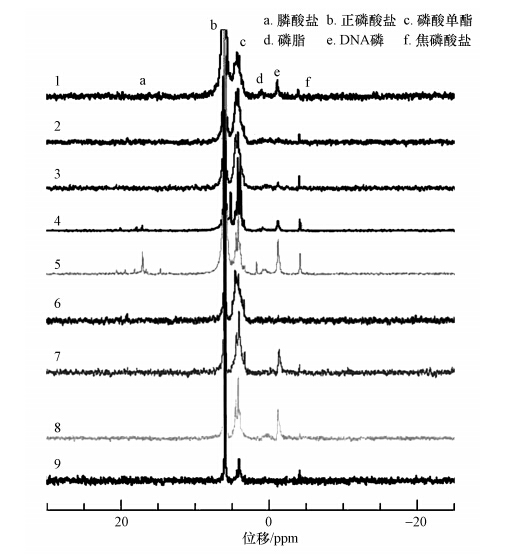 |
| 图 4 表层土壤液相31P-NMR图谱 Fig. 4 31P-NMR spectra of NaOH extracts of the surface soils |
提取液中NaOH-TP的含量范围为 232.74~418.41 mg · kg-1,占到HCl-TP的49.06%~67.38%.正磷酸盐为NaOH-TP 提取液的主要成分,其含量范围为181.69~350.64 mg · kg-1,占到NaOH-TP 的54.79%~94.39%.磷酸单酯是NaOH-TP 提取液中OP的主要成分,其含量范围为17.06~146.56 mg · kg-1,占NaOH-TP的5.25%~37.17%.DNA-P在部分湿地含量较多,其含量范围为0~29.96 mg · kg-1.焦磷酸盐的含量远远小于正磷酸盐,其含量范围为0~8.58 mg · kg-1,占NaOH-TP的0~2.25%.磷脂和膦酸盐含量较少,只在部分湿地检出,其范围分别为0~12.85 mg · kg-1和0~2.44 mg · kg湿地土壤中正磷酸盐和磷酸单酯分别为总磷和有机磷的主要组成成分(图 5).湿地土壤中正磷酸盐所占比例最大,含量在230.00 mg · kg-1左右,其中,4号点七里海湿地正磷酸盐含量最高,达到350.60 mg · kg-1.正磷酸盐被认为是可溶解性总磷中最易被生物利用的磷形态,常用来作为研究湖泊富营养化状态的参数.图谱所得到的无机磷成分还有焦磷酸盐和多聚磷酸盐,具有较高的活性,可以被水生生物直接利用,从而成为藻华爆发的潜在风险源.而在所有土壤样品中,没有发现多聚磷酸盐,而且焦磷酸含量较低,最多只有8.57 mg · kg-1,释放风险较小.
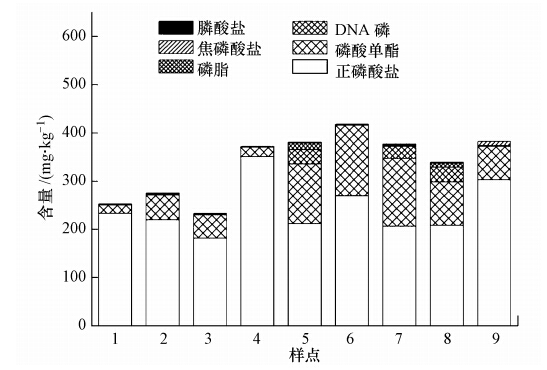 |
| 图 5 31P-NMR分析所得土壤各部分磷含量 Fig. 5 Phosphorus fractionation of soil by 31P-NMR |
有机磷中磷酸单酯含量最多,占总量的5.25%~37.17%,其包括了一大类有机磷化合物,主要有肌醇磷酸、磷酸糖类等,在环境中可以和多价离子结合产生沉淀,稳定性较高(Reitzel et al., 2007).从图 5可看出,北大港、南大港湿地(样点5、6、7)磷酸单酯含量明显高于其他湿地,说明土壤磷组成较稳定,不易释放.磷酸二酯也包含了一大类有机化合物,最典型的为DNA、RNA这样的具有遗传功能的大分子,以及磷脂等细胞壁成分.这类物质易被微生物利用,稳定性低于磷酸单酯,同时还可以指示微生物的丰度(Watts et al., 2002).在湿地土壤中,DNA磷含量普遍高于磷脂,其中,5、7、8号点DNA 磷在20.00 mg · kg-1以上,其余点在1.00 mg · kg-1左右,且4、6号点未检出,说明部分湿地微生物较丰富,较适宜微生物生存;而对于磷脂,3、4、6、9号点都未检出,其余点含量也较少,这与二酯极易分解,采样过程和样品保存过程可能导致二酯含量的减少也有关系.膦酸盐是碳原子直接与磷原子连接的一类化合物,化学性质较为稳定,不易参与磷在水体中的循环,在土壤、富营养化的湖泊及海洋底泥中检出有少量存在(Kittredge et al., 1969).在样点辽河湿地、南大港湿地检出了少量的膦酸盐,其中,6号南大港含量最多,达到2.44 mg · kg-1.
由上述分析可得出,渤海湾南部湿地土壤中(北大港湿地、南大港湿地、黄河口湿地)有机磷含量明显高于北部湿地(辽河湿地、七里海湿地),湿地土壤中有机磷以稳定性较高的磷酸单酯为主;同时,DNA磷较多地存在于南部湿地,北部湿地含量极少,说明南部湿地微生物活性较高.而通常存在于富营养化湖泊中的膦酸盐只在南大港湿地检出较多,说明渤海湾湿地土壤磷结构较稳定,不易造成富营养化.
3.4 不同形态磷含量间的相关性分析通过对湿地土壤不同方法得到的磷形态含量进行数理统计分析,得出相关系数矩阵.结果显示,不同磷形态之间都呈现出显著的相关性.HCl-TP和EDTA-TP显著相关,相关系数达到0.872,且回收率(EDTA-TP/HCl-TP)稳定在50%以上,平均值为59.00%,说明两种分析方法都是科学有效的,都可以反映样品的实际含量和分布规律,不会因为分析手段的不同而掩盖磷在不同土壤中的真实分布规律.
| 表2 不同形态磷含量间的相关性 Table 2 Pearson correlation coefficients between various phosphorus fractions in the soils |
HCl-P与总磷相关性显著,相关系数在0.8以上,而NaOH-P与总磷却呈负相关.其原因可能是目标土壤磷以无机磷为主,而绝大多数无机磷是HCl-P,这种磷主要与样品所在区域的地质、地球化学背景及水体酸碱度有关,一般被看作永久性的P汇(朱广伟等,2004).而NaOH-P所占比例较小,且其主要与无定形或非结晶氧化矿物含量有关,通过吸附等方式滞留磷(Bai et al., 2009).同时,有机磷、磷酸单酯等主要与有机质有关,和无机磷的相关性不显著.
4 结论(Conclusions)1)环渤海典型湿地土壤呈偏碱性.由于湿地较高的初级生产力,湿地土壤中总磷和有机质比一般土壤高,其中,总磷含量在410.35~691.57 mg · kg-1之间,不同湿地间含量差异较大.
2)湿地土壤中的磷主要是无机磷,且主要是不易释放的HCl-P,较易释放的NaOH-P比例只有5%~22%,因此,释放风险较小.有机磷的主要组分是磷酸单酯,且南部湿地土壤中有机磷含量明显高于北部湿地,在南部湿地发现含量较高的DNA磷,说明其微生物活性较高.除此之外,在受到水产养殖污染的湿地,其有机磷含量会相对偏高,造成磷累积.
3)HCl-TP和EDTA-TP相关性显著,且回收率稳定在50%以上,表明SMT分级方法和改进的液相31P-NMR分析方法都是科学有效的,可以反映样品的实际含量.
| [1] | Bai X L, Ding S M, Fan C X, et al. 2009. Organic phosphorus species in surface sediments of a large, shallow, eutrophic lake, Lake Taihu, China[J]. Environmental Pollution, 157(8/9): 2507-2513 |
| [2] | 白秀玲, 周云凯, 李斌, 等. 2011. 基于液相31P核磁共振分析的沉积物样品制备方法研究[J]. 环境科学, 32(7): 1980-1985 |
| [3] | Cade-Menun B J. 2005. Characterizing phosphorus in environmental and agricultural samples by 31P nuclear magnetic resonance spectroscopy[J]. Talanta, 66(2): 359-371 |
| [4] | 陈宜瑜. 1995. 中国湿地研究[M]. 长春: 吉林科学技术出版社 |
| [5] | Correll D L. 1998. The role of phosphorus in the eutrophication of receiving waters: A review[J]. Journal of Environmental Quality, 27(2): 261-266 |
| [6] | Delgado-Baquerizo M, Maestre F T, Gallardol A, et al. 2013. Decoupling of soil nutrient cycles as a function of aridity in global drylands[J]. Nature, 502(7473): 672-676 |
| [7] | Dyhrman S T, Chappell P D, Haley S T, et al. 2006. Phosphonate utilization by the globally important marine diazotroph Trichodesmium[J]. Nature, 439(7072): 68-71 |
| [8] | Gao X L, Zhou F X, Chen C T. 2014. Pollution status of the Bohai Sea: an overview of the environmental quality assessment related trace metals[J]. Environment International, 62: 12-30 |
| [9] | Heiri O, Lotter A F, Lemcke G. 2001. Loss on ignition as a method for estimating organic and carbonate content in sediments: reproducibility and comparability of results[J]. Journal of Paleolimnology, 25(1): 101-110 |
| [10] | 黄清辉, 王磊, 王子健. 2006. 中国湖泊水域中磷形态转化及其潜在生态效应研究动态[J]. 湖泊科学, 18(3): 199-206 |
| [11] | 金相灿, 屠清瑛. 1990. 湖泊富营养化调查规范[M]. 北京: 中国环境科学出版社 |
| [12] | Kittredge J S, Roberts E. 1969. A carbon-phosphorus bond in nature[J]. Science, 164(3875): 37-42 |
| [13] | 刘景双. 2006. 湿地生物地球化学研究[J]. 湿地科学, 3(4): 302-309 |
| [14] | 刘志杰, 李培英, 张晓龙, 等. 2012. 黄河三角洲滨海湿地表层沉积物重金属区域分布及生态风险评价[J]. 环境科学, 33(4): 1182-1188 |
| [15] | Meyers P A. 1994. Preservation of elemental and isotopic source identification of sedimentary organic matter[J]. Chemical Geology, 114(3/4): 289-302 |
| [16] | Nichols D S. 1983. Capacity of natural wetlands to remove nutrients from wastewater[J]. Water Pollution Control Federation, 55(5): 495-505 |
| [17] | Pant H K, Reddy K R, Lemon E. 2001. Phosphorus retention capacity of root bed media of sub-surface flow constructed wetlands[J]. Ecological Engineering, 17(4): 345-355 |
| [18] | 钱轶超, 陈英旭, 楼莉萍, 等. 2010. 核磁共振技术在沉积物磷素组分及迁移转化规律研究中的应用[J]. 应用生态学报, 21(7): 1892-1898 |
| [19] | Reitzel K, Ahlgren J, DeBrabandere H, et al. 2007. Degradation rates of organic phosphorus in lake sediment[J]. Biogeochemistry, 82(1): 15-28 |
| [20] | Ruban V, López-Sánchez J, Pardo P, et al. 2001. Development of a harmonised phosphorus extraction procedure and certification of a sediment reference material[J]. Journal of Environmental Monitoring, 3(1): 121-125 |
| [21] | Turner B L, Cade-Menun B J, Condron L M, et al. 2005. Extraction of soil organic phosphorus[J]. Talanta, 66(2): 294-306 |
| [22] | Watts E E, Dean P A W, Martin R R. 2002. 31P nuclear magnetic resonance study of sediment microbial phospholipids[J]. Canadian Journal of Analytical Sciences and Spectroscopy, 47(5): 127-133 |
| [23] | Williams J D H, Syers J K, Walker T W. 1967. Fractionation of soil inorganic phosphate by a modification of Chang and Jackson's procedure[J]. Soil Science Society of America Journal, 31(6): 736-739 |
| [24] | Worsfold P J, Gimbert L J, Mankasingh U, et al. 2005. Sampling, sample treatment and quality assurance issues for the determination of phosphorus species in natural waters and soils[J]. Talanta, 66(2): 273-293 |
| [25] | Worsfold P J, Monbet P, Tappin A D, et al. 2008. Characterisation and quantification of organic phosphorus and organic nitrogen components in aquatic systems: a review[J]. Analytica Chimica Acta, 624(1): 37-58 |
| [26] | 肖笃宁, 韩慕康, 李晓文, 等. 2003. 环渤海海平面上升与三角洲湿地保护[J]. 第四纪研究, 23(3): 237-246 |
| [27] | 于君宝, 陈小兵, 孙志高, 等. 2010. 黄河三角洲新生滨海湿地土壤营养元素空间分布特征[J]. 环境科学学报, 30(4): 855-861 |
| [28] | Zhang R Y, Wu F C, Liu C Q, et al. 2008. Characteristics of organic phosphorus fractions in different trophic sediments of lakes from the middle and lower reaches of Yangtze River region and Southwestern Plateau, China[J]. Environmental Pollution, 152(2): 366-372 |
| [29] | Zhang W Q, Shan B Q, Zhang H, et al. 2013. Assessment of preparation methods for organic phosphorus analysis in phosphorus-polluted Fe/Al-rich Haihe river sediments using solution 31P-NMR[J]. PLoS One, 8(10): e76525 |
| [30] | 张文强, 单保庆. 2013. 基于液相31P核磁共振(NMR)技术的巢湖沉积物中有机磷形态研究[J]. 环境科学学报, 33(7): 1967-1973 |
| [31] | 赵玉灵, 聂洪峰, 杨金中, 等. 2007. 环渤海湾-莱州湾地区湿地现状遥感调查[J]. 国土资源遥感, 19(1): 86-88 |
| [32] | 朱广伟, 秦伯强, 高光, 等. 2004. 长江中下游浅水湖泊沉积物中磷的形态及其与水相磷的关系[J]. 环境科学学报, 24(3): 381-388 |
 2015, Vol. 35
2015, Vol. 35


