珠江广州段位于珠江下游,受工农业废水和生活污水污染严重.近年来,随着珠三角地区工业化发展,珠江广州段受到严重的氮、磷污染,水质日趋恶化,河段呈富营养化趋势,导致蓝藻频繁暴发(Lu et al., 2009).国内外学者对水体富营养化的研究已做了大量工作,然而对富营养化发生的机制仍然不清楚,目前形成了几种假说:①氮磷元素限制假说(Conley et al., 2009);②钼元素限制假说(Goldman,1960);③铁元素限制假说(邢伟,2007);④温度、pH、光照等物理因子影响假说等(Jöhnk et al., 2008;Brookes et al., 2011).在这些理论中,氮磷元素限制假说是一直以来最为流行的解释富营养化发生机制的假说.Stumm等(1996)基于藻类化学成分分析提出了藻类的“经验分子式”为C106H263O110N16P.理论上每生成1 g 藻需要供给0.009 g 磷和0.063 g 氮,根据利贝格最小定律:植物生长取决于外界提供给它的所需养料中数量最少的一种,由此认为,磷是控制河流湖泊富营养化的主要限制性因素.
无机磷是蓝藻优先利用的磷,有机磷必须通过微生物的酶解作用将磷酸盐释放出来才能被利用,因此,微生物酶对水体富营养化的发生起着重要作用(Dyhrman et al., 2007; Harke et al., 2012;White,2009).碱性磷酸酶(EC 3.1.3.1,Pfam: PF00245)是一种独特的水解酶,它能够对有机物去磷酸化,通过水解磷酸酯将底物分子上的磷酸基团除去,并生成正磷酸盐(谢春生,2012).目前国内外的研究已证实APase基因家族存在3种类型:phoA、phoX、phoD(Sebastian et al., 2009; Pop et al., 2002; Yamane et al., 1978).Luo等(2011)研究发现,海洋环境中phoD比phoA和phoX丰富.为了研究珠江水体富营养化与碱性磷酸酶之间的关系,本文构建了细菌碱性磷酸酶基因phoD克隆文库,以此分析phoD在微生物中的分布,初步揭示对有机磷中磷释放起重要作用的细菌类群.
2 材料与方法(Materials and methods) 2.1 样品采集与处理选取珠江广州段上、中、下游3个点(穗石、坦尾、南沙)作为采样点,采集表层江水10 L,迅速运回实验室处理,4 ℃下12000 r · min-1离心10 min,去上清,收集沉淀,作为提取基因组样品.
2.2 水样中基因组的提取采用CTAB法提取水样DNA(Luo et al., 2010).收集的珠江水沉淀用600 μL TE充分悬浮,加30 μL溶菌酶(50 mg · mL-1),37 ℃水浴30 min;再加30 μL SDS溶液(10 mg · mL-1)和3 μL蛋白酶K(20 mg · mL-1),37℃水浴1 ~1.5 h;随后加入等体积的氯仿-异戊醇(体积比24 ∶ 1),于冰上放置5 min,12000 r · min-1离心5 min后,将上清液转移到新的无菌离心管中,重复此步骤,直至上清液清澈透明,最后将上清液转入1.5 mL EP管中;加入0.6~0.8倍体积的异丙醇,1/10体积的乙酸钠,轻轻混匀,于-20 ℃沉淀3 h;12000 r · min-1离心5 min,弃上清,加入1 mL预冷的70%乙醇,12000 r · min-1离心5 min,弃上清后室温自然风干,提取的DNA加30 μL TE溶解,-20 ℃保存.
2.3 phoD基因的PCR扩增从GenBank中获取了100多条细菌phoD氨基酸序列,利用CODEHOP简并引物设计程序(Rose et al., 2003),得到phoD简并引物:phoDF(5′-GACGGCGTGATGntntggacnmg-3′),phoDR(5′-GTCGTTGGCGACCtcrtgrtcrtc-3′),phoD片段长度为560 bp.PCR反应条件为:94 ℃预变性30 s;94℃变性30 s,降落式(65~55 ℃)退火45 s,每个循环退火温度下降0.5 ℃,72 ℃延伸1 min,19个循环;再以55 ℃退火增加9个循环,72 ℃延伸10 min.25 μL 反应体系包括:12.5 μL Taq PCR Mix(TaKaRa公司),正反向引物(20 μmol · mL-1)各2.5 μL,1 μL DNA(大约20 ng),无菌超纯水补足25 μL.
2.4 细菌克隆文库的构建与阳性克隆的筛选按照试剂盒(TaKaRa)说明书,将经凝胶回收试剂盒纯化回收后的PCR产物与pMD19-T载体连接;连入目的片段的质粒转化入E.coli DH5α 感受态细胞,细胞悬浮液涂布于制备好的 LB 琼脂平板(含 20 μL IPTG、100 μL X-Gal和100 μg · mL-1 氨苄青霉素),37 ℃ 过夜培养;通过蓝白斑筛选阳性克隆子,随机挑取白色克隆子,采用载体特异引物RV-M和M13-47进行菌落PCR;1%的琼脂糖凝胶电泳检测PCR产物大小.
2.5 RFLP 分型测序与进化树构建
用限制性内切酶Hae Ⅲ和MspⅠ对扩增产物进行酶切,产生长短、种类、数目不同的限制性片断,酶切总体系10 μL,37 ℃水浴90 min,酶切产物用10%的聚丙烯酰胺凝胶电泳(PAGE)(200 V,1 h).对限制性酶切片段进行归类,主条带相同的样品归为一类(赵兰凤等,2013;翟文,2008),每种类型样品均送一个测序(上海生物工程公司).核苷酸序列相似度不小于98%的序列归为一个操作分类单元(OTU).利用NCBI Blastx对phoD序列进行分析,选择相似度最高的序列和目的序列利用软件MEGA6.0中的邻接法(Neighbor-Joining)建立phoD基因的系统发育树,进行系统发育分析,Bootstrap values设置为1000.进化距离计算使用泊松校正方法.香农-威纳指数H表示生境中群落多样性,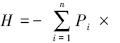 InPi,其中,Pi为第i种酶切类型出现的频率,Pi=Ni/N,Ni为第i种酶切类型所包含的克隆数;Simpson指数公式为:D=1-∑Pi2,其中,Pi为第i种个体数占群落中总个体数的比例;克隆覆盖指数用公式C=1-n/N计算,其中,n为仅在文库中出现一次的OTUs数量,N为一个克隆文库中总的克隆子数(许晴等,2011).
InPi,其中,Pi为第i种酶切类型出现的频率,Pi=Ni/N,Ni为第i种酶切类型所包含的克隆数;Simpson指数公式为:D=1-∑Pi2,其中,Pi为第i种个体数占群落中总个体数的比例;克隆覆盖指数用公式C=1-n/N计算,其中,n为仅在文库中出现一次的OTUs数量,N为一个克隆文库中总的克隆子数(许晴等,2011).
3 个样品的phoD基因扩增结果如图 1所示,phoD基因目的片段约560 bp,扩增特异性良好,可用于后续RFLP研究.
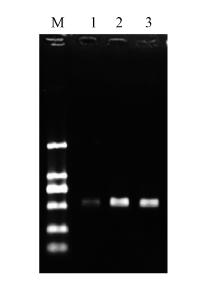 |
| 图 1 phoD扩增片段琼脂糖凝胶电泳(M为DL2000 Marker,1.穗石水样,2.坦尾水样,3.南沙水样) Fig. 1 Amplified fragment of phoD separated by agarose gel electrophoresis(M.DL2000 Marker,1.Suishi sample,2.Tanwei sample,3.Nansha sample) |
3 个基因文库的白色克隆子数量都为600~800个,从每个基因克隆文库中挑取约120个阳性克隆子进行RFLP分型分析.根据PAGE图谱(图 2)将菌落PCR产物大致分为21个类型,21个测序结果除去相似性高于98%的,得到17个OTUs,说明珠江水体中有丰富的含phoD基因菌群存在.从图 2中可以看到,电泳条带清晰,PCR扩增的DNA片段酶切后产生了不同长度的限制性片段,在PAGE中都得到了有效的分离,样品酶切条带数目和迁移率都有一定的差异.片段数目和迁移率都相同,可归为一个类型,如泳道7和泳道25、泳道6和泳道22,而其他泳道片段数目或迁移率不同的初步分为不同类型.因此,根据PAGE图谱分型,各采样点显示出一定的微生物多样性与差异性.
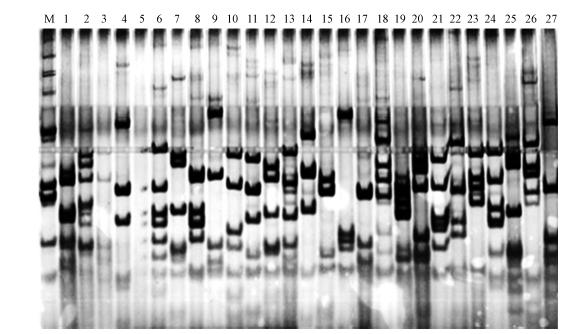 |
| 图 2 部分phoD片段双酶切PAGE凝胶电泳(M:DL2000 DNA Marker,1~27:部分phoD扩增片段双酶切产物) Fig. 2 PAGE gel electrophoresis of phoD fragment degested by double enzyme(M: DL2000 Marker,1~27:phoD fragment digested double enzyme) |
3 个环境样品共得到17个OTUs,穗石、坦尾、南沙3个采样点细菌phoD基因文库分别含有15、17、13个OTUs,并且穗石、南沙两点的OTUs都包含在坦尾样品OTUs中;其中,OTU3和OTU7只在坦尾点出现,坦尾的OTUs种类最丰富,但坦尾的OTU3和OTU7也仅分别含2个克隆子;OTU11和OTU15仅在南沙点中不存在;除上述4个OTUs外,余下13个OUTs在3个采样点所含克隆子数较平均且在3个采样点普遍存在;这17个OTUs中,12个OTUs克隆子数量在10个以上,且占有明显的优势(图 3),不同文库中单次出现的克隆子数仅有2个,可见优势的OTUs基本已经在文库中显示出来.
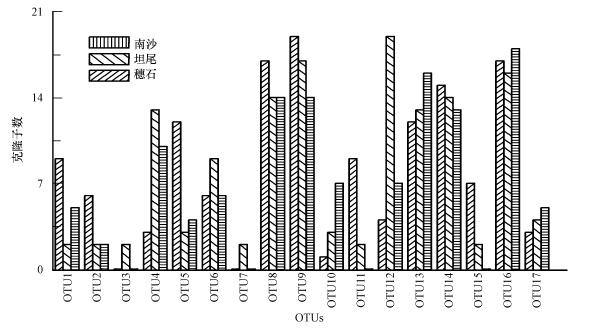 |
| 图 3 珠江水样中phoD基因OUTs分布情况比较 Fig. 3 Abundance of each OUTs in three clone libraries |
从表 1可知,3个点的克隆覆盖指数都是100%,说明该文库基本覆盖了样品中不同类型的phoD基因,基本可以代表样品的种群类型.3个克隆文库多样性差异不大,文库丰富度最高的是穗石水样,最低的是南沙水样.穗石点的香农-威纳指数最高,Simpson指数也最高,微生物多样性高,物种分布最均匀.南沙点的香农-威纳指数为3.489,较其他两点略低,Simpson指数为0.099,较穗石(0.910)、坦尾(0.909)低;此处的物种多样性、均匀度都较其他两个点低.但整体来说,上述3点的Shannon和Simpson指数相差不多,结果表明,珠江广州段上、中、下游的群落结构差异很小,从上游到下游,生物多样性指数呈轻微下降趋势.
| 表1 根据phoD文库得到的多样性指数 Table 1 Diversity index of phoD gene library |
将文库phoD基因序列提交到GenBank中,序列号为(KJ710627-KJ710644).NCBI Blastx的比对结果表明,文库中phoD基因与数据库中序列的相似度较低,仅有37%~74%(表 2).phoD基因序列系统进化发育分析表明,珠江水体中的phoD基因主要来源于Limnohabitans、Pirellula、Plesiocystis等属的细菌.其中,来源于Limnohabitans属的最多,共有8个OTUs,其克隆子数占克隆文库的44%~50%;另外,来源于Pirellula属的克隆子占10.7%~15.7%,来源于Plesiocystis属的克隆子占克隆文库的11.6%~13.6%;比较特殊的是,从图中可以看到OTU9与其他微生物的相似性最小,与其最相近的菌Plesiocystis的相似度仅有37%,因此,与其他的序列都进化较远,在进化树上和其它序列独立开来(图 4).
| 表2 序列与最相关蛋白序列的相似度及3个phoD基因文库中每个OTU的丰富度 Table 2 Similarity,the closest related protein sequences, and abundance of each OTU in three phoD gene clone libraries |
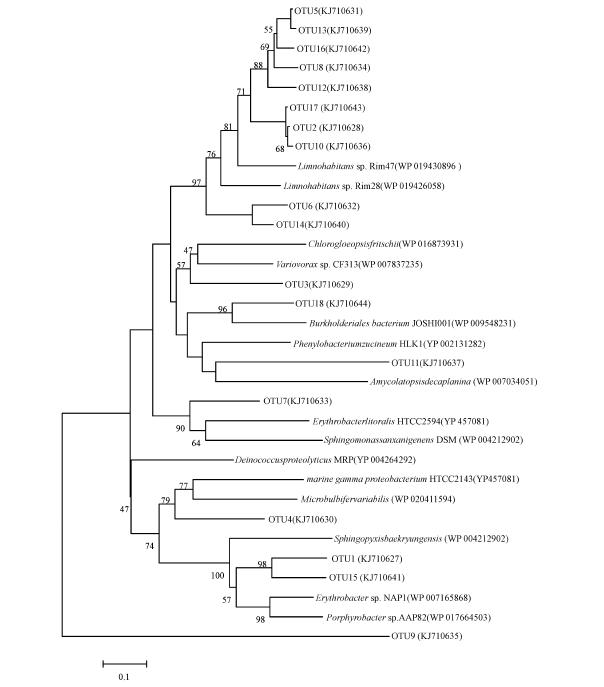 |
| 图 4 phoD基因系统发育树 Fig. 4 Phylogenetic tree of phoD gene |
碱性磷酸酶(APase)是最主要的有机磷水解酶,在无机磷匮乏的情况下,APase释放的无机磷供藻类利用,致使藻类大量繁殖,磷酸酶可通过增加磷的生物可利用性促进富营养化过程.因此,phoD基因编码的碱性磷酸酶可能在珠江水体的富营养化过程中有重要的作用(Yaman et al., 1978;宋春雷等,2005).本文以phoD基因作为碱性磷酸酶的标记基因,扩增珠江水体上、中、下游3个点细菌的phoD基因,研究采样点含phoD基因的细菌类群与丰度.3个采样点均有较为丰富的phoD基因,证明在珠江水体中普遍含有phoD基因,并且穗石水样的含phoD基因的细菌类群丰富度、均匀度都比其他两点高,这可能与穗石采样点紧靠穗石村、新造镇等居民生活区有关,有较多生活污水排放,水体中营养物质氮、磷含量较高(冯胜等,2007).南沙水样的细菌类群丰富度、均匀度都较其他两点低.此前有研究报道在高盐条件下,细胞内的磷含量会减少(Kageyama et al., 2011),南沙点位于珠江下游入海口,水体中盐分使含phoD基因的群落种类下降.上述3点的环境差异,特别是水质差异,以及不同的生态环境条件为含phoD基因的细菌繁殖与进化提供了特有的环境,因此,导致微生物的分布存在差异.整体来说,珠江广州段上、中、下游中含phoD基因的细菌群落差异较小,从上游到下游呈略下降趋势,穗石水体细菌的多样性相对较多.
本实验3个不同采样点克隆的phoD基因与NCBI中提交的已知菌序列和未培养菌序列的相似度都比较低(37%~74%),文库中phoD基因的谱系分散,氨基酸序列一致性比较低.测序结果显示,序列与提交的序列相似度低,说明在不同的环境下还有其他类群种类非常丰富的含碱性磷酸酶的细菌.本文研究发现,Limnohabitans、Pirellula、Plesiocystis属细菌是珠江主要的phoD来源.Limnohabitans属细菌在富营养化水体和废水的磷循环中有重要作用,是主要的淡水浮游生物(Mcmahon et al., 2013;Salcher,2013);Pirellula属细菌存在于活性污泥的磷酸盐分解菌的群落结构中(Bond et al., 1995);Plesiocystis属细菌是一种海洋生态环境中磷酸酯和磷酸酶的分解细菌(Villarreal-Chiu et al., 2012).实验结果表明,珠江水体含有丰富的磷转化微生物菌种,并且具有较强的分解有机磷能力,这些微生物碱性磷酸酶的有机磷水解能力可能对减缓珠江水体的富营养化有重要作用.
5 结论(Conclusions)限制性酶切片段多态性(RFLP)分析结果表明,上述穗石、坦尾、南沙3个点的phoD基因分别含有15、17、13个操作分类单元(OTU),穗石点的多样性(Shannon指数和Simpson指数)均高于其他两个点.phoD基因序列系统发育分析表明,珠江水体中phoD基因主要来源于Plesiocystis、Limnohabitans、Pirellula等属的细菌,而Limnohabitans属的phoD基因在文库中含量最高,占文库的44%~50%.研究表明,珠江水体中细菌的phoD基因具有较高的多样性,这些基因编码的碱性磷酸酶可能在珠江水体的富营养化过程中有重要的作用.
| [1] | Bond P L,Hugenholtz P,Keller J,et al.1995.Bacterial community structures of phosphate-removing and non-phosphate-removing activated sludges from sequencing batch reactors[J].Applied and Environmental Microbiology,61(5): 1910-1916 |
| [2] | Brookes J D,Carey C C.2011.Resilience to blooms[J].Science,334(6052): 46-47 |
| [3] | Conley D J,Paerl H W,Howarth R W,et al.2009.Controlling eutrophication: nitrogen and phosphorus[J].Science,323(5917): 1014-1015 |
| [4] | Dyhrman S T,Ammerman J W,Van Mooy B A S.2007.Microbes and the marine phosphorus cycle[J].Oceanography,20(2): 110-116 |
| [5] | 冯胜,秦伯强,高光.2007.细菌群落结构对水体富营养化的响应[J].环境科学学报,27(11): 1823-1829 |
| [6] | Goldman C R.1960.Molybdenum as a factor limiting primary productivity in Castle Lake,California[J].Science,132(3433): 1016-1017 |
| [7] | Harke M J,Berry D L,Ammerman J W,et al.2012.Molecular response of the bloom-forming cyanobacterium,Microcystis aeruginosa,to phosphorus limitation[J].Microbial Ecology,63(1): 188-198 |
| [8] | Jöhnk K D,Huisman J,Sharples J,et al.2008.Summer heatwaves promote blooms of harmful cyanobacteria[J].Global Change Biology,14(3): 495-512 |
| [9] | Kageyama H,Tripathi K,Rai A K,et al.2011.An alkaline phosphatase/phosphodiesterase,phoD,induced by salt stress and secreted out of the cells of Aphanothece halophytica,a halotolerant cyanobacterium[J].Applied and Environmental Microbiology,77(15): 5178-5183 |
| [10] | Lu F H,Ni H G,Liu F,et al.2009.Occurrence of nutrients in riverine runoff of the Pearl River Delta,South China[J].Journal of Hydrology,376(1/2): 107-115 |
| [11] | Luo J F,Lin W T,Guo Y.2010.Method to detect only viable cells in microbial ecology[J].Applied Microbiology and Biotechnology,86(1): 377-384 |
| [12] | Luo H W,Zhang H M,Long R A,et al.2011.Depth distributions of alkaline phosphatase and phosphonate utilization genes in the North Pacific Subtropical Gyre[J].Aquatic Microbial Ecology,62(1): 61-69 |
| [13] | McMahon K D,Read E K.2013.Microbial contributions to phosphorus cycling in eutrophic lakes and wastewater[J].Annual Review of Microbiology,67: 199-219 |
| [14] | Pop O,Martin U,Abel C,et al.2002.The twin-arginine signal peptide of phoD and the TatAd/Cd proteins of Bacillus subtilis form an autonomous Tat translocation system[J].Journal of Biological Chemistry,277(5): 3268-3273 |
| [15] | Rose T M,Henikoff J G,Henikoff S.2003.CODEHOP (COnsensus-DEgenerate hybrid oligonucleotide primer) PCR primer design[J].Nucleic Acids Research,31(13): 3763-3766 |
| [16] | Salcher M M.2013.Same same but different: ecological niche partitioning of planktonic freshwater prokaryotes[J].Journal of Limnology,73(S1): 74-87 |
| [17] | Sebastian M,Ammerman J W.2009.The alkaline phosphatase phoX is more widely distributed in marine bacteria than the classical phoA[J].The ISME Journal,3(5): 563-572 |
| [18] | 宋春雷,曹秀云,李建秋,等.2005.湖泊磷酸酶与微生物活性对内源磷负荷的贡献及其与富营养化的关系[J].中国科学 D辑: 地球科学,35(S2): 90-100 |
| [19] | Stumm W,Morgan J J.1996.Aquatic Chemistry: Chemical Equilibria and Rates in Natural Waters[M].New York: Wiley-Interscience Publication |
| [20] | Villarreal-Chiu J F,Quinn J P,McGrath J W.2012.The genes and enzymes of phosphonate metabolism by bacteria,and their distribution in the marine environment[J].Frontiers in Microbiology,3(19): 1-13 |
| [21] | White A E.2009.New insights into bacterial acquisition of phosphorus in the surface ocean[J].Proceedings of the National Academy of Sciences of the United States of America,106(50): 21013-21014 |
| [22] | 谢春生.2012.碱性磷酸酶在点面污染源磷形态转化中的作用研究[D].杭州: 浙江大学.1-92 |
| [23] | 邢伟.2007.铁对水华蓝藻的生态生理学效应研究[D].武汉: 中国科学院水生生物研究所.1-157 |
| [24] | 许晴,张放,许中旗,等.2011.Simpson 指数和 Shannon-Wiener 指数若干特征的分析及 "稀释效应"[J].草业科学,28(4): 527-531 |
| [25] | Yamane K,Maruo B.1978.Purification and characterization of extracellular soluble and membrane-bound insoluble alkaline phosphatases possessing phosphodiesterase activities in Bacillus subtilis[J].Journal of Bacteriology,134(1): 100-107 |
| [26] | 翟文.2008.铬污染土壤修复过程中土壤细菌群落多样性RFLP分析[D].西安: 西北农林科技大学.1-51 |
| [27] | 赵兰凤,张丽娟,胡伟,等.2013.RFLP法研究生物复混肥及香蕉枯萎病对土壤细菌群落多样性的影响[J].中国生物防治学报,29(3): 406-416 |
 2015, Vol. 35
2015, Vol. 35


