2. 广东省菌种保藏与应用重点实验室, 广州 510070;
3. 中山大学药学院微生物与生化药学实验室, 广州 510006
2. Guangdong Provincial Key Laboratory of Microbial Culture Collection and Application, Guangzhou 510070;
3. Department of Microbial and Biochemical Pharmacy, School of Pharmaceutical Sciences, Sun Yat-sen University, Guangzhou 510006
双酚A(Bisphenol A,BPA)是人类日常生活中接触最广泛的工业化合物之一.BPA具有与雌激素类似的结构且化学性质稳定,可以通过食物链富集和环境暴露进入机体并在机体内长期蓄积,难以生物降解和排出,进而干扰机体的内分泌系统,是一类典型的环境雌激素(Rubin,2011).近年来,大量实验证实,BPA能干扰人体生殖系统、神经系统、免疫系统、胚胎发育的正常功能,并能促进乳腺癌、前列腺癌及儿童生殖系统肿瘤等多种肿瘤的发生发展(Rogers et al.,2013;Vom Saal et al.,2012;秦定霞等,2010).
肿瘤浸润与转移是恶性肿瘤的基本特征和重要标志,也是大多数癌症患者的主要致死原因(Hanahan et al.,2011).最新研究发现,BPA能够增强恶性肿瘤浸润与迁移能力,并促进肿瘤的转移(Derouiche et al.,2013),然而相关作用机制还有待进一步明确.上皮细胞间质化(Epithelial\|Mesenchymal Transition,EMT)是指呈上皮样表型的细胞失去极性,通过特定程序转化为具有间质表型细胞的生物学过程,是上皮细胞来源的恶性肿瘤细胞获得迁移和侵袭能力的重要生物学过程,被认为是肿瘤转移过程中的关键事件(Lamouille et al.,2014).本研究旨在探讨BPA对人乳腺癌MCF\|7细胞EMT发生的诱导作用及作用机制,以期为明确BPA在肿瘤发生发展中的作用提供新线索.
2 材料与方法(Materials and methods) 2.1 材料胎牛血清、DMEM培养基、胰蛋白酶购自Gibco公司,BPA购自sigma公司,E\|cadherin、Vimentin、GAPDH抗体购自Santa Cruz公司,Snail抗体购自CST公司,HRP标记山羊抗鼠IgG、山羊抗兔IgG购自北京鼎国生物技术有限公司,Quick Start Bradford蛋白定量试剂购自Bio\|Rad公司,ECL化学发光底物试剂盒购自Pierce公司,反转录试剂盒、RT\|PCR试剂盒购自TaKaRa公司,PCR引物由上海生工公司合成,其余试剂均为国产分析纯以上.
2.2 细胞培养人乳腺癌MCF\|7细胞购自中科院上海细胞库,采用含10%胎牛血清(Fetal Bovine Serum,FBS)的DMEM培养液,于37 ℃、5% CO2的培养箱内饱和湿度培养.
2.3 MTT法检测BPA对细胞活力的影响取对数生长期的MCF\|7细胞,调整细胞密度为3×103个 · mL-1,接种于96孔板.24 h后,用不同浓度(0、10、100 ng · mL-1)BPA处理该细胞,然后置于37 ℃、饱和湿度培养箱中培养24 h或48 h.每孔各加100 μL浓度为0.25 mg · mL-1的MTT,置于37 ℃孵箱中孵育4 h后弃上清,每孔加100 μL DMSO,振荡均匀后于酶标仪570 nm处测定吸光度.
2.4 Transwell肿瘤细胞迁移实验将Transwell小室放入培养板中,在上室加入300 μL预温的无血清培养基,室温下静置15~30 min,使基质胶再水化.消化细胞,用PBS洗2遍,用无血清培养基重悬,调整细胞密度至2×105个 · mL-1. 取细胞悬液200 μL加入24孔板Transwell小室,24孔板下室加入500 μL含FBS的培养基,对种在24孔板Transwell小室的细胞进行处理.继续培养48 h后,对下室细胞进行苏木素染色,每组随机取5个视野进行计数,并做柱状图分析药物对细胞侵袭能力的影响.
2.5 Real\|time RT\|PCR按照Trizol(Invitrogen)说明书方法提取细胞总RNA,按Primescript RT reagent Kit反转录试剂盒(TaKaRa)说明书将RNA逆转录为cDNA.引物由上海生工生物工程有限公司设计并合成,引物序列如下:E\|cadherin上游引物:5′\|TACACTGCCCAGGAGCCAGA\|3′,下游引物:5′\|TGGCACCAGTGTCCGGATTA\|3′;Vimentin上游引物:5′\|TGAGTACCGGAGACAGGTGCAG\|3′,下游引物:5′\|TAGCAGCTTCAACGGCAAAGTTC\|3′; Snail上游引物:5′\|GACCACTATGCCGCGCTCTT\|3′,下游引物:5′\|TCGCTGTAGTTAGGCTTCCGATT\|3′;GAPDH上游引物:5′\|GCACCGTCAAGGCTGAGAAC\|3′,下游引物:5′\|TGGTGAAGACGCCAGTGGA\|3′.Real\|time PCR反应体系及条件参照SYBR Premix Ex TapTM试剂盒(TaKaRa),2-△△CT法计算mRNA的相对表达量,以GAPDH作为内参.每个实验组重复3次.
2.6 蛋白提取和Western Blot分析收集细胞,经PBS洗涤后用三去污裂解液(50 mmol · L-1 Tris\|Cl,150 mmol · L-1 NaCl,0.2 g · L-1叠氮钠,100 mg · L-1 Aprotin,100 mg · L-1 PMSF,1 g · L-1 SDS,10 g · L-1 NP\|40,5 g · L-1去氧胆酸钠)裂解,离心后收集上清,用Bradford法测定蛋白浓度;等量蛋白样品经10%的SDS\|PAGE电泳分离后,转印至PVDF膜上,5%脱脂奶粉室温封闭2 h,E\|cadherin、Vimentin、Snail、GAPDH一抗均以1 ∶ 1000比例稀释,4 ℃孵育过夜.经PBST洗涤后,加入HRP标记的特异性二抗以1 ∶ 5000比例稀释,室温下孵育2 h,最后用ECL化学发光试剂对X光片显影,扫描图片.
2.7 统计学方法各组实验均重复3次,应用软件GraphPad Prism 5.0进行统计学分析,组间比较用One\|way analysis of variance(单因素方差分析),p<0.05表示有统计学差异.
3 结果(Results) 3.1 BPA对MCF\|7细胞增殖的影响以0、10、100 ng · mL-1 BPA作用于MCF\|7细胞, 分别于加药后12、24、48 h检测BPA对MCF\|7细胞活力的影响(图 1).结果发现,在12 h时,BPA对细胞增殖没有明显的影响;而加入BPA处理24 h与48 h能明显促进细胞的增殖,且具有浓度和时间的依赖性.
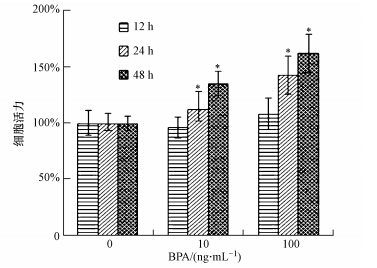 |
| 图 1 BPA对MCF\|7细胞增殖的影响(实验重复3次,*p<0.05,下同) Fig.1 Effects of BPA on cell proliferation of MCF\|7 cells(Experiment was repeated three times,*p<0.05,the same below) |
BPA(100 ng · mL-1)处理MCF\|7细胞48 h后,采用Transwell试验检测MCF\|7细胞的迁移能力.结果显示,BPA处理组穿过Matrigel及Transwell小室滤膜到达滤膜下层的MCF\|7细胞数明显增多(图 2a),BPA干预后MCF\|7细胞转移能力(279±15)比对照组(73±12)显著提高(p <0.05)(图 2b).
 |
| 图 2 Transwell实验检测BPA对MCF\|7细胞迁移能力的影响(a.各组Transwell小室滤膜下方细胞HE染色图;b.各组迁移至Transwell小室滤膜下方细胞计数) Fig.2 Effects of BPA on cell migration of MCF\|7 cells(a.Transwell cell migration assay of PC3 cells treated with 100 ng · mL-1 BPA for 48 h,b.Number of migration cells) |
BPA(100 ng · mL-1)处理MCF\|7细胞48 h后,分别提取细胞总RNA和细胞总蛋白,Real\|Time RT\|PCR、Western Blot检测细胞内上皮型蛋白标志物E\|cadherin、间质型蛋白标志物Vimentin及EMT相关转录因子Snail、Slug表达变化.如图 3所示,BPA能明显抑制E\|cadherin mRNA和蛋白的表达,促进Vimentin及Snail mRNA和蛋白的表达.
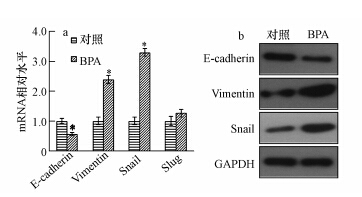 |
| 图 3 BPA对MCF\|7细胞EMT标志物表达的影响(a.mRNA表达水平;b.蛋白表达水平) Fig.3 Effects of BPA on the EMT markers expression in MCF\|7 cells(a.mRNA expression,b. protein expression) |
乳腺癌是雌激素依赖的恶性肿瘤,流行病学数据显示,长期暴露高水平的雌激素能增加乳腺癌的发生率(Li et al.,2003).环境雌激素是一类具有干扰体内正常内分泌物质合成、释放,激活或抑制内 分泌系统功能的化合物,包括人工合成化合物及植物天然雌激素(Sonnenschein et al.,1998).BPA是一种典型的环境雌激素,广泛应用于塑料制造业中.长期暴露BPA能够促进乳腺癌、子宫内膜癌等激素依赖的肿瘤发生发展(Fern and ez et al.,2010,杨淋清等,2010).我们发现,BPA能够显著促进乳腺癌MCF\|7细胞的增殖,且具有时间和浓度依赖性.研究表明,BPA能够与雌激素受体(Estrogen Receptors,ER)直接结合(Kuiper et al.,1998),因此,BPA促进乳腺癌细胞的增殖可能与BPA激活雌激素受体信号相关(Sengupta et al.,2013; 卫立等,2006).此外,基因表达谱分析发现,BPA能够通过调节多种类型基因的表达而赋予肿瘤细胞凋亡逃避、细胞周期异常、微环境胁迫抵抗的能力(Dairkee et al.,2008),说明BPA促进乳腺癌的恶性进展是通过复杂的信号传导通路来完成的,并可能影响多重肿瘤生物学特性.
最新研究发现,BPA能够增强前列腺癌细胞、神经母细胞瘤的浸润能力(Derouiche et al.,2013;Zhu et al.,2010).肿瘤浸润与转移是恶性肿瘤的重要特征之一(Hanahan et al.,2011),而EMT被认为是肿瘤转移的关键起始步骤,参与包括乳腺癌在内的多种肿瘤的侵袭、转移过程(Thiery,2002).我们发现,BPA处理能增强乳腺癌MCF\|7细胞的侵袭与迁移能力,且BPA显著抑制MCF\|7细胞上皮型蛋白标志物E\|cadherin的表达,促进间质型蛋白标志物Vimentin的表达,提示BPA能够诱导肿瘤细胞EMT发生,从而增强细胞的浸润与迁移能力.
肿瘤细胞EMT发生主要受一类转录抑制因子超家族成员所调控,其中,Snail转录因子是肿瘤EMT发生的一个重要的调节因子.Snail通过抑制E\|cadherin的表达诱导肿瘤细胞EMT发生,从而赋予肿瘤细胞移动和侵袭的能力(Batlle et al.,2000).我们发现,BPA能够促进Snail的表达,提示Snail可能是BPA诱导MCF\|7细胞EMT发生的关键分子.已知GPR30/EGFR信号是乳腺癌发生发展中的一条重要转导通路,EGFR可以直接调控Snail的表达、核定位及活性而诱导EMT的发生(Lee et al.,2008).我们前期研究及他人研究均发现BPA能迅速激活GPR30/EGFR信号(Ge et al.,2014,张巍等,2013).因此,BPA可能通过GPR30/EGFR信号促进乳腺癌MCF\|7细胞Snail的表达与活化,进而下调E\|cadherin的表达,上调Vimentin的表达,最终导致EMT的发生.
总之,本研究首次提出BPA通过诱导肿瘤EMT发生进而增强乳腺癌细胞的浸润与迁移能力,且转录因子Snail在BPA诱导肿瘤EMT效应中发挥了重要的作用,为进一步明确BPA等环境雌激素对恶性肿瘤的影响提供了新的线索.
5 结论(Conclusions)研究发现,低浓度BPA能够促进MCF\|7细胞的增殖,显著增强细胞的迁移能力.BPA处理能抑制E\|cadherin的表达,促进Vimentin及Snail的表达.研究结果提示,BPA处理可能通过促进Snail的表达而调控EMT相关蛋白标志物的表达,进而增强乳腺癌MCF\|7细胞的迁移能力.
| [1] | Batl le E,Sancho E,Francí C,et al.2000.The transcription factor Snail is a repressor of E-cadherin gene expression in epithelial tumour cells[J].Nature Cell Biology,2(2): 84-89 |
| [2] | Dairkee S H,Seok J,Champion S,et al.2008.Bisphenol A induces a profile of tumor aggressiveness in high-risk cells from breast cancer patients[J].Cancer Research,68(7): 2076-2080 |
| [3] | Derouiche S,Warnier M,Mariot P,et al.2013.Bisphenol A stimulates human prostate cancer cell migration via remodelling of calcium signalling[J].Springerplus,2(1): 54 |
| [4] | Fernandez S V,Russo J.2010.Estrogen and xenoestrogens in breast cancer[J].Toxicologic Pathology,38(1): 110-122 |
| [5] | Ge L C,Chen Z J,Liu H Y,et al.2014.Involvement of activating ERK1/2 through G protein coupled receptor 30 and estrogen receptor α/β in low doses of bisphenol A promoting growth of Sertoli TM4 cells[J].Toxicology Letters,226(1): 81-89 |
| [6] | Hanahan D,Weinberg R A.2011.Hallmarks of cancer: the next generation[J].Cell,144(5): 646-674 |
| [7] | Kuiper G G,Lemmen J G,Carlsson B,et al.1998.Interaction of estrogenic chemicals and phytoestrogens with estrogen receptor beta[J].Endocrinology,139(10): 4252-4263 |
| [8] | Lamouille S,Xu J,Derynck R.2014.Molecular mechanisms of epithelial-mesenchymal transition[J].Nature Reviews Molecular Cell Biology,15(3): 178-196 |
| [9] | Lee M Y,Chou C Y,Tang M J,et al.2008.Epithelial-mesenchymal transition in cervical cancer: correlation with tumor progression,epidermal growth factor receptor overexpression,and snail up-regulation[J].Clinical Cancer Research,14(15): 4743-4750 |
| [10] | Li C I,Malone K E,Porter P L,et al.2003.Relationship between long durations and different regimens of hormone therapy and risk of breast cancer[J].The Journal of the American Medical Association,289(24): 3254-3263 |
| [11] | 秦定霞,崔毓桂,刘嘉茵.2010.双酚 A 对生殖系统的影响及其作用机制[J].国际生殖健康/计划生育杂志,29(1): 26-29 |
| [12] | Rogers J A,Metz L,Yong V W.2013.Review: Endocrine disrupting chemicals and immune responses: a focus on bisphenol-A and its potential mechanisms[J].Molecular Immunology,53(4): 421-430 |
| [13] | Rubin B S.2011.Bisphenol A: an endocrine disruptor with widespread exposure and multiple effects[J].The Journal of Steroid Biochemistry and Molecular Biology,127(1/2): 27-34 |
| [14] | Sengupta S,Obiorah I,Maximov P Y,et al.2013.Molecular mechanism of action of bisphenol and bisphenol A mediated by oestrogen receptor alpha in growth and apoptosis of breast cancer cells[J].British Journal of Pharmacology,169(1): 167-178 |
| [15] | Sonnenschein C,Soto A M.1998.An updated review of environmental estrogen and androgen mimics and antagonists[J].The Journal of Steroid Biochemistry and Molecular Biology,65(1/6): 143-150 |
| [16] | Thiery J P.2002.Epithelial-mesenchymal transitions in tumour progression[J].Nature Reviews Cancer,2(6): 442-454 |
| [17] | Vom Saal F S,Nagel S C,Coe B L,et al.2012.The estrogenic endocrine disrupting chemical bisphenol A (BPA) and obesity[J].Molecular and Cellular Endocrinology,354(1/2): 74-84 |
| [18] | 卫立,王斌,刘树深,等.2006.低剂量双酚A与17β雌二醇对MCF-7细胞增殖作用的剂量效应关系及其联合作用探索[J].环境科学学报,26(6): 968-972 |
| [19] | 杨淋清,庄志雄.2010.低剂量双酚A与乳腺癌关系研究进展[J].中国公共卫生,26(12): 1157-1159 |
| [20] | 张巍,谭岩,方艳秋.2013.GPR30-EGFR 信号通路在双酚A促乳腺癌细胞增殖中的作用[J].中国妇幼保健,28(14): 2286-2289 |
| [21] | Zhu H T,Zheng J C,Xiao X M,et al.2010.Environmental endocrine disruptors promote invasion and metastasis of SK-N-SH human neuroblastoma cells[J].Oncology Reports,23(1): 129-139 |
 2015, Vol. 35
2015, Vol. 35


