砷污染在全世界范围内普遍发生,如孟加拉国、印度的西孟加拉邦、阿根廷、越南、缅甸以及拉丁美洲的一些国家的地下水受到砷污染,导致几百万人遭受到不同程度的砷危害(Feroze and Ahmed, 2014; Rahman et al., 2013; Sigrist et al., 2013; Agusa et al., 2013; van Geen et al., 2014; Bundschuh et al., 2012).Zhang等(2013)的研究表明,中国有近两千万人生活在地下水砷超标的高风险地区.湖南素有“有色金属之乡”的美誉,在开采和冶炼等人为活动中,由于“三废”的不当处理,使得矿区和冶炼区周围的农田土壤受到不同程度的砷污染.陈同斌等(1992)报道湖南严重受到砷污染的土壤中砷含量是世界土壤中砷平均含量的8~544倍.廖晓勇等(2003)报道湖南常宁县水口山附近的大面积水稻田受到砷污染,其含量为92~840 mg · kg-1.土壤砷污染不仅影响水稻的生长发育,而且严重影响水稻的产量和品质.蔡保松等(2004)报道我国谷类作物中砷含量为0.07~0.83 mg · kg-1,而在砷污染严重的地区,水稻籽粒中砷的含量可达0.50~7.50 mg · kg-1(Liao et al., 2005).稻米中砷通过食物链的传递进入人体,从而对人体健康构成严重威胁.王振刚等(1999)研究表明,石门县雄黄矿附近的3个村庄土壤中砷含量为84~296 mg · kg-1,当地3000多居民中,有1200多人被确诊为砷中毒.2014年,该矿区从1971年到2013年期间,有600多名砷中毒者去世,其中400多人死于癌症(http://epaper.dfdaily.com/dfzb/html/2014-02/14/content_864296.htm).因此,开展阻控土壤砷向水稻迁移的研究,不仅关系到农业安全生产的问题,而且关系到人类健康安全的问题.
土壤是水稻吸收砷的最主要来源,水稻中砷含量与土壤中砷的含量呈正相关关系,减少稻米中砷含量的关键是降低土壤砷的生物有效性,控制其向水稻的迁移.纳米材料作为一种新兴的功能材料,由于本身的结构和特性使其在许多方面有着广阔的应用前景,是修复受污染土壤和地下水方面理想的分离富集材料(Chen et al., 2004; Joo et al., 2004; Yang and Lee, 2005).近年来,锰氧化物因其具有电荷零点低、比表面积大、酸性位点多、吸附能力强、氧化和催化活性高等多种环境属性(鲁安怀,2001;高翔,2002),而引起国内外学者越来越多的关注,如谢正苗等(1989)研究表明,土壤中δ-MnO2对As(Ⅲ)的氧化动力学符合假一级速率方程,且土壤中氧化铁、氧化铝和碳酸钙与δ-MnO2的包蔽能改变氧化反应速率.陈红等(1998)利用软锰矿的氧化性和吸附性直接对含As(Ⅲ)的废水进行了吸附实验,并就其吸附特性进行研究,结果表明MnO2对As(Ⅲ)有着较强的吸附能力.当前,将锰氧化物纳米材料运用于阻控土壤砷迁移的研究还鲜见报道.本研究通过制成二氧化锰纳米材料,利用盆栽种植水稻,向砷污染土壤中添加不同浓度的纳米级二氧化锰材料,分析水稻各个时期各部位的砷和锰含量变化特征以及土壤溶液中锰和砷的含量变化,以期阻控土壤砷向水稻迁移,为解决当前农田土壤砷污染问题提供理论依据.
2 材料与方法(Materials and methods) 2.1 试验材料土壤样品采自湖南省郴州市某As污染农田(蔡保松,2004;Liao et al., 2005),该土壤为石灰性水稻土(0~20 cm),土壤经自然风干后过5 mm筛备用,其基本理化性质分析方法见土壤农业化学分析方法(鲁如坤,1999),结果如表 1所示.供试水稻品种为玉针香(购自湖南水稻所).
| 表 1 供试土壤样品基本理化性质 Table 1 Basic properties of the soils studied |
纳米级二氧化锰材料用水热法制备.具体操作步骤为:将MnSO4 · H2O与K2S2O8放入锥形瓶,加入蒸馏水后加入浓硫酸,混在一起用磁力搅拌器搅拌10 min后放入50 mL 高压反应釜,然后放入电热恒温鼓风干燥箱,在110 ℃条件下反应6 h后取出,冷却到室温,放入离心机离心3次,每次离心后去除上清液并用蒸馏水洗涤,直至pH=7,放入电热恒温鼓风干燥箱中,在60 ℃的条件下干燥8 h,得到黑色粉末MnO2.制出的二氧化锰纳米材料宏观上是一种常温下非常稳定的黑色粉末状固体,微观形貌通过透射电镜观察.
2.2 试验设计水稻种子用30% H2O2消毒10 min后,用去离子水冲洗3次,播种于湿润珍珠岩中,在光照培养箱中培养,第30 d后移栽水稻秧苗.移栽前将As污染土壤装入培养盆,每盆15.0 kg,施用4.29 g磷酸铵、2.93 g尿素、3.30 g碳酸钾作为基肥,然后每盆分别加入质量比为0、0.2%、0.5%、1.0%、2.0%的纳米级二氧化锰材料(分别简称CK、0.2%、0.5%、1.0%和2.0%),基肥、纳米级二氧化锰材料和土壤充分混合均匀后加水平衡7 d.水稻移栽后模拟水田条件并保持土壤淹水,在水稻整个生长期都使盆内表土以上保持3.0 cm左右的水层,每个处理设3个平行,共计15盆,采用随机排列的方式在湖南农业大学的温室进行培养,直至水稻成熟.第45 d(从育秧开始计算,此时处于分蘖后期)开始每隔15 d抽取土壤溶液(总计取样5次),分析其中pH值以及锰和砷的含量;在水稻的分蘖期、抽穗期和成熟期采集水稻植株样品,分析水稻植株各器官(根、茎、叶和谷粒)中锰和砷的含量.
2.3 分析方法土壤溶液用土壤溶液提取装置(由一次性注射器和土壤溶液提取管组成)抽取.溶液收集到15 mL后,用滤膜规格为0.45 μm的针头过滤器过滤,立即用便携式pH计(pHB-4型,上海日岛科学仪器有限公司)测量土壤溶液pH,测量完之后加入1滴浓硝酸,于0~4 ℃的条件下保存待测,土壤溶液中锰含量采用电感耦合等离子发射光谱仪(ICP-OES iptima 8300 Perkinelmer)测定,砷含量用原子荧光光谱仪(AFS-920,北京吉天仪器有限公司)测定.
水稻植株采用HNO3法消煮(鲁如坤,1999),同时用植物国家标准参比物质(灌木枝叶GBW07603(GSV-2)和大米GBW10010(GSB-1))和平行全空白样进行分析质量控制,标样测定结果均在允许误差范围内.水稻中锰的含量采用电感耦合等离子体发射光谱仪(ICP-OES iptima 8300 Perkinelmer)测定,砷含量采用原子荧光光谱仪(AFS-920,北京吉天仪器有限公司)测定.分析过程中所用试剂均为优级纯.
文中数据计算采用Excel 2007完成,统计分析和绘图采用SPSS18.0完成.
3 结果(Results) 3.1 纳米级二氧化锰材料纳米级二氧化锰材料的扫描电子显微镜照片如图 1所示.图 1中a和b分别为制出的纳米级二氧化锰材料放大20000倍和25000倍的效果图,c和d为该材料放大10000倍效果图.从图 1可以看出,纳米级二氧化锰材料成团簇状,结构均匀、分散的球状团聚结构,团簇微球的尺寸为1000~1500 nm,单个的纳米针是直径约为50 nm,长度约为500 nm.纳米材料是指在三维空间中至少有一维处于纳米尺度范围(1~100 nm)或由它们作为基本单元构成的材料,本方法合成的纳米级二氧化锰材料为二维纳米材料.
 |
| 图 1 制备纳米MnO2的扫描电子显微镜照片 Fig. 1 Scanning electron micrograph on nano-MnO2 |
土壤溶液pH值随水稻生长时间的变化如图 2所示,土壤溶液pH值最高时间是在第45 d(7.25~7.55),随着时间的推移,土壤溶液pH值有所下降,到105 d时为最低(6.28~6.76),适合水稻的生长.在45 d时,添加纳米级二氧化锰材料的土壤溶液中pH范围为7.36~7.55,较没有添加(CK)时的pH值(7.25)大,随后都呈下降趋势,表明添加纳米级二氧化锰材料并没有显著改变土壤溶液pH值.
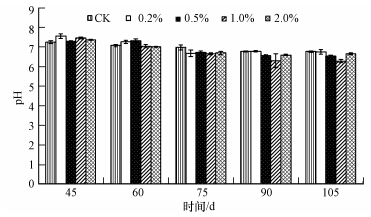 |
| 图 2 土壤溶液pH值 Fig. 2 pH of soil solution |
添加不同浓度纳米级二氧化锰材料后,水稻不同生长时期土壤溶液中砷、锰的含量变化规律如图 3所示.从图 3a中可看出,与对照组相比,添加不同浓度的纳米级二氧化锰材料后土壤溶液中砷的含量在第45 d时都有很明显的降低,且随着纳米级二氧化锰材料含量的增加,土壤溶液中砷的含量降低越多;随着水稻生长时间的增加,CK组土壤溶液中砷的含量一直下降,在第105 d时达到最低值(13.26±0.95)μg · L-1,0.2%处理的土壤溶液砷的含量与CK组类似,是持续降低的过程;而0.5%、1.0%和2.0%处理后的土壤溶液中砷的含量随培养时间的增加,呈先上升后下降的趋势,且上升阶段大致在孕穗期与抽穗期.从图 3b中可看出,随着水稻生长时间的增加,土壤溶液中锰的含量随之增加;在第60 d之后,持续下降,到第105 d后降到最低.
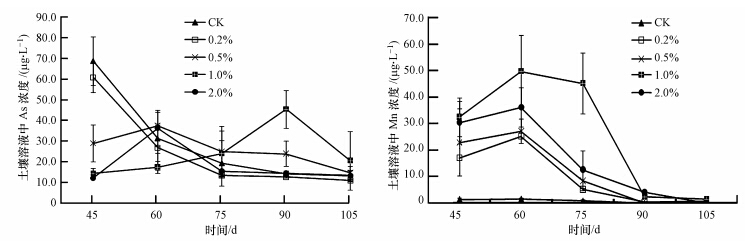 |
| 图 3 土壤溶液中As和Mn的变化趋势 Fig. 3 Contents of As and Mn in soil solution |
水稻各个时期不同部位中砷和锰的含量如表 2所示.从表 2可知,无论是否添加纳米级二氧化锰材料,砷在水稻根、茎和叶的分布规律都是:根>茎>叶.
| 表 2 各时期水稻根、茎、叶中砷和锰的含量 Table 2 As and Mn concentrations of cultivar in different periods |
添加了纳米级二氧化锰材料后,每个时期的水稻各部位砷的含量和CK组相比,都有不同程度的降低,即添加纳米级二氧化锰材料后能够阻碍土壤砷迁移到水稻植株内.处理后的水稻在整个生长周期,砷浓度呈先下降后上升的趋势,这可能是水稻在分蘖和成熟阶段其体内的砷含量较高,而在孕穗和抽穗阶段,水稻体内的砷含量相对较少.同时可以看到,添加纳米级二氧化锰材料后,与CK相比,不同生长时期内,水稻植株各部位锰的含量显著增加(p<0.05).随着纳米级二氧化锰材料添加量增加,水稻植株各部位锰的含量也随着增加,即水稻根、茎和叶中锰的含量顺序是:2.0%>1.0%>0.5%>0.2%>CK.
3.5 纳米级二氧化锰材料对稻谷积累砷的影响水稻谷壳和糙米中砷含量如表 3所示.由表 3可知,纳米级二氧化锰材料使糙米和谷壳中总砷的含量显著降低(p<0.05),而锰的含量却显著增加(p<0.05).与CK相比,不同添加量条件下,谷壳中总砷的含量分别降低了36.4%、24.0%、12.6%和15.5%;糙米中总砷的含量分别降低17.8%、36.4%、65.4%和60.7%,表明纳米级二氧化锰材料能阻止土壤中砷进入水稻的糙米内,其中添加1.0%纳米级二氧化锰材料条件下,糙米中总砷的含量为最低(0.37 mg · kg-1).添加纳米级二氧化锰材料后,谷壳中锰的含量分别增加了55.8%、79.3%、102.0%和133.3%;糙米中锰的含量分别增加148.7%、174.6%、295.5%和310.4%,可见,糙米中锰的含量增加最多.
| 表 3 谷壳和糙米中砷含量 Table 3 Contents of As and Mn in husk and brown rice |
不同生长时期水稻中As和Mn之间的关系如图 4所示.由图 4可知,水稻植株中Mn含量与As含量之间的关系式是CAs=-1.55×lnCMn+24.29,呈显著负相关(p <0.05),随着Mn含量的增加,水稻植株As含量显著下降.
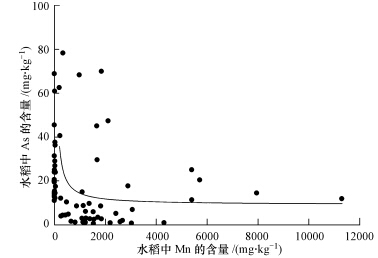 |
| 图 4 水稻中Mn与As含量之间的关系 Fig. 4 Correlations between Mn and As in rice plant |
供试土壤pH=8.15,呈碱性,总砷含量为(72.71±0.98)mg · kg-1,分别是土壤环境质量标准(GB15618—1995)和湖南土壤重金属平均背景值的 3.6和5.2倍,表明该土壤受到砷污染.土壤中锰的含量是(432.18±13.26)mg · kg-1,我国土壤中锰的含量范围是10~5532 mg · kg-1,平均值为710 mg · kg-1,一般土壤缺锰的临界值为 100 mg · kg-1(刘铮,1991).可见,供试土壤锰含量在我国土壤锰含量范围之内,不属于缺锰土壤.
无论是否添加纳米级二氧化锰材料,水稻中砷含量在空间分布顺序都是地下部分>地上部分,这和其他研究结果相一致(Abedin et al., 2002; Xu et al., 2008).与对照组相比,添加不同浓度的纳米级二氧化锰材料后,水稻各器官中砷的含量要显著低于对照组水稻各器官中砷的含量(p<0.05),这可能是纳米级二氧化锰材料能阻止砷进入水稻内,降低砷在水稻内的含量.研究表明,土壤中锰的生物有效性主要受 pH、Eh、有机质含量、锰矿物类型及其结晶程度的影响(Mckenie,1989; Ritchie,1989; Tu et al., 1994).本研究中对照组和添加纳米级二氧化锰材料后土壤溶液的pH值范围在水稻生育期内分别是6.28~6.76和7.36~7.55.同时,本研究中盆栽水稻一直处于淹水状态,从开始育秧算起第30 d开始淹水.由图 1可知,添加了纳米级二氧化锰材料的土壤溶液中锰的含量比对照组土壤溶液中锰的含量要高,这表明纳米级二氧化锰材料中锰在土壤中有溶解现象.刘学军等(1997)的研究表明,淹水状态影响氧化还原电位,使得土壤中MnO2、Mn3O4、MnOOH、MnCO3和MnSiO3等次生矿物中的锰会溶解进入土壤溶液,锰的有效性增多.在我国南方,大范围的酸性土壤和冷浸田中,锰在其中会明显的积累,易产生锰毒,影响当地的作物种植及生长(刘鑫等,2003).添加了纳米级二氧化锰材料的土壤溶液中锰总量随着时间的变化大致可以分为两个阶段:60 d之前,处理后的土壤溶液中总锰浓度都在增加,60 d之后,处理后的土壤溶液中总锰浓度迅速下降,直到105 d时,土壤溶液中锰含量接近0 mg · L-1,这可能是随着水稻的生长,溶液中Mn2+一方面被水稻所吸收利用,另外一方面是Mn2+逐渐转变成Mn8+和Mn4+的氧化物,有效性下降(刘铮,1991).在长期淹水、pH值6.28~7.55的条件下,土壤溶液三价砷和五价砷并存.从45 d开始,处理后的土壤溶液中砷浓度较对照组都有很明显的降低,且处理浓度越大,其降低效率越明显,这可能是纳米级二氧化锰材料与土壤中砷发生某些化学反应,阻止砷在土壤中迁移,且随着纳米级二氧化锰材料的浓度增加,这种抑制效应增强.对照组和0.2%处理的土壤溶液中砷浓度随着水稻生长而缓慢减少;而其它处理组,土壤溶液中砷的浓度随着水稻生长时间先上升后降低,在105 d,土壤溶液中砷的含量范围是13.26~20.49 μg · L-1,Sadiq(1986)分析了19种未污染的土壤,发现溶液中砷的含量为5~17 μg · L-1.由图 4可知,水稻植株中砷含量与锰含量呈显著负相关(p<0.05),随着锰含量的增加,水稻植株中砷含量显著下降,表明纳米二氧化锰材料能抑制水稻对土壤砷的吸收.添加纳米二氧化锰材料能促进水稻根部形成铁锰胶膜,阻控土壤中砷向水稻的迁移,且随着浓度的增加,这种阻控效应增强.在水稻植株的根部,铁锰氧化膜也能很好的阻控水稻吸收和转运砷(胡莹等,2013).
由表 2和表 3可知,与对照组相比,添加纳米二氧化锰材料后,水稻植株各部位(根、茎、叶、谷壳和糙米)中锰的浓度也随着增加,顺序是:根>茎>叶>谷壳>糙米.本研究中糙米中锰含量范围是20.78~85.28 mg · kg-1.Ritchie(1989)报道植物体内的正常含锰量为 20~100 mg · kg-1.锰是作物生长发育不可缺少的微量元素之一,可以增强光合作用、促进氮素代谢等(Tu et al., 1994).由表 3可知,糙米中总砷的含量范围是0.37~1.07 mg · kg-1,而《食品中污染物限量(GB2762—2012)》中砷限量指标是无机砷含量(0.2 mg · kg-1).Heikens(2006)的研究表明,大米中无机砷的含量占总砷的50%以上,据此推算,本研究中糙米中无机砷含量范围是0.19~0.54 mg · kg-1,其中添加1.0%纳米级二氧化锰材料,水稻中无机砷含量(0.19 mg · kg-1)在食品中砷限量之内.通过添加纳米级二氧化锰材料,能有效的阻控土壤砷向水稻迁移,为探讨纳米级二氧化锰材料降低土壤砷的危害风险提供了科学依据.
5 结论(Conclusions)1)纳米级二氧化锰材料不能影响砷在水稻各时期各器官内的空间分布,即水稻中砷的含量是根>茎>叶,纳米级二氧化锰材料可以减少水稻中砷的累积量.
2)纳米级二氧化锰材料对水稻生长的土壤pH没有显著影响,土壤溶液中锰的含量都是先上升后降低,砷浓度在处理量为0.5%、1.0%、2.0%的土壤溶液中有先上升后降低的趋势,水稻植株中锰和砷的关系呈显著负相关.
3)纳米级二氧化锰材料能够有效的降低糙米的砷含量,且添加量为1.0%时,糙米的砷含量低于食品中砷限量指标,表明纳米级二氧化锰材料能阻控砷在土壤-水稻中的迁移.
| [1] | Abedin M J. Cresset M S, Meharg A A, et al. 2002. Arsenic accumulation and metabolism in rice (Oryza sativa L.) [J]. Environmental Science and Technology, 36(5): 962-968 |
| [2] | Agusa T, Trang P T K, Lan V M, et al. 2013. Human exposure to arsenic from drinking water in Vietnam [J]. Science of the Total Environment, 488-489: 562-569 |
| [3] | Bundschuh J, Litter M I, Parvez F, et al. 2012. One century of arsenic exposure in Latin America: A review of history and occurrence from 14 countries [J]. Science of the Total Environment, 429: 2-35 |
| [4] | 蔡保松, 陈同斌, 廖晓勇, 等. 2004. 土壤砷污染对蔬菜砷含量及食用安全性的影响[J]. 生态学报, 24(4): 711-716 |
| [5] | 陈红, 叶兆杰, 方士, 等. 1998. 不同状态MnO2对废水中As(Ⅲ)的吸附研究[J]. 中国环境科学, 18(2): 126-130 |
| [6] | Chen S S, Hsu H D, Li C W. 2004. A new method to produce nanoscale iron for nitrate removal[J]. Journal of Nanopart Research, 6(6): 639-647 |
| [7] | 陈同斌, 刘更另, 谢开云, 等. 1992. 湖南省高砷地区土壤含砷量及其作物污染的临界值[J]. 土壤肥料, (2): 1-4 |
| [8] | Feroze A M, Ahmed T. 2014. 1.8-Status of Remediation of Arsenic Contamination of Groundwater in Bangladesh [J]. Reference Module in Earth Systems and Environment Sciences, from Comprehensive Water Quality and Pvfrification. 1: 104-121 |
| [9] | 高翔, 鲁安怀, 郑辙, 等. 2002. 锰的氧化物和氢氧化物在污染水体净化中的应用研究现状[J]. 矿物岩石, 22(1): 77-82 |
| [10] | Heikens A. 2006. Arsenic contamination of Irrigation Water, Soil and Crops in Bangladesh: Risk Implications for Sustainable Agriculture and Food Safety in Asia[M]. Bangkok: Food and Agriculture Organization of the United Nations, Regional Office for Asia and the Pacific. 12 |
| [11] | 胡莹, 黄益宗, 黄艳超, 等. 2013. 根表铁锰膜对不同生育期水稻吸收和转运As的影响[J]. 生态毒理学报, 8(2): 163-171 |
| [12] | Joo S H, Feitz A J, Waite T D. 2004. Oxidative degradation of the carbothioate herbicide, molinate, using nanoscale zero-valent iron [J]. Environmental Science and Technology, 38(7): 2242-2247 |
| [13] | 廖晓勇, 陈同斌, 肖细元, 等. 2003. 污染水稻田中土壤含砷量的空间变异特征[J]. 地理研究, 22(5): 635-643 |
| [14] | Liao X Y, Chen T B, Xie H, et al. 2005. Soil As contamination and its risk assessment in areas near the industrial districts of Chenzhou City, Southern China[J]. Environment International, 31(6): 791-798 |
| [15] | 刘学军, 吕世华, 张福锁, 等. 1997. 土壤中锰的化学行为及其生物有效性: 土壤中锰的化学行为及其影响因素[J]. 土壤农化通报, 12(3): 41-47 |
| [16] | 刘铮. 1991. 土壤与植物中锰的研究进展[J]. 土壤学进展, 19(6): 1-10; 22 |
| [17] | 刘鑫, 朱端卫, 雷宏军, 等. 2003. 酸性土壤活性猛与pH、Eh关系及其生物反应[J]. 植物营养与肥料学报, 9(3): 317-323 |
| [18] | 鲁安怀. 2001. 环境矿物材料基本性能——无机界矿物天然自净化功能[J]. 岩石矿物学杂志, 20(4): 371-381 |
| [19] | 鲁如坤. 1999. 土壤农业化学分析方法[M]. 北京: 中国农业科学出版社 |
| [20] | Mckenie R M. 1989. The manganese oxides and hydroxides//Dixon J B, Weed S B. Minerals in soil environments[M]. Madison, USA. 439-465 |
| [21] | 潘佑民, 杨国治. 1988. 湖南土壤背景值及研究方法[M]. 北京: 中国环境科学出版社. 338 |
| [22] | Rahman M M, Mondal D, Das B, et al. 2013. Status of groundwater arsenic contamination in all 17 blocks of Nadia district in the state of West Bengal, India: A 23-year study report [J]. Journal of Hydrology, 518(Part C): 363-372 |
| [23] | Ritchie G S P. 1989. The chemical behavior of aluminum, hydrogen and manganese in acid soils//Robson A D. Soil acidity and plant growth[M]. Auseralia: Academic Press. 35-59 |
| [24] | Sadiq M. 1986. Solubility relationships of arsenic in calcareous soils and its uptake by corn[J]. Plant and Soil, 91(2): 241-248 |
| [25] | Sigrist M, Albertengo A, Brusa L, et al. 2013. Distribution of inorganic arsenic species in groundwater from Central-West Part of Santa Fe Province, Argentina [J]. Applied Geochemistry, 39: 43-48 |
| [26] | Tu S, Racz G J, Goh T B. 1994. Transformations of synthetic birnessite as affected by pH and manganese concentration[J]. Clay and Clay Minerals, 42(3): 321-330 |
| [27] | van Geen A, Win K H, Zaw T, et al. 2014. Confirmation of elevated arsenic levels in groundwater of Myanmar [J]. Science of the Total Environment, 478: 21-24 |
| [28] | 王振刚, 何海燕, 严于伦, 等. 1999. 石门雄黄矿地区居民砷暴露研究[J]. 卫生研究, 28(1): 12-14 |
| [29] | 谢正苗, 朱祖祥, 袁可能, 等. 1989. 土壤中二氧化锰对As(Ⅲ)的氧化及其意义[J]. 环境化学, 8(2): 1-5 |
| [30] | Xu Y Y, McGrath S P, Mcharg A A, et al. 2008. Growing rice aerobically markedly decrease arsenic accumulation [J]. Environment Science and Technology, 42(15): 5574-5579 |
| [31] | Yang G C C, Lee H L. 2005. Chemical reduction of nitrate by nanosized iron: Kinetics and pathways [J]. Water Research, 39(5): 884-894 |
| [32] | Zhang Q, Rodriguez-Lado L, Liu J, et al. 2013. Coupling predicted model of arsenic in groundwater with endemic arsenism occurrence in Shanxi Province, Northern China [J]. Journal of Hazardous Materials, 262: 1147-1153 |
 2015, Vol. 35
2015, Vol. 35


