2. 北京理工大学化工与环境学院, 北京 100081
2. School of Chemical Engineering and Environment, Beijing Institute of Technology, Beijing 100081
废旧锌锰电池中约含12%~28%的锌和26%~45%的锰(Li et al., 2005;Sayilgan et al., 2009),它们大多随着生活垃圾填埋而进入环境,造成了潜在的环境危害并极大地浪费了锌锰资源.目前,对于锌锰电池资源化的研究更多关注的是酸释、碱释浸提锌锰参数的优化(Shin et al., 2009;Sayilgan et al., 2010;Belardi et al., 2012;Buzatu et al., 2013),或是制备软磁、纳米等材料(Nan et al., 2006; Xin et al., 2008; Gabal et al., 2013),而缺乏对电池内部材料的分类和成分表征研究.在湿法处理工艺中常采用的是电池整体的处理手段(Bernardes et al., 2004; Sayilgan et al., 2009).如果对废旧锌锰电池中锌锰的含量及组成状况有更精准的认识,就可以改进或是开发新的回收方法,从废旧电池的组件中更好地分离出锌和锰,使回收更具针对性,从而实现回收过程中设备的小型化,进而降低回收能耗,减少污染(Vassura et al., 2009).为此,本文以废旧锌锰电池为研究对象,采用化学分析、BCR连续萃取技术、SEM-EDS、XRD等手段对拆分的电极材料中的锌锰元素成分进行分析表征,为废旧锌锰电池资源化研究提供理论依据.
2 材料与方法(Materials and methods) 2.1 锌锰电池分类 2.1.1 碱性锌锰电池碱性锌锰电池(Alkaline Batteries,A-A)以二氧化锰为正极,锌为负极,氢氧化钾为电解液,电池外壳由惰性金属制成并与正极相连,电池的负极通过集电针与电池底部相连,电池的结构如图 1a所示(Belardi et al., 2011).
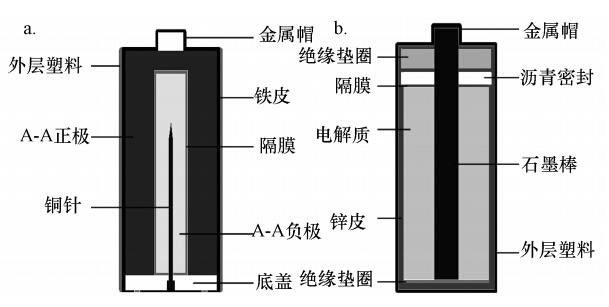 |
| 图 1 A-A电池(a)和Zn-C电池(b)结构示意图 Fig. 1 Schematic representation of an A-A battery(a) and a Zn-C battery(b) |
酸性锌锰电池(Zinc-Carbon Batteries,Zn-C)正极由粉末状的二氧化锰和碳构成,电池内部有一层由NH4Cl和ZnCl2所构成的糊状液体,糊状液体通过一个纸层与粉末状的碳和二氧化锰隔开,粉末填充在碳棒周围,最外层的锌是电池的负极.电池的结构如图 1b所示(Belardi et al., 2011).
2.2 废旧锌锰电池样品准备取市面上常见的10个5号废旧南孚电池(A-A),称量后将每个电池切割小口,于烘箱内烘干至恒重后称量.按图 2手工拆分出塑料、金属皮、垫圈、集电铜针、碳棒、牛皮纸及正、负极材料,称量各组件并取平均值.对收集的电池正、负极材料,分别碾磨过100目筛,混合均匀后作为待测样品.Zn-C电池(5号华太电池)样品准备方法同上.
 |
| 图 2 A-A电池和Zn-C电池实验室拆解图 Fig. 2 Separation of the spent A-A and the spent Zn-C batteries components in laboratory |
重金属对环境的危害程度与其形态密切相关(胡恭任等,2011;乔敏敏等,2013),因此,对电池中重金属的研究不仅要关注总量,也要关注其形态分布.本文利用BCR连续萃取技术分级处理电池样品(Rauret et al., 2009;郭鹏然等,2009),同时,对样品进行微波消解,利用原子吸收分光光度计测定消解液中锌锰离子含量.所有实验均为3个平行样.
2.4 SEM-EDS、XRD分析对废旧A-A电池和Zn-C电池样品进行SEM-EDS和XRD微观分析,考察电极材料中锌锰元素的物质结构、形貌特征及微区元素组分含量.
2.5 主要实验仪器用微波消解仪(MDS-2003F,上海)消解样品,原子吸收分光光度计(AAS,岛津AA6300C)测定锌锰离子浓度,样品形貌特征通过扫描电子显微镜(SEM,日立S-4800)观察,微区元素组分用X 射线能谱仪(EDS,日立S-4800)分析,结构分析通过X射线衍射(岛津XRD6000)完成.
3 结果与讨论(Results and discussion) 3.1 废旧电池主要成分的组成特征干燥恒重的A-A电池平均质量为23.5 g,正极和负极材料分别为13.5 g和3.6 g.在拆解过程中发现,A-A电池的负极和正极中间以牛皮纸隔膜分隔,组分特征明显,易于同其它组件分开.正极的质量百分比达到57.5%,负极为15.4%,两项占到了电池总质量的72.9%,其余组分含量如图 3a所示.
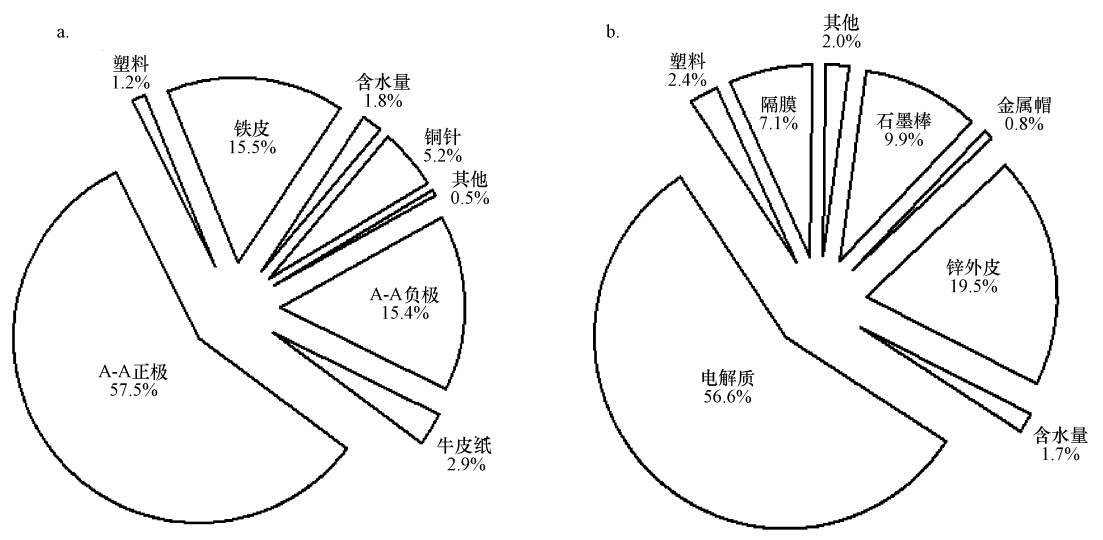 |
| 图 3 A-A电池(a)和Zn-C电池(b)各组分质量分布 Fig. 3 Product analysis of the A-A batteries(a) and the Zn-C batteries(b) |
与A-A电池不同,反应后的Zn-C电池中NH4Cl和ZnCl2所构成的糊状液体和正极电解质物质处于混合聚集状态,不易手工分开,这与电池结构有关.干燥恒重的Zn-C电池平均质量为11.1 g,负极锌皮质量为2.2 g,混合电解质质量为6.3 g,占到电池质量的56.6%,剩余可回收组分如金属、塑料皮等物质的含量如图 3b所示.分析可知,锌锰电池的电极材料质量比高,A-A电池负极和正极可以分离利用,而Zn-C电池则应针对混合电解质加以回收.
3.2 废旧电池锌锰的连续提取形态特征 3.2.1 废旧A-A电池由表 2可知,A-A电池负极样品中不含硫化物及有机结合态或残渣态锌锰,Zn的酸溶解态和氧化物结合态含量分别为(550.8±12.1)mg · g-1和(20.3±1.5)mg · g-1,分别占电极材料的55.1%和2.0%;而Mn的酸溶解态和氧化物结合态两项均未检出,对于A-A电池负极材料来说,锌的酸溶出是较易实现的.正极样品中4种状态的锌含量分别为15.2、9.6、8.1和35.5 mg · g-1,含量分布变化不大;4种状态的锰含量分别为8.6、32.5、21.6和169.1 mg · g-1,主要以残渣态存在,占到了样品质量的16.9%和总锰的73.0%,可见锰的溶出是较为困难的.也有研究人员(Baba et al., 2009; Sayilgan et al., 2009;2010)尝试在强酸中加入还原性物质(如H2O2和SO2)或有机物(如葡萄糖、蔗糖、乳酸、柠檬酸等),实施还原酸浸来获得锰的高效溶出,但这也增加了溶释成本.
| 表2 废旧电池样品BCR、消解处理后锌锰溶出量a Table 2 Extraction calculations of Zn/Mn in spent batteries by using BCR and microwave digestion method |
Zn-C电池样品中的酸溶锌含量最大,其次为残渣态锌;锰大多数以残渣态存在,也占到了样品质量的15.1%和总锰的72.3%,表明锰的溶出同样是困难的,而且同A-A电池正极样品一样,也存在较难溶出的残渣锌物质.
从消解数据可知,锌锰电池锌锰含量高且集中,便于回收利用,此外,A-A电池负极锌消解值与BCR总和值一致;而A-A电池正极和Zn-C电池电解质中的锌锰BCR总和值均小于消解值,原因是存在BCR不能萃取完全的物质.由此可见,A-A电池负极中的锌易于进入环境中;而A-A电池和Zn-C电池正极中的锌锰主要以残渣态存在,潜在的环境生态危害不大,但相对资源化利用也是较为困难的.
3.3 废旧电池的形貌特征 3.3.1 废旧A-A电池A-A电池负极样品形貌为针状或棒状的团聚物(图 4a),而正极样品形貌为块状的聚集体(图 4b).由A-A电池负极样品的谱图可知(图 5a),负极材料中除含有Zn、O元素外,还含有来自电 解液氢氧化钾的K元素.由EDS分析可知(表 3),分析微区中Zn质量百分比为56.7%,与BCR和微波消解值近似;图谱分析也未检出Mn.由正极微区谱图(图 5b)和表 3可知,正极的C、O、Mn元素含量分别为14.5%、47.6%和26.6%,也近似于消解值.此外,电池经过放电反应后,Mn发生了价态变化但依旧在正极中,而负极的一部分Zn、K元素以离子态进入正极中(Almeida et al., 2006),其中,Zn为8.4%,近似于消解值,可见SEM-EDS分析与消解结果较为吻合.
| 表3 A-A电池负极、正极和Zn-C电解质样品EDS元素质量分析 Table 3 Analysis of the anode materials,cathode materials of A-A batteries and electrolyte of Zn-C batteries |
 |
| 图 4 A-A电池负极样品(a)、正极样品(b)和Zn-C电解质(c)扫描电镜图 Fig. 4 SEM images of the anode materials(a),cathode materials(b)of A-A batteries and electrolyte of Zn-C batteries(c) |
 |
| 图 5 A-A电池负极(a)、正极(b)和Zn-C电解质(c)样品的扫描电镜-能谱图 Fig. 5 SEM-EDS images of the anode materials(a),cathode materials(b)of A-A batteries and electrolyte of Zn-C batteries(c) |
Zn-C电解质材料成不规则块状,表面光滑成型(图 4 c).由EDS分析可知,电解质含有9.9%的Cl元素,其主要来自于NH4Cl+ZnCl2与负极Zn反应后的残余物.此外,Mn元素含量达到27.7%,Zn元素为17.8%,与消解分析结果Mn的含量(27.9%)和Zn的含量(17.1%)十分吻合.
3.4 废旧电池主要成分的化学组成特征 3.4.1 废旧A-A电池A-A电池负极中的Zn以ZnO晶体存在(图 6a),也是负极Zn放电反应后的产物,这与Belardi等(2011)研究结果一致;正极的Mn和Zn主要以ZnMn2O4晶体存在(图 6b),Belardi等(2011)也报道了在A-A电池中发现ZnMn2O4物质的存在,属于四方体锌锰矿结构.此外,还存在一些不同的研究结论:Freitas等(2007)认为是Mn3O4,Shin等(2009)分析认为是立方体铁锰矿Mn2O3,Xin(2012)则发现是Mn3O4 、Mn2O3混合物.原因可能是锌锰电池在放电时反应复杂,放电过程中反应物质相互碰撞而形成了不同的中间产物或是最终产物(Almeida et al., 2006).
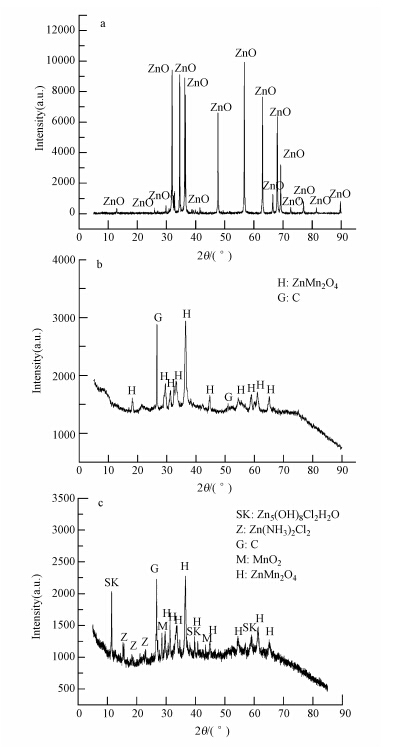 |
| 图 6 A-A电池负极样品(a)、正极样品(b)和Zn-C电解质(c)XRD图 Fig. 6 XRD images of the anode materials(a),cathode materials(b)of A-A batteries and electrolyte of Zn-C batteries(c) |
Zn-C电池电解质中的Mn元素主要以ZnMn2O4和MnO2晶体存在(图 6c);Zn元素除了以ZnMn2O4晶体存在外,还以Zn5(OH)8Cl2·H2O、 Zn(NH3)2Cl2物质存在.MnO2是未参与反应的电极原料粉末残留物,Zn(NH3)2Cl2是电池反应的产物,Zn5(OH)8Cl2 · H2O则有可能是氯化锌作为电池电解液时电池反应过程中的中间产物,这与Belardi等(2012)和Xin(2012)等的研究相一致.对比A-A电池和Zn-C电池可知,电池正极中的Mn元素主要是以ZnMn2O4晶体存在,而Zn-C电池中Zn元素的存在物质则相对复杂.
从锌锰电池电极材料的化学组成来看,A-A电池负极材料适合直接回收利用,而A-A电池正极和Zn-C电池电解质可以混合处理回收锌锰元素.
4 结论(Conclusion)1)废旧A-A电池负极和正极的组分特征明显,易于拆分分离,正、负极质量占到了电池总质量的72.9%,其中,正极占57.5%,负极占15.4%;Zn-C电池负极锌皮可直接拆卸,其质量占电池总质量的19.5%,而Zn-C电池正极电解质物质呈混合聚集状态,不易分离,混合电解质占到电池总质量的56.6%.
2)废旧A-A电池Mn含量占正极材料的49.2%,集中在残渣态中;Zn占负极材料的52.5%,为酸溶解态和氧化物结合态.废旧Zn-C电池电解质中,Zn、Mn分别占25.2%和41.8%,Zn以酸溶锌含量最大,Mn则集中在残渣态中.
3)SEM-EDS分析结果与化学分析结果较为吻合.XRD分析发现,A-A电池负极Zn元素以ZnO晶体存在,正极Mn、Zn元素以ZnMn2O4四方体锌锰矿结构晶体存在;Zn-C电池电解质Mn元素以ZnMn2O4和MnO2晶体存在,Zn元素以ZnMn2O4、Zn5(OH)8Cl2·H2O和Zn(NH3)2Cl2等晶体存在.
4)废旧A-A电池中的锌以ZnO存在于负极中,当采用酸溶浸提工艺时,应考虑分离回收,以降低酸用量;而 A-A电池正极和Zn-C电池电解质适宜混合处理,但Zn、Mn元素集中在残渣态中且以结构稳定的ZnMn2O4存在,需更为高效的溶释技术.
| [1] | Almeida M F, Xará S M, Delgado J, et al. 2006. Characterization of spent AA household alkaline batteries[J]. Waste Management, 26(5): 466-476 |
| [2] | Baba A A, Adekola A F, Bale R. 2009. Development of a combined pyro- and hydro-metallurgical route to treat spent zinc-carbon batteries[J]. Journal of Hazardous Materials, 171(1/3): 838-844 |
| [3] | Belardi G, Ballirano P, Ferrini M, et al. 2011. Characterization of spent zinc-carbon and alkaline batteries by SEM-EDS, TGA/DTA and XRPD analysis[J]. Thermochimica Acta, 526(1/2): 169-177 |
| [4] | Belardi G, Lavecchia R, Medici F, et al. 2012. Thermal treatment for recovery of manganese and zinc from zinc-carbon and alkaline spent batteries[J]. Waste Management, 32(10): 1945-1951 |
| [5] | Bernardes A M, Espinosa D C R, Tenório J A S. 2004. Recycling of batteries: a review of current processes and technologies[J]. Journal of Power Sources, 130(1/2): 291-298 |
| [6] | Buzatu T, Popescu G, Birloaga I, et al. 2013. Study concerning the recovery of zinc and manganese from spent batteries by hydrometallurgical processes[J]. Waste Management, 33(3): 699-705 |
| [7] | Freitas M B J G, Pegoretti V C, Pietre M K. 2007. Recycling manganese from spent Zn-MnO2 primary batteries[J]. Journal of Power Sources, 164(2): 947-952 |
| [8] | Gabal M A, Al-luhaibi R S, Al Angari Y M. 2013. Mn-Zn nano-crystalline ferrites synthesized from spent Zn-C batteries using novel gelatin method[J]. Journal of Hazardous Materials, 246-247: 227-233 |
| [9] | 郭鹏然, 牟德海, 王畅, 等. 2009. 连续萃取法研究海湾养殖区沉积物中重金属形态[J]. 分析化学, 37(11): 1645-1650 |
| [10] | 胡恭任, 戚红璐, 于瑞莲, 等. 2011. 大气降尘中重金属形态分析及生态风险评价[J]. 有色金属, 63(2): 286-291 |
| [11] | Li Y Q, Xi G X. 2005. The dissolution mechanism of cathodic active materials of spent Zn-Mn batteries in HCl[J]. Journal of Hazardous Materials, 127(1/3): 244-248 |
| [12] | Nan J M, Han D M, Cui M, et al. 2006. Recycling spent zinc manganese dioxide batteries through synthesizing Zn-Mn ferrite magnetic materials[J]. Journal of Hazardous Materials, 133(1/3): 257-261 |
| [13] | 乔敏敏, 季宏兵, 朱先芳, 等. 2013. 密云水库入库河流沉积物中重金属形态分析及风险评价[J]. 环境科学学报, 33(12): 3324-3333 |
| [14] | Rauret G, López-Sánchez J F, Sahuquillo A, et al. 1999. Improvement of the BCR three step sequential extraction procedure prior to the certification of new sediment and soil reference materials[J]. Journal of Environmental Monitoring, (1): 57-61 |
| [15] | Sayilgan E, Kukrer T, Civelekoglu G, et al. 2009. A review of technologies for the recovery of metals from spent alkaline and zinc-carbon batteries[J]. Hydrometallurgy, 97(3/4): 158-166 |
| [16] | Sayilgan E, Kukrer T, Yigit N O, et al. 2010. Acidic leaching and precipitation of zinc and manganese from spent battery powders using various reductants[J]. Journal of Hazardous Materials, 173(1/3): 137-143 |
| [17] | Shin S M, Senanayake G, Sohn J S, et al. 2009. Separation of zinc from spent zinc-carbon batteries by selective leaching with sodium hydroxide[J]. Hydrometallurgy, 96(4): 349-353 |
| [18] | Vassura I, Morselli L, Bernardi E, et al. 2009. Chemical characterisation of spent rechargeable batteries[J]. Waste Management, 29(8): 2332-2335 |
| [19] | Xin B P, Huang Q, Chen S. 2008. High-purity Nano Particles ZnS Production by a Simple Coupling Reaction Process of Biological Reduction and Chemical Precipitation Mediated with EDTA[J]. Biotechnology Progress, 24(5): 1171-1177 |
| [20] | Xin B P, Jiang W F, Li X, et al. 2012. Analysis of reasons for decline of bioleaching efficiency of spent Zn-Mn batteries at high pulp densities and exploration measure for improving performance[J]. Bioresource Technology, 112: 186-192 |
 2015, Vol. 35
2015, Vol. 35


