2. 上海海洋大学, 上海 203360
2. Shanghai Ocean University, Shanghai 203360
随着经济的高速发展,环境污染物的排海总量也在不断增加,导致近海海域水质恶化.尤其是海上石油开采、油轮溢油等引起的突发性石油污染事件频发,以及船舶运输、码头作业等导致大量石油污染物进入海洋,严重威胁海洋及陆域生态环境,使得我国海洋石油污染风险不断增加(黄逸君等,2010).
酶是机体生物化学反应的重要物质,酶活性被认为是一种能够快速而灵敏地反映环境胁迫对生物体影响的生化指标(Scott-Fordsmand et al., 2000).抗氧化防御系统是生物体应对外源化合物氧化胁迫的重要组成成分,对抗氧化防御机制的研究能够有效预测环境中污染物的生物效应及毒理学特征.抗氧化防御系统由多种酶组成,主要包括各类抗氧化酶——超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷光甘肽硫转移酶(GST)及过氧化物酶(POD)等(李飞等,2005).在污染物毒性研究中,抗氧化酶的灵敏性特征能够有效解决常规生态毒理学方法无法监测的低浓度污染问题,为污染物环境风险提供早期预警(万斌,2000;李传慧等,2011;夏斌等,2011).由于酶活力在污染条件下既有抑制又有诱导,且各类酶活性对生物毒性的暴露响应不同步,不同的酶对污染的敏感程度有所差异,因此,将几种酶甚至其它生物标志物结合起来分析,才能更有效地评估污染情况.综合生物标志物响应(Integrated Biomarker Responses,IBR)指标可将不同生物指标的联合生物效应量化表示,已广泛应用于鱼类毒性测定的综合研究(Pytharopoulou et al., 2008).通过量化的IBR数值可直观分析化合物毒性大小的差异,将抗氧化效应的影响量化表达,进一步准确有效地预测化学物质毒性差异.Beliaeff和Burgeot(2002)利用贻贝消化腺中 CAT、GST和鳃中AChE、GST共4种生物标志物的测定值计算IBR值,研究得出塞纳河口的PAH和PCB浓度与生物毒性测试的综合生物标志物IBR之间存在一定的相关关系.
基于此,本研究以缢蛏为目标生物,在实验生态条件下研究0#柴油和平湖原油胁迫对缢蛏消化腺抗氧化酶活性的影响,运用综合生物标志物响应(IBR)指数评价0#柴油和平湖原油对缢蛏胁迫的毒性效应,以期为利用分子生物标志物指示环境油污染提供基础的实验依据.
2 材料与方法(Materials and methods) 2.1 材料实验用缢蛏取自启东市黄海滩涂公司缢蛏养殖区,实验前暂养1周,贝体平均壳长(5.90±0.31)cm,壳宽为(1.99±0.11)cm,体重(14.60±2.62)g.实验用水为经过滤的天然海水,盐度为23~25,pH为7.80~7.90.
将0#柴油、平湖油气田产原油分别与过滤海水按1 ∶ 10(V ∶ V)配比,置于超声振荡器中连续振荡3 h,再静置3 h后,吸取表层下水相即为乳化液母液,母液置于4 ℃冰箱保存,实验前稀释(贾晓平等,2000).海水中0#柴油和平湖原油浓度的测定采用紫外分光光度法(国家质量监督检验检疫总局,2008).
2.2 实验方法随机选取缢蛏分为4组,分别为对照组(天然海水)、低浓度组、中浓度组和高浓度组(0#柴油和平湖原油乳化液),0#柴油和平湖原油的乳化液实验浓度梯度分别为4、0.8、0.16 mg · L-1和5、1、0.2 mg · L-1.每组约40只缢蛏,置于含14 L沙滤海水的玻璃箱(容积30 L)中,24 h连续充氧,实验期间水温为23.60~25.40 ℃.每日100%换水1次,更换相同浓度的实验液,及时清除排泄物和活力不好的贝体,贝类饵料为单独培养扁藻,每天定时定量喂食2次,扁藻密度为2×104 cells · mL-1.胁迫实验进行15 d,15 d后将实验液全部换成清洁沙滤海水进行为期6 d的恢复实验.分别于实验开始后的第0、3、7、15和21 d采集贝类消化腺样品,采样时仔细分离出消化腺,双蒸水冲洗后用铝箔折成的小袋装取,液氮保存待测定.
2.3 组织蛋白含量及酶活性的测定消化腺中蛋白含量的测定采用考马斯亮蓝法;消化腺组织中CAT、SOD、POD和GST活性的测定均采用南京建成生物公司提供的检测试剂盒,相应操作参照说明书进行.在实验条件下每分钟每毫克蛋白使酶增加0.001为1个酶活力单位(U · mg-1,以prot计).
2.4 数据处理实验结果进行统计处理,酶活性数据均为平均值±标准差(Means±SD)(n=3).数据用SPSS 13.0统计软件进行方差分析(ANOVA),并用均值多重比较分析法(LSD法)检验组内及组间的差异显著性,p<0.05为差异显著,p<0.01为差异极显著.
IBR数值处理具体过程参照文献(Beliaeff et al., 2002)中所描述的方法,首先将原始数据标准化,之后将可用来衡量生物指标综合影响的可视化的生物标志结果呈现在星状图中计算出来,最后,依照Oliveira等(2010)介绍的方法,得到IBR值.IBR值越大,表明生物所受影响越大.
3 结果(Results) 3.1 0#柴油和平湖原油对缢蛏消化腺SOD、CAT、POD和GST的剂量效应关系0#柴油对缢蛏消化腺SOD、GST、CAT和POD活性(均以proteinit)影响的试验结果如图 1所示.由图可知,第3 d各浓度组消化腺SOD活性都有所上升,只有高浓度组(4 mg · L-1)和中浓度组(0.8 mg · L-1)与对照组有显著差异(p<0.05);第7 d 除低浓度组外,高浓度和中浓度组(SOD)活性均下降,至第15 d高浓度组SOD活性下降幅度较中低浓度组(0.8、0.16 mg · L-1)大,与对照组差异性显著(p<0.05),而中、低浓度组间没有显著差异.胁迫解除后,第21 d各浓度组SOD活性均下降,且SOD活性都有不同程度的恢复,虽然仍高于对照组,但已无显著差异.曝油第3 d时,各浓度组GST 活性较对照组有所增加,高、中浓度组与对照组差异性显著(p<0.05).曝油第7 d时,各浓度组GST活性达到峰值,而CAT活性开始小幅下降,高浓度组GST和CAT活性与对照组仍有显著性差异(p<0.05);曝油15 d时,各浓度组GST和CAT活性继续下降,组间差异不显著.胁迫解除后,第21 d各浓度组GST和CAT活性均下降,GST和CAT活性都有不同程度的恢复,除高浓度组略高于对照组外,中低浓度组GST和CAT活性基本与对照组趋于一致,各组间已无显著差异.0#柴油胁迫后第3 d缢蛏消化腺POD 活性均出现不同程度下降,与对照组显著差异(p<0.05).第 7 d活性又开始小幅升高,除高浓度组POD活性显著低于对照组外(p<0.05),中低浓度组POD活性与对照组均无显著差异.第15 d各浓度组POD活性均达到一个高峰值,与对照组无显著差异(p>0.05),到恢复实验(第21 d),各浓度组POD活性均有所恢复,与对照组无显著差异(p>0.05).
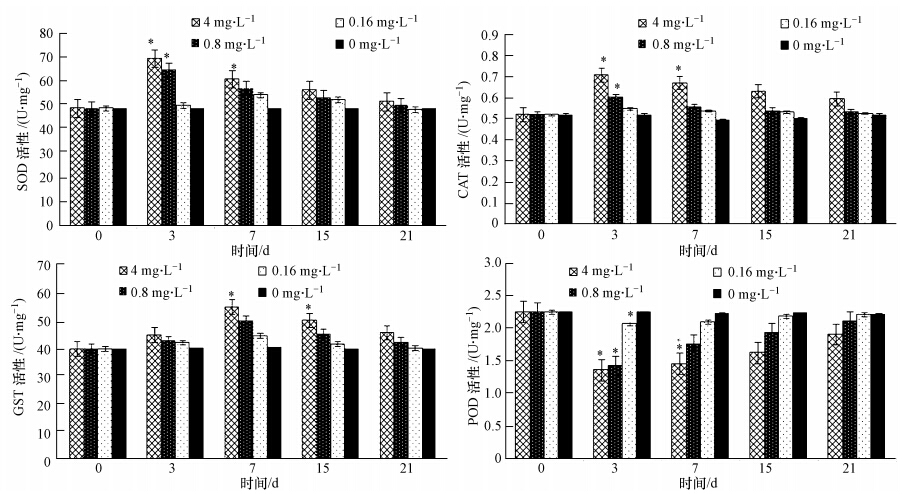 |
| 图 1 柴油对缢蛏消化腺SOD、GST、CAT和POD活性的影响(*表示与对照组相比差异性显著(p<0.05),n=60) Fig. 1 Effects of No.0 fuel oil on digestive gl and s SOD,GST,CAT and POD activity of Sinonovacula constricta |
平湖原油对缢蛏消化腺SOD、GST、CAT和POD活性影响的试验结果如图 2所示.由图 2可知,第3 d各浓度组消化腺SOD活性均有升高,且活性均达到峰值,各浓度组间差异不显著,除低浓度组外,高中浓度组均与对照组有显著差异(p<0.05);第7 d各浓度组SOD活性呈阶梯状下降,至第15 d各浓度组SOD活性与对照组无显著差异(p>0.05).胁迫解除后,第21 d各浓度组SOD活性继续下降,但都有不同程度的恢复,尤其是低浓度组SOD活性基本恢复到对照组水平.曝油第3 d时,各浓度组GST和CAT活性均有所上升,高、中浓度组GST活性与对照组差异不显著(p>0.05),而CAT则表现与对照组差异性显著(p<0.05).曝油第7 d时,各浓度组GST和CAT活性开始下降,CAT活性下降幅度略高于GST活性下降幅度,但各浓度组CAT活性与对照组无显著差异(p>0.05).曝油15 d时,各浓度组GST和CAT活性继续下降,组间差异不显著.曝油解除后,第21 d各浓度组GST活性基本恢复到与对照组同一水平,CAT活性虽然仍略高于对照组,但差异不显著(p>0.05).胁迫后第3 d缢蛏消化腺POD 活性出现下降,各浓度组与对照组显著差异(p<0.05).第 7 d POD活性又开始小幅上升,组间差异不显著,与对照组均无显著差异(p>0.05).第15 d各浓度组POD活性达持续增加,与对照组仍无显著差异(p>0.05),到恢复实验(第21 d),各浓度组POD活性差异消除,均与对照组趋于一致(p>0.05).
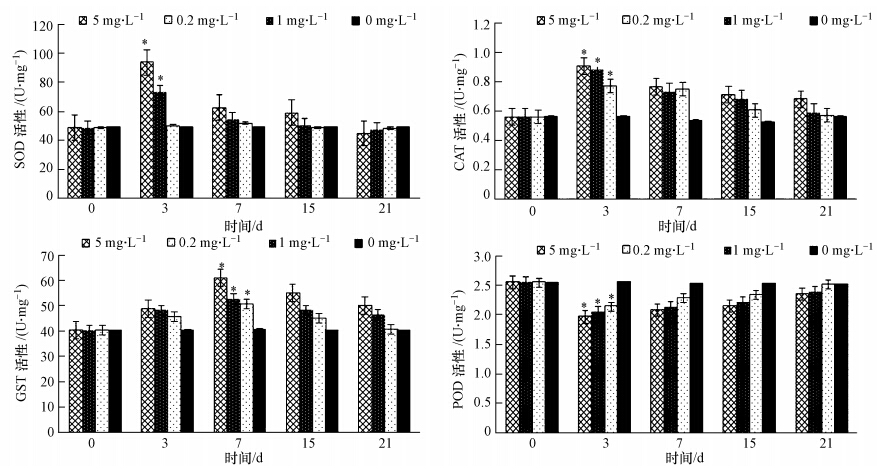 |
| 图 2 平湖原油对缢蛏消化腺SOD、GST、CAT和POD活性的影响(*表示与对照组相比差异性显著(p<0.05),n=60) Fig. 2 Effects of Pinghu crude oil on digestive gl and s SOD,GST,CAT and POD activity of Sinonovacula constricta |
0#柴油和平湖原油暴露下缢蛏消化腺SOD活性的诱导及抑制情况见表 1.从表 1可以看出,0#柴油和平湖原油与SOD的剂量-效应关系非常显著.高中浓度组的最大诱导先于低浓度组出现,而且诱导量大于低浓度组.而从抑制情况来看,同样是高中浓度组均出现在低浓度组之前,且抑制率均高于低浓度组,平湖原油低浓度组甚至没有出现抑制.从2种油对SOD酶活性的影响来看,0#柴油低浓度组浓度绝对数值(0.16 mg · L-1)虽然低于平湖原油低浓度组浓度数值(0.2 mg · L-1),但其诱导量均高于平湖原油中低浓度组,且低浓度组最大诱导出现时间要早于平湖原油.在抑制阶段,0#柴油低浓度组较平湖原油低浓度组有更大的抑制率.
| 表 1 不同浓度0#柴油和平湖原油对缢蛏消化腺SOD酶活性影响比较 Table 1 Dose- and time-dependent formation of different concentrations of No.0 fuel oil and Pinghu crude oil on digestive gl and s SOD activity of Sinonovacula constricta |
0#柴油和平湖原油暴露下缢蛏消化腺GST活性的诱导及抑制情况见表 2.不论是低浓度组还是高浓度组,均使GST产生了诱导,最大诱导时间均出现在实验第7 d,且高浓度的诱导量大于低浓度组.随着曝油时间的延长,不同浓度组基本上均出现抑制,但高浓度组抑制率大于低浓度组,剂量-效应关系显著.2种石油对GST酶活性诱导阶段,最大诱导量高浓度组明显高于低浓度组,在抑制阶段,0#柴油各浓度组抑制率与平湖原油基本持平.
| 表 2 不同浓度0#柴油和平湖原油对缢蛏消化腺GST酶活性影响比较 Table 2 Dose- and time-dependent formation of different concentrations of No.0 fuel oil and Pinghu crude oil on digestive gl and s GST activity of Sinonovacula constricta |
0#柴油和平湖原油暴露下缢蛏消化腺CAT活性的诱导及抑制情况见表 3.CAT酶活性的变化规律比较好,验第3 d 2种油各浓度组均对CAT活性产生诱导,浓度越高,诱导量越大.实验第7 d均表现为抑制,且浓度越高,抑制率越高,表现出明显的剂量-效应关系.从2种油对CAT酶活性的影响来看,2种油最大诱导出现时间和抑制出现时间均相同.
| 表 3 不同浓度0#柴油和平湖原油对缢蛏消化腺CAT酶活性影响比较 Table 3 Dose- and time-dependent formation of different concentrations of No.0 fuel oil and Pinghu crude oil on digestive gl and s CAT activity of Sinonovacula constricta |
0#柴油和平湖原油暴露下缢蛏消化腺POD活性的诱导及抑制情况见表 4.由表可见,2种油各浓度组实验第3 d先出现抑制,且抑制率随实验浓度的增加而增加.而到实验末期(15 d)才出现诱导,且诱导率随浓度的增加而增加,剂量-效应关系较显著.比较2种油对POD活性的影响,在抑制阶段,0#柴油中浓度组(0.8 mg · L-1)浓度数值虽然低于平湖原油中浓度组(1 mg · L-1)浓度数值,但其抑制率要高于平湖原油;在诱导阶段,0#柴油中、低浓度组(0.8、0.16 mg · L-1)浓度数值虽然低于平湖原油中、低浓度组(1、0.2 mg · L-1)浓度数值,但其诱导量要高于平湖原油3倍多.
| 表 4 不同浓度0#柴油和平湖原油对缢蛏消化腺POD酶活性影响比较 Table 4 Dose- and time-dependent formation of different concentrations of No.0 fuel oil and Pinghu crude oil on digestive gl and s POD activity of Sinonovacula constricta |
通过IBR方法计算本实验中不同暴露时间、不同石油浓度暴露下综合生物标志物水平,结果见图 3.在IBR星状图中4种生物标志物(SOD、CAT、GST和POD)分别代表图中的4个方向轴,计算出的IBR值和在图形的半径值均显示于坐标图中.由图 3中IBR的数值来看,各种生物标志物表现出巨大的差异.在各个取样时间点,2种石油污染物不同处理浓度组对4种生物标志物的影响也呈现出各自的特征;而随着暴露时间点的变化,2种石油污染物产生的影响也发生着变化.需要特别指出的是,高中浓度处理组对所有生物标志物均产生较大的影响,这可以通过星状图中较大的区域面积得到证实.
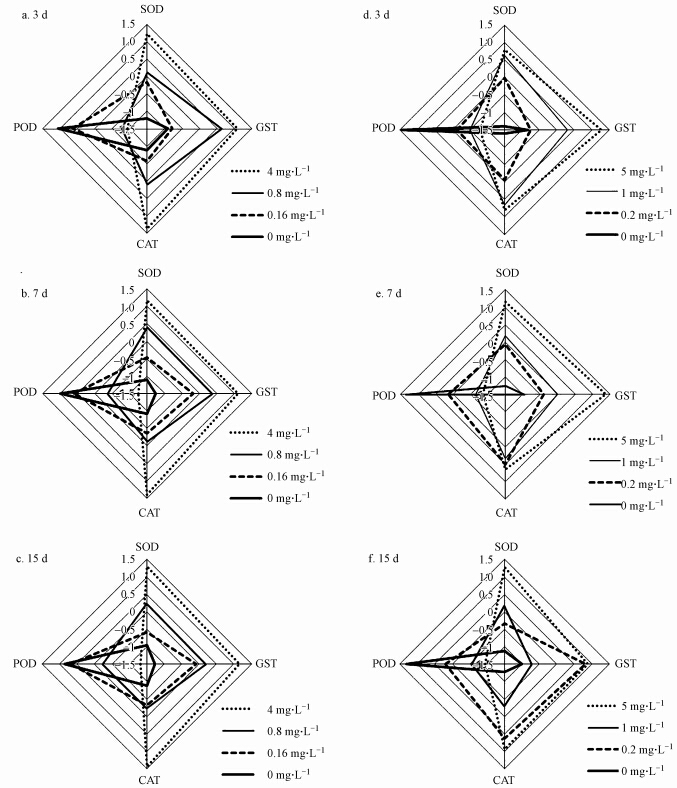 |
| 图 3 0#柴油(a,b,c)和平湖原油(d,e,f)对缢蛏体内综合生物标志物响应 Fig. 3 IBR of Sinonovacula constricta in No.0 fuel oil(a,b,c) and Pinghu crude oil(d,e,f)pollution stress |
图 4为IBR值与时间效应关系图,从IBR值随时间变化趋势来看,0#柴油胁迫下,实验前期各浓度组IBR值与曝油时间基本呈正相关关系(r=0.86),随暴露时间延长而增大,而实验中后期IBR值与曝油时间基本无相关关系.从IBR值与曝油浓度的关系来看,不同浓度与IBR值没有明显变化规律.在平湖原油胁迫下,实验前期IBR值与曝油时间呈正相关关系(r=0.71),随暴露时间延长而增大,实验终期IBR值均有所下降.IBR值与平湖原油浓度基本成正相关关系(r=0.79).根据图 4显示的2种石油IBR值所体现出的数据变化,可推测出一定浓度的油处理诱发缢蛏消化腺产生氧化应激的能力水平大小顺序:4 mg · L-10#柴油>5 mg · L-1平湖原油>0.8 mg · L-10#柴油>1.0 mg · L-1平湖原油>0.16mg · L-1 0#柴油>0.2 mg · L-1平湖原油.
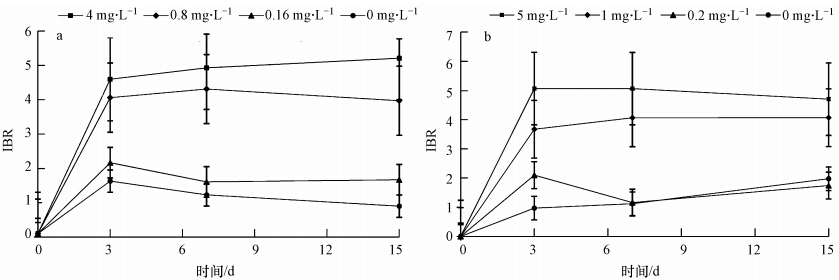 |
| 图 4 0号柴油(a)和平湖原油(b)对缢蛏体内综合生物标志物随时间、剂量的变化(n=48) Fig. 4 IBR variation with time and dose of Sinonovacula constricta exposed to No.0 fuel oil(a) and Pinghu crude oil(b) |
外源物质通过影响或阻断呼吸链、电子传递链、酶促反应等体内正常生理代谢,导致活性氧自由基增加使机体处于氧化应激态,从而诱导抗氧化酶类活性增加,各类酶通过联合作用组成机体的抗氧化酶防御系统,对累积的活性氧进行清除(Richardson et al., 2008;Jena et al., 2009).在本实验过程中,抗氧化酶在不同石油浓度处理组中的响应呈现多样性的变化趋势(图 1和图 2).对于2种石油处理组的酶活性变化来说,SOD酶多呈持续酶诱导状态,只有在胁迫末期(15 d)酶活性出现一定降低,尤其是高中浓度组SOD酶活力影响相对较大(p<0.05).造成这种结果的原因可能是由于高浓度油渗透进入细胞内,为快速清除自由基来减轻脂质过氧化对缢蛏机体造成的损伤,从而诱导SOD活性产生快速响应(高静等,2011).与SOD酶的变化趋势不同,CAT活性在实验初期3 d出现诱导,剩余实验过程中并没有呈现明显的诱导,相反却受到抑制呈一定程度的下降趋势.CAT是一种末端血红素氧化酶,其功能是催化H2O2分解为H2O和O2,它可防止H2O2含量过高对机体组织造成的损伤,对细胞起保护作用(刘冰等,2005).一般而言,SOD酶活性诱导和CAT酶活性抑制通常相伴出现(李莹,2013),当SOD酶活性上升提高缢蛏机体清除氧自由基的能力,从而导致H2O2的积累,将一定程度上抑制CAT功能的发挥.GST是谷胱甘肽结合反应的关键酶,能够催化谷胱甘肽结合反应的起始步骤,作为抗氧化防御系统第二阶段的解毒酶,参与到自由基的清除过程中(丁秀蓉等,2007).与SOD的抗氧化作用相似,GST也参与到H2O2的分解过程,防止机体出现H2O2的累积.GST与CAT酶活性变化趋势相类似,但不如CAT酶变化明显(p>0.05).本实验发现,在0#柴油和平湖原油的胁迫下,高中浓度处理组缢蛏消化腺SOD和CAT于实验开始3 d受到显著诱导(p<0.05),时间上明显早于GST(7 d).这也印证了SOD和CAT是最先参与活性氧自由基清除作用的酶,是抗氧化防御系统的第一道防线(王晓蓉等,2006).POD对细胞生理代谢过程中产生的活性氧具有清除作用,防止活性氧自由基启动膜脂过氧化或膜脂脱酯作用,减少自由基对正常细胞的损伤,从而提高机体的解毒免疫能力(许燕等,2010).实验中观察到POD的活性变化与SOD活性成反比关系,这可能与抗氧化防御系统中醇参与抵御氧化损伤的序列有关(王丽平等,2007).缢蛏在2种石油污染物引起的氧化压力强度和氧化胁迫持续时间内,自身的抗氧化酶共同发挥作用,以维持活性氧的产生和抗氧化防御系统之间的平衡.
依据IBR的星状图(图 3)显示的各个取样时间点,高浓度和中浓度处理组对抗氧化酶产生强烈的酶诱导或者酶抑制,在不同时间的影响或表现为含量上升或呈现出含量下降.而低浓度处理组对综合生物指标产生了相对较小的作用,显示2种石油类污染物不同浓度胁迫的毒性之间存在差异,表明一定浓度范围内缢蛏机体对外界刺激产生防御应激的敏感性.实验前期IBR值呈现上升趋势,可能是由于前期各种酶活性均对2种石油污染胁迫有所响应,后期大部分酶活性已经逐渐恢复或接近对照水平(图 1和图 2),IBR值出现一定的降低.
我们从各取样时间点形状多样、覆盖区域不同的星状图(图 3)得到不同石油污染处理组对各生物标志物影响的细节信息,显示2种石油污染物存在毒性差异,能够引起对生物体产生氧化胁迫.0#柴油最高浓度处理组(4 mg · L-1)和平湖原油最高浓度处理组(5 mg · L-1)在各个时间点均有较大的星状图覆盖面积,这与其高毒性对生物体产生的氧化胁迫是相关的.根据本实验IBR值计算结果(图 4),0#柴油最高浓度处理组(4 mg · L-1)发生最高数值范围的变化(3.38~2.60).由此可以得出,0#柴油最高浓度处理组能够引起最为显著的生物效应变化,显示该石油污染物高毒性的特征.0#柴油处理组各生物标志物在实验过程中呈现出较大范围的变化,IBR值发生最大范围的数据变化(0.36~3.39),而平湖原油处理组IBR值仅从0.04变化至2.04,表明生物体机体防御能力过程在不同的时间段产生了多样性的代谢中间物质,这也在一定程度上说明开展生物体毒性研究,需要对污染物在生物体内产生的代谢过程做连续的监测以便得到预测污染物毒性的准确结果.
不同油类的毒性差异是由其所含组分差异而造成的,许多学者都对石油的总烃、芳香烃进行分析,由于烷烃及其取代物、杂环化合物等物质的毒性相对较小,因此,决定毒性大小的关键因素是其所含芳香烃及低分子量烷烃量(刘娜等,2006).0#柴油中芳香烃约占总组分的20%~30%,而平湖原油中芳香烃约占总组分的25%~35%,且一般原油同时含有胶质、沥青和石蜡等杂质(贾晓平等,2000).从2种石油对SOD、GST、POD酶活性的时间影响看(表 1、表 2和表 4),中低浓度处理组最大诱导出现时间(3 d)要早于平湖原油(7 d),0#柴油诱导量均高于平湖原油(尤其是POD的诱导量相差3倍),抑制率则低于平湖原油,可见缢蛏对2种石油的敏感性差异显著,酶活性受0#柴油的胁迫影响更为显现.在对2种石油不同浓度处理下的IBF值计算分析也发现,尽管0#柴油最高浓度组绝对数值(4 mg · L-1)低于平湖原油最高浓度组绝对数值(5 mg · L-1),0#柴油最低浓度组绝对数值(0.16 mg · L-1)低于平湖原油最低浓度组绝对数值(2 mg · L-1),但两者的IBF值均以0#柴油高,表明缢蛏受到0#柴油的毒性影响诱发产生氧化应激的能力水平更大,这一结论与其他学者(贾晓平等,2000;吴彰宽等,1988)得出的0#柴油毒性高于平湖原油的实验结果相一致.
从 IBR值与曝油浓度的关系来看,尤其是实验后期,两者IBR值没有明显变化规律.由于不同的酶对2种石油污染物胁迫的响应敏感程度不同,难以选取某一特定时间的酶活性直接代入计算IBR.而本试验中的生物标志物种类还不够丰富,未能系统综合不同量纲的生物标志物所致.因此,在今后研究中为保证综合生物标志物评价体系获得更为客观可信的结果,需对生物标志物进行必要的筛选比较,以敏感性高的指标作为IBR计算的基本参数,从而为有毒有害物质污染效应评价和现场监测的生物标志物评价提供更为科学、简便、快捷的评价方法.
5 结论(Conclusions)缢蛏在0#柴油和平湖原油暴露下,前期消化腺中的4种酶均表现出诱导或抑制,但对4种酶的影响存在时间顺序性,SOD、CAT和GST的酶活性表现为升高-降低的趋势,POD的酶活性表现为降低-升高的趋势,SOD和CAT活性达到峰值的时间要早于GST和POD.IBR数值显示,高浓度0#柴油能够引起最为显著的生物效应变化,表明该石油污染物高毒性的特征,且0#柴油的生物毒性大于平湖原油的生物毒性.
致谢: 本实验得到了江苏省启东市金海岸水产研究所朱善央老师的大力支持和帮助,在此表示感谢!| [1] | Beliaeff B,Burgeot T.2002.Integrated biomarker response: A useful tool for ecological risk assessment [J].Environmental Toxicology and Chemistry,21(6): 1316-1322 |
| [2] | 丁秀蓉,李正炎,王波,等.2007.壬基酚对牙鲆肝脏EROD和GST酶活性的影响[J].中国海洋大学学报,37(S1): 101-104 |
| [3] | 高静,牛亚青,胡南,等.2011.硫酸锰废渣浸出液对斑马鱼的毒性及抗氧化酶活性的影响[J].生态毒理学报,6(4): 389-396 |
| [4] | 国家质量监督检验检疫总局.2008.GB 17378—2007 海洋监测规范[S].北京: 中国标准出版社 |
| [5] | 黄逸君,陈全震,曾江宁,等.2010.原油和消油剂对海洋桡足类的急性毒性效应[J].应用与环境生物学报,16(4): 566-571 |
| [6] | Jena K B,Verlecar X N,Chainy G B N.2009.Application of oxidative stress indices in natural populations of Perna viridis as biomarker of environmental pollution [J].Marine Pollution Bulletin,58(1): 107-113 |
| [7] | 贾晓平,林欣,蔡文贵,等.2000.原油和燃油对南海重要海水增养殖生物的急性毒性试验[J].水产学报,24(1): 32-36 |
| [8] | 李传慧,夏斌,陈碧娟,等.2011.胜利原油对半滑舌鳎幼鱼肝脏谷胱甘肽过氧化物酶和谷胱甘肽转硫酶活性的影响[J].海洋环境科学,30(6): 827-830 |
| [9] | 李飞,张其中,赵海涛.2005.氨氮对南方鲶两种抗氧化酶和抗菌活力的影响[J].淡水渔业,35(6): 11-15 |
| [10] | 李莹.2013.三种典型有机污染物对鲫鱼抗氧化防御系统影响的研究.南京: 南京大学 |
| [11] | 刘冰,梁婵娟.2005.生物过氧化氢酶研究进展[J].中国农学通报,21(5): 223-232 |
| [12] | 刘娜,熊德琪,高会,等.2006.柴油和燃料油对小球藻的急性毒性试验研究[J].海洋环境科学,25(S1): 29-32 |
| [13] | Oliveira M,Ahmad I,Maria V L,et al.2010.Monitoring pollution of coastal lagoon using Liza aurata kidney oxidative stress and genetic endpoints: An integrated biomarker approach [J].Ecotoxicology,19(4): 643-653 |
| [14] | Pytharopoulou S,Sazakli E,Grintzalis K,et al.2008.Translational responses of Mytilus galloprovincialis to environmental pollution: integrating the responses to oxidative stress and other biomarker responses into a general stress index [J].Aquatic Toxicology,89(1): 18-27 |
| [15] | Richardson B J,Mak E,De Luca-Abbott S B,et al.2008.Antioxidant responses to polycyclic aromatic hydrocarbons and organochlorine pesticides in green-lipped mussels (Perna viridis ): Do mussels "integrate" biomarker responses? [J].Marine Pollution Bulletin,57(6/12): 503-514 |
| [16] | Scott-Fordsmand J J,Weeks J M.2000.Biomarkers in earthworms [J].Reviews of Environment Contamination and Toxicology,165: 117-159 |
| [17] | 万斌.2000.生态毒理学中生物标志物研究进展[M].国外医学卫生学分册,27(2): 110-112 |
| [18] | 王丽平,郑丙辉,孟伟.2007.环境污染物对水生生物产生氧化压力的分子生物标志物[J].生态学报,27(1): 380-388 |
| [19] | 王晓蓉,罗义,施华宏,等.2006.分子生物标志物在污染环境早期诊断和生态风险评价中的应用[J].环境化学,25(2): 320-325 |
| [20] | 吴彰宽,陈国江.1988.二十三种有害物质对对虾的急性致毒试验[J].海洋科学,(4): 36-40 |
| [21] | 夏斌,陈碧娟,李传慧,等.2011.胜利原油对半滑舌鳎肝脏超氧化物歧化酶和过氧化氢酶活性的影响[J].渔业科学发展,32(1): 53-59 |
| [22] | 许燕,杨洁,孙静秋,等.2010.凡纳滨对虾不同组织内SOD、POD酶的细胞化学定位[J].水生生物学报,34(2): 402-409 |
 2015, Vol. 35
2015, Vol. 35


