2. 西北农林科技大学水土保持研究所, 杨凌 712100;
3. 中科院水利部水土保持研究所, 杨凌 712100
2. Institute of Soil and Water Conservation, Northwest A&F University, Yangling 712100;
3. Institute of Soil and Water Conservation, Chinese Academy of Sciences and Ministry of Water Resources, Yangling 712100
近年来土壤重金属污染问题日益严重,其中,以铅为代表的重金属污染因其生物毒害性和富集性引起了人们的广泛关注.相关资料统计显示,我国约有1.3×104 hm2的耕地受到铅等重金属污染,不仅导致粮食减产10×106 t(张从等,2000),也给人体健康带来了极大危害(余彬等,2007;代全林,2007).在污染土壤中添加修复材料以稳定土壤中的重金属、减少重金属在作物中的吸收积累,是土壤重金属污染治理和土壤改良的重要途径之一(桑爱云等,2007;彭丽成等,2011;高俊杰等,2010;刘昭兵等,2010).砒砂岩是黄土高原晋陕蒙接壤区的水相沉积物,结构松散,很容易形成水土流失,但其具有较强的吸附能力和较低的重金属本底值.利用这一特性将其应用于该区域的土壤重金属污染修复,可以降低重金属污染土壤修复的成本.
评价一种材料对重金属污染土壤修复效果主要是评价修复材料对土壤中重金属的形态及有效态变化的影响.但这一评价指标具有一定的局限性,因为土壤是复杂的有机系统,除了修复材料与重金属间的物理化学作用外,土壤其他指标也是很重要的因素,其可以表征土壤的健康状况并反映修复材料是否对土壤质量状况造成影响.砒砂岩传统上被看作是一种易引起水土流失的介质,以往的研究较少有将修复材料投向砒砂岩,导致对砒砂岩修复重金属污染土壤及对土壤质量的响应还缺乏了解.基于此,本文通过室内模拟试验,研究不同用量砒砂岩对土壤中铅形态转化及TCLP毒性溶出变化的影响,结合土壤基本理化指标的测定,来评价砒砂岩对铅污染土壤的修复效果,以期为土壤重金属污染的治理提供理论参考.
2 材料与方法(Materials and methods) 2.1 试验材料供试土壤为采自内蒙古准格尔旗大路镇(40°2.738′N,111°22.225′E)的风沙土(0~20 cm),土壤样品经自然风干并过2 mm尼龙筛,供室内试验.试验用的土壤修复材料为砒砂岩(红色),采自内蒙古准格尔旗暖水乡(39°44′23.6″N,110°34′34.3″E).土壤及砒砂岩基本理化性质见表 1.其中,颗粒组成(吸管法)、pH、CEC、有机质和Pb、Cd、As本底含量采用常规分析方法(鲁如坤,2000)测定,比表面积采用BET比表面积测定仪测定,矿物组成采用粉晶X射线衍射仪(D/MAX-2600pc)测定.
| 表 1 风沙土和砒砂岩基本理化性质 Table 1 Basic chemical and physical properties of Aeolian s and y soil and Pisha s and stone |
模拟试验在西北农林科技大学水土保持研究所干旱大厅温室中进行.试验所需的铅污染土壤由外源添加Pb(NO3)2金属盐溶液的形式,按照国家土壤环境质量三级标准近似1.5 倍的量模拟而成,即铅含量为700 mg · kg-1.模拟污染土壤维持土壤水分为田间持水量的60%,于温室中培养20 d后,进行后续污染土壤修复试验.
试验中土壤修复材料砒砂岩的添加量(质量百分比)分别为0(空白对照CK)、10%、30%和50%,共计4个处理.将模拟铅污染土壤与以上不同比例砒砂岩混合均匀后装于塑料桶(高10 cm×直径10 cm)中,每个处理设3个重复,保持土壤水分为田间持水量的60%并在温室中培养,分别在第10、20、30、40 d取土壤样品测定土壤基本理化性质(在第40 d测定土壤田间持水量)、重金属形态、TCLP含量及土壤脲酶和过氧化氢酶的活性.
2.3 试验方法土壤样品基本理化性质采用常规分析方法测定,土壤孔隙度采用土壤容重与土壤密度换算法计算所得,其中,土壤密度采用土壤平均密度2.65 g · cm-3.土壤pH采用1∶2.5 的土水比(田有国等,2006),用pH玻璃电极进行测定;田间持水量采用环刀法测定.土壤重金属的形态分级采用改进的BCR连续提取法(Mossop et al., 2003)分析,具体步骤见表 2.重金属毒性浸出量通过醋酸缓冲溶液法进行提取(孙叶芳等,2005),考虑到供试土壤的pH>5,则采用将5.7 mL · L-1冰醋酸(保证pH=2.88±0.05)缓冲液按照1∶20的土/缓冲液比进行TCLP提取,以(30±2)r · min-1的速度在常温下振荡(18±2)h,离心,过滤.最后用原子吸收分光光度计(Z-2000)测定形态提取液和TCLP提取液的Pb(II)含量.土壤脲酶、过氧化氢酶活性测定参照关松荫(1986)的方法,其中,脲酶测定采用靛蓝法(土壤脲酶活单位以24 h后每克土壤中NH3-N质量(mg)表示,即mg · g-1 · d-1),过氧化氢酶测定采用高锰酸钾滴定法(土壤过氧化氢酶活性单位以每克干土在24 h内消耗0.02mol · L-1 KMnO4的体积(mL)表示,即mL · g-1 · d-1).
| 表 2 改进的BCR连续提取法 Table 2 Modified BCR sequential extraction schemes |
表 3为模拟铅污染土壤添加砒砂岩修复前后重金属铅各化学形态含量及百分含量.如表 3所示,对照土壤中铅的有效态含量较高,主要以弱酸提取态(F1)存在,其占全部形态的质量分数超过50%.
| 表 3 砒砂岩对污染土壤铅化学形态含量及分布的影响 Table 3 Effects of Pisha s and stone on the contents of Pb forms |
添加10%、30%、50%三种剂量砒砂岩后,使得混合后新构土体土壤中铅总含量被稀释,含量呈相对减少趋势,但从混合土体各化学形态铅含量的占比可知,与对照相比,在处理10 d后,砒砂岩的添加显著减少了高活性的弱酸提取态(F1)铅百分含量,且随着砒砂岩投加剂量的增加,土壤弱酸提取态(F1)铅含量逐渐降低.其中,砒砂岩50%、30%、10%处理使弱酸提取态(F1)铅含量在总量中的占比分别比对照显著降低了27.38%、16.64%、8.05%,彼此之间亦表现出显著性差异;可还原态(F2)铅百分含量则由于砒砂岩的处理而显著提高,且随着处理剂量的增加可还原态(F2)铅百分含量逐渐增加,其中,砒砂岩10%、30%、50%处理后的可还原态(F2)铅百分含量与对照相比增幅分别为6.52%、13.27%,21.24%;究其处理后的可氧化态(F3)铅与残渣态(F4)铅百分含量均未因砒砂岩的添加表现出规律性变化影响,但从总趋势来看,可氧化态(F3)铅百分含量比对照有所降低,残渣态(F4)铅百分含量比对照有所增加.在处理20、30和40 d后,其各形态变化与10 d的结果相似,处理天数之间差异不显著.
综上所述,砒砂岩的添加显著降低了土壤弱酸提取态铅含量,同时增加了可还原态铅含量和残渣态铅含量,并随着砒砂岩剂量的增大降幅或增幅越大,且弱酸提取态(y1)和可还原态铅(y2)百分含量与砒砂岩剂量(x)表现出了较好的线性关系:y1=-50.433x+54.071(R2=0.965),y2=39.06x+36.966(R2=0.942),残渣态铅百分含量(y3)与砒砂岩剂量(x)的线性关系不明显:y3=13.538x+5.6784(R2=0.449);在时间尺度上,随着处理时间的变化,各形态含量变化不大.对于重金属污染土壤原位钝化修复技术,主要是通过钝化剂与重金属发生吸附沉淀、络合螯合等物理化学反应,改变重金属在土壤中的化学形态和赋存状态,从而降低重金属的活性、影响其环境行为,以达到修复污染土壤的目的(Kumpiene et al., 2008;Bolan et al., 2003).在本研究中,砒砂岩的添加使污染土壤中铅活性最高的弱酸提取态含量显著降低,而使活性相对较低的可还原态与残渣态含量显著升高,这表明砒砂岩可促使铅由高活性形态向低活性形态转化,从而显著降低铅的生物有效性和迁移性,进而达到钝化修复的目的.考虑到砒砂岩具有较高的pH、自身较强的吸附性能,它可能通过提高土壤pH、吸附反应、离子交换、化学沉淀等来钝化稳定土壤中较高活性的铅组分,以转向低活性组分.
土壤pH的提高,一方面影响其中重金属的存在形态和赋存状态,另一方面影响土壤吸附过程.砒砂岩的添加使土壤pH升高,并维持在一个相对较高的稳定值,且随砒砂岩添加剂量的增大,pH相应增大(具体结果详见3.3.3节).试验进一步将砒砂岩处理前后的土壤pH与土壤中各形态铅百分含量进行相关分析,结果见表 4.由表 4可知,土壤弱酸提取态铅百分含量与土壤pH呈显著负相关(p<0.01),可还原态与残渣态铅百分含量则与土壤pH呈显著正相关(p<0.01),这表明土壤中铅含量由高活性态转向低活性态,与砒砂岩改变了土壤pH有密切关系.
| 表 4 土壤各形态铅含量与土壤pH、砒砂岩吸附铅量相关关系 Table 4 Relationship between Pb forms and pH of soil and Pb(Ⅱ)adsorption |
砒砂岩具有较强的吸附性,吸附量大约为53.05 mg · g-1(温婧等,2014),随着砒砂岩添加量的增大,其吸附铅的容量自然增大,可能对铅的有效含量产生影响.将砒砂岩对铅的吸附量与处理前后土壤中各形态铅百分含量进行相关分析可知(表 4),土壤中高活性的弱酸提取态铅百分含量与砒砂岩吸附铅量呈显著负相关(p<0.01),低活性的可还原态与残渣态铅百分含量与砒砂岩吸附量呈显著正相关(p<0.01),这进一步表明砒砂岩的吸附性直接关系着土壤中铅的活性状态.
3.2 砒砂岩对土壤铅溶出特性影响TCLP(Toxicity Characteristic Leaching Procedure)法是由美国环保局(USEPA)提出的一种环境污染评价方法,同时也是美国最新的用以评估重金属生态环境风险的法定重金属污染评价方法(Sun et al., 2006).目前,国内外已有研究将该方法用于评价钝化剂对重金属污染土壤钝化修复的效果,即采用该方法分析钝化修复前后土壤中重金属元素的浸出量,以此来评价钝化剂在重金属生物有效性和迁移能力上的修复效果(Hettiarachchi et al., 2000;陈杰华等,2009).
砒砂岩不同添加剂量对污染土壤铅的TCLP毒性溶出量及其随时间变化的影响见表 5.结果显示,在铅污染土壤中添加砒砂岩后,铅的毒性溶出量显著降低.当处理到10 d时,砒砂岩50%添加剂量下的土壤重金属铅毒性溶出量由428.11 mg · kg-1降低到118.35 mg · kg-1,并且其占全量的比值分别比CK、10%、30%水平下显著减少了26.97%、17.59%、8.70%.由此可以看出,随着砒砂岩剂量的增加,土壤中铅毒性溶出量随之降低,并且降低显著,同时铅毒性溶出比例(y)与砒砂岩添加量(x)同样表现出了较好的线性关系:y=-52.043x+56.456(R2=0.936).当处理进行到第40 d时,砒砂岩10%、30%、50%剂量下的土壤铅毒性溶出量分别为第10 d时毒性溶出量的88.99%、90.92%、91.13%.由此可见,随着砒砂岩处理时间的延长,土壤中铅毒性溶出量呈下降趋势,但下降不明显.
| 表 5 砒砂岩对污染土壤铅毒性溶出量及所占百分比含量的影响 Table 5 Effects of Pisha s and stone on the contents of Pb TCLP |
土壤铅毒性溶出量之所以随砒砂岩的添加而降低可能是由于砒砂岩的施入增加了土壤pH,使铅以较稳定形态存在.此外,土壤中砒砂岩能有效增加土壤的吸附性能和吸附亲和力,其原因为:①砒砂岩具有较大的阳离子交换量(45.79 cmol · kg-1),重金属离子可与砒砂岩中的Ca2+、Mg2+等进行离子交换而吸附在砒砂岩表面;②砒砂岩可通过静电作用吸附Pb2+;③Pb2+与砒砂岩中的CO2- 3形成PbCO3沉淀(温婧等,2014).进一步将土壤铅毒性溶出量与砒砂岩处理前后土壤pH和其对铅的吸附量进行相关分析得知,土壤中铅毒性溶出量的多少与土壤pH、砒砂岩吸附钝化铅的含量有着密切关系,它们之间呈现出显著负相关性(TCLP-pH,r = -0.981,p<0.01;TCLP-吸附量,r = -0.967,p<0.01).这说明砒砂岩在通过改变土壤pH、增大土壤吸附量来抑制土壤铅迁移方面发挥着积极的作用.
3.3 砒砂岩对污染土壤理化特性的影响 3.3.1 砒砂岩对土壤总孔隙度的影响土壤孔隙度也是表征土壤质量好坏的一个关键物理数值.土壤孔隙度与土壤容重有关,一般通过土壤容重与土壤密度计算得到.因此,土壤孔隙度与土壤容重类似,也可以说明土壤的结实程度及土壤的通气状况、水分运动等.
图 1结果显示,在土壤中添加砒砂岩可以明显改善土壤孔隙度,使土壤孔隙度增大.与对照土壤孔隙度(39.62%)相比,砒砂岩10%、30%、50%添加比例处理后的土壤孔隙度分别增大到了40.38%、43.40%和46.04%,并且随砒砂岩添加比例的增大土壤孔隙度相应增大.这说明砒砂岩在一定程度上改善了土壤结构,使原本孔隙度为39.62%的紧实土壤得以疏松,增大了土壤通气状况,并使得土壤水分有利输送,进而营造了植物、微生物生长的有利环境.
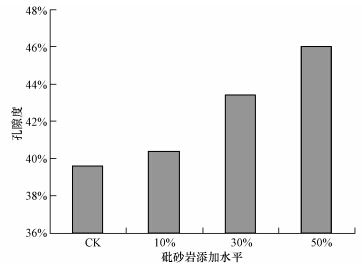 |
| 图 1 不同剂量砒砂岩对土壤孔隙度的影响 Fig. 1 Effects of Pisha s and stone with different doses on soil porosity |
田间持水量作为土壤所能保持的、作物能有效生长的最大含水量,是影响土壤质量和作物生长的重要因素,其大小与土壤质地、结构等因素有关.图 2结果表明,添加砒砂岩处理较对照能显著增加土壤田间持水量,其中,10%、30%、50%处理分别比对照增加田间持水量5.00%、7.97%和9.72%.这可能与砒砂岩含有30%的蒙脱石及羟基等强亲水基团有关,对土壤水分有良好的吸收和保持作用.土壤含水量的增加是促进作物良好生长的基础,这表明砒砂岩在土壤保水方面具有一定的改良作用.
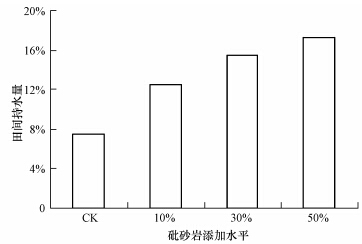 |
| 图 2 不同剂量砒砂岩对土壤田间持水量的影响 Fig. 2 Effects of Pisha s and stone with different doses on field capacity |
不同剂量砒砂岩对污染土壤pH的影响见图 3.与对照相比,各培养期内砒砂岩的添加都提高了土壤pH,且随添加剂量的增加pH逐渐增加,增加幅度分别为:30%处理比10%处理增加了0.22~0.28,50%处理比30%处理增加了0.20~0.33.随着培养时间的推移,各个处理土壤pH没有表现出较大的变化,在整个培养期内砒砂岩10%、30%、50%处理分别使土壤pH维持在8.47~8.57、8.74~8.83、8.94~9.16的较高水平,对土壤pH表现出一定的持久性.可见,添加砒砂岩显著提高了污染土壤pH,这可能是由于砒砂岩自身的高pH,添加后使土壤pH值增加.
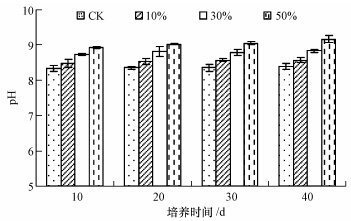 |
| 图 3 不同剂量砒砂岩随不同时间对污染土壤pH的影响 Fig. 3 Effects of Pisha s and stone with different doses at different times on pH |
由图 4a可知,在试验设定范围内,与对照相比,砒砂岩10%、30%及50%处理均增加了土壤过氧化氢酶活性,且随着投加剂量的增加,过氧化氢酶活性增幅逐渐降低.与此同时,在不同处理时间下的过氧化氢酶活性变化均表现为:随着时间的推移,土壤过氧化氢酶活性总体呈现下降趋势.砒砂岩的添加对土壤脲酶活性的影响如图 4b所示.在本试验设定范围内,与对照相比,不同剂量砒砂岩的添加对土壤脲酶活性影响不大.
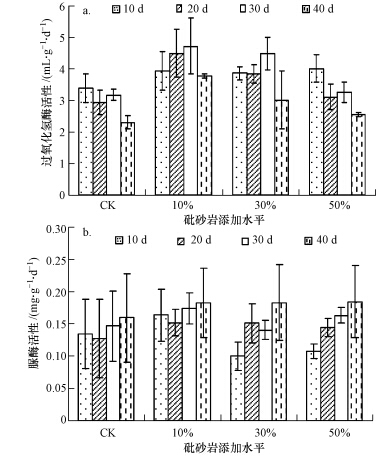 |
| 图 4 砒砂岩对土壤过氧化氢酶活性(a)和脲酶活性(b)的影响 Fig. 4 Effects of Pisha s and stone on the activities of hydrogen peroxidase(a) and urease(b) |
低含量的重金属对土壤酶活性有一定的激活作用,但随着重金属含量的升高,土壤酶活性会受到抑制,当重金属含量较高时土壤酶失活(林匡飞等,2005;滕应等,2008;Belyaeva et al., 2005;Chen et al., 2005).砒砂岩的添加对土壤过氧化氢酶活性的提高,则可能就是由于砒砂岩不同程度地降低了土壤中重金属铅的活性,尤其是显著地降低了土壤弱酸提取态铅含量及毒性溶出量,减轻了对土壤酶活性的抑制作用.另外,砒砂岩的添加也显著提高了土壤pH,土壤pH的提高有利于增加土壤微生物的数量,形成优势微生物,其分泌的胞外酶数量也相应增多,导致土壤过氧化氢酶活性提高(Frankenberger et al., 1982;王涵等,2008).而过氧化氢酶活性在各处理间随砒砂岩添加剂量的增加呈现下降趋势,则可能与有关研究认为在一定浓度范围内,过氧化氢酶活性会随着重金属铅含量的降低而逐渐减小有关(Yang et al., 2006;杨志新等,2001).对于脲酶各处理与对照相比变化不大,可能是由于砒砂岩各个添加水平处理后的土壤重金属含量仍然在抑制脲酶活性的重金属含量范围内.
3.4 砒砂岩实际应用价值由上述分析可知,砒砂岩在降低土壤铅有效态含量的同时,并未对土壤质量造成影响,反而在一定程度上改良了土壤.相比其他材料而言:①砒砂岩在晋陕蒙区域分布广泛,可就地取材用于修复该区域土壤重金属污染,这减少了材料的运输成本;②砒砂岩不像生物碳、碳纳米管、有机堆肥等材料在应用之前需要合成加工或是前期处理,它极易风化可直接应用不需处理,这减少了材料生产成本;③砒砂岩也不像石灰、磷酸盐类物质,使用后可能对土壤质量状况产生影响,这减少了后续治理成本;④砒砂岩易水蚀风蚀,对当地环境造成一定的影响,被当地人视为废弃物,它在作为土壤修复剂上的潜能为其资源化再利用开辟了新途径.
4 结论(Conclusions)1)砒砂岩具有一定的修复铅污染土壤的作用,对土壤中的铅有稳定固化的效果.砒砂岩的添加显著降低了土壤弱酸提取态铅百分含量,增加了可还原态和残渣态铅百分含量,并随砒砂岩添加剂量的增大高活性态降幅越大、低活性态增幅越大;同时,砒砂岩显著降低了土壤铅毒性溶出量,使铅生物有效性和迁移能力、土壤毒性得以降低,且降幅程度与砒砂岩用量成正比.
2)砒砂岩的较强吸附特性及可以提高土壤pH是固化土壤重金属铅的重要因素.砒砂岩还可改善土壤理化特性,在一定程度上对污染土壤起改良、调节作用.
| [1] | Belyaeva O N,Haynes R J,Birukova O A.2005.Barley yield and soil microbial and enzyme activities as affected by contamination of two soils with lead,zinc or copper[J].Biology and Fertility of Soils,41(2): 85-94 |
| [2] | Bolan N S,Duraisamy V P.2003.Role of inorganic and organic soil amendments on immobilisation and phyto availability of heavy metals: A review involving specific case studies[J].Australian Journal of Soil Research,41(3): 533-555 |
| [3] | Chen C L,Liao M H,Huang C Y.2005.Effect of combined pollution by heavy metals on soil enzymatic activities in areas polluted by tailings from Pb-Zn-Ag mine[J].Journal of Environmental Sciences,17(4): 637-640 |
| [4] | 陈杰华,王玉军,王汉卫,等.2009.基于TCLP法研究纳米羟基磷灰石对污染土壤重金属的固定[J].农业环境科学学报,28(4): 645-648 |
| [5] | 代全林.2007.植物修复与超富集植物[J].亚热带农业研究,3(1): 51-56 |
| [6] | Frankenberger W T Jr,Johanson J B.1982.Effect of pH on enzyme stability in soils[J].Soil Biology and Biochemistry,14(5): 433-437 |
| [7] | 高俊杰,梁锦,徐丽,等.2010.环境矿物材料对重金属污染的修复研究[J].中山大学研究生学刊(自然科学、医学版),31(1): 52-59 |
| [8] | 关松荫.1986.土壤酶及其研究法[M].北京: 农业出版社.295-297; 323 |
| [9] | Hettiarachchi G M,Pierzynski G M,Ransom M D.2000.In situ stabilization of soil lead using phosphorus and manganese oxide[J].Environmental Science & Technology,34(21): 4614-4619 |
| [10] | Kumpiene J,Lagerkvist A,Maurice C.2008.Stabilization of As,Cr,Cu,Pb and Zn in soil using amendments—a review[J].Waste Management,28(1): 215-225 |
| [11] | 林匡飞,徐小清,金霞,等.2005.土壤硒污染对土壤酶的生态毒理效应[J].中国环境科学,25(Supp1): 94-97 |
| [12] | 刘昭兵,纪雄辉,王国祥,等.2010.赤泥对Cd污染稻田水稻生长及吸收累积Cd的影响[J].农业环境科学学报,29(4): 692-697 |
| [13] | 鲁如坤.2000.土壤农业化学分析方法[M].北京: 中国农业科技出版社 |
| [14] | Mossop K F,Davidson C M.2003.Comparison of original and modified BCR sequential extraction procedures for the fractionation of copper,iron,lead,manganese and zinc in soils and sediments[J].Analytica Chimica Acta,478(1): 111-118 |
| [15] | 彭丽成,黄占斌,石宇,等.2011.环境材料对Pb、Cd污染土壤玉米生长及土壤改良效果的影响[J].中国生态农业学报,19(6): 1386-1392 |
| [16] | 桑爱云,夏炜林,王华,等.2007.不同改良剂对铅污染砖红壤的修复效果[J].中国农学通报,23(8): 503-506 |
| [17] | 孙叶芳,谢正苗,徐建明,等.2005.TCLP法评价矿区土壤重金属的生态环境风险[J].环境科学,26(3): 152-157 |
| [18] | Sun Y F,Xie Z M,Li J,et al.2006.Assessment of toxicity of heavy metal contaminated soils by the toxicity characteristic leaching procedure[J].Environmental Geochemistry and Health,28(1/2): 73-78 |
| [19] | 滕应,骆永明,李振高.2008.土壤重金属复合污染对脲酶、磷酸酶及脱氢酶的影响[J].中国环境科学,28(2): 147-152 |
| [20] | 田有国,辛景树,任意,等.2006.NYT 1121.2—2006 土壤检测 第2部分: 土壤pH的测定[S].北京: 中国标准出版社 |
| [21] | 王涵,王果,黄颖颖,等.2008.pH变化对酸性土壤酶活性的影响[J].生态环境,17(6): 2401-2406 |
| [22] | 温婧,朱元骏,殷宪强,等.2014.砒砂岩对Pb(Ⅱ)的吸附特性研究[J].环境科学学报,34(10):2491-2499 |
| [23] | 杨志新,刘树庆.2001.重金属Cd、Zn、Pb复合污染对土壤酶活性的影响[J].环境科学学报,21(1): 60-63 |
| [24] | Yang Z X,Liu S Q,Zheng D W.2006.Effects of cadium,zinc and lead on soil enzyme activities [J].Journal of Environmental Sciences,18(6): 1135-1141 |
| [25] | 余彬,郑钦玉.2007.土壤铅污染的防治技术[J].安徽农学通报,13(13): 56-60 |
| [26] | 张从,夏立江.2000.污染土壤生物修复技术[M].北京: 中国环境科学出版杜.1-42 |
 2015, Vol. 35
2015, Vol. 35


