中国湖泊富营养化导致蓝藻水华频繁暴发.其中,微囊藻水华是淡水水华中危害最严重的一类,它产生的微囊藻毒素(MCs)是具有生物活性的七肽单环肝毒素,是目前发现的最强的肝脏肿瘤促进剂(Nimptsch et al.,2008).世界卫生组织(WHO)规定:水体中MCs的安全剂量为1 μg · L-1(WHO,1998),然而自然界水体中微囊藻毒素含量通常在0.1~100 μg · L-1内,当藻类大量死亡时MCs在短时间内可高达1800 μg · L-1(Jones et al.,1994).自1995年Kós等(1995)首次报道MC-LR及其粗提物能够抑制荠菜幼苗的生长后,被MCs污染的灌溉用水对陆生生态系统的潜在风险也逐渐受关注(李慧明等,2009).McElhiney等(2001)研究发现,当MC-LR含量分别为0.5~5.0 mg·kg-1和1.12 mg·kg-1时,马铃薯和菜豆的生长发育均受到显著抑制.然而,已有报道多集中在MCs对植物影响的浓度效应和时间效应研究上(Gehringer et al.,2003,Chen et al.,2011,Lahrouni et al.,2012),却少有关于水体中MCs浓度因湖泊底泥或土壤的吸附、生物降解等(Holst et al.,2003; Liu et al.,2008)而变化时对农作物的影响研究.光合作用是植物生长的基础,原初反应是光合作用的起始过程,包括光合色素分子对光能的吸收、传递与转换各环节.叶绿素荧光参数可反映各环节的信息,为探悉逆境胁迫对光合作用影响机理提供直接证据.鉴于此,本文以水稻为试材,考察不同浓度MCs处理胁迫期与恢复期(无MCs胁迫)内水稻生长、叶绿素含量与叶绿素荧光参数的变化,同步运用酶联免疫法(ELISA)测量MCs在水稻叶片中的富集量,探究MCs对农作物光合作用的影响机理,以期为客观全面地评价MCs的生态安全风险及水稻田MCs污染防控提供基础信息.
2 材料与方法(Materials and methods) 2.1 MCs的制备称取1 g干燥的藻粉,加入40 mL 5%的冰乙酸,室温抽提2 h,8000 r · min-1离心10 min,沉淀用40 mL 5%冰乙酸继续搅拌抽提,重复2次,合并3次抽提的上清液,调节pH为3.0;然后离心去除杂质蛋白,过0.45 μm滤膜,调节pH为7.0,采用固相萃取装置,将粗提取液过Sep-pak C18柱(Supelco Envi218,Waters Corporation,美国).富集步骤参照文献(王娓敏等,2014):10 mL甲醇(100%)润洗,10 mL纯水润洗,进样,10 mL甲醇(100%)洗脱,旋转蒸发,收集MCs溶于1 mL纯水.采用高效液相色谱法(Ultimate 3000,美国戴安公司)测定MCs含量,紫外可见光检测器波长 238 nm,色谱柱温度 40 ℃,流动相为甲醇和pH=3的磷酸盐缓冲液(二者的体积比为57 ∶ 43),柱流速 1 mL · min-1(中华人民共和国国家质量监督检验检疫总局和中国国家标准化管理委员会,2006).结果显示,只有MC-LR和MC-RR有明显出峰,且峰值稳定.
2.2 试材培养供试水稻(Oryza sativa)为“淮稻8号”.挑选籽粒饱满的水稻种子用0.1% HgCl2消毒10 min,用去离子水浸泡后置于25 ℃恒温光照培养箱中催芽2 d,移入6.88 L周转箱中蛭石培养25 d至2叶1心,然后移栽至周转箱进行水培.营养液每隔3 d更换1次以调节pH值(每次用H2SO4或NaOH将营养液pH调至5.5).光照强度为300 μmol-1 · m-2 · s-1,光照12 h,昼/夜温度为30 ℃/24 ℃,相对湿度为60%.水稻幼苗长至4叶1心期时进行MCs胁迫处理.
2.3 试材处理将高浓度的MCs母液用营养液稀释成4个MCs浓度(1、100、1000、3000 μg · L-1),以不含MCs的营养液作为对照(CK),每个处理3次重复.处理7 d后进行各指标的测定,然后将处理过的植株在对照组培养条件下恢复培养7 d再取样测定.
2.4 实验测定方法 2.4.1 MCs在水稻叶片中的含量测定称取0.5 g新鲜幼苗叶片,蒸馏水洗涤4次,然后用滤纸吸干表面水分,用2 mL 80% 甲醇研磨后超声破碎,离心取上清液,富集步骤参考2.1节进行,采用酶联免疫法(ELISA)确定MCs的总含量(张琳等,2012).
2.4.2 生长指标测定植株的叶面积用CI-203激光叶面积仪测定,然后以单株为单位,取其叶片,用去离子水洗涤3次后用吸水纸吸干,于电热恒温干燥箱中100 ℃杀青10 min,80 ℃烘12 h至恒重,称其干重.
2.4.3 叶绿素含量测定叶绿素含量采用二甲亚枫法测定(DMSO法)(Arnon,1949).
2.4.4 叶绿素荧光参数测定选取不同处理下同一叶位的叶片,用脉冲调制荧光仪PAM-210(WALZ,德国)测定叶绿素荧光参数,实验方法参照文献(Demmig-Adams et al.,1996)
3 结果(Result) 3.1 MCs在水稻叶片中的吸收量由图 1可知,不同浓度MCs(1、100、1000、3000 μg · L-1)处理7 d后,MCs在水稻叶片的含量随着MCs浓度的增大而升高,分别为0.024、0.126、0.224、0.249 μg · g-1;当MCs浓度为3000 μg · L-1时,水稻叶片对MCs的吸收量最高,分别是1、100、1000 μg · L-1处理组的10.375、1.976、1.112倍.恢复期内,水稻叶片对MCs的吸收量变化趋势与胁迫期一致,但均小于同一处理组在胁迫期时的吸收量.
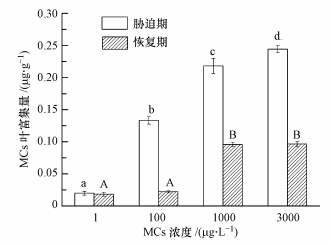 |
| 图 1 MCs在水稻幼苗叶片中的积累(不同字母表示各处理间差异显著(p<0.05),大、小写字母分别表示恢复期、胁迫期差异显著性) Fig.1 MCs accumulation in leaves of rice seedlings |
表 1显示,7 d的MCs胁迫后,与CK相比,1 μg · L-1 MCs处理下的叶鲜重和叶干重分别增加了27.89%和14.47%,叶面积无显著变化;高浓度(≥100 μg · L-1)MCs导致叶鲜重、叶干重、叶面积降低,降幅分别是44.82%、14.48%、13.19%(100 μg · L-1),62.35%、37.5%、41.96%(1000 μg · L-1)和63.75%、42.76%、47.93%(3000 μg · L-1),即MCs 浓度越高对生长的抑制程度越大.恢复期7 d后,1 μg · L-1 MCs处理组下的叶鲜重和叶干重明显高于CK,叶面积则未发生明显改变;100 μg · L-1 MCs处理组下的叶鲜重、叶干重和叶面积虽然低于CK,但相比对应的胁迫组却升高;而1000、3000 μg · L-1 MCs处理组的鲜干重及叶面积不仅低于CK,且低于相应的胁迫组.
| 表 1 MCs对水稻幼苗生长的影响 Table 1 Effects of MCs on growth of rice seedlings |
由图 2可以看出,在MCs处理7 d后,与CK相比,1 μg · L-1 MCs处理下,叶绿素含量(以鲜重计)上升了8.27%,100、1000、3000 μg · L-1处理下,叶绿素含量下降,降幅分别为7.86%、27.19%、35.99%.恢复7 d后,1 μg · L-1 MCs处理下水稻叶片的叶绿素含量无明显变化,100 μg · L-1 MCs处理组叶绿素含量虽然低于CK但却高于胁迫期,而高浓度(≥1000 μg · L-1)MCs处理组的叶绿素含量依然下降,且低于胁迫期.
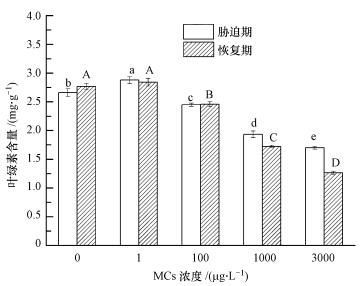 |
| 图 2 MCs对水稻幼苗叶片叶绿素的影响 Fig.2 Effects of MCs on chlorophyll content in leaves of rice seedlings |
叶绿素荧光是表示光抑制的良好指标和探针,其中,初始荧光参数F0表示PSⅡ反应中心处于完全开放时的荧光产量,Fv/Fm表示PSⅡ原初光能转化效率(袁红艳等,2010),F0上升Fv/Fm下降说明PSⅡ反应中心遭到破坏.胁迫期内,当MCs浓度为1 μg · L-1时,F0显著下降,而Fv/Fm、ETR、qP和qN均未发生显著改变(p>0.05);而在高浓度MCs(100、1000、3000 μg · L-1)处理下,F0明显上升,增幅与MCs处理浓度正相关(r=0.963),当MCs浓度为100 μg · L-1时,Fv/Fm、ETR和qP显著下降,降幅分别为4.35%、14.52%和6.98%,qN则明显上升,增幅为6.16%,说明该处理下的水稻虽然能够利用不断增强的qN来进行热耗散,抵抗MCs胁迫,但仍然难以维持较高的光化学效率,而在高浓度MCs(≥1000 μg · L-1)处理下,Fv/Fm、ETR、qP和qN显著下降,降幅分别为11.73%和18.71%、39.11%和45.56%、17.38%和28.49%、23.74%和34.25%.恢复7 d后,对于1 μg · L-1 MCs处理组的F0仍低于CK,而Fv/Fm、ETR仍未有显著变化,qP和qN显著升高;100 μg · L-1 MCs处理组各荧光参数均接近CK;高浓度MCs(≥1000 μg · L-1)处理组的F0仍高于CK,而Fv/Fm、ETR、qP和qN不仅低于CK更低于胁迫期.
| 表 2 不同MCs浓度下荧光参数的变化 Table 2 Effects of MCs on F0、Fv/Fm、ETR、qP and qN in leaves of rice seedlings |
本实验结果表明,MCs处理浓度越高,水稻叶片MCs的吸收量越大.当MCs浓度为1 μg · L-1时,MCs在水稻叶片的含量最低,水稻叶片的鲜/干重明显上升,这与前人得到的某些结论相反,易能等(2009)发现低浓度MCs(<50 μg · L-1)对油菜幼苗的株高和生物量无显著影响,这可能与MCs胁迫方式和物种有关.高浓度MCs(≥100 μg · L-1)处理下,水稻叶片的鲜/干重显著下降,叶面积也减少,说明高浓度MCs导致水稻叶片生物量下降,这与已有研究结果一致(李慧明等,2010).恢复7 d,MCs吸收量依然与处理浓度呈正相关,但明显低于胁迫期,这可能是因为恢复期的水稻生长较胁迫期好(表 1),因此,单位鲜重MCs的含量降低.也可能是MCs转移至水稻幼苗其他器官,如根系(王娓敏等,2014).Chen等(2004)也发现,MCs粗提液对水稻和油菜生长都有显著抑制作用,并同时检测到MCs在水稻和油菜幼苗体内积累.MCs能在植物体内积累也许就是MCs影响植物生长发育的直接原因之一.
4.2 MCs对水稻叶片叶绿素含量的影响环境中污染因子引起的叶绿体色素含量变化是影响植株光合功能的原因之一(吕廷良等,2010).本实验中,MCs对叶绿素含量影响呈现“低促高抑”的现象.1 μg · L-1 MCs能促进叶绿素的合成,这与低毒物的刺激效应有关(惠红霞等,2004);而高浓度MCs(≥1000 μg · L-1)导致叶片中叶绿素含量降低,其主要原因可能是由于MCs促进叶绿素酶活性,加速叶绿素分解,抑或是与叶绿素合成有关的酶活性受到抑制,叶绿素合成受阻(袁红艳等,2010).恢复处理7 d,100 μg · L-1MCs处理组的叶绿素含量接近CK,表明此浓度对叶绿素含量的影响有一定程度的恢复,而高浓度MCs(≥1000 μg · L-1)处理组的叶绿素含量不仅低于CK,甚至低于胁迫期,说明高浓度的MCs对水稻叶片叶绿素合成与分解过程造成不可逆伤害.
4.3 MCs对水稻叶片叶绿素荧光的影响胁迫因子如干旱、热害和冷害均使PSⅡ光能利用效率下降,引发光抑制(杨晓青等,2004).F0是PSⅡ反应中心处于完全开放时的最低荧光产量,它与叶绿素含量有关,叶绿素含量上升,F0降低,而PSⅡ反应中心失活或损伤又使其升高(赵玉国等,2011),上升程度越高,表明SPII受损程度就越严重(Schnettger et al.,1994).Fv/Fm是植物逆境条件下产生光抑制的敏感指标(Bjrkman,1987),ETR是PSII的表观电子传递速率,体现的是光合电子经SPII反应中心向光化学反应方向的传递速率.qP体现PSII传递活性,qN是PSII天线色素吸收光能的热耗散部分.我们发现,在低浓度MCs(1 μg · L-1)胁迫下,水稻叶片F0下降,这与叶绿素含量上升有关(图 2),而Fv/Fm、ETR、qP、qN未发生显著变化,说明低浓度MCs并没有导致PSⅡ反应中心受损,甚至促进了PSⅡ反应中心活性.100 μg · L-1胁迫下,F0上升,Fv/Fm、ETR和qP下降,而qN上升,说明该浓度处理下水稻利用热耗散(qN上升)来缓解MCs胁迫造成的伤害,却难维持较高的光化学效率.当MCs浓度较高(≥1000 μg · L-1)时,F0上升,Fv/Fm、ETR、qP、qN则显著降低,表明此浓度MCs胁迫会抑制 PSⅡ的光化学活性及能量转化效率,使光合电子传递受阻、光合原初反应过程及热耗散能力受到抑制,最终导致光合作用效率降低,这与Perron 等(2012)的研究结果一致.恢复7 d后,100 μg · L-1 MCs处理组的Fv/Fm、ETR、qP和qN均高于胁迫期,表明此浓度MCs对光合作用的抑制有一定程度的恢复;高浓度MCs(≥1000μg · L-1)处理组的F0依然高于CK,且高于胁迫期,而Fv/Fm则低于胁迫期,表明高浓度MCs胁迫使水稻叶片光能向光化学传递受阻,光能过剩产生大量活性氧,破坏了叶绿体结构和功能(Jiang et al.,2011).
5 结论(Conclusions)1)MCs在水稻叶片中的含量随MCs处理浓度的增大而上升,对水稻叶片生长的抑制程度与处理浓度正相关,且恢复效果受处理浓度制约.
2)叶绿素含量在MCs胁迫下呈现低促高抑的现象.恢复期叶绿素含量变化趋势与胁迫期一致,而高浓度MCs(≥1000 μg · L-1)处理组的叶绿素含量低于胁迫期,表明高浓度MCs对水稻叶片光合系统的伤害不可逆.
3)低浓度MCs(1 μg · L-1)促进了PSⅡ的光化学活性,而高浓度MCs(≥100 μg · L-1)对水稻叶片PSⅡ产生伤害,使PSⅡ的光化学活性及能量转化率下降,且对水稻叶片PSⅡ的伤害不可逆.
| [1] | Arno n D I.1949.Copper enzymes in isolated chloroplasts.Polyphenoloxidase in Beta Vulgaris[J].Plant Physiology, 24(1): 1-15 |
| [2] | Bjrkman O.1987.High-irradiance Stress in higher plants and interaction with other stress factors//Biggins J.Progress in Photosynthesis Research (Volume 4)[M].Netherlands: Springer. 11-18 |
| [3] | Chen J Z,Ye J Y,Zhang H Y,et al.2011.Freshwater toxic cyanobacteria induced DNA damage in apple (Malus pumila),rape (Brassica napus) and rice (Oryza sativa) [J].Journal of Hazardous Materials,190(1/3): 240-244 |
| [4] | Chen J S,Song L R,Dai J,et al.2004.Effects of microcystins on the growth and the activity of superoxide dismutase and peroxidase of rape (Brassica napus L.) and rice (Oryza sativa L.) [J].Toxicon,43(4): 393-400 |
| [5] | Demmig-Adams B,Adams W W,Barker D H,et al.1996.Using chlorophyll fluorescence to assess the fraction of absorbed light allocated to thermal dissipation of excess excitation[J].Physiologia Plantarum,98(2): 253-264 |
| [6] | Gehringer M M,Kewada V,Coates N,et al.2003.The use of Lepidium sativum in a plant bioassay system for the detection of microcystin-LR[J].Toxicon,41(7): 871-876 |
| [7] | Holst T,Jørgensen N O G,Jørgensen C,et al.2003.Degradation of microcystin in sediments at oxic and anoxic,denitrifying conditions [J].Water Research,37(19): 4748-4760 |
| [8] | 惠红霞,许兴,李前荣.2004.NaCl胁迫对枸杞叶片甜菜碱、叶绿素荧光及叶绿素含量的影响[J].干旱地区农业研究,22(3): 109-114 |
| [9] | Jiang J L,Gu X Y,Song R,et al.2011.Microcystin-LR induced oxidative stress and ultrastructural alterations in mesophyll cells of submerged macrophyte Vallisneria natans (Lour.) Hara [J].Journal of Hazardous Materials,190(1/3): 188-196 |
| [10] | Jones G J,Orr P T.1994.Release and degradation of microcystin following algicide treatment of a Microcystis aeruginosa bloom in a recreational lake,as determined by HPLC and protein phosphatase inhibition assay [J].Water Research,28(4): 871-876 |
| [11] | Kós P,Gorzó G,Surányi G,et al.1995.Simple and efficient method for isolation and measurement of cyanobacterial hepatotoxins by plant tests (Sinapis alba L.)[J].Analytical Biochemistry,225(1): 49-53 |
| [12] | Lahrouni M,Oufdou K,Faghire M,et al.2012.Cyanobacterial extracts containing microcystins affect the growth,nodulation process and nitrogen uptake of faba bean (Vicia faba L.,Fabaceae) [J].Ecotoxicology,21(3): 681-687 |
| [13] | 李慧明,薛延丰,易能,等.2009.藻毒素对青菜生长的影响及其在幼苗体内的积累[J].江苏农业学报,25(3): 680-684 |
| [14] | 李慧明,干晓宇,邓蕾,等.2010.微囊藻毒素(MC-LR)在黑麦草幼苗体内的积累及对其生长的影响[J].农业环境科学学报,29(1): 49-53 |
| [15] | Liu B B,Gong Y,Xiao B D,et al.2008.A laboratory study on risk assessment of microcystin-RR in cropland [J].Journal of Environmental Management,86(3): 566-574 |
| [16] | 吕廷良,孙明高,宋尚文,等.2010.盐、旱及其交叉胁迫对紫荆幼苗净光合速率及其叶绿素含量的影响[J].山东农业大学学报(自然科学版),41(2): 191-195 |
| [17] | McElhiney J,Lawton L A,Leifert C.2001.Investigations into the inhibitory effects of microcystins on plant growth,and the toxicity of plant tissues following exposure[J].Toxicon,39(9): 1411-1420 |
| [18] | Nimptsch J,Wiegand C,Pflugmacher S.2008.Cyanobacterial toxin elimination via bioaccumulation of MC-LR in aquatic macrophytes: An application of the "Green Liver Concept"[J].Environmental Science & Technology,42(22): 8552-8557 |
| [19] | Perron M C,Qiu B S,Boucher N,et al.2012.Use of chlorophyll a fluorescence to detect the effect of microcystins on photosynthesis and photosystem II energy fluxes of green algae [J].Toxicon,59(5): 567-577 |
| [20] | Schnettger B,Critchley C,Santore U,et al.1994.Relationship between photoinhibition of photosynthesis,D1 protein turnover and chloroplast structure: effects of protein synthesis inhibitors [J].Plant,Cell & Environment,17(1): 55-64 |
| [21] | 王娓敏,邓玙,邹华,等.2014.微囊藻毒素对水稻根系生长和抗氧化系统的影响[J].环境科学,35(4): 1468-1472 |
| [22] | WHO.1998.Guidelines for Drinking-water Quality: Health Criteria and other Supporting Information[M].USA: World Health Organization |
| [23] | 杨晓青,张岁岐,梁宗锁,等.2004.水分胁迫对不同抗旱类型冬小麦幼苗叶绿素荧光参数的影响[J].西北植物学报,(5): 812-816 |
| [24] | 易能,薛延丰,李慧明,等.2009.微囊藻毒素对油菜幼苗生长及抗氧化酶活性的影响 [J].西北植物学报,29(6): 1207-1213 |
| [25] | 袁红艳,刘嘉琦,陆小平.2010.铅胁迫对费菜叶绿素含量及抗氧化酶活性的影响[J].安徽农业科学,38(23): 12445-12447 |
| [26] | 张琳,李晶晶,高庚申.2012.微囊藻毒素的酶联免疫法分析影响因素探讨[J].环境污染与防治,34(4): 58-62 |
| [27] | 赵玉国,王新忠,吴沿友,等.2011.高温胁迫及恢复对水稻叶绿素荧光动力学特性和保护酶活性的影响[J].安徽农业科学,39(27): 16487-16488 |
| [28] | 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.2006.GB/T20466-2006 水中微囊藻毒素的测定[S].北京:中国标准出版社 |
 2015, Vol. 35
2015, Vol. 35


