2. 同济大学环境科学与工程学院, 上海 200092
2. College of Environmental Science and Engineering, Tongji University, Shanghai 200092
分枝杆菌属(Mycobacterium spp.)包含许多机会致病菌,会引起一系列的人畜疾病(Marras et al., 2002).目前,在环境样品中已经分离出150多种分枝杆菌,且其数目还在不断增多(Tortoli,2003).研究发现,分枝杆菌广泛存在于环境水体、市政管网和室内管网中(Falkinham et al., 2001; Radomski et al., 2010; Dubrou et al., 2013),而快速、准确的分枝杆菌检测方法是有效控制、预防传染性疾病暴发的技术关键.目前,传统的分枝杆菌检测方法是培养法(Greenbery et al., 2005; Jjemba et al., 2010).然而,分枝杆菌生长缓慢,培养周期长(1~2个月)(Fernandez-Rendon et al., 2012),且检出率较低,培养法无法实现对分枝杆菌的快速监测和预警.此外,已有研究报道,当营养物质缺乏时分枝杆菌会进入VBNC(Viable but nonculturable)状态(Stopa et al., 2000),无法在培养基上形成菌落,但仍能保持其代谢活性与致病性(Liu et al., 2010),可在营养物质充分的条件下恢复可培养性(Shleeva et al., 2002; Mukamolova et al., 2003).因此,培养法无法准确检测环境样品中的分枝杆菌,需要开发新型的检测手段以辅助培养法对水环境中的分枝杆菌进行快速、准确的定量检测.近年来,环境样品中分枝杆菌的检测、鉴定技术在不断发展(Beumer et al., 2010; Aboagye et al., 2011; Kuznetsov et al., 2004),其中,发展于20世纪90年代末的qPCR技术实现了对分枝杆菌的快速定量检测.但基于DNA的qPCR检测技术的主要缺点在于不能够区分活性菌与非活性菌,会高估样品中活性菌的数量及相应的卫生学风险,甚至可能产生假阳性结果(Nocker et al., 2007).基于RNA的PCR检测技术是活性菌检测手段之一(Bergeron et al., 2011; Miller et al., 2011),相比DNA,RNA半衰期较短(Maurer,2006),能够在非活性菌内快速降解而在活性体内稳定存在,可很好地指示活性菌的存在.
基于此,本研究以环境中大量存在的分枝杆菌为研究对象,建立逆转录定量PCR(RT-qPCR)方法选择性检测环境样品中的活性分枝杆菌,并考察样品基质对该检测方法的影响,评估RT-qPCR方法对活性分枝杆菌的选择性,最后应用该方法检测实际环境样品并分析其灵敏性.
2 材料与方法(Materials and methods) 2.1 主要试剂与仪器本研究中使用的标准菌株购自中国普通微生物菌种保存中心,为耻垢分枝杆菌(Mycobacterium smegmatis,CGMCC1.2621).分枝杆菌的培养采用营养肉汤培养基:牛肉膏 5 g,蛋白胨 10 g,NaCl 5 g,去离子水 1000 mL,琼脂(固体培养基)15 g,121 ℃ 灭菌20 min.
RT-qPCR所需的试剂及仪器:逆转录试剂盒(TaKaRa Code:DRR 037A)、荧光定量PCR试剂盒SYBR® Premix Ex TaqTM(Code:DRR041A)均购自TaKaRa;相关的普通PCR和荧光定量PCR仪(Stepone)均购自ABI.
其他试剂与仪器:全基因组RNA提取试剂盒FastRNA® Pro Soil-Direct Kit(MP Cat:116070050),全基因组DNA提取采用FastDNA® Spin Kit for Soil(MP Cat:6560200),高速离心机购自德国Eppendorf 公司,Biosepc-mini核酸蛋白仪购自日本岛津公司.
2.2 实验方法 2.2.1 生长曲线的测定由于RNA在活性菌体内的拷贝数不稳定,为了确定其在分枝杆菌不同生长周期时的拷贝数,采用培养法、qPCR及RT-qPCR测定分枝杆菌的生长曲线.将1 mL培养至稳定期的分枝杆菌液接种到100 mL的营养肉汤培养基中,设3个平行样,在(35 ± 2)℃、150 r · min-1条件下培养.每隔一段时间取一次样,测定其细菌浓度(平板计数,计数结果用菌落形成单位(Colony formation unit,CFU)表示).此外,取1 mL样品于1.5 mL离心管中,12000 r · min-1下离心2 min,弃去上清液,贮存于-20 ℃下用于DNA的测定;取1 mL样品于1.5 mL离心管中,12000 r · min-1下离心2 min,弃去上清液,贮存于-80 ℃下用于RNA的测定.
2.2.2 qPCR引物的选择本研究采用hsp65基因作为目的基因.hsp65基因为分枝杆菌的热休克蛋白,广泛存在于分枝杆菌属的各种细菌中,相对较为保守,可用于分枝杆菌的鉴定、检测(谭笑,2012).本研究中采用的目的基因及相应的引物序列见表 1(Jjemba et al., 2010).
| 表 1 qPCR采用的目的基因及相应引物序列 Table 1 Gene targets and primers used for qPCR |
本研究中采用的标准品为大肠杆菌质粒标准品,操作方法见参考文献(胡秀华等,2008).提取的质粒DNA采用核酸蛋白仪测定DNA的浓度,按下述公式换算成基因拷贝数:
G=(n × Mw)/(NL×10-9)
式中,G为基因拷贝数(copies · ng-1);n为序列核苷酸的长度(bp);Mw为核苷酸质量,双链DNA的一对核苷酸的相对分子质量为660;NL为阿伏伽德罗常数,取值为6.02×1023.将提前纯化后的DNA标准品按10倍梯度稀释得到标准品,本研究中分枝杆菌标准品的浓度为1.4×102 copies · μL-1.
2.2.4 逆转录及qPCR本研究中分枝杆菌的逆转录(TaKaRa Code:DRR 037A)按照说明书提供的反应体系和反应程序进行(反应体系中总RNA的加入量为6.5 μL),反应得到的cDNA于-80 ℃ 保存,保存不宜超过2 d.
本研究中用于分枝杆菌qPCR反应体系为(20 μL):SYBRPremix Ex TaqTM 10 μL,上下游引物各0.5 μL(终浓度0. 25 μmol · L-1),DNA(标准品或样品)5 μL,双蒸水4.5 μL.qPCR 反应程序如下:94 ℃预变性1 min;94 ℃变性60 s,60 ℃退火60 s,72 ℃延伸60 s(收集荧光),45个循环;熔解曲线过程为:95 ℃变化1 min,从60 ℃ 开始每30 s 温度升高0.5 ℃,总共进行71 个循环,结束温度为95 ℃,反应结束之后于4 ℃ 保存.
2.2.5 实际样品及预处理方法本研究实际水样分别采自上海市某城区河道河水、某小区池塘水及某湖泊湖水,取样设备在每次实验前进行消毒,每个样品采样体积为3 L.样品置于保温箱(内置冰块)中保存,当天运回实验室,样品到实验室后在24 h内完成培养法及DNA、RNA的提取.水样中菌体的收集采用膜过滤法,取1 L样品经过0.45 μm醋酸纤维薄膜过滤后,将滤膜上的菌体收集.经PBS冲洗后,将洗涤液经10000 r · min-1离心10 min,弃去上清液,然后进行DNA及RNA的提取.实际样品分枝杆菌的培养采用Middlebrook 7H10 Agar培养基(BD,美国,Catalog:262710)(Jjemba et al., 2010),同时加入增强剂Middlebrook OADC Enrichment(BD,美国,Catalog:212351).检测时,每100 mL样品中加入500 μL质量分数为0.005%的氯化十六烷基吡啶(Cetylpyridinium chloride,CPC),氯化十六烷基吡啶可以在一定程度上抑制杂菌的生长.具体操作按照生产商提供的说明书进行.
3 结果与讨论(Results and discussion) 3.1 qPCR的线性检测区间与特异性本研究中分枝杆菌qPCR的线性检测区间为1.4×102~1.4×109 copies · μL-1.以标准品浓度的对数值为横坐标,反应的临界循环数为纵坐标作标准曲线图.由图 1可知,本研究中分枝杆菌标准品的线性可决系数(R2)大于0.99,PCR的扩增效率在100%~110%之间.溶解曲线呈单一的熔点峰,峰窄且尖.将qPCR产物进行凝胶电泳验证产物的单一性,结果如图 2所示,其中,阳性对照表示反应模板带有该目的基因的qPCR产物,阴性对照表示反应模板为去离子水的qPCR.由图 2可知,条带仅出现在440 bp处,引物二聚体不显著.上述结果表明,本研究中所使用的检测分枝杆菌RNA的qPCR方法检测限低、定量区间广泛、特异性强,符合qPCR标准曲线的要求.
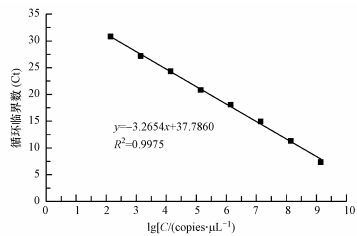 |
| 图 1 分枝杆菌的qPCR标准曲线 Fig. 1 qPCR st and ard curve for Mycobacterium spp. |
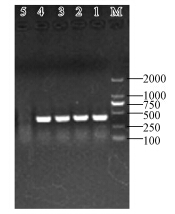 |
| 图 2 分枝杆菌的RT-qPCR产物电泳图(1. 标准品最高浓度(1.4×109 copies · μL-1)qPCR的产物,2、3. 稳定期分别为48 h和144 h时分枝杆菌的RT-qPCR产物,4. 阳性对照,5. 阴性对照) Fig. 2 Agarose gel electrophoresis profile of RT-qPCR products for Mycobacterium spp. |
用培养法、qPCR及RT-qPCR测定分枝杆菌的生长曲线,结果如图 3所示.由图 3a可知,本研究共培养144 h,培养8 h后进入对数生长期,到48 h后达到稳定期.由图 3b可知,在停滞期(0~8 h)内,单位细胞内DNA和RNA的拷贝数均迅速上升,分别达到13 copies · CFU-1和10 copies · CFU-1;进入对数生长期(8~48 h)后,单位细胞内的DNA和RNA拷贝数均迅速下降;稳定期(48~144 h),单位细胞内的DNA和RNA拷贝数均维持在约1 copy · CFU-1.这主要是由于在停滞期,单个细胞内会存在多个复制的染色体(Cooper et al., 1968),而到了稳定期后,单个分枝杆菌细胞内仅存在单个hsp65基因,因此,DNA和RNA拷贝数稳定在1 copy · CFU-1(Telenti et al., 1993).由此可知,本研究中,1个hsp65基因的RNA拷贝代表 1个活性分枝杆菌.
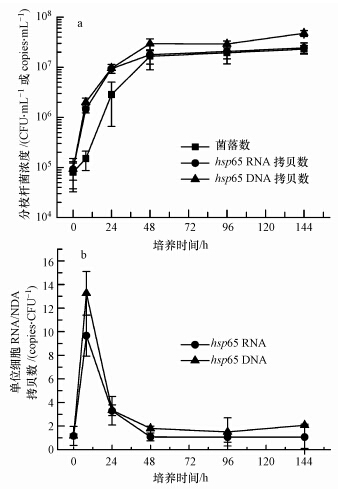 |
| 图 3 分枝杆菌的生长曲线(a)与单位菌落上hsp65基因的DNA/RNA拷贝数(b) Fig. 3 Growth curve of Mycobacterium smegmatis(a) and copy numbers of hsp65 gene DNA or RNA per CFU |
为了验证RT-qPCR对活性分枝杆菌检测的选择性,取1 mL处于稳定期的分枝杆菌在(35 ± 2)℃下培养48 h,在60 ℃热灭活30 min,作为非活性菌,该灭菌法对致病菌的灭菌效率可达97.3%~99.9%以上.将非活性菌与活性菌分别按照0 ∶ 1000、100 ∶ 900、500 ∶ 500、900 ∶ 100、1000 ∶ 0的比例投加,同时采用培养法、RT-qPCR和qPCR方法进行检测,结果如图 4所示.
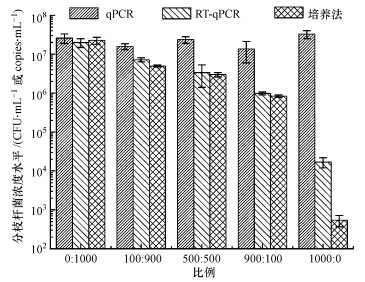 |
| 图 4 RT-qPCR和qPCR对非活性/活性分枝杆菌的检测结果 Fig. 4 RT-qPCR and qPCR detection results for dead/viable Mycobacterium smegmatis |
由图 4可知,qPCR无法很好地区分活性菌与非活性菌,说明经过加热灭活后分枝杆菌的DNA仍然存在,能够被检测到,qPCR高估了样品中活性分枝杆菌的浓度水平;而RT-qPCR的检测结果显著低于qPCR,与培养法相近.对于全部为非活性菌的样品,RT-qPCR方法的检测结果较qPCR下降了近3个数量级,即RT-qPCR能够有效去除99%的非活性分枝杆菌.值得注意的是,经过60 ℃灭活30 min后,仅去除了约5个数量级的分枝杆菌.已有研究报道,在热水(浴室、温泉、足浴)中检测到了分枝杆菌(Mangione et al., 2001;Falkinham III,2009;Winthrop et al., 2002).分枝杆菌的细胞膜富含脂类,细胞膜厚,具有疏水性,使得分枝杆菌对外界环境的抵抗性较强(Brennan et al., 1995; Daffé et al., 1997).有研究指出,60 ℃灭活30 min后(初始浓度为106 cells · mL-1),去除了约6个数量级的分枝杆菌(Gumber et al., 2009;Grant et al., 1996).本研究中当初始浓度为107 cells · mL-1时,去除率约为99.99%.值得注意的是,RT-qPCR的检测结果比培养法高约2个数量级.这可能是由于在高温下,部分分枝杆菌进入到了VBNC状态,无法在培养基上形成菌落,但其RNA仍存在.
3.4 样品中底物基质对RT-qPCR的影响为评估RT-qPCR检测实际环境样品时,底物基质对检测结果的影响,将稳定期的分枝杆菌(103~107 cells · mL-1)接种到10 mL经过高压灭菌(121 ℃、15 min)的去离子水和实际水样中,其中,实际水样采自上海市某河流.将投加后的样品经10000 r · min-1离心10 min收集菌体,提取全基因组RNA.将每组实验设置3个平行样品和阴性对照,检测结果如图 5所示.
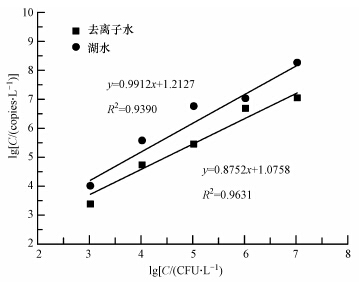 |
| 图 5 样品基质对RT-qPCR检测结果的影响 Fig. 5 Effects of matrix in samples on the detection results of RT-qPCR |
由图 5可知,当分枝杆菌接种到经高压灭菌的去离子水中时,RT-qPCR与培养法之间存在较好的线性关系(R2=0.9631);当分枝杆菌接种到灭菌后的实际水样中时,RT-qPCR与培养法的线性关系仍较强(R2=0.9390).但当细菌浓度较低时,RT-qPCR的检测结果与阴性对照相似.由此可知,本研究建立的RT-qPCR方法对不同样品的检测结果均较好,底物基质对本方法的影响较小,RT-qPCR能够用于实际样品中活性分枝杆菌的检测.
3.5 RT-qPCR检测实际样品的灵敏性采用RT-qPCR、qPCR和培养法检测实际样品(河水1~5、湖水6~10、池塘水11~14)中的分枝杆菌,结果如图 6所示.由图可知,3种不同检测方法的检测结果基本一致,但qPCR的检测结果显著高于培养法和RT-qPCR.这是因为环境样品中同时存在活性及非活性分枝杆菌,其DNA在细菌死后一段时间内会稳定存在,使得qPCR的检测结果偏高.此外,RT-qPCR的检测结果也略高于培养法的检测结果.这是由于不同分枝杆菌的生长周期不同,有些分枝杆菌生长缓慢无法形成可见的菌落,有些分枝杆菌则可能处于VBNC状态,无法采用培养法检测到,而这些细菌还保持逆转录活性,可以由RT-qPCR检测到.
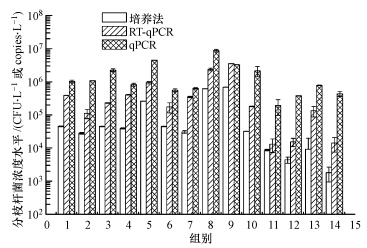 |
| 图 6 RT-qPCR、qPCR和培养法检测实际样品中的分枝杆菌 Fig. 6 Detection of Mycobacterium spp. by RT-qPCR,qPCR and culture-based method in environmental samples |
采用SPSS19对不同检测方法的检测结果进行单因素方差分析(one-way ANOVA),结果见表 2.不同检测结果之间的差异性采用p值表示,当p<0.05时,说明两种方法检测结果的差异性显著(95%置信区间);当p=1时,说明两种方法的检测结果完全相同.
| 表 2 不同检测方法对分枝杆菌检测结果的单因素方差分析(p值) Table 2 One-way ANOVA for results of Mycobacterium spp. by different detection methods |
由表 2可知,培养法与qPCR的检测结果之间存在显著差异性,而RT-qPCR与培养法、RT-qPCR与qPCR之间的差异性不显著.由此表明,qPCR方法由于检测的是所有的分枝杆菌(包括活性、非活性及VBNC状态),培养法仅检测到了具有可培养性的分枝杆菌,因此,常规的qPCR方法无法准确检测环境样品中具有活性的分枝杆菌,而RT-qPCR可以较准确地检测环境样品中具有逆转录活性的分枝杆菌.
将RT-qPCR、qPCR和培养法的检测结果进行回归分析,结果如图 7所示.由图 7可知,RT-qPCR/qPCR与培养法检测结果的可决系数(R2)分别为0.8845和0.6895.这表明RT-qPCR和qPCR对分枝杆菌的检测结果与培养法的检测结果均呈良好的线性关系,且与qPCR相比,RT-qPCR与培养法检测结果之间的线性关系较好.已有研究表明,qPCR的检测结果与培养法的检测结果之间具有明显的正相关性(Torvinen et al., 2010; Kralik et al., 2011).本研究中,采用RT-qPCR方法与培养法的的正向关系更显著.由此可见,与培养法相比,RT-qPCR方法能够快速(24 h以内)、准确(能够检测到所有具有逆转录活性的分枝杆菌)地检测环境样品中的分枝杆菌;与qPCR相比,RT-qPCR则在一定程度上去除了非活性(不具有逆转录活性的)的分枝杆菌,检测结果更为准确.因此,RT-qPCR检测方法能够满足环境样品中活性分枝杆菌的检测要求,且检测结果相比于传统培养法更为快速、准确.
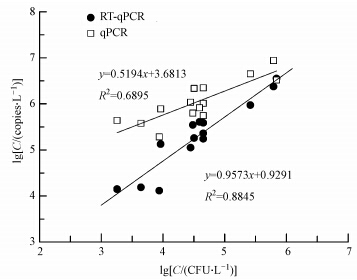 |
| 图 7 RT-qPCR /qPCR与培养法检测结果的回归分析 Fig. 7 Correlations between results detected by RT-qPCR,qPCR and culture-based method for Mycobacterium spp. by regression analysis |
1)采用培养法、qPCR及RT-qPCR方法检测不同比例的活性菌/非活性菌样品,RT-qPCR方法能够区分3个数量级的非活性菌,检测结果显著低于qPCR,因此,RT-qPCR方法能够有效区分活性菌与非活性菌.
2)比较去离子水和湖水不同底物基质对RT-qPCR检测方法的影响,结果表明,底物基质对该方法的影响不大,对于实际样品,RT-qPCR与培养法之间仍存在较好的线性关系,可决系数R2为0.9390.
3)采用本研究建立的RT-qPCR方法检测14个环境样品(包括河水、湖水及池塘水),结果表明,RT-qPCR的检测结果更接近于培养法;单因素方差分析表明,qPCR与培养法的检测结果之间存在显著差异性,而RT-qPCR与培养法检测结果之间的差异性不显著;RT-qPCR的检测结果与培养法的检测结果之间具有良好的正向关系,R2达0.8845.由此可以表明,RT-qPCR方法能够满足实际环境样品中活性分枝杆菌的快速检测要求,且其检测结果比培养法、qPCR更为准确.
| [1] | Aboagye G, Rowe M T. 2011. Occurrence of Mycobacterium avium subsp. paratuberculosis in raw water and water treatment operations for the production of potable water[J]. Water Research, 45(11): 3271-3278 |
| [2] | Bergeron P, Oujati H, Catalán Cuenca V, et al. 2011. Rapid monitoring of Escherichia coli and Enterococcus spp. in bathing water using Reverse Transcription-quantitative PCR[J]. International Journal of Hygiene and Environmental Health, 214(6): 478-484 |
| [3] | Beumer A, King D, Donohue M, et al. 2010. Detection of Mycobacterium avium subsp. paratuberculosis in drinking water and biofilms by quantitative PCR[J]. Applied and Environmental Microbiology, 76(21): 7367-7370 |
| [4] | Brennan P J, Nikaido H. 1995. The envelope of mycobacteria[J]. Annual Review of Biochemistry, 64(1): 29-63 |
| [5] | Cooper S, Helmstetter C E. 1968. Chromosome replication and the division cycle of Escherichia coli B-r[J]. Journal of Molecular Biology, 31(3): 519-540 |
| [6] | Daffé M, Draper P. 1997. The envelope layers of mycobacteria with reference to their pathogenicity[J]. Advances in Microbial Physiology, 39: 131-203 |
| [7] | Dubrou S, Konjek J, Macheras E, et al. 2013. Diversity, community composition, and dynamics of nonpigmented and late-pigmenting rapidly growing mycobacteria in an urban tap water production and distribution system[J]. Applied and Environmental Microbiology, 79(18): 5498-5508 |
| [8] | Falkinham III J O. 2009. Surrounded by mycobacteria: nontuberculous mycobacteria in the human environment[J]. Journal of Applied Microbiology, 107(2): 356-367 |
| [9] | Falkinham J O, Norton C D, LeChevallier M W. 2001. Factors influencing numbers of Mycobacterium avium, Mycobacterium intracellulare, and other mycobacteria in drinking water distribution systems[J]. Applied and Environmental Microbiology, 67(3): 1225-1231 |
| [10] | Fernandez-Rendon E, Cerna-Cortes J F, Ramirez-Medina M A, et al. 2012. Mycobacterium mucogenicum and other non-tuberculous mycobacteria in potable water of a trauma hospital: a potential source for human infection[J]. Journal of Hospital Infection, 80(1): 74-76 |
| [11] | Grant I R, Ball H J, Neill S D, et al. 1996. Inactivation of Mycobacterium paratuberculosis in cows' milk at pasteurization temperatures[J]. Applied and Environmental Microbiology, 62(2): 631-636 |
| [12] | Greenbery A, Trussell R Clesceri L. 2005. Standard methods for the examination of water and wastewater (20th ed.)[M]. American Public Health Association, American Water Works Association, Water Environment Federation. 254-255 |
| [13] | Gumber S, Whittington R J. 2009. Analysis of the growth pattern, survival and proteome of Mycobacterium avium subsp. paratuberculosis following exposure to heat[J]. Veterinary Microbiology, 136(1/2): 82-90 |
| [14] | 胡秀华, 何苗, 刘丽, 等. 2008. 水中轮状病毒实时定量 PCR 外标准品的构建[J]. 环境科学, 29(2): 380-385 |
| [15] | Jjemba P K, Weinrich L A, Cheng W, et al. 2010. Regrowth of potential opportunistic pathogens and algae in reclaimed-water distribution systems[J]. Applied and Environmental Microbiology, 76(13): 4169-4178 |
| [16] | Kralik P, Slana I, Kralova A, et al. 2011. Development of a predictive model for detection of Mycobacterium avium subsp. paratuberculosis in faeces by quantitative real time PCR[J]. Veterinary Microbiology, 149(1/2): 133-138 |
| [17] | Kuznetsov B A, Davydova M E, Shleeva M O, et al. 2004. Electrochemical investigation of the dynamics of Mycobacterium smegmatis cells' transformation to dormant, nonculturable form[J]. Bioelectrochemistry, 64(2): 125-131 |
| [18] | Liu Y M, Wang C, Tyrrell G, et al. 2010. Production of Shiga-like toxins in viable but nonculturable Escherichia coli O157: H7[J]. Water Research, 44(3): 711-718 |
| [19] | Mangione E J, Huitt G, Lenaway D, et al. 2001. Nontuberculous mycobacterial disease following hot tub exposure[J]. Emerging Infectious Diseases, 7(6): 1039-1042 |
| [20] | Marras T K, Daley C L. 2002. Epidemiology of human pulmonary infection with mycobacteria nontuberculous[J]. Clinics in Chest Medicine, 23(3): 553-567 |
| [21] | Maurer J J. 2006. PCR methods in foods[M]. Springer. 27-40 |
| [22] | Miller N D, Davidson P M, D'Souza D H. 2011. Real-time reverse-transcriptase PCR for Salmonella Typhimurium detection from lettuce and tomatoes[J]. LWT-Food Science and Technology, 44(4): 1088-1097 |
| [23] | Mukamolova G V, Kaprelyants A S, Kell D B, et al. 2003. Adoption of the transiently non-culturable state-a bacterial survival strategy?[J]. Advances in Microbial Physiology, 47: 65-129 |
| [24] | Nocker A, Sossa K E, Camper A K. 2007. Molecular monitoring of disinfection efficacy using propidium monoazide in combination with quantitative PCR[J]. Journal of Microbiological Methods, 70(2): 252-260 |
| [25] | Radomski N, Cambau E, Moulin L, et al. 2010. Comparison of culture methods for isolation of nontuberculous mycobacteria from surface waters[J]. Applied and Environmental Microbiology, 76(11): 3514-3520 |
| [26] | Shleeva M O, Bagramyan K, Telkov M V, et al. 2002. Formation and resuscitation of'non-culturable’cells of Rhodococcus rhodochrous and Mycobacterium tuberculosis in prolonged stationary phase[J]. Microbiology, 148(5): 1581-1591 |
| [27] | Stopa P J, Bartoszcze M A. 2000. Rapid Methods for Analysis of Biological Materials in the Environment[M]. Springer. 49-65 |
| [28] | 谭笑. 2012. 基于hsp65基因的PCR技术在检测临床标本中结核杆菌的应用[J]. 湖南师范大学学报(医学版), 9(4): 61-64 |
| [29] | Telenti A, Marchesi F, Balz M, et al. 1993. Rapid identification of mycobacteria to the species level by polymerase chain reaction and restriction enzyme analysis[J]. Journal of Clinical Microbiology, 31(2): 175-178 |
| [30] | Tortoli E. 2003. Impact of genotypic studies on mycobacterial taxonomy: the new mycobacteria of the 1990s[J]. Clinical Microbiology Reviews, 16(2): 319-354 |
| [31] | Torvinen E, Torkko P, Rintala A N. 2010. Real-time PCR detection of environmental mycobacteria in house dust[J]. Journal of Microbiological Methods, 82(1): 78-84 |
| [32] | Winthrop K L, Abrams M, Yakrus M, et al. 2002. An outbreak of mycobacterial furunculosis associated with footbaths at a nail salon[J]. New England Journal of Medicine, 346(18): 1366-1371 |
 2015, Vol. 35
2015, Vol. 35
