2. 北京工业大学 北京市水质科学与水环境恢复工程重点实验室, 北京 100124
2. Key Laboratory of Beijing for Water Quality Science and Water Environment Recovery Engineering, Beijing Institute of Technology, Beijing 100124
目前我国绝大部分的城市生活污水和工业废水都采用活性污泥法处理,其原理是微生物以水中污染物为底物,通过一系列生化反应的降解和同化而去除,所以其生理状态就成为决定处理效果的关键因素.污泥龄(SRT)是活性污泥比增长速率的倒数,它与活性污泥中微生物的生长状态、代谢活性、世代时间等关系密切.近十几年来,关于SRT对污水生物处理系统中种群组成、絮体结构、运行表现、水解酸化等方面影响的研究取得了长足进展(田兆运等,2012;Yoon et al., 2004).低溶解氧丝状菌污泥微膨胀是近年来提出的一项新的节能工艺,其核心思想是通过调低溶解氧浓度诱发丝状菌适度生长,利用丝状菌比表面积大和降解低浓度底物能力强的特点,在节能的基础上改善出水水质(彭永臻等,2008).到目前为止,对该工艺的研究多集中在调控方法以及出水效果上.Guo等通过缺氧/好氧(AO)反应器处理实际生活污水,实现了低氧丝状菌微膨胀的稳定维持(Guo et al., 2010);Peng等利用SBR反应器,开发了调控低氧丝状菌微膨胀状态下污泥沉降性的简易方法(Peng et al., 2012);Tian等考察了低氧丝状菌微膨胀状态下水中污染物的去除特性(Tian et al., 2011).作为活性污泥法的重要参数,SRT对微膨胀的影响还鲜有报道.本文着重考察SRT对丝状菌微膨胀系统的污泥沉降性、污染物去除和污泥特性等方面的影响,意在为该工艺的实际应用提供理论支持和技术指导.
2 材料与方法(Materials and methods) 2.1 试验用水来源和水质为便于分析机理,试验采用人工配水.配方为每升水中添加0.66 g CH3COONa·3H2O,0.17 g NH4Cl,0.04 g KH2PO4,0.38 g NaHCO3,0.04 g CaCl2·2H2O,0.08 g MgSO4和0.3 mL营养液(Smolders et al., 1994),C:N:P浓度比为24.4:5.1:1. 主要水质成分及其浓度如表 1所示.
| 表 1 废水水质 Table 1 Water quality of wastewater |
SBR反应器由有机玻璃制成,上部为圆柱形,下部为圆锥体,高700 mm,直径200 mm,总有效容积12 L.在器壁的垂直方向设置一排间隔10 cm的取样口,用于取样和排水.底部设有放空管,用于放空和排泥.采用刚玉微孔曝气器,由转子流量计调节曝气量(图 1所示).每周期由瞬时进水(3 L)、厌氧搅拌、好氧曝气、静止沉淀,滗水排放和闲置待机组成.曝气末段排放一定体积的泥水混合液来控制SRT.试验种泥取自本课题组培养的丝状菌微膨胀污泥,污泥容积指数(SVI)在330 mL · g-1左右,脱氮除磷性能良好.鉴于厌氧/好氧和单级好氧运行方式分别是抑制和引发丝状菌生长的有效手段(Peng et al., 2012),本研究开展了两组试验.第一组采用3个反应器,按照厌氧/好氧的方式运行;第二组采用4个反应器,按照单级好氧的方式运行.具体方式详见表 2.
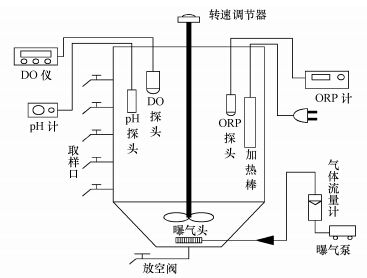 |
| 图 1 试验装置 Fig. 1 Schematic diagram of experimental equipment |
| 表 2 不同试验阶段的运行方式 Table 2 Operational model under different experimental stages |
COD、NH4+-N、NO2--N、NO3--N、PO43--P、SV、SVI和MLSS等均采用国家标准方法测定(国家环境保护总局,2002).水样经过定量滤纸过滤后迅速放到4 ℃冰箱内保存,并在3 h内测定.比好氧速率(SOUR)采用Joanna等提出的方法测定(Surmacz-Gorska et al., 1996).胞外聚合物(EPS)采用热提取法提取(Bura et al., 1998),多糖浓度采用苯酚-硫酸法测定(Dubois et al., 1956),蛋白质采用Folin-酚试剂法测定(Lowry et al., 1951).用于测定 SOUR和EPS 的污泥均取自好氧段的0.5 h时.微生物相采用OLYMPUS BX51型光学显微镜观察,粘度采用NDJ-79粘度仪测定,DO和pH用WTW 340i溶解氧仪在线检测.
3 结果与讨论(Results and discussion) 3.1 SRT对丝状菌微膨胀系统污泥沉降性的影响在两组试验中,MLSS都随剩余污泥排放量的增加而降低,具体情况如图 2所示.从图 2可见,第一组的平均MLSS依次为2576、2060和1650 mg · L-1,第二组的依次为2236、1883、1491和1223 mg · L-1,剩余污泥排放量显著地改变了反应器中的污泥浓度.SRT对污泥沉降性的影响较为复杂,大体上呈现出随着SRT的降低而改善的趋势,其原因分析如下.理论上认为,丝状菌是活性污泥的骨架,絮状菌附着其上形成活性污泥絮体,两者比例合适时沉降性能良好(Sezgin et al., 1978).动力学选择理论认为,在低底物浓度下,丝状菌因其半饱和常数较低而具有更大的比增殖速率(Chudoba et al., 1973),从而增加污泥絮体中丝状菌的含量而导致污泥沉降性的恶化.由于SRT与有机负荷成反比例关系,因此SRT越低时产生的高底物浓度环境对丝状菌的抑制也越明显.两组试验都验证了这一规律,但是第一组的SBR2和第二组的SBRD出现异常,其原因各不相同.
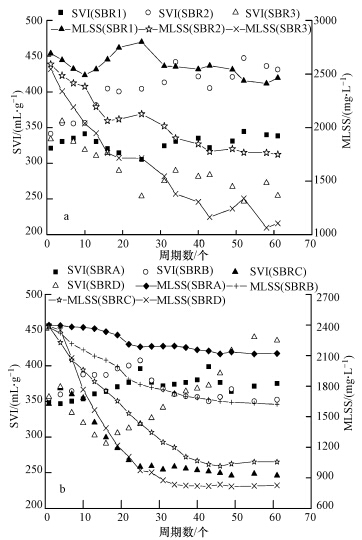 |
| 图 2 SRT对丝状菌微膨胀系统沉降性的影响(a. 厌氧/好氧运行方式;b. 单级好氧运行方式) Fig. 2 Impacts of SRT on sludge settleability under limited filamentous sludge bulking system(a. anaerobic/aerobic operation pattern; b. single aerobic operation pattern) |
厌氧/好氧运行时,SBR2的搅拌桨有一个桨板在试验进行中出现故障,为了维持相同的泥水混合状态转速稍快,这强化了搅拌时混合液的富氧效果.其厌氧段的DO浓度超过0.2 mg · L-1,而其它反应器的则不超过0.1 mg · L-1.Martins等曾经报道,厌氧段的微氧环境非常易于激发丝状菌生长(Martins et al., 2004).通过镜检观察,也发现SBR2中的丝状菌含量比其它反应器中的稍多,导致发生过度丝状菌膨胀.单级好氧运行时,SBRD的SRT仅为1.25 d,此时有机负荷高达0.64 kg · kg-1 · d-1,微生物大量分泌EPS,增加了沉降过程的阻力,导致污泥沉降性显著恶化(Sponza,2002).镜检发现此时活性污泥中的丝状菌含量没有显著增长,产生的膨胀属于黏性污泥膨胀.
3.2 厌氧/好氧下SRT对丝状菌污泥微膨胀系统脱氮除磷的影响第一组试验采用厌氧/好氧方式运行,曝气量控制在40 L · h-1,脱氮除磷过程如图 3所示.虽然好氧段的平均DO浓度很低(表 2所示),但是曝气段8 h的水力停留时间足够充分,确保硝化过程进行彻底,出水中都几乎没有氨氮.考虑到同化作用对氮的去除,计算得出好氧段各反应器的硝化速率分别为4.92、4.06和3.66 mg · L-1 · h-1,随SRT减小而下降.其主要原因是微生物量随SRT的减小而降低.MLSS的降低造成氨氮负荷增大,单位质量微生物可利用的底物增多,导致比硝化速率升高,分别为2.00、2.32和3.31 mg · g-1 · h-1.
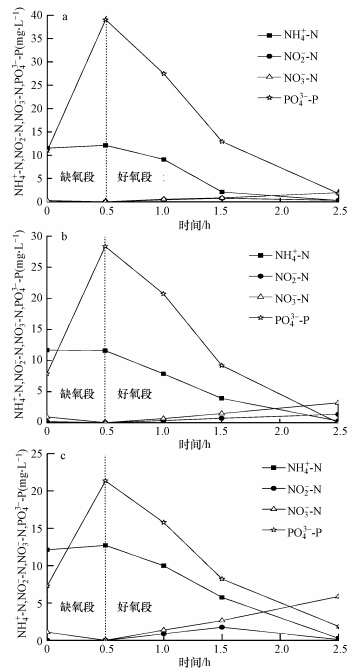 |
| 图 3 典型周期内SRT对厌氧/好氧方式运行下丝状菌微膨胀系统脱氮除磷过程的影响(a. SBR1,SRT = 12.5 d;b. SBR2,SRT = 6.25 d;c. SBR3,SRT = 3.125 d) Fig. 3 Impacts of SRT on nitrogen and phosphorus removal performance under limited filamentous sludge bulking system operated in anaerobic/aerobic pattern in a typical cycle(a. SBR1,SRT=12.5 d;b. SBR2,SRT=6.25 d;c. SBR3,SRT=3.125 d) |
另外,好氧段的平均DO浓度处于0.6~1.3 mg · L-1的低水平,有助于同步硝化反硝化(SND)的发生.计算各反应器的SND率(SND率=100%×SND去除的氮/被硝化的氨氮)分别为63.87%、31.54%和10.97%,随SRT减小而降低.这主要是因为SRT越高的反应器中污泥浓度越高,造成溶解氧的传质困难,容易产生缺氧微环境,从而促进了SND的发生(Mahendran et al., 2012).
生物除磷分为厌氧放磷和好氧(缺氧)吸磷两步骤,本试验从这两方面考察除磷表现.当SRT减少时,由于污泥浓度降低,厌氧释磷量和好氧吸磷量也都减少,但是单位聚磷菌可利用的底物浓度增加,其活性也逐渐上升,比释磷速率与比吸磷速率分别为22.74、23.40、25.41 mg · g-1 · h-1和7.51、8.10、8.81 mg · g-1 · h-1.各反应器进水中的PO43--P浓度相同,出水中都几乎为零,说明各剩余污泥中的磷含量接近相同.通过对磷进行物料衡算,发现各SBR剩余污泥中的含磷量分别为8.8%、4.6%和2.6%,随SRT减小而降低.
3.3 单级好氧下SRT对丝状菌污泥微膨胀系统脱氮除磷的影响第二组试验采用单级好氧方式运行,曝气时间和曝气量都与第一组相同,硝化过程如图 4所示.各反应器的硝化速率分别为4.14、3.55、2.39和1.17 mg · L-1 · h-1,随SRT减小而下降.与第一组试验不同的是比硝化速率随SRT减小而降低,分别为1.85、1.88、1.61、0.96 mg · g-1 · h-1.其主要原因是第二组试验采用单级好氧方式运行,这有助于培养去除有机物的异养菌,而不利于自养型硝化菌的生长.另外,SBRC和SBRD的SRT分别仅为2.5 d和1.25 d,有碍世代时间较长的硝化菌的富集.尽管如此,SBRC和SBRD中的氨氮的去除效果仍然良好,出水中几乎没有残留.其原因主要有以下两点:① 本试验进水碳氮比适中,一部分氨氮可被微生物同化吸收,并通过排放剩余污泥而去除;② 硝化菌分为氨氧化菌(AOB)和亚硝氮氧化菌(NOB)两大类,AOB比NOB的世代时间短,在SRT较低的条件下AOB比NOB具有竞争优势(Kowalchuk and Stephen, 2001),因此大部分氨氮被AOB氧化为亚硝氮,导致出现了明显的亚硝氮积累,如图 4(d)所示.
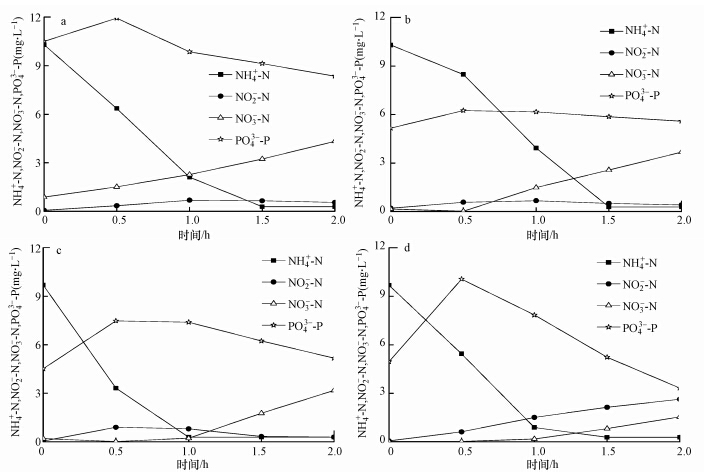 |
| 图 4 典型周期内SRT对单级好氧方式运行下丝状菌微膨胀系统脱氮除磷过程的影响(a. SBRA,SRT=10.0 d;b. SBRB,SRT=5.0 d;c. SBRC,SRT=2.5 d;d. SBRD,SRT=1.25 d) Fig. 4 Impacts of SRT on nitrogen and phosphorus removal performance under limited filamentous sludge bulking system operated as single aerobic pattern in a typical cycle(a. SBRA,SRT=10.0 d;b. SBRB,SRT=5.0 d;c. SBRC,SRT=2.5 d;d. SBRD,SRT=1.25 d) |
第二组试验在好氧过程中也发生了SND现象,计算得出各反应器的SND率分别为41.41%、33.79%、16.69%和1.30%,依然是随SRT减小而降低.进一步分析发现,第二组试验的SND率相比于第一组的有所下降,其主要原因有以下两点:① 第一组试验采用厌氧/好氧方式运行,在厌氧放磷过程中,聚磷菌会吸收大量的小分子有机酸转化为体内的聚羟基脂肪酸(PHA),这些贮存于菌体内的有机聚合物在好氧期间可为SND的反硝化过程提供内碳源,而采用单级好氧方式运行时则缺少这部分内碳源(Meyer et al., 2005);② 虽然两组试验的曝气量与曝气时间都相同,但是第二组试验好氧期间的平均DO要高于第一组(表 2所示,产生原因见3.4节讨论),较高的DO浓度不利于缺氧微环境的形成,直接抑制了SND的进行程度.
第二组试验未设厌氧段,除磷过程显著恶化.在好氧段初期,有机物浓度较高,且低溶解氧会产生厌氧微环境,进而引发轻微的释磷现象.陈滢等(2004)采用实际生活污水,在单级好氧SBR中实现过良好的除磷,Wang等(2009)以葡萄糖作碳源,也发现了类似现象.其原因是在单级好氧条件下,糖原(Glycogen)能够代替PHA为吸磷过程提供能量,但是其具体机理还有待进一步的研究.各反应器出水PO43--P浓度分别为8.14、7.47、6.62和3.80 mg · L-1,随SRT减小而降低.通过对磷进行物料衡算,得到污泥中的磷含量分别为0.6%、0.9%、1.0%和1.5%,不再随SRT减小而降低,且与第一组相比出现大幅下降.其原因是在单级好氧运行方式下,聚磷菌难以得到有效富集,活性污泥中的磷含量维持在低水平.SBRD的SRT仅为1.25 d,此时高有机负荷引发活性污泥分泌大量的EPS.由于EPS具有贮存磷的功能(周健等,2008),因此污泥中的磷含量在SRT过低的情况下出现小幅增加.
3.4 SRT对活性污泥特性的影响污泥沉降性、脱氮除磷之所以会随SRT而变化,是因为SRT改变了活性污泥的特性.本文以SOUR和EPS为主要表征参数,考察了污泥特性在不同SRT下的变化情况,结果如表 3所示.发现无论何种运行方式,SOUR都随SRT的减小而增加.其主要原因是SRT越小的反应器中污泥浓度也越小,造成在进水相同的条件下有机负荷较高,导致处于对数增长期的新陈代谢旺盛的微生物比例升高,反映到宏观上就是SOUR的增加.好氧段曝气量保持恒定,而除碳和硝化等耗氧过程主要发生在曝气初期1.5 h内,导致曝气后期混合液中DO浓度升高.各组试验的好氧段平均DO浓度如表 2所示,随SRT减小而升高.这是因为SOUR越高的活性污泥,其除碳和硝化等耗氧过程进行得越快,延长了曝气后期DO的上升时间.另一方面,SRT小的反应器中微生物量较低,其通过内源呼吸作用消耗的DO也较少.
| 表 3 不同试验阶段的污泥特性 Table 3 Sludge characteristics under different experimental stages |
EPS的主要成分是多糖、蛋白质、核酸和其他大分子有机物,其中多糖和蛋白质所占比重很大(Liu et al., 2010),故本试验在计算中忽略其它组分.在两组试验中发现当SRT减小时,多糖含量逐渐增加,蛋白质含量逐渐减小,多糖与蛋白质含量的比值增加,Liao等也曾发现类似现象(Liao et al., 2001).这是因为多糖与蛋白质含量的比值随SRT的变化与活性污泥的生长速率和菌群组成密切相关.EPS中蛋白质的主要来源是细胞内源呼吸的分解,SRT较低时微生物内源呼吸作用减弱,分解的蛋白质量减小.EPS中多糖的来源则主要是细胞的分泌和内源呼吸的分解(Andreadakis,1993).当SRT较低时活性污泥代谢旺盛,造成微生物不能把所有的碳源都用于自身生长,导致过量的碳源被转化为胞内聚合物或者EPS.当SRT较高时活性污泥代谢缓慢,一部分贮存在胞内聚合物或者EPS中的碳源会被分解,以用作微生物自身的生长.由于多糖是亲水性物质,蛋白质是疏水性物质,所以两者比值的升高也增加了活性污泥的亲水性(Frolund et al., 1994).SBRD的多糖与蛋白质的比值高达9.1,远大于其它试验阶段的比值.过高的糖含量增加了污泥的亲水性,反映到宏观上就是污泥变黏,泥水分离效果恶化.SBRD的污泥粘度高达2.45 mPa · s,而其它的污泥粘度分别为1.21、1.25和1.32 mPa · s.当微生物大量分泌EPS时,细胞之间的接触会受到阻碍(Schuler and Jang, 2007),镜检发现此时的污泥絮体疏松多孔.相反的,高SRT下形成的污泥絮体则密实紧凑.限于试验条件,本试验仅从宏观参数上考察了SRT对丝状菌污泥微膨胀系统的影响,诸如菌群组成、丝状菌丰度等微观参数都需要今后进一步的研究.
4 结论(Conclusions)1)当SRT位于5~12.5 d时,适当减小SRT有助于改善污泥的沉降性,丝状菌微膨胀系统可以维持在稳定的状态.厌氧/好氧运行时,搅拌过快产生的厌氧段微氧环境易引起丝状菌增殖而产生丝状菌膨胀;单级好氧运行时,SRT过小增加的EPS易增加污泥亲水性而产生黏性膨胀.
2)在丝状菌微膨胀状态下,当好氧段平均DO浓度在0.6~1.8 mg · L-1,水力停留时间为8 h时,硝化过程能够充分地进行,且有助于SND的发生.厌氧/好氧运行时,适当地减小SRT会提高污泥的比硝化速率,SND率和剩余污泥中的含磷量与SRT成正比,比释磷速率和比吸磷速率与SRT成反比;单级好氧运行时,减小SRT对比硝化速率没有明显提升作用,且SRT过低时很难富集硝化菌,出现亚硝态氮的积累.单级好氧运行体系也具有轻微的除磷能力,出水PO43--P浓度随SRT减小而降低.
3)活性污泥的特性与SRT密切相关.SRT与活性污泥的SOUR,EPS中多糖与蛋白质含量的比值,以及污泥粘度成反比.当SRT由大变小时,污泥絮体结构从密实向疏松转化.
| [1] | Andreadakis A D. 1993. Physical and chemical properties of activated sludge floc [J]. Water Research, 27(12): 1707-1714 |
| [2] | Bura R, Cheung M, Liao B, et al. 1998. Composition of extracellular polymeric substances in the activated sludge floc matrix [J]. Water Science and Technology, 37(4/5): 325-333 |
| [3] | 陈滢, 彭永臻, 杨向平, 等. 2004. 低溶解氧SBR除磷工艺研究 [J]. 中国给水排水, 20(8): 40-42 |
| [4] | Chudoba J, Grau P, Ottova V. 1973. Control of activated-sludge filamentous bulking-II. selection of microorganisms by means of a selector [J]. Water Research, 7(10): 1389-1398; 1399-1406; IN1-IN2 |
| [5] | Dubois M, Gilles K A, Hamilton J K, et al. 1956. Colorimetric method for determination of sugars and related substances [J]. Analytical Chemistry, 28(3): 350-356 |
| [6] | Frolund B, Keiding K, Nielsen P H. 1994. A comparative study of biopolymers from a conventional and an advanced activated sludge treatment plant [J]. Water Science and Technology, 29(7): 137-141 |
| [7] | Guo J H, Peng Y Z, Peng C Y, et al. 2010. Energy saving achieved by limited filamentous bulking sludge under low dissolved oxygen [J]. Bioresource Technology, 101(4): 1120-1126 |
| [8] | 国家环境保护总局. 2002. 水和废水监测分析方法(第4版)[M]. 北京: 中国环境科学出版社 |
| [9] | Kowalchuk G A, Stephen J R. 2001. Ammonia-oxidizing bacteria: a model for molecular microbial ecology [J]. Annual Review of Microbiology, 55(1): 485-529 |
| [10] | Liao B Q, Allen D G, Droppo I G, et al. 2001. Surface properties of sludge and their role in bioflocculation and settleability [J]. Water Research, 35(2): 339-350 |
| [11] | Liu X M, Sheng G P, Luo H W, et al. 2010. Contribution of extracellular polymeric substances (EPS) to the sludge aggregation [J]. Environmental Science and Technology, 44(11): 4355-4360 |
| [12] | Lowry O H, Rosebrough N J, Farr A L, et al. 1951. Protein measurement with the folin phenol reagent [J]. Journal of Biological Chemistry, 193(1): 265-275 |
| [13] | Mahendran B, Lishman L, Liss S N. 2012. Structural, physicochemical and microbial properties of flocs and biofilms in integrated fixed-film activated sludge (IFFAS) systems [J]. Water Research, 46(16): 5085-5101 |
| [14] | Martins A M P, Heijnen J J, van Loosdrecht M C M. 2004. Bulking sludge in biological nutrient removal systems [J]. Biotechnology and Bioengineering, 86(2): 125-135 |
| [15] | Meyer R L, Zeng R J, Giugliano V, et al. 2005. Challenges for simultaneous nitrification, denitrification, and phosphorus removal in microbial aggregates: mass transfer limitation and nitrous oxide production [J]. FEMS Microbiology Ecology, 52(3): 329-338 |
| [16] | 彭永臻, 郭建华, 王淑莹, 等. 2008. 低溶解氧污泥微膨胀节能理论与方法的发现、提出及理论基础 [J]. 环境科学, 29(12): 3342-3347 |
| [17] | Peng Z X, Peng Y Z, Yu Z B, et al. 2012. Control of sludge settleability and nitrogen removal under low dissolved oxygen condition [J]. Frontiers of Environmental Science & Engineering, 6(6): 884-891 |
| [18] | Schuler A J, Jang H. 2007. Causes of variable biomass density and its effects on settleability in full-scale biological wastewater treatment systems [J]. Environmental Science and Technology, 41(5): 1675-1681 |
| [19] | Sezgin M, Jenkins D, Parker D S. 1978. A unified theory of filamentous activated sludge bulking [J]. Water Pollution Control, 50(2): 362-381 |
| [20] | Smolders G J F, van der Meij J, van Loosdrecht M C M, et al. 1994. Stoichiometric model of the aerobic metabolism of the biological phosphorus removal process [J]. Biotechnology and Bioengineering, 44(7): 837-848 |
| [21] | Sponza D T. 2002. Extracellular polymer substances and physicochemical properties of flocs in steady and unsteady-state activated sludge systems [J]. Process Biochemistry, 37(9): 983-998 |
| [22] | Surmacz-Gorska J, Gernaey K, Demuynck C, et al. 1996. Nitrification monitoring in activated sludge by oxygen uptake rate (OUR) measurements [J]. Water Research, 30(5): 1228-1236 |
| [23] | Tian W D, Li W G, Zhang H, et al. 2011. Limited filamentous bulking in order to enhance integrated nutrient removal and effluent quality [J]. Water Research, 45(16): 4877-4884 |
| [24] | 田兆运, 谭学军, 王国华, 等. 2012. 泥龄对剩余污泥产率影响的中试研究[J]. 中国给水排水, 28(13): 109-111 |
| [25] | Wang D B, Li X M, Yang Q, et al. 2009. The probable metabolic relation between phosphate uptake and energy storages formations under single-stage oxic condition [J]. Bioresource Technology, 100(17): 4005-4011 |
| [26] | Yoon S H, Kim H S, Yeom I T. 2004. The optimum operational condition of membrane bioreactor (MBR): Cost estimation of aeration and sludge treatment [J]. Water Research, 38(1): 37-46 |
| [27] | 周健, 栗静静, 龙腾锐, 等. 2008. 胞外聚合物EPS在废水生物除磷中的作用[J]. 环境科学学报, 28(9): 1758-1762 |
 2015, Vol. 35
2015, Vol. 35


