2. 厦门大学生命科学学院, 厦门 361102;
3. 四川大学生命科学学院, 成都 610064;
4. 广东科学技术职业学院, 珠海 519090
2. College of Life and Science, Xiamen University, Xiamen 361102;
3. College of Life and Science, Sichuan University, Chengdu 610064;
4. Guangdong Institute of Science and Technology, Zhuhai 519090
环境雌激素(Environmental Estrogens,EEs)是主要的环境内分泌干扰物(Environmental Endocrine Disruptors,EEDs)之一,广泛分布于环境中,其对生物体与环境的危害已引起人们的广泛关注(Colborn et al., 1993).有报道表明,环境雌激素是引起生殖障碍(Tyler et al., 1998)、发育异常(Silver et al., 2006)、代谢紊乱(Miller et al., 2001)及某些恶性肿瘤发病率增加的主要原因之一(Fernandez et al., 2010),不仅影响当代人的身体健康,同时还威胁到后代的健康(Andersen et al., 2000).环境雌激素的种类多、危害大、分布广、作用机制复杂,且毒性和持久性强,可对人体健康和生态环境的平衡造成严重的影响(vom Saal et al., 2007),因此,需要建立快速、简便又灵敏的环境雌激素检测方法.
目前,国内外建立的检测环境雌激素的重组酵母测评系统(Recombinant Yeast Estrogen Assay)主要采用人雌激素受体基因片段(Human Estrogen Receptor,her)构建表达质粒,而用her构建的重组酵母不便于与体内实验进行相互印证,技术本身也有待完善(Routledge et al., 1996;何世华等,2002;Kaiser et al., 2010).环境雌激素易在水体中汇集,对水生生物危害严重(Tyler et al., 1998; Layton et al., 2000; Körner et al., 2001; Fernandez et al., 2007).常见的水生实验动物如斑马鱼(Danio rerio)、青鳉(Oryzias latipes)等已被广泛用于内分泌干扰物的相关研究(Hawkins et al., 2000; Menuet et al., 2004;Kamata et al., 2011),且有关雄鱼雌性化的相关报道不断增加(Sumpter et al., 1995,2013; Mills et al., 2005).而唐鱼(Tanichthys albonubes)是我国土著淡水鱼,易饲养,且对生存环境的变化反应灵敏,是用生物方法监测环境污染的一个极好的生物标志物(王瑞龙等,2006; Wang et al., 2010; Liu et al., 2012).
本研究利用唐鱼雌激素受体(Tanichthys albonubes estrogen receptor α,terα)基因片段构建表达质粒pGADT7/TERα,用人工合成爪蟾(Xenopus laevis)卵黄蛋白原基因雌激素效应元件(ere),连接β-半乳糖苷酶报告基因片段lacZ构建报告质粒pMP206/ERE-LacZ,将两个重组质粒转入带有营养缺陷筛选标记的AH109酵母菌株构建基因重组酵母,建立简便、快速且灵敏的定量检测环境雌激素系统.同时,选取天然雌激素17β-雌二醇(17β-estradiol,E2)、合成雌激素17α-乙炔基雌二醇(17α-ethynylestradiol,EE2)、异源雌激素双酚A(Bisphenol A,BPA)、壬基酚(nonylphenol,NP)及其混合物作为检测化合物,测定该酵母系统的灵敏性.检测系统可对环境样本中的雌激素类物质进行高通量筛选,并可与后期唐鱼体内实验进行相互印证,为环境评价和环境监测提供理论、技术上的支持.
2 材料与方法(Materials and methods) 2.1 实验材料与试剂唐鱼购自广州花地湾花鸟鱼虫市场,雄性体长约3 cm,体重约0.45 g,雌性体长约2.8 cm,体重约0.55 g.pMD18-T质粒、感受态大肠杆菌DH5α、限制性内切酶EcoRI、XhoI、PstⅠ、HindⅢ、XbaⅠ、DNA连接酶T4 DNA Ligase等购自宝生物工程(大连)公司,通用基因组DNA、小量试剂盒购自生工生物工程(上海)有限公司,质粒小量提取试剂盒、氨苄青霉素、卡那霉素购自Tiangen 生物试剂公司,二甲基亚砜(DMSO)、17β-雌二醇(E2)、17α-乙炔基雌二醇(EE2)、双酚A(BPA)及4-壬基酚(NP,各支链壬基酚的混合物)均购自美国Sigma-Aldrich公司,DO/-Leu/-Trp/-Ura、DO/-Leu Base、SD Base购自Clontech公司,β-半乳糖苷酶检测试剂盒购自威格拉斯生物技术有限公司,pGADT7质粒、AH109 酵母菌株由华南师范大学生命科学学院阳成伟教授惠赠,pMP206质粒由江南大学生物工程学院王正祥教授惠赠.
2.2 主要仪器设备My Cycler型PCR仪(美国Bio-RAD公司),CT15RT高速冷冻离心机(上海天美科学仪器有限公司),Bio-CAPT software凝胶成像系统(Vilbar Lourmat公司),Biophotometer6131核酸蛋白检测仪(Eppendorf),PHS-3C型酸度计(上海精密科学仪器有限公司).
2.3 表达质粒构建选取本实验室克隆的唐鱼雌激素受体terα的cDNA序列为模板,设计合成特异性引物,上游引物为5′-A GAATTC ATGGTGATGTCTGGAGGGCA-3′;下游引物为5′-A CTCGAG TTAGGTATCTGGACTTTGGCTAA-3′,引物5′端分别设计EcoRI和XhoI酶切位点(下划线所示),两端各加一个保护碱基.PCR扩增terα基因完整开放阅读框(ORF)片段,反应体系为:1×Buffer,0.2 mmol · L-1 dNTP Mixture,0.4 μmol · L-1上下游引物,cDNA 2.5 μL,0.5 U TaKaRa LA Taq.反应程序为:94 ℃预变性3 min;94 ℃变性30 s,58 ℃退火30 s,72 ℃延伸2 min,30个循环;72 ℃延伸10 min.将所得目的片段与克隆载体pMD18-T 连接,其连接反应体系为:pMD18-T Vector 0.5 μL,Solution(含连接酶、Buffer)4.0 μL,terα片段5.5 μL,总体系为10.0 μL.将上述组分混匀,于16 ℃循环水浴反应过夜,经转化、筛选,获得重组质粒pMD18-T/ TERα,该质粒经EcoRI和XhoI双酶切,胶回收terα片段并与质粒pGADT7连接,连接产物经转化后,挑单克隆菌,用terα上下游引物进行菌液PCR,筛选阳性克隆,并进一步用酶切鉴定(酶切体系为:1×H Buffer,pGADT7/TERα 5.0 μL,EcoRI 1.0 μL,总体系为10 μL),获得含有terα基因的重组表达质粒,命名为pGADT7/TERα,序列由华大基因公司测序,测序结果用GenBank BLAST分析.
2.4 报告质粒的构建报告质粒的构建参照陈春波等(2005)的方法.人工合成爪蟾卵黄蛋白原基因雌激素效应元件ere,在其5′和3′端分别增加HindⅢ和PstⅠ酶切黏性末端(下划线所示),同时对5′端进行磷酸化修饰.序列如下:5′-p AGCTT AAAGTCAGGTCACAGTGACCTGATCAAATCTAGAAGATCCAAAGTCAGGTC ACAGT GACCTGATCAAA CTGCA -3′;5′-pGTTTGATCAGGTCACTGTGACCTGACTTTGGATCTTCTAGATT TGATCAGGTCACTGTGACCTGACTTTA-3′.按陈春波等(2005)的方法使2条ere相互配对形成双链DNA.将该片段与线性化的pMP206载体相连接,使其置于细胞色素氧化酶基因启动子(CYC1)上游构建质粒pMP206/ERE-LacZ,选用XbaⅠ进行酶切鉴定,反应体系为:1×M Buffer,0.1% BSA 1.0 μL,pMP206/ERE-LacZ 3.0 μL,XbaⅠ0.5 μL,总体积10 μL.挑选酶切鉴定为阳性的质粒pMP206/ERE-LacZ送华大基因公司测序,测序引物为5′-GGATGTGCTGCAAGGCGATTAAGT-3′.
2.5 酵母转化采用乙酸锂法(LiAC)将重组质粒pGADT7/TERα转化到酵母AH109,转化产物涂布于SD/-Leu选择培养基平板上,30 ℃恒温培养3~4 d,至酵母菌落直径达2~3 mm左右.用保鲜膜密封置于4 ℃冰箱中保存,将此酵母菌株命名为AHpTERα.进一步把pMP206/ERE-LacZ质粒转化到AHpTERα酵母菌株,转化产物涂布于SD/-Leu/-Ura选择培养基平板上培养3~4 d,选单克隆菌,小量提取法提取酵母质粒,并用PCR法鉴定.用于鉴定唐鱼雌激素受体基因的引物为克隆TERα时的引物,反应条件及体系同2.3节所述.用于鉴定pMP206/ERE的上游引物为5′-AGCGAGGAAGCGGAAGAG-3′,下游引物为5′-TGGGTACGCCAGGGTTTT-3′,其反应体系为:1×Buffer,0.2 mmol · L-1 dNTP Mixture,0.4 μmol · L-1上下游引物,质粒 1 μL,0.5 U TaKaRa LA Taq,PCR反应程序为:94 ℃预变性3 min;94 ℃变性45 s,55 ℃ 退火45 s,72 ℃延伸1 min,30个循环;72 ℃延伸10 min.PCR均为阳性的酵母为重组基因酵母,命名为AHpTERα/ERE.
2.6 重组酵母诱导及β-半乳糖苷酶活性测定用DMSO配置不同浓度的E2、EE2、NP、BPA溶液,在每个Eppendorf管中加入培养至光密度值OD600读数为 0.1~0.6的菌液995 μL,再分别加入5 μL不同浓度的各试验化学物质(溶解在DMSO中),并以10 μL DMSO做空白对照,不同浓度17β-雌二醇(E2)作为阳性对照.将加入了酵母和各试验化学物质的Eppendorf管放置于 30 ℃的恒温振荡器里振荡培养18 h,测定并记录培养液的OD600,取1 mL培养液置于1.5 mL离心管中,14000 r · min-1 离心30 s,去上清,加入1 mL Z Buffer(Na2HPO4 · 12H2 O 21.5%,NaH2PO4 · 2H2O 6.22%,KCl 0.75%,MgSO4·7H2O 0.25%),离心并弃上清.加入100 μL Z Buffer重悬沉淀,离心管中即为已诱导完毕的待测酵母.向每个离心管中加100 μL 1×ULB(Universal Lysis Buffer),恒温振荡裂解酵母细胞5 min,14000 r · min-1离心30 s,取上清依次加入到96孔板中.在96孔板的每个孔中加入100 μL 新鲜配置的邻硝基苯β-D-半乳吡喃糖苷(ONPG)底物溶液,将96孔板置于微孔板振荡器上在室温下进一步恒温培养1 h,立即开始计时,当孔板中的培养液呈现明显的黄色时记录下每个孔板的作用时间,当溶液都变黄时,取出96孔培养板,在酶标仪上测定 405 nm波长下的吸光度,计算酶活力,每一个处理重复3次.酶活力计算公式为:
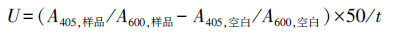
式中,U为β-半乳糖苷酶活力,t为酶反应时间(min),A405为405 nm波长下的吸光值,A600为600 nm波长下的吸光值.
2.7 数据处理与分析运用Graphpad prism5.01软件作图,用SPSS16.0软件分析所得数据,所有数据均以平均值±标准差表示.
3 结果(Results) 3.1 测序鉴定将PCR鉴定后的pGADT7/TERα和pMP206/ERE-LacZ质粒送华大基因公司进行测序,pGADT7/TERα核苷酸序列分析结果(图 1a)显示:插入pGADT7的DNA片段的核苷酸序列全长1824 bp,与本课题组已克隆的TERα基因相应核苷酸序列同源性为99%.pMP206/ERE-LacZ核苷酸序列分析结果显示,ERE(单下划线部分)序列已插入到CYC1(双下划线部分)启动子的上游,波浪线部分为报告基因lacZ序列(图 1b).表明表达质粒与报告质粒构建成功.
 |
| 图 1 表达质粒pGADT7/TERα(a)和报告质粒pMP206/ERE-LacZ(b)的测序结果 Fig.1 Sequence analysis of the pMD18-T/TERα plasmid(a) and pMP206/ERE-LacZ plasmid(b) |
图 2为重组酵母细胞的PCR电泳图,PCR产物经1.2%琼脂糖凝胶电泳,可看到大小约为1800 bp的特异性条带(图 2中2、3泳道所示),此为唐鱼雌激素受体基因terα片段.图 2中4、5泳道可见600 bp左右的两条特异性条带,此为pMP206/ERE-LacZ质粒中的部分序列片段,说明该重组酵母含有雌激素受体和雌激素反应元件,可用于环境雌激素的检测,可进行下一步的诱导验证.
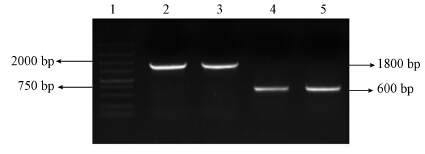 |
| 图 2 重组酵母AHpTERα/ERE的PCR 鉴定(1:2000 bp Marker;2,3:terα基因片段;4,5:ere基因片段) Fig.2 PCR identification for the recombinant yeast AHpTERα/ERE |
由图 3可见,重组酵母AHpTERα/ERE在不同浓度E2的诱导下,β-半乳糖苷酶的活性随E2浓度的升高而呈现出“S”型的剂量-效应关系,与DMSO对照组相比,E2浓度大于10-3 nmol · L-1时,E2诱导的重组酵母表现出β-半乳糖苷酶活性增强的现象,说明E2可以诱导该重组酵母.在E2浓度为10 nmol · L-1时重组酵母产生最大效应,随后逐渐稳定,其EC50为(0.521±0.700)nmol · L-1.由图 4可见,重组酵母在不同浓度EE2、NP、BPA及E2(阳性对照)的诱导下,均呈现出剂量-效应关系,且灵敏度表现为E2>EE2>NP>BPA.各化合物的EC50值见表 1.表明本研究所构建的基因重组酵母测评系统较为稳定,能较灵敏地评价环境雌激素化合物,初步判断此基因重组酵母可应用于环境雌激素的检测.
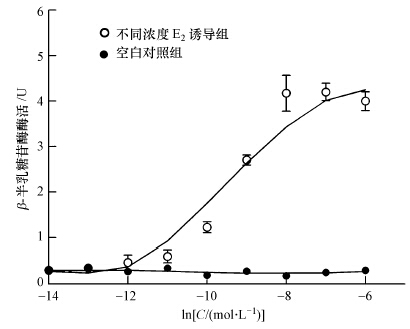 |
| 图 3 E2对重组酵母β-半乳糖苷酶活性诱导的剂量-效应曲线 Fig.3 Dose-response curves of recombinant yeast AHpTERα/ERE induced by E2 |
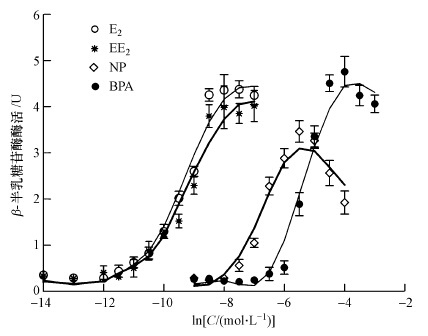 |
| 图 4 不同化合物对重组酵母β-半乳糖苷酶活性诱导的剂量-效应曲线 Fig.4 Dose-response curves of recombinant yeast induced by different chemicals |
| 表 1 不同化合物的EC50值 Table 1 EC50 values of different chemicals |
随着全球工业化的迅速发展,每年都有大量新合成的化学物质释放到环境中,其中包括一些环境雌激素.环境雌激素种类多,化学结构多样,存在与其他化合物联合作用的问题,增加了其危害作用的复杂性(Silva et al., 2002).利用重组基因酵母系统筛选环境雌激素类物质已被广为应用,是一种高效、稳定、经济的方法(Katzenellenbogen et al., 2000),除采用人雌激素受体基因片段外,已有不少学者采用鱼雌激素受体基因片段来构建重组酵母,用于环境雌激素的检测.例如,Le Guevel和Pakdel(2001)采用虹鳟鱼(Oncorhynchus mykiss)雌激素受体基因片段ER构建重组酵母,在E2的诱导下其EC50值为5.2 nmol · L-1;Fu等(2007)采用台湾铲颌鱼(Varicorhinus barbatulus)雌激素受体基因片段erα 构建的重组酵母细胞检测E2、BPA、NP及4-叔辛基酚(4tOP)的EC50值分别为4.1、10000、640和410 nmol · L-1;Kamata等(2011)采取日本青鳉(Oryzias latipes)雌激素受体基因构建重组酵母检测E2,发现与利用人雌激素受体基因片段构建的重组酵母相比具有更强的灵敏度.本研究所构建的重组酵母在E2的诱导下,其灵敏度略高于以上几位学者研究的结果,可能与不同物种er敏感性差异有关,也与唐鱼个体特性有关.例如,唐鱼对一些环境污染物如重金属(王瑞龙等,2006)、农药毒性(王瑞龙等,2007;杨志聪等 2007)响应敏感(Jing et al., 2013).在不同浓度EE2、NP、BPA及E2的诱导下,均呈现出剂量-效应关系,表明该系统对雌激素效应的化合物的检测非常灵敏,灵敏度表现为E2>EE2>NP>BPA,与Balsiger等(2010)所构建的重组酵母检测情况相似.表明利用唐鱼雌激素受体基因构建重组酵母进行环境雌激素物质的筛选和监测是有效的,建立高效、方便、快捷的环境雌激素检测方法是值得探索的.
与其他环境雌激素的检测系统相比,本系统最大的创新在于利用土著鱼的雌激素受体基因片段构建重组酵母.而目前较多学者采用哺乳动物er进行环境雌激素类物质的检测,但对于某些雌激素类化合的检测,鱼的er比哺乳动物er具有更强的灵敏性(Dang,2010).例如,Matthews 等(2000)研究表明,BPA、t-辛基酚(OP)及o,p′-滴滴涕(o,p′-DDT)与虹鳟erα的结合能力约比人和老鼠erα 受体高10倍.Fent等(2001)对o,p′-DDT相关化学毒性的研究表明,鱼的体外细胞毒性往往与体内毒性相关,由于鱼类与哺乳类相关基因的差异较大,建议对鱼类进行风险评估时最好利用鱼类特有的系统.野生唐鱼对水环境要求较高,因此,可探究其雌激素受体基因片段对其环境雌激素的敏感性.
虽然重组基因酵母法有许多优点,但该方法没有考虑化合物代谢作用及其在生物体内的慢性累积效应,而这种影响在活体中可能成为十分重要的一个因素.此外,已知具有内分泌干扰效应的化合物中,并不是所有化合物都是通过和雌激素受体结合而产生效应,因此,重组基因酵母技术还有待进一步的应用、验证和完善.本实验室构建的重组酵母测评系统可用于快速初筛环境雌激素,以确定是否有必要进行进一步的化学分析,今后可与唐鱼体内卵黄蛋白原实验、胚胎致畸实验和种群生态实验相互印证,构建一套以唐鱼为实验动物的完整的检测环境雌激素效应物的体系,可检测和防止内分泌干扰物对野生动物潜在的影响.
5 结论(Conclusions)1)本研究通过构建含唐鱼雌激素受体基因(terα)的表达质粒pGADT7/TERα和由ere调控β-半乳糖苷酶表达的报告质粒pMP206/ERE-LacZ,并将其转入营养缺陷酵母AH109中,成功构建了唐鱼terα基因重组酵母AHpTERα/ERE.
2)所构建的基因重组酵母AHpTERα/ERE在不同浓度E2的诱导下与β-半乳糖苷酶的活性呈现出明显的剂量-效应曲线,其EC50为(0.521±0.700)nmol · L-1,在不同浓度EE2、NP、BPA及E2(阳性对照)的诱导下,均呈现出剂量-效应关系,且灵敏度表现为E2>EE2>NP>BPA.这一系统的高灵敏性体现了唐鱼作为一种实验动物的优越性.初步确定该基因重组酵母可应用于环境、食品中雌激素的检测.
致谢(Acknowledgements): 华南师范大学生命科学学院阳成伟老师、陈世文老师、管盺、贾佳、赵文娟、陈纯纯等同学在实验中给予了很大的帮助,在此表示感谢!
| [1] | Andersen A G,Jensen T K,Carlsen E,et al.2000.High frequency of sub-optimal semen quality in an unselected population of young men[J].Human Reproduction,15(2): 366-372 |
| [2] | Balsiger H A,de la Torre R,Lee W Y,et al.2010.A four-hour yeast bioassay for the direct measure of estrogenic activity in wastewater without sample extraction,concentration,or sterilization[J].Science of the Total Environment,408(6): 1422-1429 |
| [3] | 陈春波,罗方妮,李湘鸣.2005.环境雌激素调控的β-半乳糖苷酶酵母细胞的建立[J].扬州大学学报: 农业与生命科学版,26(3): 21-24 |
| [4] | Colborn T,vom Saal F S,Soto A M.1993.Developmental effects of endocrine-disrupting chemicals in wildlife and humans[J].Environmental Health Perspectives,101(5): 378-384 |
| [5] | Dang Z C.2010.Comparison of relative binding affinities to fish and mammalian estrogen receptors: the regulatory implications[J].Toxicology Letters,192(3): 298-315 |
| [6] | Fent K.2001.Fish cell lines as versatile tools in ecotoxicology: Assessment of cytotoxicity,cytochrome P4501A induction potential and estrogenic activity of chemicals and environmental samples[J].Toxicology in Vitro,15(4/5): 477-488 |
| [7] | Fernandez M P,Campbell P M,Ikonomou M G,et al.2007.Assessment of environmental estrogens and the intersex/sex reversal capacity for chinook salmon (Oncorhynchus tshawytscha) in primary and final municipal wastewater effluents[J].Environment International,33(3): 391-396 |
| [8] | Fernandez S V,Russo J.2010.Estrogen and xenoestrogens in breast cancer[J].Toxicologic Pathology,38(1): 110-122 |
| [9] | Fu K Y,Chen C Y,Chang W M.2007.Application of a yeast estrogen screen in non-biomarker species Varicorhinus barbatulus fish with two estrogen receptor subtypes to assess xenoestrogens[J].Toxicology in Vitro,21(4): 604-612 |
| [10] | Hawkins M B,Thornton J W,Crews D,et al.2000.Identification of a third distinct estrogen receptor and reclassification of estrogen receptors in teleosts[J].Proceedings of the National Academy of Sciences of the United States of America,97(20): 10751-10756 |
| [11] | 何世华,梁增辉,战威,等.2002.环境雌激素重组酵母测评系统的建立[J].环境与健康杂志,19(1): 57-59 |
| [12] | Jing J,Liu H C,Chen H H,et al.2013.Acute effect of copper and cadmium exposure on the expression of heat shock protein 70 in the Cyprinidae fish Tanichthys albonubes [J].Chemosphere,91(8): 1113-1122 |
| [13] | Kaiser C,Uhlig S,Gerlach T,et al.2010.Evaluation and validation of a novel Arxula adeninivorans estrogen screen (nAES) assay and its application in analysis of wastewater,seawater,brackish water and urine[J].Science of the Total Environment,408(23): 6017-6026 |
| [14] | Kamata R,Shiraishi F,Nakajima D,et al.2011.Estrogenic effects of leachates from industrial waste landfills measured by a recombinant yeast assay and transcriptional analysis in Japanese medaka[J].Aquatic Toxicology,101(2): 430-437 |
| [15] | Katzenellenbogen B S,Choi I,Delage-Mourroux R,et al.2000.Molecular mechanisms of estrogen action: selective ligands and receptor pharmacology[J].The Journal of Steroid Biochemistry and Molecular Biology,74(5): 279-285 |
| [16] | Körner W,Spengler P,Bolz U,et al.2001.Substances with estrogenic activity in effluents of sewage treatment plants in southwestern Germany.2.Biological analysis[J].Environmental Toxicology and Chemistry,20(10): 2142-2151 |
| [17] | Layton A C,Gregory B W,Seward J R,et al.2000.Mineralization of steroidal hormones by biosolids in wastewater treatment systems in Tennessee U.S.A[J].Environmental Science & Technology,34(18): 3925-3931 |
| [18] | Le Guevel R,Pakdel F.2001.Assessment of oestrogenic potency of chemicals used as growth promoter by in-vitro methods[J].Human Reproduction,16(5): 1030-1036 |
| [19] | Liu H C,Chen H H,Jing J,et al.2012.Cloning and characterization of the HSP90 beta gene from Tanichthys albonubes Lin (Cyprinidae): Effect of copper and cadmium exposure[J].Fish Physiology and Biochemistry,38(3): 745-756 |
| [20] | Matthews J,Celius T,Halgren R,et al.2000.Differential estrogen receptor binding of estrogenic substances: a species comparison[J].The Journal of Steroid Biochemistry and Molecular Biology,74(4): 223-234 |
| [21] | Menuet A,Le Page Y,Torres O,et al.2004.Analysis of the estrogen regulation of the zebrafish estrogen receptor (ER) reveals distinct effects of ERalpha,ERbeta1 and ERbeta2[J].Journal of Molecular Endocrinology,32(3): 975-986 |
| [22] | Miller D, Wheals B B, Beresford N, et al. 2001. Estrogenic activity of phenolic additives determined by an in vitro yeast bioassay[J]. Environ Health Perspect, 109 (2): 133-138 |
| [23] | Mills L J,Chichester C.2005.Review of evidence: are endocrine-disrupting chemicals in the aquatic environment impacting fish populations?[J]. Science of the Total Environment,343(1/3): 1-34 |
| [24] | Routledge E J,Sumpter J P.1996.Estrogenic activity of surfactants and some of their degradation products assessed using a recombinant yeast screen[J].Environmental Toxicology and Chemistry,15(3): 241-248 |
| [25] | Silva E,Rajapakse N,Kortenkamp A.2002.Something from "nothing"-eight weak estrogenic chemicals combined at concentrations below NOECs produce significant mixture effects[J].Environmental Science & Technology,36(8): 1751-1756 |
| [26] | Silver N,Best S,Jiang J,et al.2006.Selection of housekeeping genes for gene expression studies in human reticulocytes using real-time PCR[J].BMC Molecular Biology,7: 33 |
| [27] | Sumpter J P,Jobling S.1995.Vitellogenesis as a biomarker for estrogenic contamination of the aquatic environment[J].Environmental Health Perspectives,103(Suppl 7): 173-178 |
| [28] | Sumpter J P,Jobling S.2013.The occurrence,causes,and consequences of estrogens in the aquatic environment[J].Environmental Toxicology and Chemistry,32(2): 249-251 |
| [29] | Tyler C R,Jobling S,Sumpter J P.1998.Endocrine disruption in wildlife: A critical review of the evidence[J].Critical Reviews in Toxicology,28(4): 319-361 |
| [30] | vom Saal F S,Akingbemi B T,Belcher S M,et al.2007.Chapel Hill bisphenol A expert panel consensus statement: integration of mechanisms,effects in animals and potential to impact human health at current levels of exposure[J].Reproductive Toxicology,24(2): 131-138 |
| [31] | Wang R L,Gao Y,Zhang L H,et al.2010.Cloning,expression,and induction by 17-β estradiol (E2) of a vitellogenin gene in the white cloud mountain minnow Tanichthys albonubes[J].Fish Physiology and Biochemistry,36(2): 157-164 |
| [32] | 王瑞龙,马广智,方展强.2006.铜、镉、锌对唐鱼的急性毒性及安全浓度评价[J].水产科学,25(3): 117-120 |
| [33] | 王瑞龙,陈玉明,徐军,等.2007.氯氰菊酯对唐鱼肝和鳃组织超氧化物歧化酶 (SOD) 活性的影响[J].生态环境,16(3): 790-793 |
| [34] | 杨志聪,姚静,方展强.2007.DDTs 对唐鱼仔鱼的急性毒性及安全浓度评价[J].实验动物与比较医学,27(2): 123-126 |
 2015, Vol. 35
2015, Vol. 35


