20世纪70年代,长庆油田公司在陇东地区成立并逐渐发展壮大,目前已成为全国第一大油田,有“西部大庆”之称.但在石油勘探、开采、运输及储存过程中不可避免地污染了土壤生态系统,造成陇东产油区极其严重的环境问题(张胜等,2008).尤其是落地原油的污染造成了土壤理化特性变化,具体表现在土壤的孔隙结构堵塞、结构破坏、透水性降低、土壤速效磷、氮含量减少等方面,导致土壤有机质的碳氮比(C/N)和碳磷比(C/P)失衡,进而破坏了石油污染土壤的综合肥力(刘五星等,2007).土壤肥力是反映土壤保持生物生产力、环境质量及动植物健康能力的土壤内在属性,是许多物理、化学和生物学性质及其形成过程的综合体现(黄婷等,2010).而目前对于土壤综合肥力这一科学概念缺乏严格的定义,特别是缺少数量化的指标,通常以土壤养分含量的大小来衡量土壤肥力的高低,因此,土壤养分成为土壤肥力评价的主要指标(骆伯胜等,2004).近年来,聚类分析、因子分析、主成分分析和模糊数学等分析方法被应用到土壤肥力的综合评价上(吕晓男等,1999;张兴昌,1993;曹承绵等,1983;骆伯胜等,2004;吕巧灵等,2006;黄婷等,2010),并通过对大量信息的处理,得出反映土壤肥力高低的综合性指标.
目前,石油污染土壤的微生物修复技术已成为最为经济有效的污染治理技术,它具有环境影响小,且无二次污染,能最大限度地降低污染物的浓度等优点(姚治华等,2006).通过提供微生物生长所需要的氮磷等营养元素,或改善微生物生长的环境条件,来刺激土著微生物的生长,进而加速石油烃的降解(Ding et al., 2002). 由于陇东黄土高原石油污染区生态修复研究尚处于起步阶段,以往的报道多集中在土壤理化性质等方面,有关添加土著石油降解菌菌剂及现场原位修复技术,并辅以主成分分析方法对原位修复前后土壤肥力进行分析的报道却相对较少(刘五星等,2007;姚治华等,2006;Ding et al., 2002;宋歌等,2007).
为此,本研究以陇东黄土高原腹地的庆阳市西峰区董志乡采二炼油厂的石油污泥为研究对象,通过添加土著石油降解菌菌剂及复合肥添加剂,开展为期105 d的石油污染土壤的原位修复实验.定期监测石油污染土壤的总石油烃含量(TPHs)、含盐率、pH、碱解氮、速效钾、速效磷、有机质、土壤脲酶、脱氢酶、多酚氧化酶、过氧化氢酶活性及土壤微生物群落遗传多样性的动态变化情况,并运用主成分分析法对14项土壤因子进行多元分析,构建评价函数,做出综合评价,以期掌握陇东石油污染土壤原位修复中土壤肥力的动态变化趋势,为大面积开展生物修复石油烃污染土壤提供基础依据和数据参考.
2 材料与方法(Materials and methods) 2.1 自然状况研究区位于陇东黄土高原庆阳市董志乡长庆油田第二炼油厂,土壤类型为沙土,质地为轻壤.地处东经106°38′~108°40′,北纬35°69′~35°71′,海拔1380~1400 m.该区属黄土高原沟壑地貌,是典型的水土流失区之一,侵蚀面积25050.5 km2,占全区总面积的92.4%,侵蚀模数6383~9000 t · hm-2研究区.属暖温带半干旱季风气候区,光、热等气候资源丰富,作物种植制度为一年两熟.由于季风的强烈影响,冬季寒冷干燥,春季多风且干旱少雨,夏季温暖多雨,水热同期,年降水量400~600 mm,雨量分布不均,且主要集中在7—9月份,多年平均蒸发量1000 mm以上,地面蒸发量为350~560 mm,地下水位深,属雨养农业区,在黄绵土类区农业发展的主要限制因素是干旱,土壤瘠薄,水土流失严重(张希彪等,2004).
2.2 供试样地的选择原位修复样地位于甘肃省庆阳市长庆油田第二炼油厂,经实验测得,供试石油污泥的初始含油量高达1.46%(即14600 mg · kg-1),远远高于国家农业标准临界值500 mg · kg-1.
2.3 供试菌剂的分离和筛选供试菌种源自甘肃省高校陇东生物资源保护与利用省级重点实验室,为通过选择性培养基和富集培养基自主筛选的石油降解菌(押辉远等,2011).初步鉴定为假单胞菌属(Pseudomonas)、微球菌属(Micrococcus)、线菌属(Actinomayces),以及真菌类的青霉属(Penicillum)、地霉属(Geotrichum)、毛霉属(Mucor)和曲霉属(Aspergillus).
2.4 生物修复实验原位修复区内投加本实验室筛选配制的土著石油降解菌菌剂,并外源添加高塔复合肥(史丹利化肥股份有限公司),其中,N:P:K比例为25:10:16,调节土壤的N和P比例,设3个平行实验.
定期翻土保持土壤好氧状态,定期浇水保持土壤含水率为20%.实验周期为105 d,分别在25、45、60、80和105 d时用四分法取样,除利用鲜土提取土壤微生物细菌基因组总DNA外,其余土样在室温下于背阴处风干,过2 mm筛备用.
2.5 土壤理化性质测定土壤有机质和碱解氮分别采用重铬酸钾容量法-外加热法、碱解扩散法测定(鲍士旦,1999);土壤速效磷、速效钾分别采用0.5mol · L-1 NaHCO3浸提-钼锑抗比色法、火焰光度计法测定(鲍士旦,1999);土样pH值采用电位法(pHS-3酸度计)测定;含盐率采用质量法测定(唐景春等,2013);土壤中总石油烃含量(TPHs)采用超声-索氏萃取-重量法测定(王如刚等,2010).
2.6 土壤样品总DNA提取、PCR扩增和变性凝胶梯度电泳(DGGE)分析采用土壤细菌基因组试剂盒(E.Z.N.A.TM Soil DNA kit,OMEGA Company)提取土样细菌基因组总DNA,于-20 ℃保存.将提取的土样基因组总DNA作为PCR的模板,PCR扩增过程中所用的引物见表 1.
| 表 1 用于细菌16S rDNA扩增的引物 Table 1 Primers for 16S rDNA amplification |
采用巢式PCR扩增目的片段.第一轮扩增反应条件:94 ℃预变性4 min;94 ℃变性45 s,61 ℃退火45 s,72 ℃延伸1 min,30个循环;72 ℃终延伸10 min.反应体系为20 μL:2 μL 10×PCR Buffer,1 μL MgCl2(25 mmol · L-1),0.8 μL dNTP(2.5 mmol · L-1),0.4 μL PrimerⅠ(BS-for,10 μmol · L-1),0.4 μL PrimerⅡ(BS-rev,10 μmol · L-1),0.2 μL Taq酶(5 U · μL-1),1 μL 模板,补足灭菌双蒸水至20 μL.第二轮扩增以第一轮PCR扩增产物16S rDNA为模板,采用Touchdown PCR策略扩增16S rDNA V3区,反应条件为:94 ℃预变性4 min;94 ℃变性45 s,62 ℃退火45 s,72 ℃延伸1 min,之后每一循环降0.5 ℃,20个循环;94 ℃变性45 s,56 ℃退火45 s,72 ℃延伸1 min,10个循环;72 ℃终延伸10 min.反应体系与第一轮PCR相同.
3 结果与讨论(Results and discussion) 3.1 原位修复过程中石油污泥理化性质的变化情况表 2为原位修复过程中石油污泥理化性质的变化情况.原位修复过程中土壤TPHs含量、含盐率、pH、碱解氮、速效钾、速效磷、有机质均差异极显著(FTPHs=30.223>F0.01,F含盐率=62.583>F0.01,FpH=51.032>F0.01,F碱解氮=71.650>F0.01,F速效钾=53.419>F0.01,F速效磷=44.192>F0.01,F有机质=56.675>F0.01,p<0.01);多重比较(Duncan,α=0.05)结果显示,随着修复的进行,TPHs、pH、有机质含量、含盐率的变化情况不尽相同,但总体上呈下降的趋势(p<0.05);土壤碱解氮、速效磷含量总体上呈上升趋势(p<0.01);而速效钾在原位修复前80 d无显著性差别(p>0.05),至105 d显著增加(p<0.05).
| 表 2 原位修复过程中石油污泥理化性质 Table 2 Physicochemical properties of oil-contaminated sludge during the process of in-situ remediationn |
由表 2可以看出,随着修复时间的延长,含盐率呈降低趋势,与修复初期时土壤含盐率相比,经过105 d的原位修复,土壤含盐率明显降低(p<0.01).前人研究表明,石油污泥的pH值均大于7,呈碱性,超过了微生物生长的最佳pH值(7.5~7.8)范围(俞毓馨等,1990),不利于微生物的生长,甚至会有很强的抑制作用.土壤pH可能会通过影响降解过程中关键酶的酶活性来影响降解率,因此,该实验中土著微生物可能还未能最大限度地发挥其降解效能,此类问题有待进一步的分析研究.此外,Leahy和Colwell(1990)研究认为,土壤微生物在降解石油烃时会产生羧酸类中间产物,可能会使pH在一段时间内降低.本研究中,经过105 d修复后,pH显著降低(p<0.01),这可能是因为在原位修复的过程中,厌氧菌对石油烃的降解得到了强化,厌氧降解的过程容易产生酸性物质,特别是土壤中的硫酸盐还原菌(Dell′Anno et al., 2009).本研究中,尽管石油污泥中的TPHs含量在原位修复过程中有明显降低(表 2),但就国家农业标准临界值500 mg · kg-1而言,土壤仍然属于重度污染.研究表明,石油污泥中的石油烃对土壤的有机质含量有很大的贡献,石油烃含量与土壤有机质呈显著正相关关系(吴伟林等,2010),在本研究中随着石油烃含量的明显降低,土壤有机质含量也呈降低趋势,这与前人的研究结果一致.尽管在石油烃的降解过程中,微生物大量利用了土壤中的N和P等营养元素,但与修复初期时土壤的碱解氮和速效磷含量相比,土壤的碱解氮和速效磷含量都显著增加(p<0.01),土壤肥力得到一定的恢复,原因可能是污染区附近的土地已用作农田;此外,本研究中外源施加了复合肥等营养物质,在一定程度上等增加了土壤N和P等营养物质的含量,同时也说明在修复过程中微生物的呼吸速率和活性得到了很大程度的提升.
3.2 原位修复过程中土壤酶活性变化情况表 3为原位修复过程中土壤酶活性变化情况.原位修复过程中不同修复时期土壤脲酶、多酚氧化酶、脱氢酶、过氧化氢酶差异极显著(F脲酶=268.721>F0.01,F多酚氧化酶=279.791>F0.01,F脱氢酶=592.728>F0.01,F过氧化氢酶=213.707>F0.01,p<0.01);多重比较(Duncan,α=0.05)结果进一步显示,土壤脲酶及脱氢酶活性显著增加(p<0.05),多酚氧化酶及过氧化氢酶活性明显降低(p<0.05).
| 表 3 原位修复过程中土壤酶活性 Table 3 Soil enzyme activity of oil-contaminated sludge during the process of in-situ remediation |
土壤脲酶是唯一一种作用于尿素肥料的水解酶类(和文祥等,2002),它能分解有机物质,促其水解成NH3和CO2.同时,脲酶是一种中性酶,可以加速土壤中潜在养分的有效化,因而土壤中脲酶活性可以作为衡量土壤肥力的指标之一,并能部分反映土壤生产力(李慧等,2005).表 3中脲酶活性逐步增加,说明土壤肥力逐渐提升.土壤中多酚氧化酶活性的强弱直接影响到土壤中的酚含量(常学秀等,2001),而在石油烃的降解代谢过程会产生一定量的酚类物质,因此,土壤中的多酚氧化酶活性可以用来表征部分石油烃的生物降解情况.如表 3 所示,土壤中多酚氧化酶的活性在第20 d到80 d生物修复后均显著降低(p<0.05),80 d与105 d间无显著变化(p>0.05).可能的原因是石油污染对土壤中的植物、微生物产生了毒害作用,抑制了多酚氧化酶活性,导致了前80 d其活性显著降低.但随着修复过程的进行,土壤微生物群落结构逐渐发生变化,微生物代谢过程中产生的酚类物质会刺激土壤微生物产生多酚氧化酶,使其活性维持在相对稳定水平.土壤脱氢酶是石油烃降解过程中重要的参与酶,它能使被氧化有机物的氢原子活化并传递其特定的受氢体,因而脱氢酶的活性可以反映处理体系内活性微生物量及其对有机物的降解活性,进而评价修复性能(常学秀等,2001).由表 3可以看出,原位修复过程中脱氢酶活性显著增加(p<0.01),说明经过105 d的原位修复,土壤中可降解的石油烃组分得到了一定程度的去除.土壤过氧化氢酶广泛存在于微生物和植物的细胞中,是在生物呼吸过程中和有机物质的生物氧化反应过程中形成的(蔺昕等,2005).过氧化氢酶在土壤中的作用是能够破坏对生物体有毒的过氧化氢(常学秀等,2001).由表 3可见,土壤过氧化氢酶活性从25 d至60 d显著降低(p<0.05),可能是由于在石油污染土壤中的毒性作用较强,土壤中过氧化氢酶活性较低.60~80 d,过氧化氢酶活性无显著差异,究其原因可能是植物-微生物的相互作用对于土壤中过氧化氢酶活性起到了一定的保护和促进作用.80~105 d土壤中过氧化氢酶活性亦呈显著降低趋势,可能是由于土壤中的污染物降解中间代谢产物对生物有毒害作用,从而抑制了过氧化氢酶的形成,导致土壤中过氧化氢酶活性降低.本研究中,土壤过氧化氢酶活性下降的原因还有待进一步分析研究.
3.3 原位修复过程中土壤微生物功能多样性的PCR-DGGE分析本研究采用PCR-DGGE技术对原位修复过程中第25、45、60、80和150 d所得土壤样品进行微生物群落遗传多样性分析,DGGE指纹图谱见图 1,其中,图 1a为凝胶相片,图 1b为用Quantity One处理得到的谱带注解图.根据DGGE对DNA的分离原理,图谱上的条带信息即可初步反映不同石油污泥的微生物种群多样性及组成(乔俊等,2010).由图 1可以看出,随着原位修复的进行,从5个修复期土壤样品的条带分布可以看出,25 d有35条,45 d为29条,60 d为32条,80 d为41条,105 d为51条,说明石油污染土壤微生物群落遗传多样性得到了一定的恢复,表现为谱带数目的增加.
 |
| 图 1 原位修复过程中不同修复期石油污泥样品的PCR-DGGE分离谱图(a)及其模式图(b) Fig.1 DGGE b and patterns and models of oil-contaminated sludge samples at different in situ remediation times(a.DGGE b and pattern,b.DGGE b and model) |
本研究采用3种常用的多样性指标进行土壤微生物群落多样性分析,分别为Patrick 丰富度指数(S)、Shannon-Wiener多样性指数(H)、Pielou 均匀度指数(J),计算公式如下:
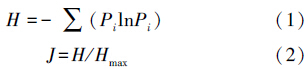
式中,S为物种数,即条带数;Pi代表土壤样品中第 i 个条带的吸光度占所有条带吸光度总和的比例;Hmax代表最大多样性值,Hmax=lnS.
图 2为原位修复过程中不同修复期土壤微生物群落遗传多样性变化情况.可以看出,随着原位修复的进行,土壤微生物群落Shannon-Wiener多样性指数和Pielou 均匀度指数均呈现出先降后增的趋势,说明原位修复初期,外源投加的石油降解菌对自然状况下土壤环境需要适应过程.
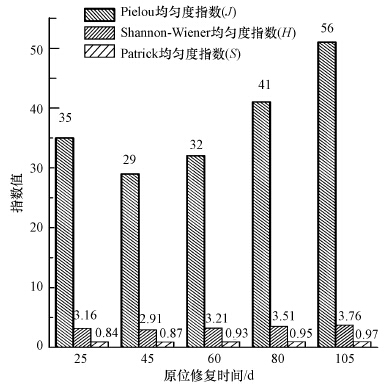 |
| 图 2 原位修复过程中不同修复期土壤微生物群落遗传多样性变化情况 Fig.2 Changes in genetic diversity of microbial community in oil-contaminated sludge during in situ remediation |
对石油污泥指标原始数据进行中心化处理,通过主成分分析法对土样原始变量的信息进行重组,包括石油污染土样的TPHs(X1)、含盐率(X2)、pH(X3)、碱解氮(X4)、速效钾(X5)、速效磷(X6)、有机质(X7)、脲酶(X8)、多酚氧化酶(X9)、脱氢酶(X10)、过氧化氢酶(X11)、Shannon-Wiener多样性指数(X12)、Pielou 均匀度指数(X13)和Patrick 丰富度指数(X14)等14个土壤肥力因子的综合分析,得出各因子的特征根、贡献率及累计贡献率(表 4).由表 4可见,前两个公因子的累积贡献率已达92.973%,能够反映出全部指标提供信息的92.973%,具有广泛的代表性,可用于评价石油污染土壤原位修复过程中土壤肥力变化情况.通过正交旋转得到因子载荷矩阵(表 5),对第1公因子起正相关作用的有土壤碱解氮、速效钾、速效磷、脲酶、脱氢酶、Shannon-Wiener多样性指数、Patrick丰富度指数及Pielou均匀度指数,起负相关作用的有土壤TPHs、含盐率、pH、有机质和多酚氧化酶和过氧化氢酶,因此,第1公因子可看作是供试土壤养分有所改善的真实反映.对第2公因子起正相关作用的有土壤速效磷、速效钾、脱氢酶、Shannon-Wiener多样性指数、Patrick丰富度指数及Pielou均匀度指数,起负相关作用的有土壤TPHs、含盐率、pH、碱解氮、有机质、脲酶、多酚氧化酶、过氧化氢酶,第2公因子可看作是对土壤污染状况的真实反映.类似的结果也可从旋转综合因子载荷矩阵看出(表 5),并由此得出因子得分函数:

式中,Y1、Y2为第1、第2公因子的得分;X1、X2……X14为土壤各属性值的标准化值,分别对应土壤的TPHs、含盐率、pH、碱解氮、速效钾、速效磷、有机质、脲酶、多酚氧化酶、脱氢酶、过氧化氢酶、Shannon-Wiener多样性指数、Pielou 均匀度指数和Patrick 丰富度指数.
| 表 4 因子分量的特征根、贡献率及累积贡献率 Table 4 Factor component characteristic root and contribution rate as well as cumulative contribution rate |
| 表 5 土壤因子旋转载荷矩阵及因子得分矩阵 Table 5 Rotating comprehensive factor loading matrix and component score coefficient matrix |
将各利用类型相对应的土壤属性值标准化值代入上述两式,并由两个公因子的特征根求出其权重分别为0.546和0.399,由下列公式进行加权求和,得出其综合评价得分.

式中,W为综合评价得分,T1、T2为第1、第2公因子的权重.
由图 3可知,原位修复第25~105 d,土壤肥力得分分别为-138.94、-48.86、20.73、79.71和96.91.原位修复伊始,土壤肥力相对较低,这说明经过石油污染的土壤,仍具有很低的肥力,可能的原因是土著微生物对污染物的自然降解作用,也可能是采集油泥区周围已用作农田,外源施加化肥等营养物质在一定程度上增加了土壤肥力.随着原位修复过程的进行,土壤主要肥力指标显著提升.
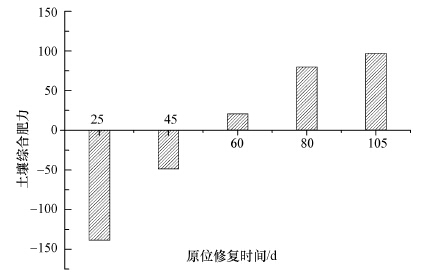 |
| 图 3 原位修复过程中土壤肥力变化情况 Fig.3 Soil fertility changes during the process of in situ remediation |
1)原位修复过程中,有机质、pH、含盐率、TPHs总含量显著降低(p<0.01),土壤碱解氮、速效磷含量呈增加趋势,且达到极显著水平(p<0.01),而速效钾呈逐步增加趋势(p<0.01).上述结果说明石油污染土壤速效养分含量有所增加.土壤脲酶及脱氢酶活性增加(p<0.01),多酚氧化酶及过氧化氢酶活性降低(p<0.01).说明土壤中可降解的石油烃组分得到一定程度的去除,土壤酶活性略有提升.
2)基于PCR-DGGE技术分析结果显示,随着原位修复的进行,土壤微生物群落Shannon-Wiener多样性指数(H)和Pielou 均匀度指数(J)均呈现出先降后增的趋势,说明原位修复初期,外源投加的石油降解菌对自然状况下土壤环境需要适应过程.此外,土壤微生物群落结构逐渐丰富、分布愈加均匀,多样性显著提升.
3)外源添加土著石油降解菌和复合肥可以有效提升石油污染土壤肥力,并为土著微生物提供优越的土壤微环境,有助于土壤微生物的生长,进而改善石油污染土壤中的土壤微生物群落结构.
| [1] | 鲍士旦.1999.土壤农化分析 (第3版) [M].北京:中国农业出版社.245-353 |
| [2] | 曹承绵,严长生,张志明,等.1983.关于土壤肥力数值化综合评价的探讨[J].土壤通报,(4): 13-15 |
| [3] | 常学秀,文传浩,沈其荣,等.2001.锌厂Pb 污染农田小麦根际与非根际土壤酶活性特征研究[J].生态学杂志,20(4): 5-8 |
| [4] | Dell'Anno A,Beolchinia F,Gabellini M,et al.2009.Bioremediation of petroleum hydrocarbons in anoxic marine sediments: Consequences on the speciation of heavy metals [J].Marine Pollution Bulletin,58(12): 1808-1814 |
| [5] | Ding K Q,Luo Y M,Sun T H,et al.2002.Bioremediation of soil contaminated with petroleum using forced-aeration composting[J].Pedosphere,12(2): 145-150 |
| [6] | 和文祥,蒋新,卞永荣,等.2002.杀虫双对土壤酶活性影响的研究[J].西北农林科技大学学报,30(1): 13-17 |
| [7] | 黄婷,岳西杰,葛玺祖,等.2010.基于主成分分析的黄土沟壑区土壤肥力质量评价——以长武县耕地土壤为例[J].干旱地区农业研究,28(3): 141-147; 187 |
| [8] | Leahy J G,Colwell R R.1990.Microbial degradation of hydrocarbons in the environment[J].Microbial Review,54(3): 305-315 |
| [9] | 李慧,陈冠雄,杨涛,等.2005.沈抚灌区含油污水灌溉对稻田土壤微生物种群及土壤酶活性的影响[J].应用生态学报,16(7): 1355-1359 |
| [10] | 蔺昕,李培军,孙铁珩,等.2005.石油污染土壤的生物修复与土壤酶活性关系[J].生态学杂志,24(10): 1226-1229 |
| [11] | 刘五星,骆永明,滕应,等.2007.我国部分油田土壤及油泥的石油污染初步研究[J].土壤,39(2): 247-251 |
| [12] | 骆伯胜,钟继洪,陈俊坚.2004.土壤肥力数值化综合评价研究[J].土壤,36(1): 104-106 |
| [13] | 吕巧灵,付巧玲,吴克宁,等.2006. 郑州市郊区土壤综合肥力评价及空间分布研究[J].中国农学通报,22(1): 166-168 |
| [14] | 吕晓男,陆允甫,王人潮.1999.土壤肥力综合评价初步研究[J].浙江大学学报 (农业与生命科学版),25(4): 378-382 |
| [15] | 乔俊,陈威,张承东.2010.添加不同营养助剂对石油污染土壤生物修复的影响[J].环境化学,29(1): 6-11 |
| [16] | 宋歌,孙波,教剑英.2007.测定土壤硝态氮的紫外分光光度法与其他方法的比较[J].土壤学报,44(2): 288-293 |
| [17] | 唐景春,刘文杰,徐婷婷,等. 2013.不同处理条件对石油污染土壤植物修复的影响[J].环境工程学报,7(8):3231-3235 |
| [18] | 王如刚,王敏,牛晓伟,等.2010.超声-索氏萃取-重量法测定土壤中总石油烃含量[J].分析化学,38(3): 417-420 |
| [19] | 吴伟林,张秀霞,单宝来,等.2010.不同处置方式对石油污染土壤理化性质和生物学特性的影响[J].石油学报,26(5): 831-834 |
| [20] | 押辉远,易力,周胜利,等.2011.南阳油污土壤微环境分析及石油降解菌筛选[J].湖北农业科学,50(6): 1132-1136 |
| [21] | 姚治华,王红旗,刘敬奇,等.2006.石油污染土壤中苯降解菌的筛选及降解特性研究[J].农业环境科学学报,25(6): 1498-1503 |
| [22] | 俞毓馨,吴国庆,孟宪庭.1990.环境工程微生物检验手册[M].北京:中国环境科学出版社.138-142 |
| [23] | 张胜,陈立,崔晓梅,等.2008.西北黄土区石油污染土壤原位微生物生态修复试验研究[J].微生物学通报,35(5): 765-771 |
| [24] | 张希彪,郭小强,周天林,等.2004.子午岭种子植物区系分析[J].西北植物学报,24(2): 267-274 |
| [25] | 张兴昌.1993.土壤肥力的数学评价初探[J].陕西农业科学,(4): 8-11 |
 2015, Vol. 35
2015, Vol. 35


