2. 华南理工大学化学与化工学院, 广州 510641;
3. 工业聚集区污染控制与生态修复教育部重点实验室, 广州 510006;
4. 华南理工大学环境与能源学院, 广州 510006
2. School of Chemistry and Chemical Engineering, South China University of Technology, Guangzhou 510641;
3. The Key Laboratory of Pollution Control and Ecosystem Restoration in Industry Clusters of Ministry of Education, Guangzhou 510006;
4. College of Environment and Energy, South China University of Technology, Guangzhou 510006
壳聚糖(Chitosan,CS)含氨基、羟基等官能团,是一种重要的基础吸附剂,其不同形态(粉末、膜、微球、纤维及交联态)均可有效吸附水中的金属离子(Juang et al., 2000;Gamage et al., 2007;Wan Ngah et al., 2002;2004;2005;2006;2008;Vieira et al., 2006a;Haider et al., 2009),其中,壳聚糖膜的吸附效能更高且更有发展前景(Ohkawa et al., 2004;2006;Vieira et al., 2006b;Twu et al., 2003;Subbiah et al., 2005).随着静电纺丝技术的发展,其在环境污染治理领域也逐渐得到应用(Desai et al., 2009;Merrifield et al., 2004; Liu et al., 2006;Zhou et al., 2009).例如,Aliabadi等(2013)将壳聚糖与聚氧乙烯以90/10的比例静电纺丝并用戊二醛交联后,制得平均直径98 nm、比表面积312.2 m2 · g-1的纳米纤维,对100 mg · L-1的Ni2+(pH=5)、Cu2+(pH=6)、Cd2+(pH=5)、Pb2+(pH=5.5)吸附2 h,发现吸附容量分别为175.1、163.7、143.8、135.4 mg · g-1.Horzum等(2010)通过静电纺丝制得壳聚糖纳米纤维膜,其比表面积是壳聚糖粉末的20倍,对低浓度Cu2+、Ag+、Cd2+、Fe3+的去除率可分别达到99%、97%、85%、78%.同样,Sajjad Haider用静电纺丝制备的壳聚糖纳米纤维膜对400 mg · L-1的Cu2+、Pb2+进行吸附,吸附容量分别为485.44 mg · g-1(2.85 mmol · g-1)和263.15 mg · g-1(0.79 mmol · g-1),是壳聚糖微球的6~11倍(Haider et al., 2009; Wan Ngah et al., 2005; Huang,1996).因此,通过静电纺丝制得的壳聚糖纳米吸附剂将更具价值.
由于壳聚糖在酸性溶液中粘度较高、带正电荷,以及分子内和分子间强化学键作用(Geng et al., 2005;Desai et al., 2008),致使其在静电纺丝过程中难以自由移动,导致纤维不连续,含珠状物,甚至纺丝断裂(Klossner et al., 2008).为此,人们曾将聚氧乙烯(Pakravan et al., 2012)、聚乙烯醇(Zhang et al., 2007)、纤维素(Devarayan,2013),聚乳酸(Chen et al., 2008)、聚己内酯(Shalumon,2011)、尼龙-6(Zhang et al., 2009)等聚合物与壳聚糖混纺,以增强纺丝的韧度和强度.
研究发现,聚乙烯醇1799(Poly(Vinyl Alcohol),PVA)常温下不溶于水且易于通过氢键与壳聚糖结合(Zhang et al., 2007),比其它聚合物具有更良好的静电纺丝性能(Ding et al., 2002),混纺可制得不溶于水的、高比表面积、连续无缺陷的纳米纤维,比单纯壳聚糖制备的膜更加坚韧耐用,原料成本也更低(Paipitaka et al., 2005).如Wang等(2013)采用壳聚糖/聚乙烯醇/硝酸铈静电纺丝,制得平均直径240 nm的纳米纤维.而将壳聚糖与聚乙烯醇混纺制备纳米纤维,并将其用于重金属吸附的研究仍有较大的完善空间.
因此,本文拟采用静电纺丝方法制备壳聚糖/聚乙烯醇纳米纤维膜(Chitosan/Poly(Vinyl Alcohol)Nanofiber,CS/PVA纳米纤维膜),并用SEM、FTIR、XRD、BET等对其性质进行表征,然后通过对模拟重金属离子水的吸附实验,探讨pH值、重金属离子初始浓度、反应温度和离子强度对Cu2+、Ni2+和Cd2+吸附的影响.同时,结合吸附动力学和吸附等温模型及吸附热力学计算探明其对重金属离子的吸附特性,以期为开发高效CS/PVA纳米纤维膜吸附剂及其在吸附水中重金属的应用提供依据.
2 材料与方法(Materials and methods) 2.1 材料与试剂壳聚糖(脱乙酰度97.5、分子量60万)、聚乙烯醇(1799聚合度为1750,醇解度为99.8%~100%)购于阿拉丁试剂有限公司,冰醋酸购于广药集团化学试剂有限公司,铜、镍和镉标准溶液购自上海晶纯试剂有限公司,硫酸铜、氯化镍、氯化镉及其它试剂均为市售分析纯试剂.壳聚糖的相对分子量通过乌式粘度计测量,脱乙酰度用电位滴定法测得.
2.2 实验方法 2.2.1 CS/PVA溶液的制备在预实验中,将溶液按照PVA与CS质量比80/20、70/30、40/60三种比例混合进行静电纺丝,电镜观察发现,当m(CS)/m(PVA)=20/80时,静电纺纤维形貌最好,基本无珠状物和断丝.因此,本实验确定20/80作为最佳纺丝配比.配置质量分数为10%的PVA溶液,在90 ℃下水浴搅拌加热2 h溶解后,将5 g的CS溶于95 g体积分数50%的醋酸溶剂中,配成5%的CS溶液,在60 ℃水浴搅拌4 h溶解.将配好的混合溶液于40 ℃水浴磁力搅拌2 h溶解后,静置至溶液冷却.
2.2.2 静电纺丝CS/PVA、CS和PVA纤维膜的制备及处理将混合液置于10 mL注射器中,使用DT-200型静电纺丝机进行纺丝,设置电压为25 kV,接收距离为15.0 cm,纺丝速度为0.15 mL · h-1,针头为12号(0.86 mm).在铝箔上接收纺丝纤维,纺丝24 h后停机,用镊子将纺丝纤维膜揭下来,于室温下干燥24 h后,用1 mol · L-1的K2CO3溶液浸泡3 h,以中和过量的醋酸.再用去离子水将残留在纤维膜表面的离子洗脱,直到pH为7.将纤维膜放入冰箱中于-18 ℃下预冻30 min后,再转入真空冷冻干燥箱,于-54 ℃下真空干燥16 h.然后放于真空干燥器中保存,以备使用.将5%的CS溶液和10%的PVA溶液按照上述步骤操作,分别制得静电纺丝CS和PVA纤维膜.
2.2.3 CS/PVA纤维膜的稳定性实验方法将干燥的CS/PVA纳米纤维膜样品称重后,浸入30 ℃、pH=7的去离子水中1~24 h,将浸泡一定时间的样品取出,先于室温下干燥,再于60 ℃的真空干燥箱中干燥过夜后称量.所有实验重复3次.
为检测样品在酸性条件下的溶解状况,用HCl将去离子水的pH值分别调为2、3、4、5、5.5,将干燥的CS/PVA纳米纤维膜样品称重后,分别浸入30 ℃的不同pH值的去离子水中,浸泡24 h后真空干燥,称重并计算其稳定性系数S:
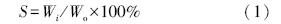
式中,Wo为纤维膜初始质量(mg),Wi为浸水i小时干燥后的纤维膜质量(mg).
2.2.4 CS/PVA纤维膜的表征方法将CS/PVA纤维膜干燥后,喷金,在 JSM-6360LV 型扫描电子显微镜下用不同倍数进行观察扫描.使用Image ProPlus软件对纤维直径进行测量,以不少于200根的纤维测量直径为准,计算平均值.
将CS、PVA和CS/PVA纤维膜样品分别与KBr 粉末以1 ∶ 99的质量比混合均匀并研磨压片后,用德国Bruker公司的Tensor27红外光谱仪进行红外光谱扫描,采用Omnic分析软件分析数据.将CS、PVA、CS/PVA纤维膜样品用X 射线衍射仪(德国Bruker 公司,D8 ADVANCE)测定XRD 图谱.采用BET分析仪(美国迈克公司,ASAP2020)测定CS/PVA纤维膜的比表面积.用INSTRON 5565型拉伸压缩材料试验机,在室温下测定样品膜的力学性能,包括在最大值处的荷载、在拉伸应力最大值处的载荷、在拉伸应变最大值处的载荷.试样尺寸为7 mm×45 μm,夹具间距为50 mm,拉伸速度为5 mm · min-1.根据应力应变值,计算材料的弹性模量.
2.2.5 吸附实验方法采用批次实验,将10 mg的CS/PVA纤维膜加入到20 mL 50~1000 mg · L-1的Cu2+、Ni2+、Cd2+溶液中,恒温振荡(25~45 ℃,150 r · min-1)2 h,取上清液在石墨炉原子吸收分光光度计上测定溶液中重金属离子浓度,计算吸附量和去除率,具体公式如下:
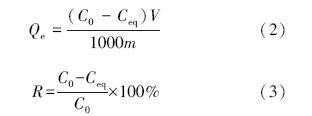
式中,Qe为CS/PVA吸附容量(mg · g-1),C0为溶液中重金属离子初始浓度(mg · L-1),Ceq为吸附平衡后溶液中重金属离子浓度(mg · L-1),R为重金属离子去除率,V为溶液体积(mL),m为吸附剂投加量(mg).
在pH影响实验中,设定温度为25 ℃,用0.1 mol · L-1的HCl 或NaOH 调节初始浓度为100 mg · L-1的Cu2+、Ni2+、Cd2+溶液的pH 值分别为2、3、4、5、5.5(林芳等,2008).
在离子强度影响实验中,设定温度为25 ℃,用NaCl 固体调节初始浓度为100 mg · L-1 的Cu2+、Ni2+、Cd2+溶液,以及3种离子浓度均为100 mol · L-1的混合溶液中离子强度分别为0、10、20、50、100 mg · L-1(以NaCl计),然后用HCl 或NaOH溶液将pH 调至5.5.
吸附等温线实验中,重金属离子初始浓度范围为50~1000 mg · L-1,温度分别设定为25、35和45 ℃.所有样品均设置2 个平行样,1个空白样.
3 结果与讨论(Results and discussion) 3.1 CS/PVA纤维膜的物理化学性质 3.1.1 稳定性实验CS/PVA纤维膜在水溶液中的稳定性实验结果如图 1所示.由图 1a可见,CS/PVA纤维膜在水溶液中的稳定性随时间变化的下降幅度较小(<20%),其主要原因是CS和PVA1799本身在常温下均不溶于水,且CS与PVA分子间形成了较为稳定的氢键结构.由图 1b可见,CS/PVA纤维膜在水溶液中的稳定性随pH值几乎无变化,即使在pH=2的条件下,整体变化幅度仍小于25%.pH对材料的稳定性无大影响,这是因为壳聚糖只有在pH=1左右才溶解,而聚乙烯醇1799均不溶于酸、碱,因此,我们有理由认为该吸附剂在水溶液中的质量比较稳定,不易流失.
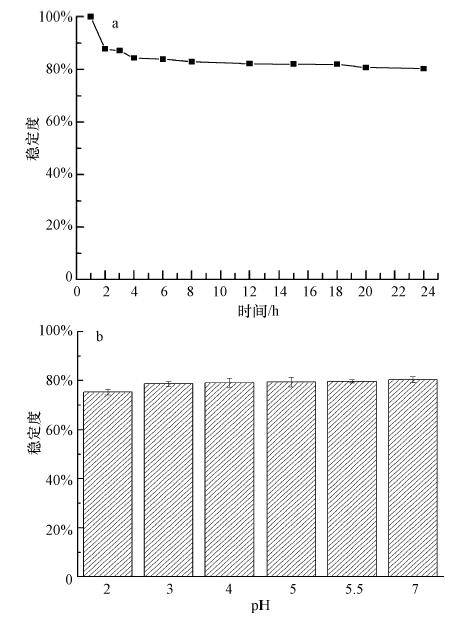 |
| 图 1 CS/PVA纤维膜稳定性随时间(a)及pH(b)的变化 Fig. 1 Degree of stability of chitosan/poly(vinyl alcohol)fiber membranes followed by(a)time and (b)pH |
纯CS、PVA和CS/PVA纤维膜的官能团可以由红外谱图(图 2)中得出.在CS膜的红外谱图中,3450 cm -1处是多糖分子的N—H和O—H延展峰,2920 cm -1处是CH2的伸缩振动,1592~1651 cm -1处为氨基变形振动峰.但1328 cm -1和1379 cm -1(分别为乙酰氨基团和C—CH3变形振动)两处吸收峰的存在,表明尚存在一定数量的乙酰氨基团.1154 cm -1和896 cm-1两处为CS糖苷键结构的特征吸收峰(Pearson et al., 1960).
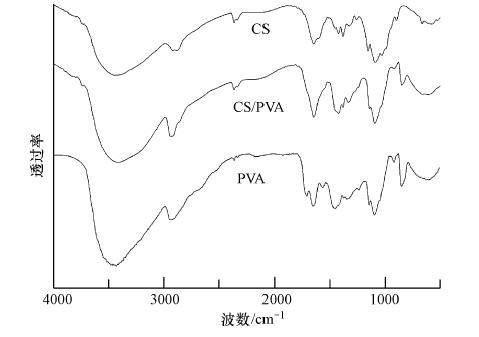 |
| 图 2 CS、PVA和CS/PVA纤维膜的红外图谱 Fig. 2 FTIR spectra of chitosan,PVA and Chitosan/PVA fiber membranes |
CS/ PVA 膜相比于PVA 膜,原来的羟基伸缩振动峰(3300~3500 cm -1)变宽,结晶峰(851 cm -1)减弱.CS/PVA膜相比于CS膜,1085 cm -1处的振动峰移动到高波数1092 cm -1处,662 cm -1处的振动峰变弱,1592~1651 cm -1处的氨基特征吸收峰也随之削弱.这说明CS/PVA膜一方面保留了CS中较高吸附性能的氨基结构,另一方面CS与PVA 分子间又存在一定的相互作用,并非只是二者之间的简单混合.
3.1.3 BET分析通过用N2吸附/脱附来检测CS/PVA纤维膜的比表面积,依据BJH和BET理论计算吸附-脱附曲线,发现该吸附剂的比表面积和孔容分别为219.423 m2 · g-1和0.339 cm3 · g-1,而CS粉末的比表面积只有0.92 m2 · g-1(Horzum et al., 2010),说明静电纺丝可以简便地提高CS/PVA纤维膜的比表面积.
3.1.4 扫描电镜分析CS/PVA纤维膜的扫描电镜分析结果如图 3所示.从图 3a(20000倍)可见,CS/PVA纤维膜中纤维与纤维之间基本上无断丝、无珠状物,像一张织出来的网,形貌好,均匀度较高.采用Image Pro Plus对不少于200根纤维进行直径测量的结果表明,CS/PVA纤维的平均直径为76.31 nm,为纳米结构,约为壳聚糖/聚乙烯醇/硝酸铈的1/3(Wang et al., 2013),直径分布频率符合Gauss分布,R2为0.99869,拟合度较高(图 3b).
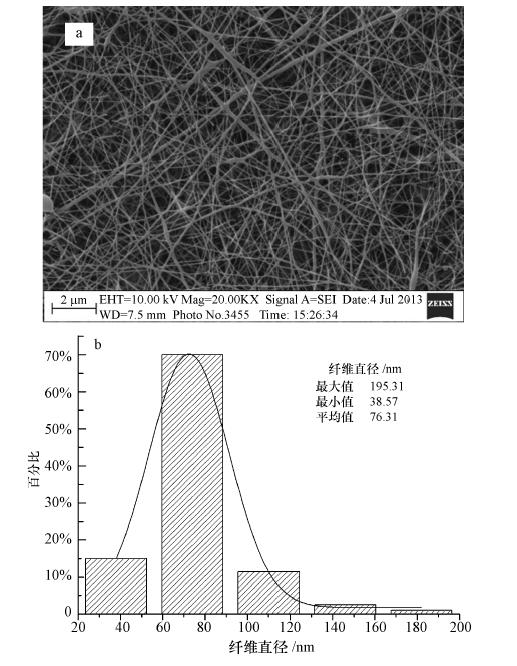 |
| 图3 CS/PV纤维膜的扫描电镜图片(a)和直径分布柱状图(b) Fig. 3 SEM micrographs of chitosan/poly(vinyl alcohol)electrospun mat(a) and diameter histogram of the electrospun fiber membrane(b) |
PVA、CS及CS/PVA纤维膜的XRD图谱如图 4所示.PVA膜在2θ为19.54°处出现强的衍射峰,在11.23°、22.57°、22.90°、40.71°处都出现了弱的衍射峰.CS膜在2θ为11.23°、20.13°和29.385° 处出现了较强的峰.而CS/PVA膜只在19.54°处有一个衍射峰,而在10.30°和15.20°处几乎无衍射峰.说明CS/PVA膜中CS和PVA存在着较强的相互作用(Zhang et al., 2007),从而影响着CS原有的结构,这与红外分析光谱的结果一致.
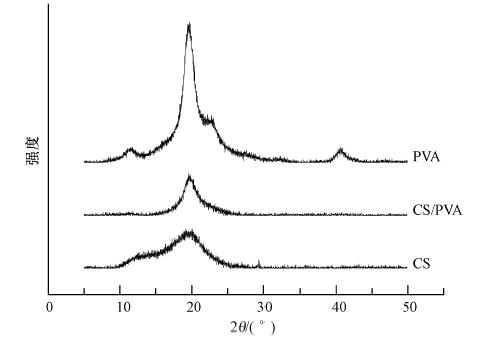 |
| 图4 CS、PVA和CS/PVA纤维膜的XRD谱图 Fig. 4 XRD patterns of chitosan,poly(vinyl alcohol) and chitosan/poly(vinyl alcohol)fiber membranes |
CS/PVA的拉伸曲线见图 5.试验结果表明,CS/PVA的最大值载荷为14.04 N,拉伸应力最大值载荷为51.98 MPa,拉伸应变最大值载荷为4.967%.计算得出CS/PVA的弹性模量为3029.35 MPa,远大于普通壳聚糖膜的(1247±21)MPa(赵茜等,2011),说明聚乙烯醇的加入增强了CS/PVA膜的机械性能.
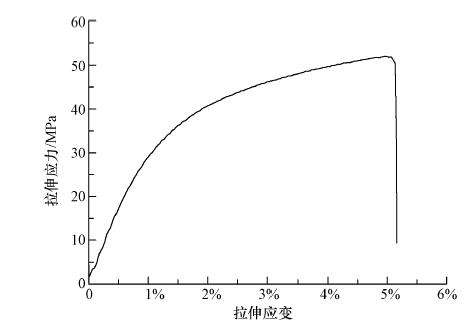 |
| 图5 CS/PVA纤维膜的拉伸曲线 Fig. 5 CS / PVA fiber membrane tensile curve |
在pH=5.5、25 ℃条件下,PVA纤维膜和CS/PVA纳米纤维膜对100 mg · L-1 Cu2+、Ni2+及Cd2+溶液的吸附平衡时间和吸附容量的变化情况见图 6.由图 6可以看出,CS/PVA纤维膜膜对Cu2+、Ni2+及Cd2+的平衡吸附均在2 h内达到吸附平衡,而PVA纤维膜却在4 h后才达到吸附平衡.CS/PVA纳米纤维膜对Cu2+、Ni2+和Cd2+的吸附容量分别达到98.65、116.89和124.23 mg · g-1,高于常规沸石(相应值分别为3.2、2.6、2.3 mg · g-1)等吸附剂(甄豪波等,2011),而PVA纤维膜的平衡吸附容量却只有12.118、15.338、20.158 mg · g-1.
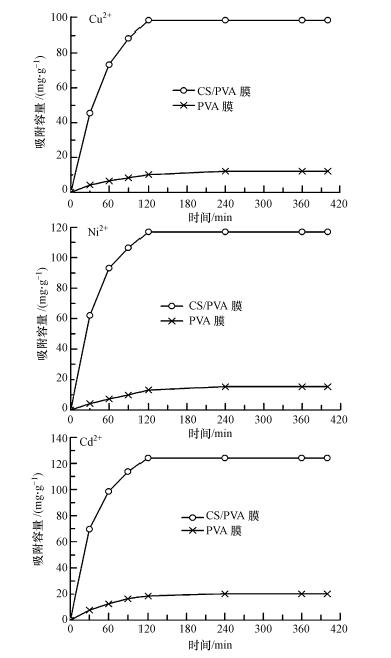 |
| 图6 CS/PVA纳米纤维膜和PVA纤维膜对Cu2+、Ni2+及 Cd2+的吸附容量 Fig. 6 Effect of reaction time on the adsorption capacity of chitosan/poly(vinyl alcohol)nanofiber membrane and poly(vinyl alcohol)fiber membrane |
CS/PVA纳米纤维膜对Cu2+、Ni2+及 Cd2+的平衡吸附量约为PVA膜的6~8倍,而CS/PVA纳米纤维膜中CS与PVA的质量比仅为20 ∶ 80.可见,PVA膜的吸附容量有限,CS/PVA纳米纤维膜对Cu2+、Ni2+及 Cd2+的吸附主要是CS起作用.
3.2.2 重金属离子初始浓度对CS/PVA纳米纤维膜吸附Cu2+、Ni2+及 Cd2+的影响不同重金属初始浓度下CS/PVA纳米纤维膜对Cu2+、Ni2+及 Cd2+的吸附容量变化如图 7a所示.从图 7a可看出,随着重金属离子初始浓度的增加,CS/PVA纳米纤维膜对3种金属离子的吸附容量急剧升高,吸附容量排序为Cd2 +>Ni2 +>Cu2 +,其中,在Cd2 +、Ni2 +、Cu2+初始浓度为1000 mg · L-1时,其吸附容量分别达到了363.21、 335.91、297.65 mg · g-1;在初始浓度为200 mg · L-1时,其吸附容量分别达到了198.55、176.96和149.00 mg · g-1,是CS粉末的4倍(孙兰萍等,2008),是CS微球的2.6倍( Wan Ngah et al., 2008).
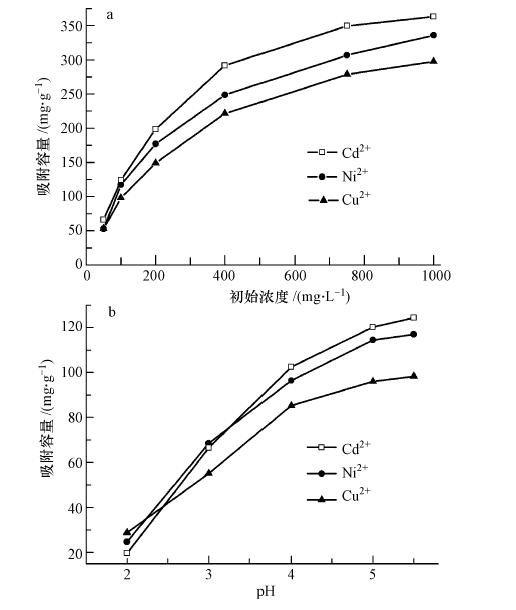 |
| 图7 重金属初始浓度(a)和pH值(b)对CS/PVA纳米纤维膜吸附重金属离子吸附容量的影响 Fig. 7 Effect of heavy metal initial concentration(a) and pH on the adsorption capacity of chitosan/poly(vinyl alcohol)nanofiber membrane(b) |
不同pH下CS/PVA纳米纤维膜对Cu2+、Ni2+及 Cd2+的吸附容量变化如图 7b所示.由图 7b可见,pH=2.0时,CS/PVA纳米纤维膜对Cd2+、Ni2+和Cu2+的吸附容量较低,分别为19.63、24.67和28.8 mg · g-1.随着pH值的升高,CS/PVA纳米纤维膜对Cd2+、Ni2+和Cu2+的吸附容量显著提高,在pH=5.5时,对 Cu2+、Ni2+和Cd2+的吸附容量分别达98.65、116.89和124.23 mg · g-1,去除率也分别达到了49.125%、58.445%和62.115%.当pH>5.5,金属离子析出产生沉淀,故本实验最高pH设为5.5.
实验结果表明,pH值是影响吸附容量的主要因素,因为CS中的—NH2既可与金属离子螯合,又可与 H+螯合,存在着一个平衡.H+的浓度能影响CS上活性基团的吸附能力,pH值降低,平衡朝着生成R—NH3+的方向进行,CS的氨基官能团(—NH2)会部分或全部去质子化(—NH3+);pH值升高,CS朝着与金属离子螯合的方向进行(贺小进等,2000).
3.2.4 离子强度对CS/PVA纳米纤维膜吸附Cu2+、Ni2+及Cd2+的影响不同NaCl 浓度下,CS/PVA纳米纤维膜对Cu2+、Ni2+及Cd2+的吸附容量变化如图 8所示.由图 8可见,CS/PVA纳米纤维膜对Cu2+、Ni2+及Cd2+的吸附容量均随NaCl浓度的增加而小幅减少.当NaCl浓度为100 mg · L-1时,Cu2+、Ni2+及Cd2+的吸附容量分别下降了8.07%、6.01%、6.57%.壳聚糖与Cu2+、Ni2+及Cd2+存在静电作用,当溶液离子强度增加时,带相同电荷的平衡离子之间的静电排斥作用会增强,使得CS/PVA的吸附容量减弱.此外,当溶液中存在电解质时,会发生盐析作用(Grover et al., 2005),盐析不利于吸附.而重金属离子在高离子强度溶液中溶解度减小,亲水性减弱,也不利于吸附.因此,较大的离子强度将有不利于CS/PVA对Cu2+、Ni2+及Cd2+的吸附.
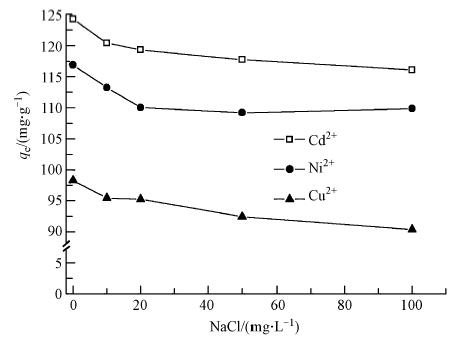 |
| 图8 离子强度对CS/PVA纳米纤维膜吸附Cu2+、Ni2+及Cd2+的影响 Fig. 8 Effect of ionic strength on adsorption of chitosan/poly(vinyl alcohol)nanofiber membrane |
CS/PVA纳米纤维膜对Cu2+、Ni2+及 Cd2+的竞争吸附随时间的变化见图 9.在25 ℃、pH=5.5的条件下,向20 mL浓度均为100 mg · L-1的Cd2+、Ni2+、Cu2+的混合金属溶液中投加15 mg吸附剂进行吸附实验,得到3种重金属离子共存条件下CS/PVA纳米纤维膜对Cu2+、Ni2+及 Cd2+的吸附动力学曲线(图 9).结果表明,在Cd2+、Ni2+、Cu2+的混合溶液中,CS/PVA纳米纤维膜无明显的选择性,去除率均在85% 以上,且吸附率排序依然为 Cd2+>Ni2+>Cu2+.
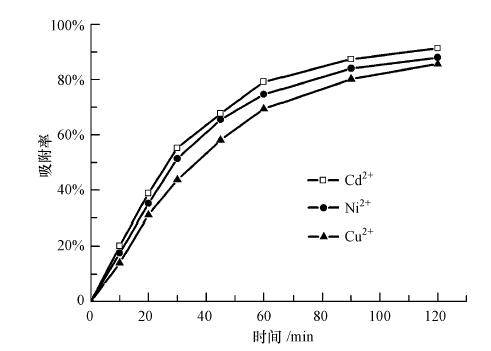 |
| 图9 CS/PVA纳米纤维膜的竞争吸附动力学曲线 Fig. 9 Kinetics curves for competitive adsorption on chitosan/poly(vinyl alcohol)nanofiber membrane |
CS/PVA纳米纤维膜对重金属离子的拟一级和拟二级吸附动力学图形见图 10,采用拟一级动力学模型(4)和拟二级动力学模型(5)拟合其吸附动力学曲线,结果见表 1.由图 6可知,CS/PVA纳米膜对Cu2+、Ni2+及Cd2+的吸附平衡时间为2 h,故本实验旨在探究其在2 h内的吸附速度.在反应初期,CS中带孤对电荷的氨基及羟基含量很高,对重金属的化学吸附作用很强,故在反应初期吸附进行得很快.在反应进行60 min时,Cu2+、Ni2+及Cd2+的吸附容量就达到了饱和吸附容量的70%以上,随反应的进行,带孤对电荷的氨基及羟基数目减少,且吸附的重金属离子会对进一步吸附存在空间位阻作用,因此,吸附作用减弱.反应至2 h,Cu2+、Ni2+及Cd2+的吸附容量基本不变,趋于平衡.
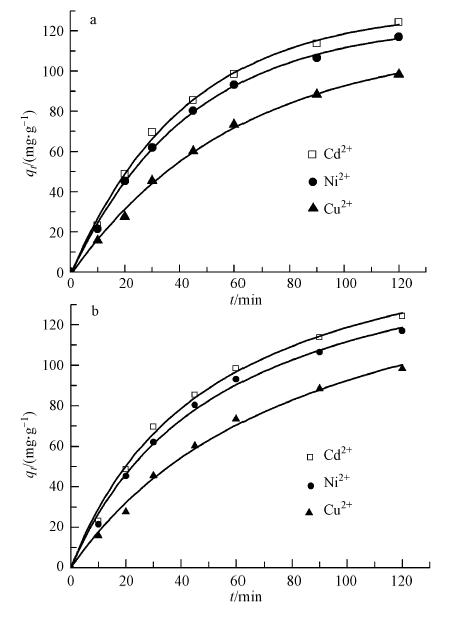 |
| 图10 CS/PVA纳米纤维膜对重金属离子的吸附动力学曲线(a.拟一级动力学吸附曲线,b.拟二级动力学吸附曲线) Fig. 10 Adsorption kinetics pseudo-first-order(a) and pseudo-second-order(b)of metal ions onto Chitosan/PVA nanofiber membrane |
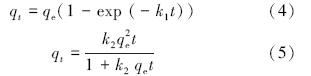
式中,qt是t时刻吸附剂的吸附容量(mg · g-1),qe是吸附平衡时的吸附容量(mg · g-1),k1为一级吸率常数(min-1),k2为二级吸附速率常数(g · mg-1 · min-1).
从表 1可知,CS/PVA纳米纤维膜对Cu2+、Ni2+及 Cd2+的吸附既符合拟一级动力学模型又符合拟二级动力学模型.吸附速率常数k2分别为6.5323×10-5、1.06315×10-4、1.0823×10-4 g · mg-1 · min-1,与Cu2+、Ni2+及 Cd2+达到吸附平衡的时间先后顺序一致,且与重金属离子竞争吸附实验结果一致.
| 表1 CS/PVA纳米纤维膜吸附 Cu2 +、Ni2 +及 Cd2 +的拟一级、拟二级动力学模型参数 Table 1 Adsorption kinetics pseudo-first-order and pseudo-second-order of metal ions onto Chitosan/PVA nanofiber membrane |
将CS/PVA纳米纤维膜对重金属离子的吸附容量Q对重金属离子的平衡浓度Ce做图,并用Langmuir等温线方程进行拟合,结果见图 11.表 2列出了Langmuir和Freundlich 吸附常数(Freundlich,1906)和可决系数.Freundlich 模型是在非均匀表面上发生吸附的模型,表达式为:
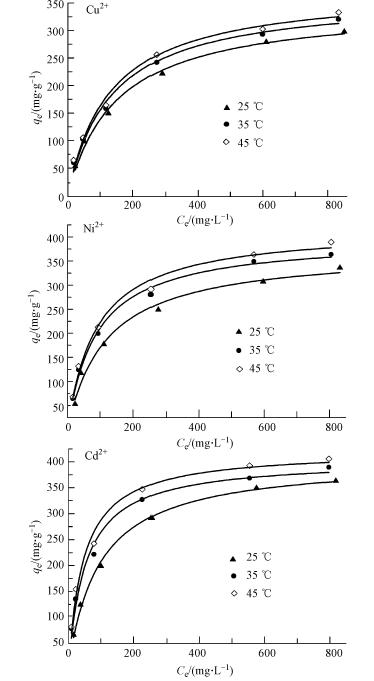 |
| 图11 CS/PVA纳米纤维膜吸附重金属的吸附等温线 Fig. 11 Adsorption isotherms of metal ions onto chitosan/poly(vinyl alcohol)nanofiber membrane |
| 表2 CS/PVA纳米纤维膜吸附 Cu2 +、Ni2 +及 Cd2+的 Langmuir 与 Freundlich 等温吸附模型参数 Table 2 Parameters of the Freundlich and Langmuir adsorption isotherms of metal ions on chitosan/poly(vinyl alcohol) |

式中,qe为平衡吸附量(mg · g-1),Ce为平衡浓度(mg · L-1),1/n是与吸附强度有关的系数(无量纲),KF是Freundlich吸附平衡常数,代表吸附能力的大小.从表 2可以看出,随着温度的升高,KF逐渐升高,1/n逐渐降低,表示吸附能力越来越大;同时,1/n>[0.1,0.5],说明CS/PVA纳米纤维膜对Cu2+、Ni2+、Cd2+的吸附为容易吸附.
Langmuir模型是非均匀分布的单分子层吸附模型,其一般形式为:

式中,qe为平衡吸附量(mg · g-1),Ce为平衡浓度(mg · L-1),参数b(L · mg-1)表征吸附材料表面的吸附点位对重金属离子亲和力的大小,b值越大,表明吸附点位对重金属离子的亲和力越大;K是吸附能力的量度,反映了吸附量的大小.表 2的结果表明,对Cu2+、Ni2+、Cd2+的吸附更符合Langmuir吸附模型,基本符合Freundlich吸附模型.在Langmuir等温吸附模型中,CS/PVA纳米纤维膜在25 ℃时对Cu2+、Ni2+、Cd2+的最大吸附量分别为345.6701、371.9959、403.8779 mg · g -1,基本符合实验所测得的数据.
应用Gibbs方程可求得CS/PVA纳米纤维膜对Cu2+、Ni2+、Cd2+的吸附自由能ΔG、吸附焓ΔH和吸附熵ΔS,其方程如下:
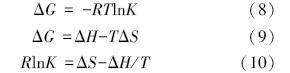
式中,R为气体摩尔常数,取值为8.314 J · K-1 · mol-1,T为绝对温度(℃),Ces和Cel分别是反应平衡时固相和液相的相对平衡浓度.K为吸附系数,若不考虑温度对ΔH和ΔS的影响,将式(10)中的RlnK对-1/T作图,从直线的斜率和截距可得ΔH和ΔS值,代入式(8)可求得ΔG,结果见表 3.
| 表3 CS/PVA纳米纤维膜对重金属的吸附热力学参数 Table 3 Thermodynamics function of sorption of metal ions on CS/PVA nanofibers |
吸附自由能ΔG可以反映吸附过程推动力的大小,其绝对值越大,吸附推动力越大.ΔG<0,说明反应属于容易进行的、自发的,而且随着温度的升高,ΔG 绝对值随温度的增加而逐渐增大,说明温度升高,该吸附反应的推动力变大,升温促有利于吸附.ΔH>0,ΔS>0,说明CS/PVA纳米纤维膜对重金属的吸附是吸热过程.
4 结论(Conclusions)1)采用静电纺丝法,在CS/PVA质量比20/80、电压25 kV、接收距离15.0 cm、流速0.15 mL · h-1的条件下,可制得纤维连续均匀、平均直径76.31 nm、表面积219.42 m2 · g-1的CS/PVA纳米纤维膜.红外光谱和XRD的结果显示,CS/PVA纳米纤维膜中CS与PVA之间形成了氢键,CS的晶体结构发生了化学变化.
2)CS/PVA纳米纤维膜对重金属离子的吸附在2 h内达到平衡,对Cu2+、Ni2+及Cd2+的吸附容量随重金属离子初始浓度的升高而升高,随着温度的升高而升高,随pH值升高而升高,在pH为5.5时达到最大.在25 ℃和pH为5.5的条件下,CS/PVA纳米纤维膜对100 mg · L-1的Cu2+、Ni2+及Cd2+的饱和吸附量分别为98.65、116.89和124.23 mg · g-1.
3)CS/PVA纳米纤维膜对水中Cu2+、Ni2+及Cd2+的吸附动力学符合Langmuir吸附模型,也基本符合Freundlich吸附模型,吸附为自发的吸热反应.
| [1] | Aliabadi M, Irani M, Piri H, et al. 2013. Electrospun nanofiber membrane of PEO/Chitosan for the adsorption of nickel, cadmium, lead and copper ions from aqueous solution[J]. Chemical Engineering Journal, 220: 237-243 |
| [2] | Chen F, Li X Q, Mo X M, et al. 2008. Electrospun chitosan-P(LLA-CL) nanofibers for biomimetic extracellular matrix[J]. Journal of Biomaterials Science, Polymer Edition, 19(5): 677-691 |
| [3] | Desai K, Kit K, Li J J, et al. 2008. Morphological and surface properties of electrospun chitosan nanofibers [J]. Biomacromolecules, 9(3): 1000-1006 |
| [4] | Desai K, Kit K, Li J J, et al. 2009. Nanofibrous chitosan non-wovens for filtration applications [J]. Polymer, 50(15): 3661-3669 |
| [5] | Devarayan K, Hanaoka H, Hachisu M, et al. 2013. Direct electrospinning of cellulose-chitosan composite nanofiber [J]. Macromolecular Materials and Engineering, 298(10): 1059-1064 |
| [6] | Ding B, Kim H Y, Lee S C, et al. 2002. Preparation and characterization of nanoscaled poly(vinyl alcohol) fibers via electrospinning [J]. Fibers and Polymers, 3(2): 73-79 |
| [7] | Freundlich H M F. 1906. Uber die adsorption in losungen [J]. Physical Chemistry, 57(A): 385-470 |
| [8] | Gamage A, Shahidi F. 2007. Use of chitosan for the removal of metal ion contaminants and proteins from water [J]. Food Chemistry, 104(3): 989-996 |
| [9] | Geng X Y, Kwon O H, Jang J. 2005. Electrospinning of chitosan dissolved in concentrated acetic acid solution [J]. Biomaterials, 26(27): 5427-5432 |
| [10] | Grover P K, Ryall R L. 2005. Critical appraisal of salting-out and its implications for chemical and biological sciences [J]. Chemical Reviews, 105(1): 1-10 |
| [11] | Haider S, Park S Y. 2009. Preparation of the electrospun chitosan nanofibers and their applications to the adsorption of Cu(II) and Pb(II) ions from an aqueous solution[J]. Journal of Membrane Science, 328(1/2): 90-96 |
| [12] | 贺小进, 谭天伟, 戚以政, 等. 2000. 球形壳聚糖树脂制备方法及吸附性能研究[J]. 离子交换与吸附, 16(1): 47-53 |
| [13] | Horzum N, Boyac E, Ero g ˇ lu A E, et al. 2010. Sorption efficiency of chitosan nanofibers toward metal ions at low concentrations[J]. Biomacromolecules, 11(12): 3301-3308 |
| [14] | Huang C, Chung Y C, Liou M R. 1996. Adsorption of Cu(II) and Ni(II) by pelletized biopolymer [J]. Journal of Hazardous Materials, 45(2/3) 265-277 |
| [15] | Juang R S, Shiau R C. 2000. Metal removal from aqueous solutions using chitosan-enhanced membrane filtration [J]. Journal of Membrane Science, 165(2): 159-167 |
| [16] | Klossner R R, Queen H A, Coughlin A J, et al. 2008. Correlation of chitosan's rheological properties and its ability to electrospin [J]. Biomacromolecules, 9(10): 2947-2953 |
| [17] | Lee M Y, Hong K J, Kajiuchi T, et al. 2005. Synthesis of chitosan-based polymeric surfactants and their adsorption properties for heavy metals and fatty acids[J]. International Journal of Biological Macromolecules, 36(3): 152-158 |
| [18] | Li N, Bai R B, Liu C K. 2005. Enhanced and selective adsorption of mercury ions on chitosan beads grafted with polyacrylamide via surface-initiated atom transfer radical polymerization[J]. Langmuir, 21(25): 11780-11787 |
| [19] | 林芳,贾新刚,秦磊,等. 2008. 壳聚糖-Cu(Ⅱ)吸附条件的优化[J].中国皮革, 27(3): 29-33 |
| [20] | Liu C X, Bai R B. 2006. Adsorptive removal of copper ions with highly porous chitosan/cellulose acetate blend hollow fiber membranes [J]. Journal of Membrane Science, 284(1/2): 313-322 |
| [21] | Merrifield J D, Davids W G, MacRae J D, et al. 2004. Uptake of mercury by thiol-grafted chitosan gel beads [J]. Water Research, 38(13): 3132-3138 |
| [22] | Ohkawa K, Cha D, Kim H, et al. 2004. Electrospinning of chitosan [J]. Macromolecular Rapid Communications, 25(18): 1600-1605 |
| [23] | Ohkawa K, Minato K I, Kumagai G, et al. 2006. Chitosan nanofiber[J]. Biomacromolecules, 7: 3291-3294 |
| [24] | Paipitaka K, Pornpra T, Mongkontalang P, et al. 2005. Characterization of PVA-chitosan nanofibers prepared by electrospinning [J]. Procedia Engineering, 8: 101-105 |
| [25] | Pakravan M, Heuzey M C, Ajji A. 2012. Core-shell structured peo-chitosan nanofibers by coaxial electrospinning[J]. Biomacromolecules, 13(2): 412-421 |
| [26] | Pearson F G, Marchessault R H, Liang C Y. 1960. Infrared spectra of crystalline Polysaccharides. V. Chitin[J]. Journal of Polymer Science, 43(141): 101-116 |
| [27] | Shalumon K T, Anulekha K H, Chennazhi K P, et al. 2011. Fabrication of chitosan/poly(caprolactone) nanofibrous scaffold for bone and skin tissue engineering [J]. International journal of biological macromolecules, 48(4): 571-576 |
| [28] | Subbiah T, Bhat G S, Tock R W, et al. 2005. Electrospinning of nanofibers [J]. Journal of Applied Polymer Science, 96(2): 557-569 |
| [29] | 孙兰萍,赵大庆,许晖,等. 2008.壳聚糖对镍吸附作用的研究[J].环境与健康杂志, 25(11): 979-982 |
| [30] | Twu Y K, Huang H I, Chang S Y, et al. 2003. Preparation and sorption activity of chitosan/cellulose blend beads[J]. Carbohydrate Polymers, 54(4): 425-430 |
| [31] | Vieira R S, Beppu M M. 2006a. Dynamic and static adsorption and desorption of Hg(II) ions on chitosan membranes and spheres[J]. Water Research, 40(8): 1726-1734 |
| [32] | Vieira R S, Beppu M M. 2006b. Interaction of natural and crosslinked chitosan membranes with Hg(II) ions[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 279(1/3): 196-207 |
| [33] | Wan Ngah W S, Endud C S, Mayanar R. 2002. Removal of copper(II) ions from aqueous solution onto chitosan and cross-linked chitosan beads[J]. Reactive and Functional Polymers, 50(2): 181-190 |
| [34] | Wan Ngah W S, Kamari A, Koay Y J. 2004. Equilibrium and kinetics studies of adsorption of copper (II) on chitosan and chitosan/PVA beads[J]. International Journal of Biological Macromolecules, 34(3): 155-161 |
| [35] | Wan Ngah W S, Ab Ghani S, Kamari A. 2005. Adsorption behaviour of Fe(II) and Fe(III) ions in aqueous solution on chitosan and cross-linked chitosan beads[J]. Bioresource Technology, 96(4): 443-450 |
| [36] | Wan Ngah W S, Kamari A, Fatinathan S, et al. 2006. Adsorption of chromium from aqueous solution using chitosan beads [J]. Adsorption, 12(4): 249-257 |
| [37] | Wan Ngah W S, Fatinathan S.2008.Adsorption of Cu(II) ions in aqueous solution using chitosan beads, chitosan-GLA beads and chitosan-alginate beads[J]. Chem Eng J,143:62-72 |
| [38] | Wang F F, Ge M Q. 2013. Fibrous mat of chitosan/polyvinyl alcohol/containing cerium(III) for the removal of chromium(VI) from aqueous solution[J]. Textile Research Journal, 83(6): 628-637 |
| [39] | Zhang H T, Li S B, Branford White C J, et al. 2009. Studies on electrospun nylon-6/chitosan complex nanofiber interactions[J]. Electrochimica Acta, 54(24): 5739-5745 |
| [40] | Zhang Y Y, Huang X B, Duan B, et al. 2007. Preparation of electrospun chitosan/poly(vinyl alcohol) membranes[J]. Colloid and Polymer Science, 285(8): 855-863 |
| [41] | 赵茜,邱东方,王晓燕,等. 2011.壳聚糖/氧化石墨烯纳米复合材料的形态和力学性能研究[J].化学学报, 69(10): 1259-1263 |
| [42] | 甄豪波,胡勇有,程建华. 2011.壳聚糖交联沸石小球对Cu2+、Ni2+及Cd2+的吸附特性[J].环境科学学报, 31(7): 1369-1376 |
| [43] | Zhou L M, Liu J H, Liu Z R. 2009. Adsorption of platinum(IV) and palladium(II) from aqueous solution by thiourea-modified chitosan microspheres[J]. Journal of Hazardous Materials, 172(1): 439-446 |
| [44] | Zhou Y S, Yang D Z, Nie J. 2007. Preparation and characterization of crosslinked chitosan-based nanofibers [J]. Chinese Chemical Letters, 18(1): 118-120 |
 2015, Vol. 35
2015, Vol. 35


