2. 福州大学环境与资源学院, 福州 351020;
3. 华侨大学土木工程学院, 厦门 361021
2. College of Environment and Resources, Fuzhou University, Fuzhou 351020;
3. College of Civil Engineering, Huaqiao University, Xiamen, Xiamen 361021
三氯乙烯(TCE)是地下水中分布最为广泛的氯代有机污染物之一.它属挥发性有机物,难降解,能在环境中持久存在,为毒性物质,且其降解中间产物二氯乙烯和氯乙烯都是有毒致癌物质,对人体和环境都具有极大的危害性.但是,由于TCE具有用途广、用量大、易渗透、难降解(Mitssumasa,2000)等特点,这就使得TCE进入地下水后很容易在地下水环境中迁移,污染地下水源,从而对环境和人类的健康构成极大的威胁(Sivavec et al., 1997),所以水体中氯代有机物的污染和治理是一个全球关注的问题.但由于氯代烃中有氯取代基,其电负性强、对微生物有很大毒性和抑制性,所以常规的生物氧化法很难对其处理,而其他的物化技术比如活性炭吸附、高级氧化、电动修复、膜分离技术以及空气吹脱等也都存在一定的局限性(Mackay and Cherry, 1989;吴德礼等,2006;钱翌等,2012).
近年,用纳米零价铁进行非生物还原脱氯引起人们的广泛关注.在许多情况下,用纳米零价铁颗粒进行还原脱氯,是解决氯代有机物问题的一种有效途径(Doong and Lai, 2006;Li et al., 2006;Lookman et al., 2004;李泽政等,2013).合成纳米铁的方法很多,但由于传统方法制备的纳米铁存在颗粒不均一、容易团聚,暴露在空气中容易发生氧化自燃等问题,限制了其广泛应用.针对上述问题,研究一种高效、廉价、性能稳定的纳米铁的合成方法非常必要.Wang等(Wang and Zhang, 1997)针对纳米铁性能的不稳定,制备了一种新型Fe/Pd双金属纳米铁材料,改性过的纳米双金属稳定性提高了,但仍然存在纳米铁的团聚和氧化现象.Quinn等(Quinn et al., 2005)提出了将纳米铁和修饰材料在乳液体系中混合,合成包覆型纳米铁,改性后纳米铁去除效果比单纯的纳米铁的去除效果好,但也存在纳米铁团聚的现象.本文针对纳米铁易氧化,采取表面包覆修饰改性技术,采用Shah法(Shah et al., 1972)配制微乳液,并利用反相微乳液(W/O)型微乳液将可聚合单体和引发剂引入油相体系中(Vaucher et al., 2002;Li et al., 2003; 薛伟,2005;金朝晖等2009),使该微乳体系原位聚合包覆,制备包覆型纳米零价铁材料(En-nZVI),考察此包覆纳米铁颗粒的稳定性和表面的亲水特性,以及对TCE的还原脱氯作用,以期为原位修复用于土壤和地下水的实际应用提供新的方法和理论依据.
2 材料和方法(Materials and methods) 2.1 主要试剂及仪器曲拉通X-100(乳化剂TX-100)(汕头市西陇化工厂有限公司),正戊醇(天津市光复精细化工厂),环己烷(上海试四赫维化工有限公司),七水合硫酸亚铁FeSO4·7H2O(国药集团化学试剂有限公司),硼氢化钾KBH4(国药集团化学试剂有限公司),甲基丙烯酸甲酯(MMA)(国药集团化学试剂有限公司),偶氮二异丁腈(国药集团化学试剂有限公司),普通铁粉(国药集团化学试剂有限公司).
X’pert PRO型X射线粉末晶体衍射仪(荷兰帕纳科公司),ThermoScientific Nicolet is10型傅立叶红外光谱仪(美国热电费世尔科技公司),JEM-2010FEF型透射电子显微镜(日本电子株式会社),Agilent7890型气相色谱(美国安捷伦公司),Agilent7890A-Agilent5975C气相色谱-质谱仪(美国安捷伦公司),DIONEX3000型离子色谱(美国戴安公司).
2.2 实验方法 2.2.1 纳米铁的制备称取一定量的TX-100和正戊醇混合液,混合摇匀,再加入适量的环己烷配置成混合体系.向混合体系中加入0.028 mol · L-1的FeSO4溶液10.00 mL,制得FeSO4微乳液体系.同理,向混合体系中加入1.5 mL的0.05 mol · L-1的KBH4溶液1.5 mL,制得KBH4微乳液体系.将FeSO4微乳液缓慢地滴加入微乳液KBH4中进行混合搅拌反应.反应结束后,置于30 ℃的恒温水浴锅中静置1 h左右.然后经过破乳,离心,洗涤,烘干,最终制得纳米铁微粒.
2.2.2 包覆型纳米铁的制备称取一定量的TX-100和正戊醇混合液,混合摇匀,再加入适量的环己烷配置成混合体系.向混合体系中加入0.028 mol · L-1的FeSO4溶液10.00 mL,制得FeSO4微乳液体系.同理,向混合体系中加入1.5 mL的0.05 mol · L-1 的KBH4溶液1.5 mL,制得KBH4微乳液体系.往FeSO4微乳液体系中加入5.00 mL甲基丙烯酸甲酯(MMA),充分振荡混匀,获得微乳液A.往KBH4微乳液体系中加入0.02 g的偶氮二异丁腈引发剂,充分振荡混匀,获得微乳液B.将微乳液B缓慢地滴加入微乳液A中进行混合搅拌反应.反应结束后,置于70 ℃的恒温水浴锅中静置,冷凝回流2 h左右.然后经过破乳,离心,洗涤,烘干,最终制得包覆型纳米铁微粒.
2.2.3 降解TCE的研究将制得的包覆型纳米铁微粒、单质铁粉、微乳液合成的纳米铁分别与初始浓度为10.00 mg · L-1的TCE于气浴振荡器中反应,并在0.5 h,1 h,2 h,5 h,12 h和24 h于取样口取样分析,考察单质铁粉,微乳液合成的纳米铁及包覆型纳米铁对TCE的去除率效果.TCE含量通过Agilent7890气相色谱仪采用顶空气相色谱法测定,色谱柱型号HP-5MS,目标污染物进样条件:柱温为60 ℃,进样口温度250 ℃;分流比为10 ∶ 1;检测器(ECD)温度为300 ℃;载气为高纯氮(99.999%);流速为1.0 mL · min-1;尾气吹扫流量为30 mL · min-1.溶液中氯离子溶度采用DIONEX3000型离子色谱仪测定.
3 结果与讨论(Results and discussion) 3.1 X射线衍射(XRD)分析采用X射线衍射仪测定样品的物相.测试条件:CuKα靶,电压为40 kV,2θ角度在30°~90°,电流为50 mA.由XRD的测试结果可知,在30°~90°扫描衍射角范围内,样品出现了44.687°和82. 326°明显的衍射峰,对照铁的标准 PDF 卡片(PDF card no.1-1267)可知:这两个峰分别对应零价铁(Fe0)的110(44.6732°)和211(82.3326°)的晶面衍射,这说明采用微乳液原位聚合的包覆型纳米铁颗粒中铁主要是以零价铁(Fe0)形态存在,未发现铁的其它晶型结构.
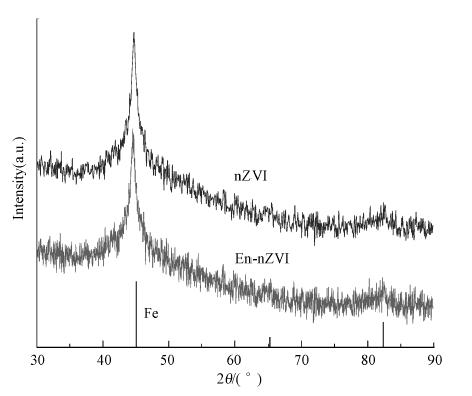 |
| 图 1 纳米铁及包覆型纳米铁的XRD分析图 Fig. 1 The powder XRD pattern of nZVI and En-nZVI particles |
包覆型纳米铁的红外光谱分析如图 2所示.由图可以看出,谱线中出现了较强的聚甲基丙烯酸甲酯(PMMA)的特征吸收峰:其中C O的伸缩振动特征吸收峰对应于1732 cm-1的吸收峰,C—O—C的特征振动峰对应于1150,1192,1242和1265 cm-1的特征峰,而CH3的伸缩振动和弯曲振动吸收峰则分别对应于1388,1454和2951 cm-1的吸收峰,在2850 cm-1也出现了微弱的CH2的特征吸收峰;而实验中并没有出现引发剂(AIBN)的峰,这是由于在微乳液原位聚合的过程中,引发剂(AIBN)遇热易发生分解,故在FT-IR的谱图中检测不到引发剂(AIBN)的特征吸收峰.这说明通过微乳液聚合法对纳米铁进行了成功的原位聚合,并且生成的包覆体PMMA包覆在纳米铁的表面.
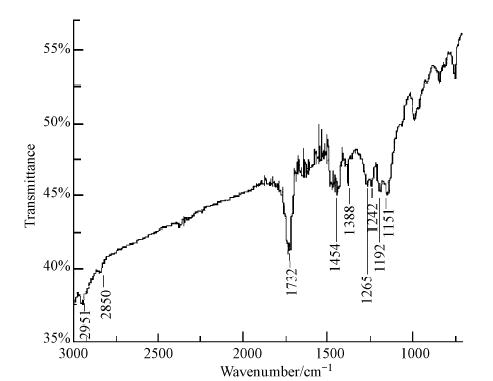 |
| 图 2 包覆型纳米铁的FT-IR图 Fig. 2 FT-IR spectrum of the En-nZVI particles |
图 3是微乳液原位聚合的包覆前后纳米铁的TEM图.测试条件:加速电压为200 kV;检验依据:JY/T 011—1996;环境温度为22.9 ℃;环境湿度为18%.测得的包覆型纳米铁的粒径如图 3所示.由图可以看出,包覆型纳米铁的平均粒径在102 nm.与纳米铁相比,包覆型纳米铁的粒径明显增大,这是由于包覆后的纳米铁由于表面包覆一层聚合有机单体PMMA,形成了具有核-壳的纳米材料结构,增大了纳米铁颗粒的粒径.另外,包覆型纳米铁会有少量的较大的包覆体出现,这是由于在微乳液原位聚合反应中,包覆是对单个纳米铁进行的多核包覆过程,这使得包覆后的纳米铁的粒径明显比单个纳米铁的粒径来得大.
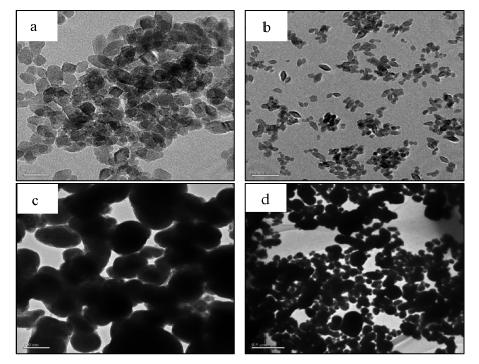 |
| 图 3 包覆前(a,b)后(c,d)纳米铁的TEM图 Fig. 3 TEM spectra of nZVI before(a,b) and after(c,d)coated |
为了考察包覆后纳米铁表面特性的改变,设计了3组接触性实验,实验中水和TCE的体积比为3 ∶ 2,实验结果如图 4所示.从图可以看出,(a)水和TCE混合后,由于TCE密度比水重而沉入底部,发生分层现象;(b)纳米铁,水和TCE混合后,由于纳米铁表面呈亲水性,存在于水和TCE的中间层;(c)包覆后的纳米铁和水混合后,由于包覆的纳米铁密度比水重,沉降在TCE的底部,与底部的TCE溶液发生了互溶并均匀地分布于TCE溶液中.这说明通过包覆,纳米铁的表面性质发生了变化,由亲水性变成了亲油性;而且,包覆后的纳米铁由于密度比水重,有利于纳米铁与水中重质非水相液体发生接触,提高了其在处理地下水中重质非水相液体污染的应用范围.
 |
| 图 4 包覆型纳米铁与TCE的接触性(a. 水和TCE;b. 纳米铁、水和TCE;c. 包覆型纳米铁、水和TCE) Fig. 4 En-nZVI particles in contacting with TCE(a.Water and TCE;b. nZVI,Water and TCE;c. En-nZVI,Water and TCE) |
通过XRD分析,观测Fe0晶体衍峰的消失,考察包覆型纳米铁在空气中的稳定性,结果如图 5所示.由图可以看出,随着放置时间的延长,包覆型纳米铁的Fe0晶体衍射峰逐渐减弱,放置3 d,Fe0的标准衍射峰的强度减弱70%,但未出现其它铁氧化物的衍射峰;当放置5 d,Fe0的标准衍射峰完全消失,同时产生三氧化二铁(Fe2O3)的100(33.10)的晶面衍射;这说明包覆后纳米铁能够在空气中稳定存在3 d,与未包覆的纳米铁暴露在空气马上发生氧化自燃相比,包覆提高了纳米铁在空气中的稳定性.
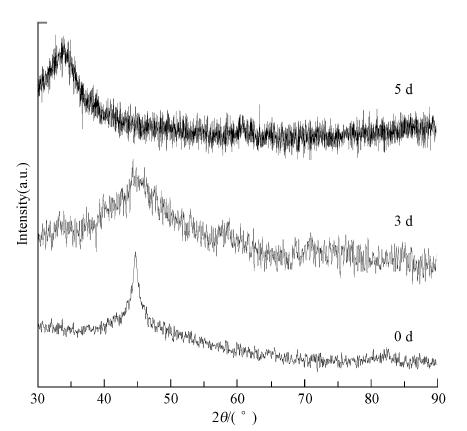 |
| 图 5 包覆型纳米铁的稳定性 Fig. 5 Stability of the En-nZVI particles |
单质铁、纳米铁和包覆型纳米铁对TCE的去除效果如图 6所示.由图可以看出,反应初期,3种材料对TCE的反应速率顺序为:纳米铁>单纯铁粉>包覆型纳米铁.这是由于未包覆纳米铁粒径小、比表面积大,能快速与TCE接触并反应;单质铁粉虽然经过一定的酸洗处理,但由于其自身粒径较大,与TCE分子发生接触的几率低于纳米铁;包覆型纳米铁由于表面包裹着一层高分子聚合物,与TCE发生反应时,TCE分子首先被表面高分子聚合物吸附在纳米铁颗粒表面,然后,TCE溶解表面高分子聚合物PMMA,穿透包覆层,进而与核内的纳米铁发生反应,因此,在反应初期,包覆型纳米铁的反应速率比纳米铁及单质铁粉的反应速率低.但是随着TCE对包覆型纳米铁表层聚合单体的溶胀,释放出的纳米铁与TCE进一步反应.反应24 h,包覆型纳米铁达到和纳米铁相同的对TCE去除率,均超过了92%.这说明包覆型纳米铁表面由于聚合单体的存在,虽然反应速率会比纳米铁的反应速率低,但是延长反应时间,包覆型纳米铁并没有降低其对TCE的去除效能,而且包覆型纳米铁表面的聚合单体能很好地解决纳米铁在空气中容易氧化的缺陷,有望拓展纳米铁在实际工程中的应用.
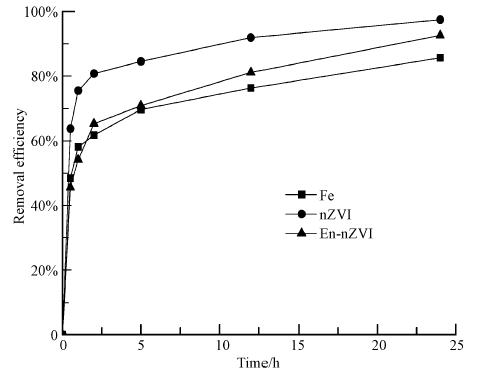 |
| 图 6 包覆型纳米铁对TCE去除率的影响 Fig. 6 Effect of the removal efficiency of TCE by En-nZVI particles valent iron |
纳米铁还原去除TCE的过程中,如果反应不彻底,就会产生含氯中间产物(如二氯乙烯、氯乙烯等),这些含氯中间产物仍然具有很高的毒性,有的甚至比TCE本身更加有害,所以,去除TCE的最终目标是对其完全脱氯,降解为烷烃或者完全矿化成CO2,而不含有任何含氯的碳氢化合物.包覆型纳米铁对TCE的还原脱氯效能如表 1所示.根据文献报道(Zhang,2003;Campbell et al., 1997;Liu et al., 2005,),结合本文试验TCE脱氯过程,反应24 h,包覆型纳米铁对氯离子的去除率达到了90.0%时,略小于理论脱氯率的95.80%,可以推断纳米铁在还原TCE的过程中,作为电子供体,提供电子给TCE,TCE作为电子受体,接受电子脱掉氯离子发生还原反应,TCE去除过程不是通过一步脱掉3个氯来完成的,可能脱氯过程中通过逐级脱氯,产生了其它含氯的中间产物,如生成二氯乙烯(DCE)、一氯乙烯(VC)及乙烯或是乙烷等小分子有机物,且脱氯的反应速率会随着有机物含氯数的减少而降低.
| 表1 包覆型纳米铁对TCE的脱氯实验 Table 1 The dechlorination of TCE by En-nZVI particles |
1)采用甲基丙烯酸甲酯(MMA)为聚合单体,偶氮二异丁腈(AIBN)为引发剂,通过微乳液原位聚合法成功制备了包覆型纳米铁.
2)XRD、FI-IR 、TEM和接触性试验表明:包覆型纳米铁粒径分布窄且均匀,平均粒径约为102 nm;微乳液原位聚合生成的PMMA包覆通过单核和多核包覆在纳米铁的表面,从而改变其表面亲水性,与纳米铁相比,更有利于吸附疏水性的TCE.
3)包覆后的纳米铁可以在空气暴露条件下稳定存在3 d,很好地克服了纳米铁在空气中容易氧化自燃的缺陷,而且该包覆纳米铁对TCE有很高的脱氯降解效果,有望扩大纳米铁在实际工程中的应用范围.
| [1] | Campbell T J, Burris D R, Roberts A L, et al. 1997. Trichloroethylene and tetrachloroethylene reduction in a metallic iron-water-vapor batch system[J]. Environmental Toxicology and Chemistry, 16(4): 625-630 |
| [2] | Doong R, Lai Y L. 2006. Effect of metal ions and humic acid on the dechlorination of tetrachloroethylene by zerovalent iron[J]. Chemosphere, 64(3): 371-378 |
| [3] | Li F, Vipulanandan C, Mohanty K K. 2003. Microemulsion and solution approaches to nanoparticle iron production for degradation of trichloroethylene[J]. Colloids and Surfaces (A: Physicochemical and Engineering Aspects), 223(1/3): 103-112 |
| [4] | Li Z H, Willms C, Alley J, et al. 2006. A shift in pathway of iron-mediated perchloroethylene reduction in the presence of sorbed surfactant—A column study[J]. Water Research, 40(20): 3811-3819 |
| [5] | 李泽政, 韩宝平, 朱雪强, 等. 2013. 零价铁去除水中三氯乙烯试验研究[J]. 江苏农业科学, 41(4): 322-324 |
| [6] | Liu Y Q, Majetich S A, Tilton R D, et al. 2005. TCE dechlorination rates, pathways, and efficiency of nanoscale iron particles with different properties[J]. Environmental Science & Technology, 39(5): 1338-1345 |
| [7] | Lookman R, Bastiaens L, Borremans B, et al. 2004. Batch-test study on the dechlorination of 1, 1, 1-trichloroethane in contaminated aquifer material by zero-valent iron[J]. Journal of Contaminant Hydrology, 74(1/4): 133-144 |
| [8] | Mackay D M, Cherry J A. 1989. Groundwater contamination: Pump-and-treat remediation[J]. Environmental Science & Technology, 23(6): 630-636 |
| [9] | Mitssumasa. 2000. Water Pollution Control Policy and Management: The Japanese Experience[M]. Japan: Published by Gyosei Co., Ltd. 25-31 |
| [10] | 钱翌, 岳飞飞, 褚衍洋. 2012. 三氯乙烯环境污染修复技术研究进展[J]. 环境化学, 31(9): 1335-1343 |
| [11] | Quinn J, Geiger C, Clausen C, et al. 2005. Field demonstration of DNAPL dehalogenation using emulsified zero-valent iron[J]. Environmental Science & Technology, 39(5): 1309-1318 |
| [12] | Shah D O, Tamjeedi A, Falco J W, et al. 1972. Interfacial instability and spontaneous formation of microemulsions[J]. AIChE Journal, 18(6): 1116-1120 |
| [13] | Sivavec T M, Mackenzie P D, Horney D P, et al. 1997. Redox-active media for permeable reactive barriers [A]//International Containment Technology Conference[c]. Florida: St. Petersburg. 753-759 |
| [14] | Vaucher S, Fielden J, Li M, et al. 2002. Molecule-based magnetic nanoparticles: synthesis of cobalt hexacyanoferrate, cobalt pentacyanonitrosylferrate, and chromium hexacyanochromate coordination polymers in water-in-oil microemulsions[J]. Nano Letters, 2(3): 225-229 |
| [15] | Wang C B, Zhang W X. 1997. Synthesizing nanoscale iron particles for rapid and complete dechlorination of TCE and PCBs[J]. Environmental Science & Technology, 31(7): 2154-2156 |
| [16] | 王薇, 金朝晖, 李铁龙. 2009. 包覆型纳米铁的制备及其去除三氯乙烯的研究[J]. 中国环境科学, 29(8): 811-815 |
| [17] | 吴德礼, 王红武, 马鲁铭. 2006. Ag/Fe催化还原体系处理水中氯代烃的研究[J]. 环境科学, 27(9): 1802-1807 |
| [18] | 薛伟. 2005. 微乳液法制备超微细包覆型催化剂及其催化苯酚氧化羰基化反应研究[D]. 北京: 北京化工大学. 27-30 |
| [19] | Zhang W X. 2003. Nanoscale iron particles for environmental remediation: an overview[J]. Journal of Nanoparticle Research, 5(3/4): 323-332 |
 2014, Vol. 34
2014, Vol. 34


