城市污水管网作为城市基础设施的重要组成部分,主要负责城市生活污水、工业废水及雨水的收集和输送.污水在长时间、长距离流动的过程中其水质发生着不断的变化,而水质的这种变化主要是由于管网内生物膜的作用(Chen et al.,2003).1995年,Özer等(1995)用一根3 m长的管段进行模拟实验,发现管壁的生物膜在有机物质的去除过程中发挥了主要作用;2001年,Chen等(2001)对一段长1.5 km的混凝土排水管道的水质进行了监测,ATP含量实验表明,污水相和沉淀相均包含活性微生物,其中,沉淀相的微生物作用是污水水质变化的重要原因.由此可以推断,管网中的生物膜对污水水质存在着不同程度的影响,生物膜的存在使污水进入管道时相当于进入了一个推流式生化反应器,污染物源源不断地发生着生化降解及转化,而这些过程的发生直接影响着后续污水处理厂的入流水质,进而影响污水处理的效果.目前,有关管网生物膜的作用受到越来越多的关注,但针对管网沿程中生物菌群的演替规律却尚无系统研究.因此,本研究通过模拟管段中试试验装置,对城市污水管网中生物膜的特性、结构及生物群落演替变化规律进行探究.
2 材料与方法(Materials and methods) 2.1 试验装置污水管道模拟反应器如图 1所示.模拟管段试验装置主体由管径25 mm的PVC管构成,总有效长度1200 m,为了充分模拟实际污水管道重力式水流状态,坡度设为5‰.管材内壁用砂纸适当打磨,以控制管道沿程阻力系数及雷诺数,使其与钢筋混凝土管的粗糙度相接近,从而保证流动特性与钢筋混凝土管相仿.模拟管段共有35层,层与层之间通过尺寸为50 mm×30 mm(直径×高)的圆柱形检查井连接,检查井材质为有机玻璃.每层模拟管段上均设有取样点,为了便于观察模拟管段内的水流状态,取样点两侧设有活结连接的长为500 mm的有机玻璃管段,每节有机玻璃管段内放置尺寸为500 mm×10 mm×3 mm(长×宽×高)的经适当打磨的有机玻璃试样片1个作为管道生物膜附着载体,同时,模拟管段外部裹有保温材料,使其处于一个避光恒温的环境中.
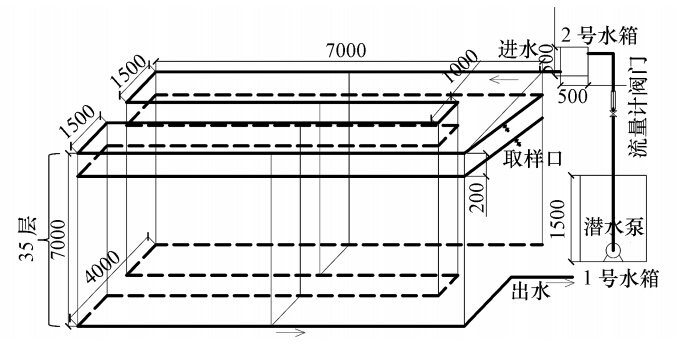 |
| 图 1 城市污水模拟管段装置(单位: mm) Fig. 1 Simulated urban sewer network system |
整个系统在室温下运行,同时保证系统具有良好的密封性,试验温度为(26±2)℃,溶解氧为(0.30±0.05)mg · L-1.系统依靠潜水泵将1号水箱内的水提升至高度为8 m的2号水箱,1号和2号水箱的尺寸分别为1200 mm×1500 mm(直径×高)、500 mm×500 mm×500 mm(长×宽×高),2号水箱底部开有直径为25 mm的出水口,污水依靠重力流入模拟管段.在连续运行期间,污水的流量为(0.12±0.02)m3 · h-1,反应器的水力停留时间为120 min,流速约为0.16 m · s-1,充满度为0.6.试验采用人工配水作为原水,其组成如表 1所示(Baban et al., 2009),原水水质见表 2.
| 表1 人工配制城市污水的组成 Table 1 Components of synthetic wastewater |
| 表2 配水水质 Table 2 Synthetic wastewater quality |
反应器共设6个取样点,分别位于距进水口200、400、600、800、1000、1200 m处.取模拟管段内载片进行生物膜厚度、pH、DO、结构及生物群落检测.模拟管段稳定运行至120 d时,分别取不同模拟管段内载片上的生物膜进行结构及种群分析.
2.3.1 生物膜厚度、pH及DO测定利用微电极(Unisense Denmark)测定管壁生物膜厚度、pH及DO,pH和DO电极顶端直径均为10 μm.具体分析方法是以用N2吹脱后的超纯水为基液,将管壁生物膜稳定在尼龙网上保持静止,从而使微电极穿透生物膜分析其内部环境(Li et al.,2004;Han et al., 2012).
2.3.2 生物膜结构分析预处理:将附着生物膜的载片置于玻璃培养皿中,加4%的多聚甲醛,使生物膜全部浸泡于其中,固定6 h以上;把固定好的生物膜于30%、50%、70%、80%、90%、100%的酒精溶液中梯度洗脱,每个浓度溶液洗脱时间为15 min;将脱水的生物膜于酒精 : 乙酸异戊酯=1 : 1的溶液中置换5 min,再在100%乙酸异戊酯溶液中置换5 min;把置换好的生物膜去掉上清液,转移到干净培养皿中并在通风橱中风干.风干的生物膜采用JSM-6510LV型扫描电子显微镜进行观察.
2.3.3 生物膜群落分析采用OMEGA E.Z.N.A.TM Soil DNA Kit D5625-01试剂盒提取管壁生物膜DNA.使用TP600型梯度PCR扩增仪,以提取的总DNA为模板,利用原核生物通用引物GC-338F(5-CGC CCG CCG CGC GCG GCG GGC GGG GCG GGG GCA CGG GGG GAC TCC TCA GGG AGG CAG CAG-3)和518R(5-ATT ACC GCG GCT GCT GG-3)为引物扩增基因.PCR扩增反应体系(50 μL)组分为:5 μL Buffer、4 μL dNTP、2 μL 338F、2 μL 518R、32.75 μL无菌超纯水、0.25 μL酶Extap.扩增条件为:94 ℃预热9 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸30 s,30个循环;72 ℃延伸7 min.反应产物用2%的琼脂糖凝胶电泳检测.
DGGE所用仪器为DCodeTM Universal Mutation Detection System(U.S.A,Bio-RAD Co).DGGE电泳所用胶的浓度为8%,其变性梯度范围为40%~70%(100%的变性剂中含有7 mol · L-1的尿素和40%的去离子甲酰胺)),上量为15 μL的PCR产物(第1轮扩增),其运行条件为:在1×TAE电缓冲液中,60 ℃条件下,130 V预沉10 min,之后80 V运行12 h,电泳完成后,Gel Red染色30 min,然后在紫外照射下观察电泳结果(Wu et al., 2013;马悦欣等,2003;刘新春等,2005).
将优势条带用专业切胶刀切割下来,放入1.5 mL的离心管,用300 μL的超纯水清洗3遍;然后加入50 μL超纯水-20 ℃冷冻,在56 ℃解冻30 min,继续-20 ℃冷冻,重复冻溶3次,上清液即为回收的DNA溶液.将割胶回收后的DNA溶液重新进行PCR扩增,扩增条件与之前相同,将扩增好的PCR产物经克隆后,将菌液寄生工生物工程(上海)有限公司进行测序.
2.3.4 细菌总数、氨化细菌数与反硝化细菌数的测定预处理:称取1 g生物膜装入已灭菌的磨口锥形瓶中,加入超纯水100 mL,加上塞子并用封口膜密封,置于摇床上振荡30 min,制成均匀悬浊液.将制成的均匀悬浊液按10倍梯度稀释法稀释成一系列梯度溶液,本文总共稀释6个梯度,分别为10-1、10-2、10-3、10-4、10-5、10-6.
采用平板法测定细菌总数,分别称取蛋白胨10 g,牛肉浸膏3 g,NaCl 5 g,琼脂18 g,加纯水1000 mL,调pH=7.4,然后分装于2个1000 mL的烧杯中,在121 ℃高压锅中灭菌30 min,灭菌后置于无菌操作台中等待降温,当温度降为45 ℃左右时,在无菌操作台中快速完成倒平板.等平板凝固后,取稀释好的样品100 μL涂平板,同时做3组平行样,并用无菌水做空白对比,然后置于(37±1)℃恒温培养箱内培养24 h,最后取出计数.
氨化细菌与反硝化细菌计数采用MPN多管发酵法.首先制备氨化细菌培养基(蛋白胨5 g,K2HPO4 0.5 g,KH2PO4 0.5 g,MgSO4 · 7H2O 0.5 g,纯水1000 mL,pH=7.2)和反硝化细菌培养基(KNO3 2 g,MgSO4 · 7H2O 0.2 g,K2HPO4 1.0 g,KH2PO4 1.0 g,柠檬酸钠5.0 g,纯水1000 mL,pH=7.2),将培养基配制好后装入试管中,每管装5 mL,塞上硅胶塞(反硝化培养基的试管中应放入倒置杜氏发酵管,以检测气体的生成),121 ℃灭菌30 min,每个样品需培养基18管.然后制备纳氏试剂、格里斯试剂I和Ⅱ及二苯胺试剂.最后将灭菌分装好的各培养基试管取出,用无菌吸管接种样品的稀释液1 mL,每个稀释度接种3管,接种6个稀释度(10-1、10-2、10-3、10-4、10-5、10-6),另取一管培养基接种1mL无菌水作为对照,并于25~30 ℃恒温培养箱中培养.
通过检测培养第3 d和5 d培养基的浑浊度,进行氨化细菌的检测.培养第7 d,取培养液5滴于白瓷比色板上,加纳氏试剂2滴,检查是否出现棕褐色,以确定是否产生氨.通过检查培养14 d后杜氏发酵罐中是否有气泡出现,培养液是否变浑浊,进行反硝化细菌的测定.用纳氏试剂检查是否有氨产生;用格利斯试剂Ⅰ及Ⅱ检测有无亚硝酸盐生成;用二苯胺试剂检测硝酸盐,判断反硝化作用进行情况.然后根据检测的结果结合MPN数值表计数.
2.3.5 水质分析实验测定的水质指标分别是COD、氨氮(NH3-N)、硝氮(NO-3-N)、总磷(TP),均采用国家标准方法测定.
3 结果与讨论(Results and discussion) 3.1 污水管网中生物膜基本特性管壁生物膜生物量是微生物活性的物质基础,一定环境条件下,管壁生物膜生物量随时间和位置而变化,相应的生物膜厚度也会随之发生变化,沿程分布规律也会由于基质浓度及微生物生长速度的不同而不同.
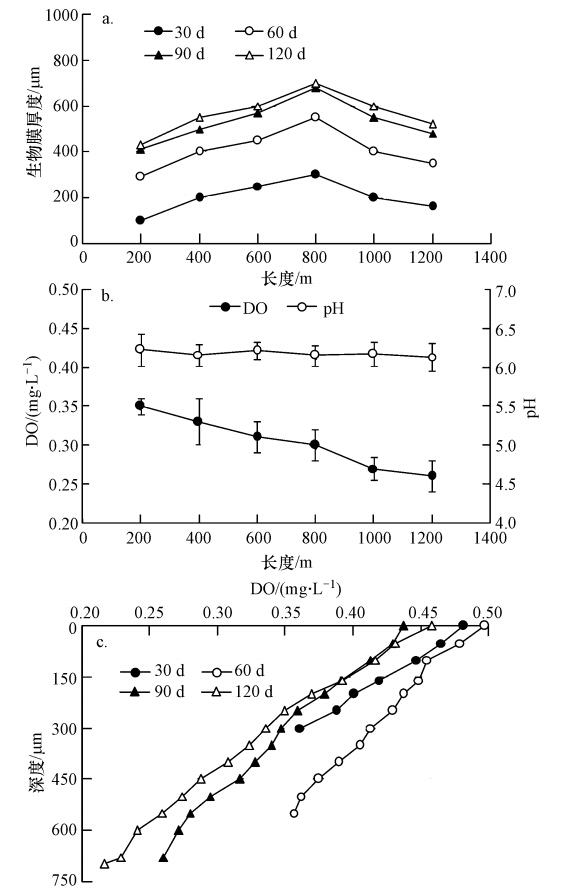 |
| 图 2 生物膜厚度、pH及DO沿程变化 Fig. 2 Variation of biofilm thickness,pH and DO along the length of simulated networks |
管道模拟反应器连续运行以来,在其运行30、60、90及120 d后分别取附着在载片上的生物膜,利用微电极测定厚度、pH及DO.当电极处于N2吹脱后的超纯水基液中时,检测线变化趋势较为稳定,当电极检测到生物膜时检测线开始发生突变,直到穿透生物膜后电极再次处于基液中时,检测线恢复平稳,从而确定生物膜厚度.不同时期内生物膜厚度的沿程变化如图 2a所示,可以看出,随着运行时间的延长生物膜厚度不断增加,到90 d后逐渐趋于稳定.运行30 d时,管网沿程生物膜厚度由最初的100 μm逐渐增大,并在800 m处达到最大厚度300 μm,随后沿程逐渐减小;运行60、90、120 d时,生物膜厚度分别由最初的290、410、430 μm开始沿程增加,并在800 m处分别增加到最大厚度550、680、700 μm,此后随距离增加逐渐减小.这主要是由于初始的水力冲刷作用较大,生物膜外层松散的结构在向外伸展的过程中被水流不断冲走,从而生物膜容易脱落(Boon,1995).随着距离的增加生物膜厚度相应地增加,其结构也在不断地发生变化,由于在增加的过程易吸收的营养物质也会源源不断地被消耗.因此,在800 m处生物膜厚度出现峰值,随后因管道中污水缺乏易吸收的营养物质而导致生物膜厚度明显降低.
利用微电极测定生物膜pH、DO沿程的变化,结果如图 2b所示.从图中可以看出,在污水输送过程中生物膜pH值变化不大,而生物膜DO随距离的增加呈逐渐降低的趋势,平均值由0.35 mg · L-1减小为0.26 mg · L-1,表明生物膜内的环境随着距离的增加缺氧程度逐渐加剧.从图 2c中可以看出,运行30、60、90、120 d时沿程800 m处的生物膜厚度分别约为300、550、680、700 μm,在90 d时达到680 μm后逐渐趋于稳定.图 2c是管道模拟反应器运行30、60、90、120 d时沿程800 m处生物膜内部DO的变化.从图中可以看出,生物膜内DO均小于0.5 mg · L-1,这表明生物膜内部基本是一个缺氧的环境.同时可以看出,DO随着生物膜厚度的增加呈逐渐降低的趋势.
3.2 生物膜结构与菌群构造变化规律利用扫描电镜进一步对生物膜结构及菌群构造变化进行分析,结果如图 3所示.从图中可以看出,在200、400 m处生物膜表面结构平整、均匀且致密;在600、800 m处生物膜表面粗糙凹凸不平且结构疏松,起伏较大;在1000、1200 m处生物膜结构进一步恶化,出现了大量的胞外聚合物,细菌细胞被粘质外鞘包裹起来,此时以各种细胞外化合物构成为主体.
 |
| 图 3 生物膜结构沿程变化 Fig. 3 Variation of biofilm structure along the length of simulated networks |
污水管网生物膜的表面平整状况及厚度取决于污水的组成成分和污水量,污水管网内的通风情况、生长期及营养物、溶解氧的供应情况和污水流动的速率等因素有关(Boon,1995).在污水刚进入管段内时,水流流速较快,管网内生物膜厚度较薄,结构致密且表面平整,均匀性好;随着生物膜的堆积及初始形成生物膜在水力冲刷作用下脱落,致使沿程生物膜厚度增加,引起水流速度开始减缓,从而生物膜更易积累增厚,导致生物膜表面凹凸不平、结构疏松.
不同管段处生物膜表面都存在如孔洞或沟渠的结构,流体在生物膜内空隙通道形成对流,从而增大了局部传质系数.粗糙生物膜结构增大了生物膜比表面积,深层生物膜除依靠扩散作用得到基质外,还从液相直接获得营养(于鑫等,2003),这种结构有利于生物膜的生长发育,从而能有效去除水中的污染物质.
从放大5000倍的沿程平面图中可以看出,在200 m处微生物呈现球状、链球状、杆状、球杆状、链杆状等形状;400 m处出现弧状菌,链球状菌、链杆状菌有所减少;600 m处的球状菌、杆状菌、球杆状菌可能被大量胞外聚合物包裹;800 m出现了形态不规则的球状菌,链杆状菌、球杆状菌有所减少;1000 m和1200 m菌群以不规则形态的球状菌群为主,同时存在少量杆状菌,由于此时营养条件趋于恶劣,菌群只有通过减小个体形态、减弱繁殖能力来适应生存,随之空隙及通道也减少.具体生物种属变化情况见PCR-DGGE分析.
对管网生物膜菌群总数利用平板计数法进行测定,结果如图 4所示.从图中可以看出,管网生物膜中细菌的数量总体上是呈随着距离的增加逐渐减少的趋势.这是由于随着距离的增加,易吸收的营养物质不断被消耗,可被微生物利用的物质也减少,相应的总细菌数就会减少.生物膜剖面图的沿程变化进一步表明,生物膜厚度先增加后减小,管壁生物膜结构及菌群构造沿程变化较大.
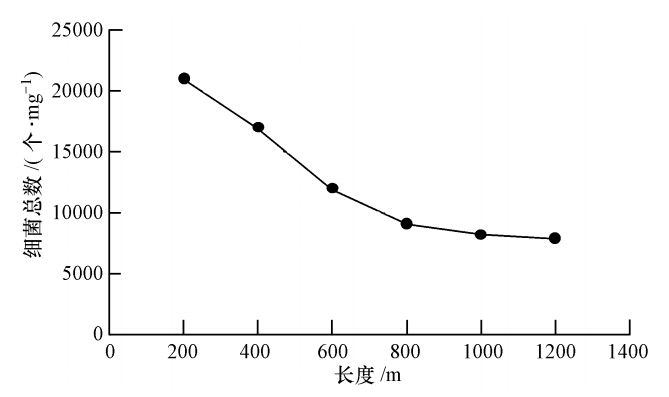 |
| 图 4 细菌总数的沿程变化 Fig. 4 Variation of total number of bacteria along the length of simulated networks |
采用PCR-DGGE技术对管网沿程生物膜菌群的变化进行研究,经测定所得到的图谱如图 5所示.模拟管段共设有6个取样点,图 5中从左到右分别以a、b、c、d、e、f表示,对应的距离依次是200、400、600、800、1000、1200 m.图谱中不同亮带表明管网生物膜中微生物种类极其丰富,尤其是在初始的200 m处,亮带数共有28条;随后菌群种数逐渐减少,在1000 m以后亮带数有13条,沿程菌群种数减少的情况与扫描电镜结果相似.沿程中主要菌群有10种,其中,条带1、5、6、9一直存在且变化不大,条带2在d泳道开始逐渐加强,条带3随着距离的增加在c泳道逐渐减弱,条带4、8从b泳道出现随后一直存在,条带7在b、c中最亮,随后逐渐减弱,条带10沿程逐渐加强,在f泳道最为清晰.从图谱中可以看出,沿程生物膜的菌群有一定的相似性,但又有差异性,开始菌群种类丰富,随着距离的增加,易于吸收的营养物质被不断地消耗,有些优势菌群保留下来,有些菌群逐渐消失,沿程菌群演替结构之间的相似性逐渐升高并形成稳定的群落结构,同时表明管网生物膜中含有丰富的菌群种数.
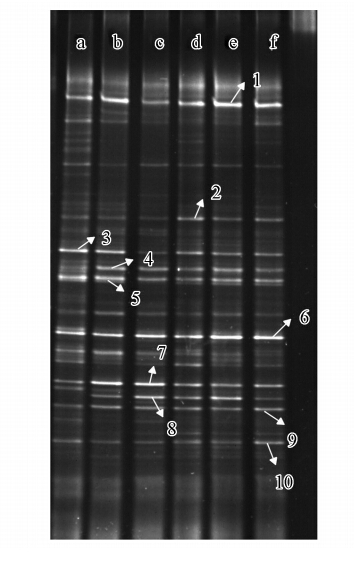 |
| 图 5 PCR-DGGE图谱 Fig. 5 PCR-DGGE results |
将所得DGGE图谱中的优势条带进行割胶回收,通过进一步的处理与扩增最后测序,存在的生物菌群结果见表 3.由表 3可知,管网沿程菌群在初始200 m处有球菌属、链球菌属、杆菌属、链杆菌属、芽孢杆菌属等菌群,随长度增加依次演替出现肠球菌、脱硫弧菌属、硫单胞菌属,1000 m以后主要有甲烷球菌、反硝化杆菌、脱氮硫杆菌,沿程菌群种数减少并形成稳定的菌群结构存在.这与图 6中沿程氨化细菌减少、反硝化细菌增加的结果一致,这些厌氧菌群的存在使得污水水质在沿程中发生一定的变化.
| 表3 生物菌群的沿程变化 Table 3 Variation of biological population along the length of simulated networks |
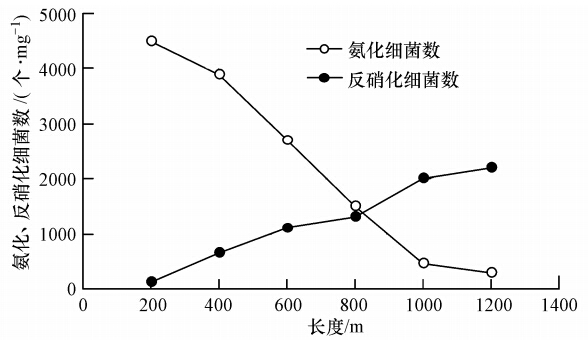 |
| 图 6 氨化菌、反硝化菌的沿程变化 Fig. 6 Variation of ammonifier and DRB along the length of simulated networks |
管道中污水水质沿程变化的连续监测结果如表 4所示.从表 4中可以看出,COD沿程降低,在开始的200 m内平均减少量为39.1 mg · L-1,随后每隔200 m的平均减少量分别为20.38、20.25、12.97、10.75、16.29 mg · L-1.NH3-N在污水管道内沿程呈上升趋势,由初始的43.90 mg · L-1在流经1200 m后增加为55.38 mg · L-1,其中,初始200 m管段内的最大增加量为4.28 mg · L-1.而NO-3-N进水的平均浓度为3.99 mg · L-1,流经1200 m后平均浓度降为0.92 mg · L-1.污水管道中水中COD、NH3-N、NO-3-N浓度的变化情况应该与上述细菌的生命活动有关,如反硝化菌、脱氮硫杆菌等微生物的脱氮作用造成的NO-3-N浓度下降.
| 表4 城市污水管网沿程水质变化 Table 4 Water quality variation of sewer network |
1)利用微电极测定管网生物膜pH、DO及厚度,结果发现,pH变化不大,DO沿程呈现降低的趋势,这也是引起生物膜群落结构变化的一个原因.生物膜厚度由于初始水力冲刷作用较大导致沿程呈现增长趋势,在800 m处达到顶峰,后段因缺乏易吸收的营养物质生物膜厚度明显降低.
2)管网生物膜结构沿程的变化较大,初始结构表面平整,沿程结构逐渐疏松,粗糙结构增大了生物膜比表面积,有利于其生长发育,从而能有效去除水中的污染物质.管网生物膜内菌群构造逐渐趋于以球菌为主,并存在少量的杆菌,初始菌群种数丰富,沿程逐渐减少,总细菌数呈现逐渐减少的分布特征,与扫描电镜结果一致.
3)PCR-DGGE生物检测结果表明,管网生物膜内存在丰富的生物相,初始200 m处有28种菌群,大量存在的菌群共有10种,在1000 m以后亮带数有13条,沿程菌群种数减少并形成稳定的菌群结构存在.其中,200 m处有球菌属、链球菌属、杆菌属、链杆菌属、芽孢杆菌属等菌群,随长度的增加依次演替出现肠球菌、脱硫弧菌属、硫单胞菌属,1000 m以后主要以甲烷球菌、反硝化杆菌、脱氮硫杆菌为主.
| [1] | Baban A, Talinli I. 2009. Modeling of organic matter removal and nitrification in sewer systems-an approach to wastewater treatment [J]. Desalination, 246(1/3): 640-647 |
| [2] | Boon, A G. 1995. Septicity in sewers: Causes, consequences and containment[J]. Water Science & Technology, 31(7): 237-253 |
| [3] | Chen G H, Leung D H W, Huang J C. 2001. Removal of dissolved organic carbon in sanitary gravity sewer [J]. Journal of Environmental Engineering, 127(4): 295-301 |
| [4] | Chen G H, Leung D H W, Hung J C. 2003. Biofilm in the sediment phase of a sanitary gravity sewer [J]. Water Research, 37(11): 2784-2788 |
| [5] | Han Y P, Liu J X, Guo X S, et al. 2012. Micro-environment characteristics and microbial communities in activated sludge flocs of different particle size [J]. Bioresource Technology, 124: 252-258 |
| [6] | Li B K, Bishop P L. 2004. Micro-profiles of activated sludge floc determined using microelectrodes [J]. Water Research, 38(5): 1248-1258 |
| [7] | 刘新春, 吴成强, 张昱, 等. 2005. PCR-DGGE法用于活性污泥系统中微生物群落结构变化的解析 [J]. 生态学报, 25(4): 842-847 |
| [8] | 马悦欣, Homstrm C, Webb J, 等. 2003. 变性梯度凝胶电泳(DGGE)在微生物生态学中的应用 [J]. 生态学报, 23(8): 1561-1569 |
| [9] | Özer A, Kasirga E. 1995. Substrate removal in long sewer lines [J]. Water Science & Technology, 31(7): 213-218 |
| [10] | Wu M L, Chen L M, Tian Y Q, et al. 2013. Degradation of polycyclic aromatic hydrocarbons by microbial consortia enriched from three soils using two different culture media [J]. Environmental Pollution, 178: 152-158 |
| [11] | 于鑫, 李旭东, 杨俊仕, 等. 2003. 微污染原水生物预处理工艺中生物膜的形态和活性 [J]. 城市环境与城市生态, 16(1): 37-39 |
 2014, Vol. 34
2014, Vol. 34


