温室气体的排放导致温室效应加剧,其中,CO2是最主要的温室气体,其捕集技术的开发已引起了世界各国的广泛关注(IPCC,2007).研究发现,在未来的若干年内,化石燃料仍将作为主要的能量来源,大气中CO2的浓度将逐年上升(D′Alessandro et al., 2010).与此同时,低浓度CO2的清除也是载人飞船等密闭空间生命保障系统的关键技术.因此,低浓度CO2的捕集研究具有重要的现实意义.
目前,CO2的分离方法主要有吸收法、膜分离法及吸附法等(刘今朝等,2012;张卫风等,2006;Wang et al., 2012).吸收法是工业中最常用的CO2捕集方法,但该技术的主要问题是CO2吸收量小、腐蚀性强、降解和吸收/再生能耗大,且在高温再生时具有加速腐蚀的趋势(Yu et al., 2012).而吸附法因具有能耗低、吸脱附速率快及无腐蚀等优点,成为一种较为理想的替代技术(Chen et al., 2013).
传统的吸附剂通常用于烟气中CO2的捕集(Wang et al., 2010;Plaza et al., 2010;Chew et al., 2010),但分子筛和活性炭等物理吸附剂由于吸附热低,对空气中CO2的捕集性能较差(Stuckert et al., 2011),同时,有水存在时,其吸附性能下降严重.而固态胺吸附剂通过化学作用可高选择性地吸附CO2,且操作温度低,吸附过程不受水的限制,非常适用于低浓度CO2的吸附捕集(Xu et al., 2003;Yue et al., 2006;Wang et al., 2013a;2013b).
目前,有关固态胺吸附剂用于空气中CO2的捕集研究还较为有限,如Satyapal等(2001)首次制备了固态胺吸附剂HSC+,并将其成功应用于美国航空舱中CO2的循环捕集;Chaikittisilp等(2011)将丙基三甲氧基硅烷接枝到经扩孔的介孔硅上制备出固态胺吸附剂,发现在25 ℃下,其对400 ppm CO2的饱和吸附量为0.98 mmol · g-1;Brilman和Veneman(2013)将四乙烯五胺担载到硅胶上制备了固态胺吸附剂,考察了其在低CO2分压(200~1600 ppm)下的吸附性能及解吸能耗;Choi等(2011)通过氮杂环丙烷的原位开环聚合制备了固态胺吸附剂,在胺含量较高时(10 mmol · g-1,以N计),其对400 ppm CO2的吸附量为1.72 mmol · g-1;Goeppert等(2012)对空气中CO2的捕集技术进行了总结,并指出固态胺吸附剂具有CO2吸附量高、再生能耗低、选择性高、耐水性好等优点.然而,固态胺吸附剂用于空气中CO2的捕集研究仍处于起步阶段,对于低浓度CO2的捕集,由于CO2动力学扩散的限制(Song et al., 2009),吸附性能及胺利用率仍较低,并且载体制备工艺复杂,导致捕集过程成本较高,难以大规模应用.
大孔吸附树脂由于具有三维立体的孔隙结构、较大的孔径与比表面积,有利于PEI在孔内部形成纳米尺度的均匀分散;此外,其极性的表面化学特征能够和有机胺发生化学作用,起到部分固定化功能.因此,本文以大孔吸附树脂为载体,采用浸渍法担载聚乙烯亚胺制备树脂基固态胺吸附剂,通过TGA吸附实验,考察担载量、吸附温度对吸附性能的影响.同时,在固定床吸附柱中研究材料在室温下对低浓度CO2的吸附性能及水对低浓度CO2下吸附性能的影响,并评价材料的循环性能.
2 实验部分(Experimental section) 2.1 吸附剂的制备本文选取商品级大孔吸附树脂HP2MGL(三菱化学)作为吸附剂载体.使用前将树脂置于100 ℃真空干燥箱内5 h以除去吸附的水.吸附剂的制备采用浸渍法,其制备步骤如下:称取一定质量的聚乙烯亚胺(PEI,Mn=600)加入到无水甲醇中,在40 ℃恒温水浴中加热并搅拌0.5 h,然后加入一定量的干燥树脂,继续恒温搅拌2 h;充分浸渍后,50 ℃搅拌使溶剂完全挥发,进一步在80 ℃真空烘箱内干燥2 h.所制备的样品命名为HP2MGL-PEI-x(x为浸渍后样品中PEI占总吸附剂的质量分数).
2.2 吸附剂的表征样品的孔隙结构在Quadrasorb SI物理吸附分析仪上测定.样品的比表面积由Brunauer-Emmett-Teller(BET)法计算,记为SBET;样品的孔径分布由BJH模型计算.用JSM-6360LV型扫描电子显微镜(SEM)来观察样品的表面形貌.材料的热稳定性由热重分析仪(TA,SDT Q600)进行测定,在氮气氛围下,以10 ℃ · min-1程序升温至800 ℃,得到材料的TGA曲线.
2.3 CO2吸附性能测试 2.3.1 热重法吸附剂对纯CO2的吸附性能采用热重法进行测定.测定前,将约10 mg样品在N2气氛(100 cm3 · min-1)中加热脱除吸附的水、CO2和其他气体至恒重(以5 ℃ · min-1升温至110 ℃保持恒温100 min),然后降温到吸附温度,切换成纯CO2(99.99%),进行吸附(100 min).样品的CO2吸附量根据测量结果进行计算.通过改变吸附温度及PEI担载量考察其对吸附性能的影响.
2.3.2 动态吸附法动态吸附实验在固定床吸附器中进行,在吸附过程中,1.0 g的吸附剂装填在石英玻璃管中,不同配比的CO2/N2混合气体以50 mL · min-1的流量通过管道,CO2浓度使用气相色谱(Shimadzu GC-2014)来测定,吸附剂的吸附量由穿透曲线,利用进气中的CO2浓度、流速、饱和时间和吸附剂的质量计算.饱和吸附量由单位质量吸附剂的吸附质量表示.吸附后,将吸附剂加热至100 ℃恒温200 min进行脱附.通过多次吸附/脱附循环来测试材料吸附CO2的稳定性.对于湿度的影响,通过测定不同相对湿度时的吸附量来考察,湿度控制的具体方法是:将N2原料气分为两路,一路直接与CO2混合,另一路经过增湿器后再与上述气体混合,通过控制两路N2的流量配比,来调节混合气体的湿度.
3 结果与讨论(Results and discussion) 3.1 吸附剂的结构表征大孔吸附树脂载体和吸附剂的氮气吸附等温线及BJH孔径分布曲线如图 1所示,计算的孔结构参数和BJH孔径分布列于表 1.从图 1a中可以看出,载体HP2MGL的氮气吸脱附等温线为Ⅳ型,存在明显的滞后环,表明样品具有一定的中大孔结构.图 1b为BJH孔径分布图,可以看出,大孔吸附树脂具有较宽的孔径分布,其平均孔径为23.6 nm.
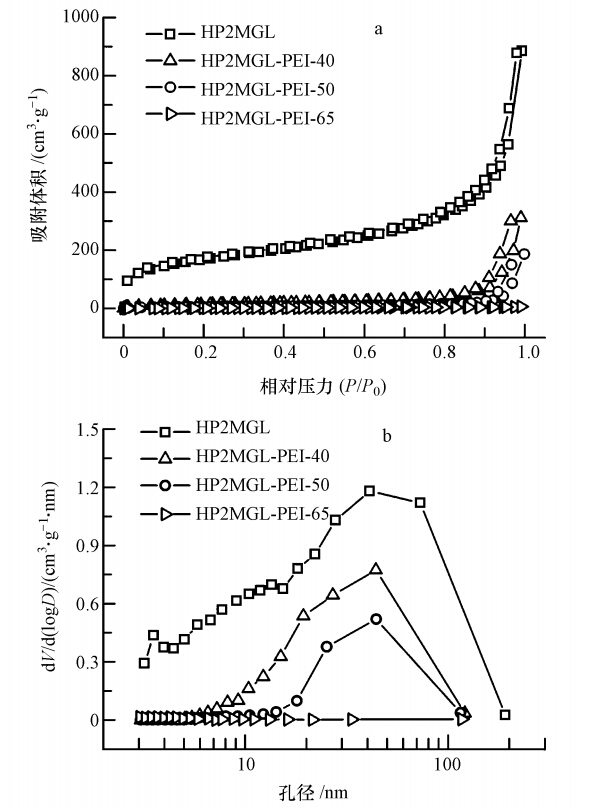 |
| 图 1 PEI担载量不同的树脂基固态胺吸附剂的氮气吸附等温线(a)和BJH孔径分布(b) Fig. 1 Nitrogen adsorption-desorption isotherms(a) and the BJH pore size distributions(b)of the resin-based solid amine sorbents with different PEI loadings |
| 表1 树脂基固态胺吸附剂的孔结构性质 Table 1 Porous property of the resin-based solid amine sorbents |
担载PEI后,吸附剂的比表面积和孔容随着担载量的增加逐渐减小,样品HP2MG-PEI-50仍具有一定的比表面积(24.4 cm2 · g-1)和孔容(0.15 cm3 · g-1);而对于HP2MG-PEI-65,由于PEI的担载量超过了根据其孔容计算的最大担载量(59%),树脂载体的表面完全被PEI覆盖,从而限制了N2分子扩散进入孔内部,因而检测不到比表面积和孔容.
 |
| 图 2 载体(a)与不同担载量(b.50%,c.60%,d.65%)的树脂基固态胺吸附剂的SEM图片 Fig. 2 SEM images of the resins(a) and the resin-based solid amine sorbents with different PEI loadings(b.50%,c.60%,d.65%) |
图 2显示了担载PEI前后HP2MGL树脂的微观结构变化.树脂载体是由纳米颗粒相互叠加形成,具有三维开孔网络结构特征,存在着大量的颗粒间中大孔(图 2a).担载50%PEI后,纳米颗粒表面被PEI覆盖,颗粒更加明显,颗粒间的孔隙减少,但仍然存在一定的残留孔隙,将会为气体吸附提供必要的扩散通道(图 2b).担载量为60%时,大多数孔隙被PEI充满或阻塞,但仍然存在少量中孔(图 2c).当担载量继续增加至65%,载体表面完全被PEI覆盖,观察不到明显的孔结构(图 2d),这一结果与氮气吸附结果相一致.
吸附剂的热稳定性通过热重进行分析,图 3显示了样品的TGA结果.PEI在加热过程中不断分解,在300~400 ℃范围内分解速率最大,在450 ℃时完全分解.树脂载体在200 ℃前几乎无热失重,在200~450 ℃范围内逐渐分解.担载PEI后,吸附剂出现了两个失重阶段:在100 ℃左右的失重为吸附剂表面吸附的水和少量溶剂甲醇的脱除;在高于200 ℃后,PEI和载体本身均开始分解.此结果表明,HP2MGL-PEI-50吸附剂在室温~200 ℃内具有一定的热稳定性.
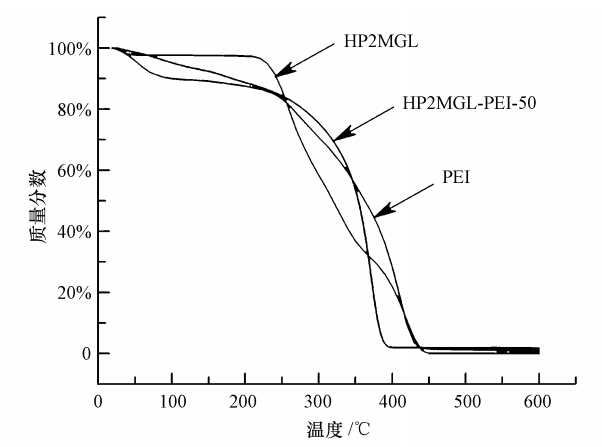 |
| 图 3 树脂基固态胺吸附剂的TGA曲线 Fig. 3 TGA curves of the resin-based solid amine sorbents |
通过热重吸附,在PEI担载量为50%时,吸附温度对CO2吸附性能的影响如图 4所示.从图中可以明显看出,CO2的吸附容量随着温度的升高而逐渐减小,但在25 ℃下,前10 min 内CO2的吸附量仅为饱和吸附量的63%,在温度高于50 ℃时,前10 min 内CO2的吸附量可达到饱和吸附量的80%以上.这是由于低温下,CO2的吸附速率较慢,而高温有利于CO2的扩散吸附,因此,吸附剂具有更高的吸附速率.本研究采用的大孔甲基丙烯酸酯吸附树脂与PEI分子具有很好的亲和性,使得PEI能够在树脂孔内比较好的分散,并提供足够多的内扩散通道和吸附界面,因此,扩散对于本体系并不是最主要的控制因素.而CO2与胺基的反应是放热反应,低温有利于高吸附量的获得.因此,CO2的吸附性能是由动力学扩散与热力学吸附共同决定,低温有利于吸附量的提高,高温有利于吸附速率的加快.
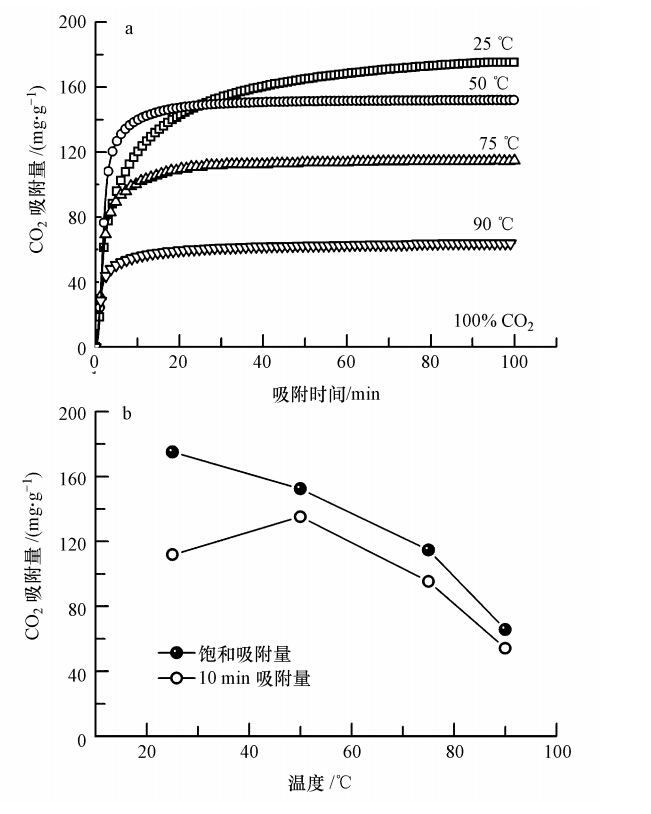 |
| 图 4 吸附温度对HP2MGL-PEI-50样品CO2吸附性能的影响(a.TG吸附曲线;b.CO2吸附量) Fig. 4 Effect of temperature on the sorption performance of CO2 on HP2MGL-PEI-50(a.TG sorption curves; b.CO2 sorption capacity) |
通过热重吸附,不同PEI担载量的吸附剂在25 ℃下的吸附曲线及相应的吸附量如图 5所示.HP2MGL载体本身对CO2的吸附量仅为1.36 mg · g-1,可忽略不计.随着PEI担载量的增加,吸附量也随之增加,并在PEI担载量为50%时最大,达到175 mg · g-1;进一步增加担载量,吸附量开始下降,在担载量为65%时急剧降为55 mg · g-1.由于HP2MGL-PEI-50具有一定的残余孔道,以易于CO2的动力学扩散,同时具有较高的PEI担载量,因而其吸附容量最大;当担载量进一步增加,残余孔道减少甚至消失,CO2内扩散成为主要控制因素,因此,吸附性能下降.根据吸附反应机理,在无水的条件下,1 mol CO2需与2 mol的胺基反应.据此,可计算固态胺吸附剂的胺利用率(图 5b),发现胺的利用率随担载量的增加而逐渐下降.在PEI担载量较低时,PEI易获得均匀的分散,内扩散阻力较小,胺利用率高;随着担载量的增加,CO2的内扩散阻力变大,未被利用的PEI增加,胺利用率逐渐减小.从吸附性能和胺利用率的角度来考虑,大孔树脂的最佳担载量为50%.
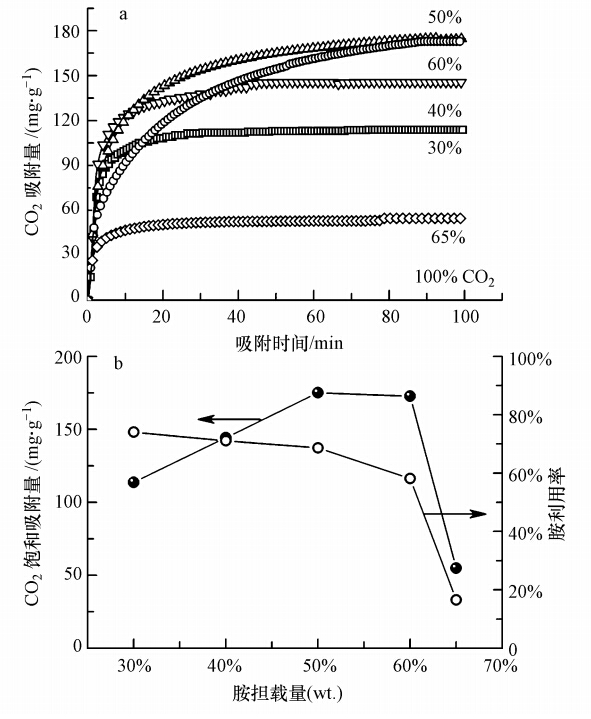 |
| 图 5 25 ℃下PEI担载量对纯CO2吸附性能的影响(a.TG吸附曲线;b.CO2饱和吸附量) Fig. 5 Effect of PEI loading amounts on the sorption performance of pure CO2 at 25 ℃(a.TG sorption curves; b.CO2 sorption capacity) |
通过对热重吸附结果分析,我们筛选出吸附剂的最佳担载量和最佳吸附温度,接下来将着重研究该优化条件下对低浓度CO2的动态吸附行为.图 6a为HP2MGL-PEI-50在25 ℃下对浓度为400 ppm~15%的CO2的动态穿透曲线.由图可知,随着CO2浓度的增加,穿透时间相应减短,吸附量降低.由图 6b中的吸附量结果可知,吸附剂对15% CO2的吸附量达到150 mg · g-1;当CO2浓度降到0.5%时,仍有较高的吸附量(93.5 mg · g-1);进一步降低CO2浓度至400 ppm(接近空气中CO2浓度),吸附量为86 mg · g-1.
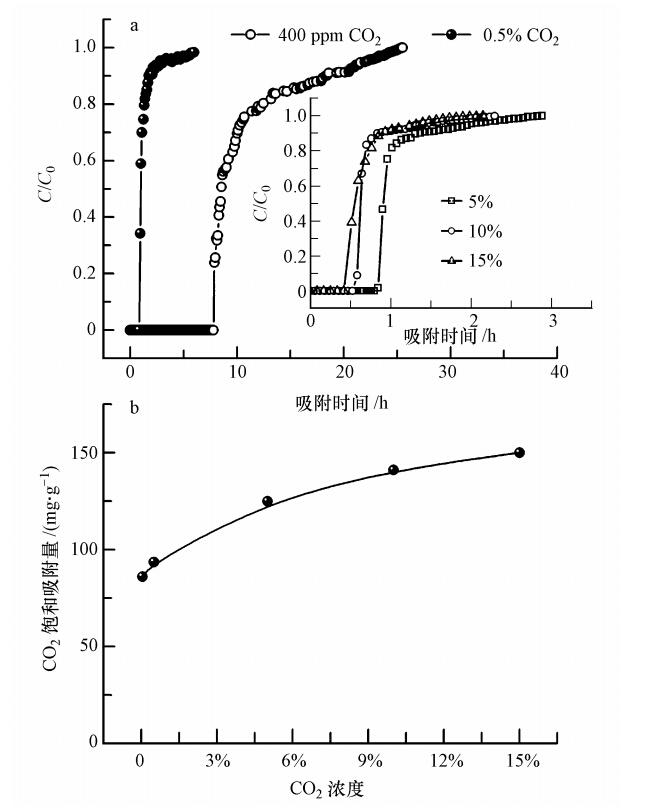 |
| 图 6 25 ℃、不同CO2浓度下HP2MGL-PEI-50的穿透吸附性能(a.动态吸附穿透曲线;b.CO2饱和吸附量) Fig. 6 Breakthrough sorption capacity of HP2MGL-PEI-50 at different CO2 concentration(a.CO2 breakthrough curves; b.CO2 sorption capacity at 25 ℃) |
水分是空气中不可避免的组成部分,本工作考察了不同湿度对CO2吸附的影响,结果如图 7所示.与干气吸附相比,在10%~60%相对湿度(RH)范围内,CO2吸附量均明显增加.这是由CO2与胺的反应机理决定:无水条件下2 mol胺基可捕获1 mol CO2,而有水条件下1 mol胺基可吸附1 mol CO2.当湿度为10%时,CO2吸附量提升最大,高达139 mg · g-1.随着相对湿度的逐渐提升,吸附量提升度下降,当湿度为60%时吸附量为101 mg · g-1.在CO2浓度为400 ppm时,过高的湿度可能会使水汽凝结成液膜,从而阻碍CO2在胺内的扩散.因此,对于空气中直接捕集CO2,需对湿度进行一定的控制,以到达最佳的吸附效果.
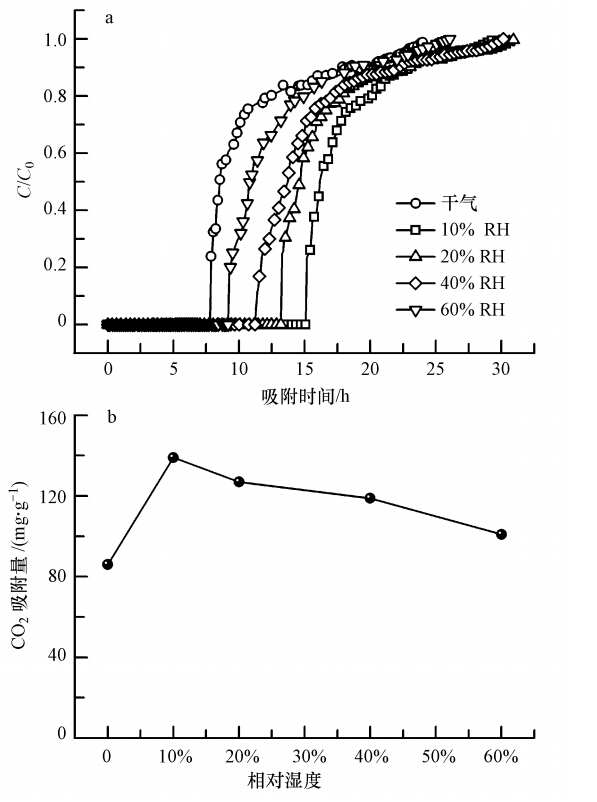 |
| 图 7 水对二氧化碳吸附性能的影响(400 ppm CO2,25 ℃) Fig. 7 Effect of humidity on CO2 sorption capacity(400 ppm CO2,25 ℃) |
再生性能是吸附剂的一个重要参数.本文考察了HP2MGL-PEI-50在25 ℃下吸附400 ppm CO2干气,并在100 ℃下脱附10次循环吸脱附的性能,结果如图 8所示.经过10次循环吸附脱附后,吸附量 仍能够达到82 mg · g-1,吸附剂的吸附量仅下降约 5%,说明HP2MGL-PEI-50具有优异的循环性能.这主要归因于载体发达的三维孔结构能够容纳并有效分散PEI分子.此外,载体的甲基丙烯酸酯化学结构可与含有氨基的官能团发生氢键作用,提高PEI在其内的固定化作用,使材料在循环过程中能够保持稳定.
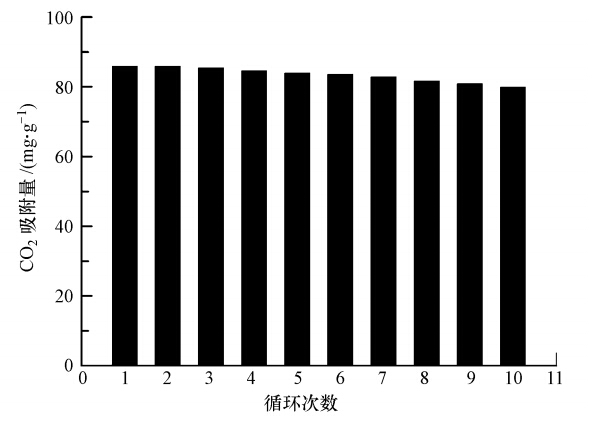 |
| 图 8 HP2MGL-PEI-50的循环性能(400 ppm CO2,25 ℃) Fig. 8 Cycle capacity of HP2MGL-PEI-50(400 ppm CO2,25 ℃) |
胺改性树脂基吸附剂在常温下对空气浓度的CO2显示出良好的吸附性能.迄今为止,关于固态胺吸附剂对空气中CO2的捕集研究较为有限,表 2列出了几种典型的固态胺吸附剂对400 ppm CO2干气的吸附性能,以与本文的结果进行比较.由表 2可以看到,在列举出的吸附剂中,本文所制备的吸附剂在25 ℃下对400 ppm CO2的吸附性能最高.同时,由于其制备工艺简单,预示着本文所制备的吸附剂在直接空气捕集CO2领域具有一定的应用前景.
| 表2 树脂基固态胺吸附剂与几种典型的固态胺吸附剂吸附性能比较 Table 2 Comparison of resin-based solid amine sorbents with other solid amine sorbents |
本文以大孔吸附树脂为载体,PEI为有机胺,通过浸渍法制备出树脂基固态胺吸附剂,用以室温直接捕集低浓度CO2.结果表明:大孔吸附树脂三维的孔结构有利于胺在孔道内的均匀分散及CO2的动力学扩散;随着PEI担载量的增加,CO2吸附量呈先增大后减小的趋势,而胺利用率逐渐下降,PEI的最佳担载量为50%;吸附剂的吸附性能由吸附热力学决定,随着吸附温度的升高吸附量逐渐减小;胺改性树脂基吸附剂在较宽的CO2浓度范围内都具有优越的吸附性能,其对空气浓度CO2的饱和吸附量为86 mg · g-1,优于现有的胺改性吸附剂;湿度对低浓度CO2吸附起促进作用,湿度为10%时,其吸附量可提高到139 mg · g-1;该吸附剂具有稳定的循环性能.本文所制备的吸附剂具有制备工艺简单、成本相对较低等特点,在直接空气捕集CO2领域具有一定的应用前景.
| [1] | Belmabkhout Y, Serna-Guerrero R,Sayari A,et al.2010.Adsorption of CO2-containing gas mixtures over amine-bearing pore-expanded MCM-41 silica: Application for gas purification[J].Industrial & Engineering Chemistry Research,49(1): 359-365 |
| [2] | Brilman D W F,Veneman R.2013.Capturing atmospheric CO2 using supported amine aorbents[J].Energy Procedia,37: 6070-6078 |
| [3] | Chaikittisilp W,Kim H J,Jones C W.2011.Mesoporous alumina-supported amines as potential steam-stable adsorbents for capturing CO2 from simulated flue gas and ambient air[J].Energy & Fuels,25(11): 5528-5537 |
| [4] | Chen Z H,Deng S,Wei H,et al.2013.Activated carbons and amine-modified materials for carbon dioxide capture-a review[J].Frontiers of Environmental Science & Engineering,7(3): 326-340 |
| [5] | Chew T L,Ahmad A L,Bhatia S.2010.Ordered mesoporous silica (OMS) as an adsorbent and membrane for separation of carbon dioxide (CO2)[J].Advances in Colloid and Interface Science,153(1/2): 43-57 |
| [6] | Choi S,Drese J H,Eisenberger P M,et al.2011.Application of amine-tethered solid sorbents for direct CO2 capture from the ambient air[J].Environmental Science & Technology,45(6): 2420-2427 |
| [7] | D'Alessandro D M,Smit B,Long J R.2010.Carbon dioxide capture: prospects for new materials[J].Angewandte Chemie International Edition,49(35): 6058-6082 |
| [8] | Gebald C,Wurzbacher J A,Tingaut P,et al.2011.Amine-based nanofibrillated cellulose as adsorbent for CO2 capture from air[J].Environmental Science & Technology,45(20): 9101-9108 |
| [9] | Goeppert A,Czaun M,May R B,et al.2011.Carbon dioxide capture from the air using a polyamine based regenerable solid adsorbent[J]. Journal of the American Chemical Society,133(50): 20164-20167 |
| [10] | Goeppert A,Czaun M,Prakash G K S,et al.2012.Air as the renewable carbon source of the future: an overview of CO2 capture from the atmosphere[J].Energy & Environmental Science,5(7): 7833-7853 |
| [11] | IPCC.2007.Summary for Policymakers//Solomon S,Qin D,Manning M,et al.Climate Change 2007: The Physical Science Basis.Contribution of Working group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change[M].Cambridge,UK,New York: Cambridge University Press |
| [12] | 刘今朝,王淑娟,赵博,等.2012.N-甲.基二乙醇胺/哌嗪溶液和氨水吸收二氧化碳的实验研究[J].环境科学学报,32(10): 2533-2539 |
| [13] | Ma X L,Wang X X,Song C S.2009.Molecular basket sorbents for separation of CO2 and H2S from various gas streams[J].Journal of the American Chemical Society,131(16): 5777-5783 |
| [14] | McDonald T M,Lee W R,Mason J A,et al.2012.Capture of carbon dioxide from air and flue gas in the Alkylamine-appended metal-organic framework mmen-Mg2 (dobpdc)[J].Journal of the American Chemical Society,134(16): 7056-7065 |
| [15] | Plaza M G,García S,Rubiera F,et al.2010.Post-combustion CO2 capture with a commercial activated carbon: Comparison of different regeneration strategies[J].Chemical Engineering Journal,163(1/2): 41-47 |
| [16] | Satyapal S,Filburn T,Trela J,et al.2001.Performance and properties of a solid amine sorbent for carbon dioxide removal in space life support applications[J].Energy & Fuels,15(2): 250-255 |
| [17] | Stuckert N R,Yang R T.2011.CO2 capture from the atmosphere and simultaneous concentration using zeolites and amine-grafted SBA-15[J].Environmental Science & Technology,45(23): 10257-10264 |
| [18] | Wang D X,Ma X L,Sentorun-Shalaby C,et al.2012.Development of carbon-based "molecular basket" sorbent for CO2 capture[J].Industrial & Engineering Chemistry Research,51(7): 3048-3057 |
| [19] | Wang J T,Wang M M,Zhao B B,et al.2013a.Mesoporous carbon-supported solid amine sorbents for low-temperature carbon dioxide capture[J].Industrial & Engineering Chemistry Research,52(15): 5437-5444 |
| [20] | Wang J T,Chen H C,Zhou H H,et al.2013b.Carbon dioxide capture using polyethylenimine-loaded mesoporous carbons[J].Journal of Environmental Sciences,25(1): 124-132 |
| [21] | Wang Q,Luo J Z,Zhong Z Y,et al.2010.CO2 Capture by solid adsorbents and their applications: Current status and new trends[J].Energy & Environmental Science,4(1): 42-55 |
| [22] | Xu X C,Song C S,Andrésen J M,et al.2003.Preparation and characterization of novel CO2 "molecular basket" adsorbents based on polymer-modified mesoporous molecular sieve MCM-41[J].Microporous and Mesoporous Materials,62(1/2): 29-45 |
| [23] | Yu C H,Huang C H,Tan C S.2012.A review of CO2 capture by absorption and adsorption[J].Aerosol and Air Quality Research,12(5): 745-769 |
| [24] | Yue M B,Chun Y,Cao Y,et al.2006.CO2 capture by as-prepared SBA-15 with an occluded organic template[J].Advanced Functional Materials,16(13): 1717-1722 |
| [25] | 张卫风,方梦祥,骆仲泱,等.2006.中空纤维膜接触器分离烟气中CO2[J].环境科学学报,26(5): 773-778 |
 2014, Vol. 34
2014, Vol. 34


