水库水体透明度大、流动性小,藻类容易停留在表层水体得到光照而大量繁殖(孙晓庆等,2007).研究表明,光照和温度是影响藻类生长的重要因素,在表层水体中,光照和温度适宜,藻类光合作用大于呼吸作用,藻类净生长;而在下层水体中,几乎没有光照,温度也较低,压力大,呼吸作用大于光合作用,藻类净衰亡(贾含帅等,2011;刘玉生等,1995;刘春光等,2005;于萍等,2006).为了控制水库表层藻类的生长,可采用混合技术混合上下水层,将下层水体提升到表层,而表层水体循环到下层,使得藻类被迁移到下层水体中,受到弱光、低温、高压作用而衰亡(丛海兵等,2005;2006;Cong et al., 2009;2011).
周村水库位于东经117°41′,北纬34°57′,在枣庄市市中区孟庄镇周村南,流域面积121 km2,总库容8404万m3,水面面积8.54 km2,最大水深19 m.周村水库建成于1960年,主要功能有防洪、灌溉和城市供水,是枣庄市城市供水水源地.1990—2008年期间,周村水库曾大量网箱养鱼,造成了严重的水污染,水库富营养化问题严重.近年来,政府部门取缔了网箱养鱼,水库水质好转,但库底沉积的高污染底泥持续向水体释放营养盐,使水库仍处于富营养化状态.为了在短期内改善城市供水水源水质,课题组研究人员准备在取水口附近采用混合控藻技术抑制藻类生长.本文主要研究在混合条件下,表层藻类被混合到不同水深处受到不同光照、温度、压力胁迫作用后的生长衰亡规律,以期为混合控藻技术提供理论技术依据.
2 材料与方法(Materials and methods) 2.1 水样在周村水库坝前200 m处,用水下取样器取得指定水深处水样,带回实验室混合均匀备用.每一组实验水样需当天现取现用,实验过程为2 d.
2.2 实验装置藻类在不同光照、温度条件下的培养装置为5 L的玻璃瓶,瓶口加塞橡胶塞,塞中间开孔,溶解氧探头从孔中伸入瓶内.藻类在压力条件下的培养装置如图 1所示,装置由密闭压力罐、加压泵及管路组成,压力罐为透明有机玻璃柱制成,容积为5 L,耐压1.0 MPa,加压泵为奥力康YU7124型滑片泵.其中,图 1a为溶解氧测定装置,溶解氧仪探头伸入压力罐中.图 1b为叶绿素和藻类活性培养测定装置,压力罐内安装气球,气球嘴与加压泵出水管连通.玻璃瓶和压力罐放入MGC-250型光照培养箱中.
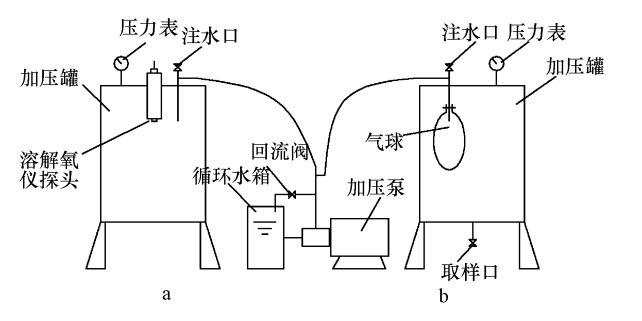 |
| 图 1 藻类压力条件下的培养装置 Fig. 1 Algae culture device under pressure |
用定水深取样器从水库的不同水深处取样,放入塑料瓶中带回实验室,测定藻类的种类、个数、叶绿素浓度,每周测定1次.1 d中选择几个特定时间,用照度计和溶解氧仪测定水库不同水深处光强和水温,半个月测定1次.用透明度盘测量水体透明度.
2.3.2 不同光照下藻类生长速率及活性从水库2 m水深处取样,分别放入2个5 L透明玻璃瓶中,其中一个玻璃瓶用于测定溶解氧变化,玻璃瓶口加盖橡皮塞,橡皮塞中心开圆孔,插入溶解氧仪探头,瓶内不留空气.另一个玻璃瓶用于测定藻类叶绿素浓度和藻类活性变化,不加盖.将玻璃瓶放入光照培养箱中,设置光照培养箱的温度为26 ℃,调节光照强度为所需值,分别为52500、32500、17500、5350、1566、0 lx.培养时间24 h,光照和黑暗转换规律与当地自然光照同步,其中,光照14 h,黑暗10 h,一般前8 h光照,中间10 h黑暗,最后6 h光照.每隔2 h测定溶解氧,从玻璃瓶中取样测定叶绿素和藻类活性.
2.3.3 不同温度条件下藻类生长速率及活性取样及培养方法同上,将2个玻璃瓶放入光照培养箱中,控制培养箱温度为需要值,分别为30、26、20、15 ℃.光照条件为藻类光合作用最适宜的光强32500 lx.取样测定方法同上.
2.3.4 不同压力条件下藻类生长速率及活性从水库2 m水深处取样,分别放入如图 1a和图 1b所示的压力罐中.调节回流阀,控制压力罐中的压力为所需的压力,分别为0.1、0.2、0.3 MPa.将压力罐放入培养箱中,培养条件为藻类光合作用适宜的光照32500 lx和温度26 ℃.取样测定方法同上.
2.3.5 现场水深综合条件下藻类生长衰亡特性从2 m水深处取样倒入桶内混匀,测定初始叶绿素和藻类活性,再将溶解氧白瓶和黑瓶注满水样,测定每个瓶中初始溶解氧,盖好瓶塞,不留气泡.白瓶为透明玻璃瓶,黑瓶为包裹了黑布的玻璃瓶,瓶内无光.在水库不同水深处悬挂一对白瓶和黑瓶,24 h后取回黑白瓶,测定溶解氧、叶绿素、藻类活性.
2.4 测试方法藻类叶绿素a按照《藻类叶绿素测试新方法》测定(丛海兵等,2007),孔径1 μm的醋酸纤维滤膜过滤水样,90%乙醇萃取叶绿素,采用上海精科UV759S型分光光度计测定提取液吸光度.
藻类活性用FDA二乙酸荧光素荧光法测定(王佳佳等,2012),取2 mL水样加入15 mL(pH=7.9)浓度为60 mmol · L-1的磷酸盐缓冲液,摇晃均匀,再加入400 μL的荧光素FDA(0.3 mg的二乙酸荧光素溶于100 mL的丙酮),摇匀,放入恒温水浴锅内,水浴温度为30 ℃,反应30 min,将样品放入仪器中测量其荧光值.采用上海棱光F97荧光光度计测定荧光值.
溶解氧采用哈希公司HQ30d便携式溶解氧仪测定,光强采用上海嘉定学联仪表ZDS-10水下照度计测定.
3 结果与讨论(Results and discussion) 3.1 水库藻类及环境条件竖向分布测定结果水库竖向环境条件及藻类浓度如图 2所示.从图中可见,7、8月份是藻类高发期,水库主要以蓝藻为主(占藻类总数80%左右),绿藻和硅藻所占比例相近.其中,蓝藻以鞘丝藻居多,绿藻主要有浮球藻、水溪绿球藻、肾形藻,而硅藻则以小环藻和针杆藻为主.水库水体的透明度一般在95~100 cm之间.水库表层水体太阳光较强,中午时分光强为1400~85000 lx,随着水深的增加光强呈指数递减,在水深4 m以下光强小于100 lx.表层水温较高,夏季在25~30 ℃左右,随着水深的增加水温逐渐减小,到14 m以下水温恒定,约为14 ℃.
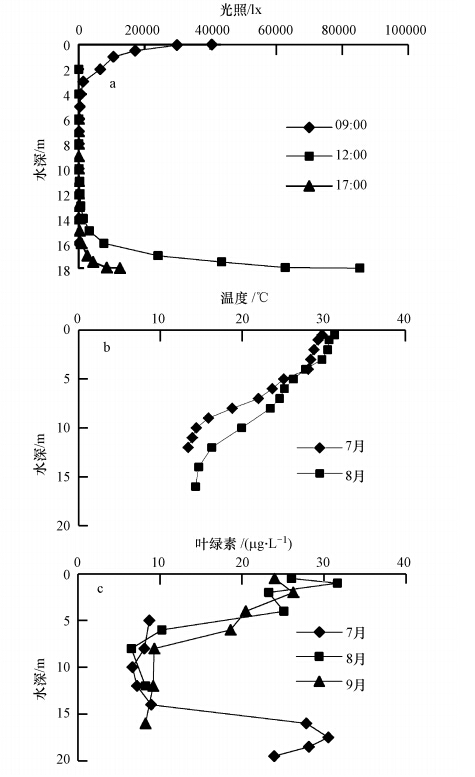 |
| 图 2 藻类及环境条件竖向分布 Fig. 2 Vertical distribution of algae and environmental conditions |
由藻类竖向分布图可以看出,表层4 m水深内藻类较多,叶绿素a浓度为22~30 μg · L-1,这与光强的竖向分布是一致的.在2 m水深出现藻类浓度峰值,此处约为2倍透明度.4~6 m水深内藻类含量锐减,以下浓度基本恒定,叶绿素a浓度为10 μg · L-1左右.
蓝藻由于浮力调节机制,其浓度峰值位于2~3倍透明度处(黄廷林等,2009),对本水库应该在2~3 m水深处.绿藻的浓度峰值一般位于0.5 m水深处(黄廷林等,2009).周村水库上层水体中蓝藻和绿藻均是优势藻种,因而其浓度峰值介于蓝藻峰值和绿藻峰值水深之间的2 m水深处.
上层4 m水深以上水体中主要是蓝藻门的鞘丝藻,占藻类总数的81%,绿藻门的浮球藻占11%,硅藻针杆藻占8%.下层7 m水深以下水体中蓝藻比例减小,硅藻和绿藻比例增加,其中,蓝藻比例占58%,硅藻占25%,绿藻占17%.
3.2 胁迫条件下藻类生长规律及其活性 3.2.1 不同光照强度对藻类生长衰亡的影响不同光照强度下藻类生长衰亡规律见图 3.从图 3a可见,前8 h和后6 h光照期溶解氧均上升,中间10 h黑暗期溶解氧小幅下降.不同光强下溶解氧上升速率不同,将前10 h溶解氧变化量除以各自初始叶绿素浓度,得到单位浓度叶绿素生产力(mg · μg-1 · h-1,以每μg Chla每小时产生的O2(mg)计),结果如图 3d所示.从图中可见,在光强32500 lx时生产速率最大,达到0.0185 mg · μg-1 · h-1,增大或减小光强生产速率均减小,其中,零光强时生产速率为-0.0022 mg · μg-1 · h-1.
从图 3b可见,前后光照期单位浓度叶绿素荧光值均上升,即藻细胞活性增强,中间黑暗期细胞活性减弱.不同光强条件下细胞活性变化速率不同,藻细胞活性一般在6~8 h达到最大,将单位浓度叶绿素荧光值变化量除以各自达到最大值所需培养时间,得到单位时间藻细胞活性变化速率,结果如图 3d所示.从图中可见,在光强32500 lx时细胞活性变化速率最大,达到2.0308 h-1,其他光强下细胞活性变化速率均减小,在零光强时细胞活性变化速率为-1.049 h-1.藻类叶绿素变化规律如图 3c所示,从图中可见,藻类生物量的变化规律与生产力变化规律相似,在32500 lx光强时增加最多,其他光强下增加较少.
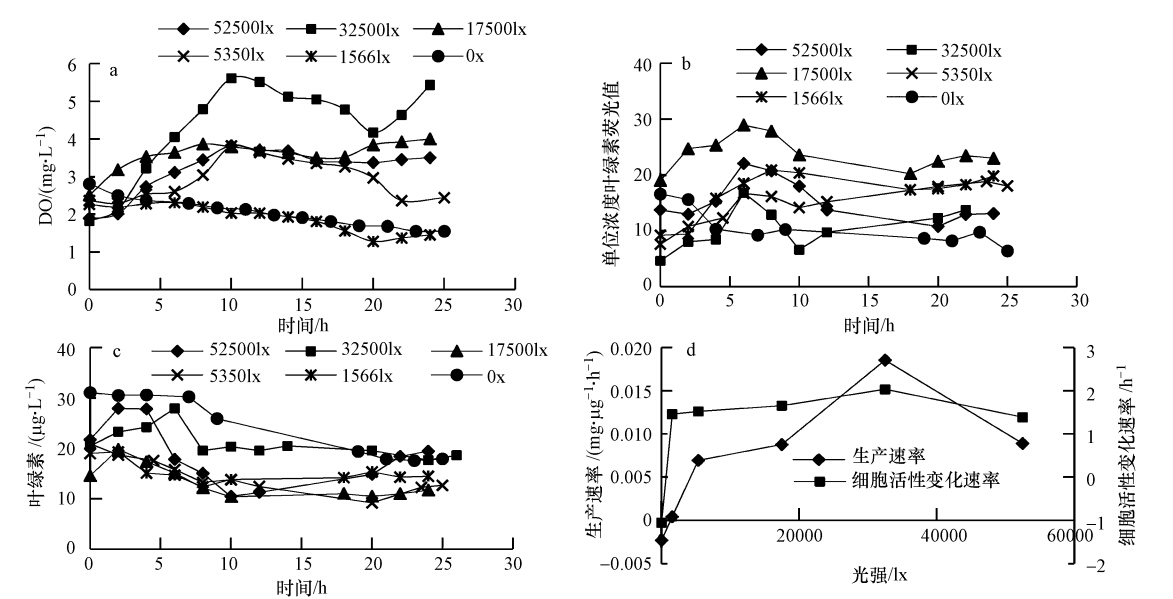 |
| 图 3 不同光照条件下藻类生长衰亡规律 Fig. 3 Growth and decay of algae under different light conditions |
在实际水库中,藻类主要聚集于0~4 m水深范围内,此范围内中午光强为85000~1400 lx,均适合于藻类进行光合作用,其它时分水中光强将减弱.蓝藻将会根据水中光强的变化自动调节其所处的位置,当光强减弱时蓝藻会上浮到水面,以获得适宜的光照强度(刘建康,1999).
3.2.2 不同温度条件对藻类生长衰亡的影响不同温度条件下藻类生长衰亡规律见图 4.从图 4a可见,前后光照期溶解氧均上升,中间黑暗期溶解氧小幅下降.不同温度下溶解氧上升速率不同,前期8~10 h内溶解氧达到最大,计算增长期单位浓度叶绿素生产力,结果如图 4d所示.从图中可见,在温度2 6 ℃时生产速率最大,达到0.0185 mg · μg-1 · h-1,增加或减小温度生产速率均减小,其中,15 ℃时生产速率为0.0125 mg · μg-1 · h-1,30 ℃时生产速率为0.0132 mg · μg-1 · h-1,两温度下生产速率相近.
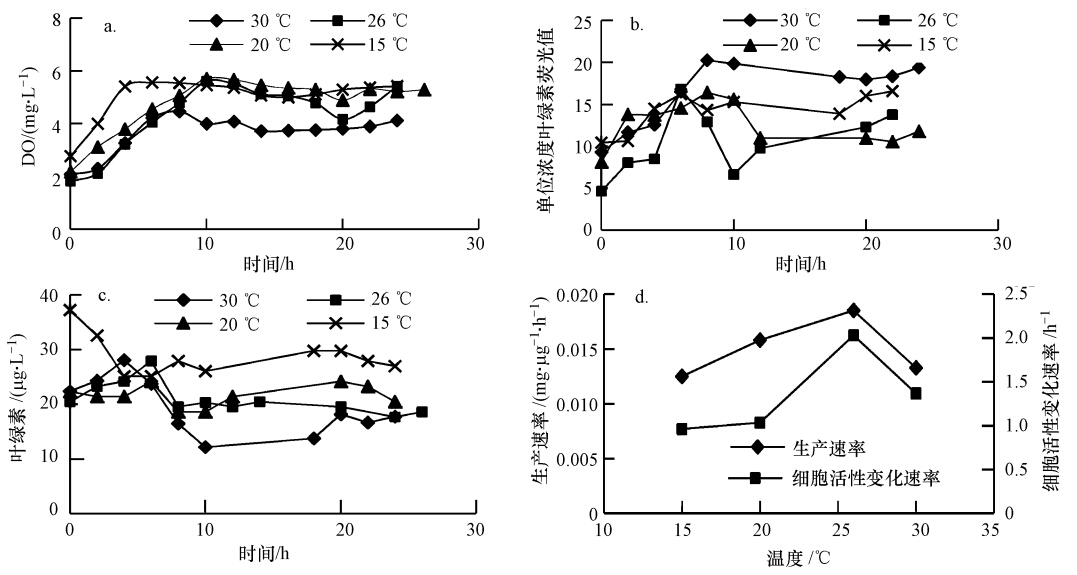 |
| 图 4 不同温度条件下藻类生长衰亡规律 Fig. 4 Growth and decay of algae under different temperature conditions |
从图 4b可见,前后光照期藻细胞活性均增大,中间黑暗期活性减弱.各温度下细胞活性变化速率不同,计算增长期细胞活性变化速率,结果如图 4d所示.由图可见,在温度26 ℃时细胞活性变化速率最大,其他温度下细胞活性变化速率均减小.在15 ℃时,温度过低,酶钝化活性变低,细胞处于休眠状,细胞活性变化小.藻类叶绿素变化规律如图 4c所示,从图中可见,温度在20 ℃以上藻类生物量增加,低温时基本不增加.
3.2.3 不同压力条件对藻类生长衰亡的影响不同压力条件下藻类生长衰亡规律见图 5.从图 5a可见,前后光照期溶解氧均上升,中间黑暗期溶解氧小幅下降.不同压力下溶解氧上升速率不同,计算增长期单位浓度叶绿素生产力,结果如图 5d所示.从图中可见,在压力0 MPa即常压时生产速率最大,为0.0185 mg · μg-1 · h-1,增大压力生产速率减小,0.3 MPa时生产速率为0.0093 mg · μg-1 · h-1,减小了50%.
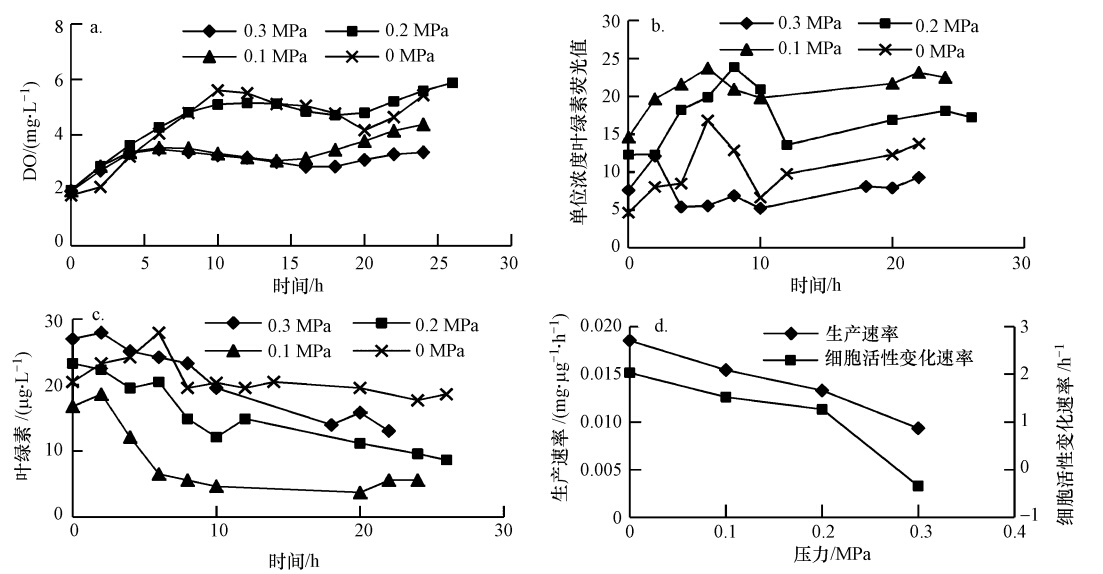 |
| 图 5 不同压力条件下藻类生长衰亡规律 Fig. 5 Growth and decay of algae under different pressure conditions |
由图 5b可见,在0~0.2 MPa时,前期光照内藻细胞活性均增强,在0.3 MPa时藻细胞活性2 h后开始下降,活性明显低于常压下.藻细胞气囊有散射性,使外界光强进入细胞内后变强,当压力达到0.3 MPa即水深达到30 m时,藻细胞气囊变小,细胞内光强减弱,光合作用下降,当压力继续增大,水深增加,气囊破裂,藻类下沉(丛海兵等,2014).计算前期6 h藻细胞活性变化速率,结果如图 5d所示.由图可见,随着压力增加藻细胞活性增加速率减小,常压时增长速率为2.0308 h-1,而0.3 MPa时为-0.3432 h-1.说明即使给予相同的温度和光照,压力对藻类生长有很强的抑制作用.藻类叶绿素变化规律如图 5c所示,从图中可见,常压以下藻类生物量增加,0.1 MPa以上压力藻类生物量减小.
3.2.4 水库现场水深综合条件下藻类生长衰亡的特性从2 m水深处取样悬挂到不同水深后,藻类的生长衰亡规律如图 6所示.由图 6a可见,藻类光合作用总生产力随着水深的增加呈线性减小,6 m水深以下为零,这与图 2中光照竖向分布是一致的,在6 m水深处光照为零.藻类呼吸作用在6 m水深以上均较大,6 m水深向下逐步减小,12 m以下基本不变.将总生产力和呼吸作用叠加,得到藻类净生产力.藻类在2.5 m水深以上净增长,2.5 m水深以下负增长,6 m水深处负增长最大,12 m水深以下负增长减小.由图 6b可见,在2 m水深处藻细胞活性最大,8 m水深以下活性基本恒定.藻类生产力及活性的变化与温度和光照随水深的变化有关,表层6 m以上水温较高,有光照,6 m以下水温降低,无光照,12 m以下低温且恒定.由图 6c可见,3 m水深以上的白瓶内叶绿素浓度均大于初始值,4 m水深以下白瓶内叶绿素浓度轻微减小.
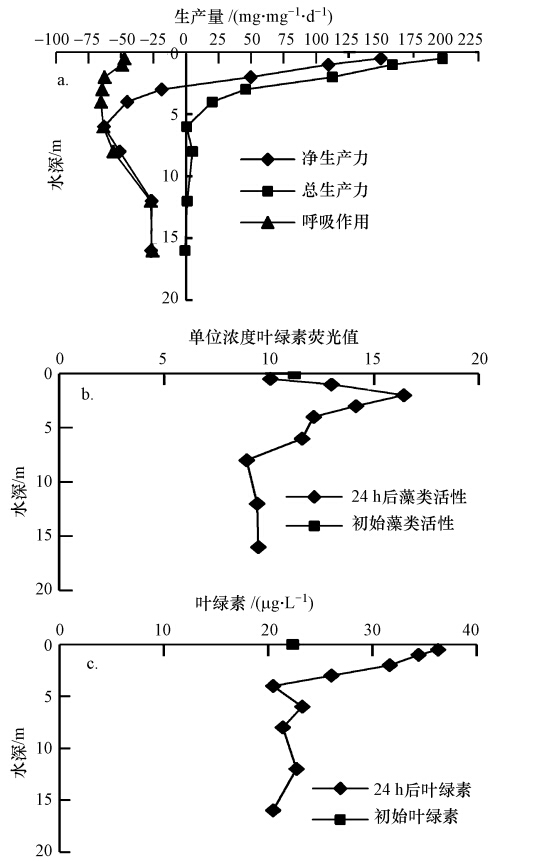 |
| 图 6 现场水深综合条件下藻类生长衰亡规律 Fig. 6 Growth and decay of algae under field depth comprehensive conditions |
将一定水深范围内单位叶绿素净生产量曲线与竖轴围成的面积相加,得出整个柱状水体的净生产力总量,此净生产力总量表示当上下层水体被充分混合,水中藻类浓度相同且为1 mg · L-1时柱状水体的净生产力.若该净生产力总量为正,说明藻类净增长,反之为负增长,藻类将得到控制.通过计算得出,当混合深度小于6.5 m时,净生产力总量为正,大于6.5 m时净生产力总量为负.当采用混合上下水层的方法控藻时,一方面要控制混合强度,使得藻类上下混合均匀,研究表明,当下向流速为1.65 cm · min-1大于藻类上浮速度,藻类上下分布已基本均匀(丛海兵等,2009);另一方面要具有一定的水深,尽可能延伸下部黑暗区的深度.
4 结论(Conclusions)1)在光强32500 lx时,周村水库水体中的藻类生产速率最大,达到0.0185 mg · μg-1 · h-1,增大或减小光强生长速率均减小,其中,零光强时生产速率为-0.0022 mg · μg-1 · h-1.
2)在温度26 ℃时,水库藻类的生产速率最大,说明该温度比较适合藻类生长.
3)常压时藻类的生产速率最大,增大压力生长速率减小,压力超过0.3 MPa时,藻类呈负增长.说明即使给予相同的温度和光照,压力对藻类生长有很强的抑制作用.
4)在水库水体中,藻类在2.5 m水深以上净生长,2.5 m水深以下藻类净衰亡,6 m水深处衰亡量最大.当采用混合上下水层的方法控藻时,混合深度必须达到一定水深,尽可能延伸下部黑暗区的深度.
| [1] | 丛海兵,黄廷林,缪晶广,等.2005.水体修复装置—扬水曝气器的开发[J].中国给水排水,21(3):41-45 |
| [2] | 丛海兵,黄廷林,赵建伟,等.2006.扬水曝气技术在水源水质改善中的应用[J].环境污染与防治,28(3):215-218 |
| [3] | 丛海兵,黄廷林,周真明,等.2007.藻类叶绿素测试新方法[J].给水排水,33(6):28-32 |
| [4] | 丛海兵,黄廷林,周真明.2009.于桥水库铜绿微囊藻上浮运动规律及其控制[J].给水排水,35(11):140-145 |
| [5] | Cong H B,Huang T L,Chai B B et al.2009.An new mixing-oxygenating technology for water quality improvement of urban water source and its implication in a reservoir[J].Renewable Ener-gy,34(9):2054-2060 |
| [6] | Cong H B,Huang T L,Chai B B.2011.Research on applying a water-lifting aerator to inhibit the growth of algae in a source-water reservoir[J].International Journal of Environment and Pollution,45(1/3):166-175 |
| [7] | 丛海兵,高郑娟,孙秀秀.2014.压力作用后太湖蓝藻沉淀性能及其去除研究[J].中国给水排水,30(1):43-47 |
| [8] | 黄廷林,段婷婷,卢金锁.2009.水源水中蓝藻生长悬浮特性及生长抑制试验研究[J].中国科技论文在线 |
| [9] | 贾含帅,刘汉湖,胡舒,等.2011.4种环境因子对景观水体绿藻生长繁殖的影响[J].中国城市林业,9(6):52-54 |
| [10] | 刘春光,金相灿,邱金泉,等.2005.光照与磷的交互作用对两种淡水藻类生长的影响[J].中国环境科学,25(1):32-36 |
| [11] | 刘建康.1999.高级水生生物学[M].北京:科学出版社.182-185 |
| [12] | 刘玉生,韩梅,梁占彬,等.1995.光照、温度和营养盐对滇池微囊藻生长的影响[J].环境科学研究,8(6):7-11 |
| [13] | 孙晓庆,董树刚.2007.藻类的生理生态学研究进展[J].海洋湖沼通报,(增刊):195-205 |
| [14] | 王佳佳,周桦,张进,等.2012.土壤样品中微生物活性的荧光分析方法[J].环境化学,31(10):1637-1643 |
| [15] | 于萍,张前前,王修林,等.2006.温度和光照对两株赤潮硅藻生长的影响[J].海洋环境科学,25(1):38-40 |
 2014, Vol. 34
2014, Vol. 34


