2. 中国环境科学研究院固体废物污染控制技术研究所,北京 100012
2. Research Institute of Solid Waste Management,Chinese Research Academy of Environmental Sciences,Beijing 100012
近年来,我国工业固体废物的产量不断增加,其中,危险废物产生量的统计数据呈不规则变化,但总体呈上升趋势(中华人民共和国环境保护部,2013).而目前我国对危险废物无害化利用和处置的保障能力不强,大量的危险废物长期堆存或无序排放,未得到有效利用处置,成为危害当地群众身体健康和周边环境的顽疾.自20世纪70年代起,欧洲、日本、美国等就开始大力开展危险废物在水泥窑等工业窑炉内的共处置技术的研究与应用,并逐步建立完善其标准管理技术体系,目前工业窑炉共处置技术已成为其废物处置技术体系的重要组成部分,是发达国家水泥行业节能减排的重要手段之一(Guo et al., 1996;Jakob et al., 1995).近年来,该技术在我国危险废物处置领域引起了广泛关注(朱雪梅等,2006;张霞等,2007;方伟,2000).危险废物水泥窑协同处置技术利用已有的装置和基础设施,使废物资源化,回收废物中的能源和资源,减小固体废物引起的环境负荷,因而得到了越来越多人们的认可(De et al., 2000;唐艳冬等,2012).
目前,国内外学者对水泥窑协同处置过程中重金属迁移特性的研究主要集中在固定特性上(杨玉飞等,2011;张俊丽等,2008;王雷等,2011c;李飞,2011;Eckert et al., 1998;Siddique et al., 2012;Sinyoung et al., 2011);另外,对监测现场重金属排放数据(朱桂珍,2000a;2000b)及热力学模拟(王雷等,2011a;2011b)等也有所研究,但这些研究更多关注稳定状态(热力学平衡)下重金属的排放规律,大多设定了特定工艺及特定危险废物,或采用重金属的氧化物代替特定的含重金属危险废物(崔敬轩等,2013),考察其在水泥工艺中挥发特性的规律.但事实上,重金属的挥发特性与重金属的化学形态密切相关,重金属氧化物的实验结论并不能直接推广到重金属的其他化学形态.另外,利用水泥窑协同处置含重金属危险废物时,重金属在水泥窑内首先发生是一系列非热力学平衡过程,而且最终也不一定都能达到热力学平衡状态.因此,现有的热力学平衡状态下的研究结论也很难用于实际的水泥窑协同处置过程中的重金属挥发预测.
Pb、Cd作为常见的环境污染物,对人体和其他生物体的神经系统、骨骼等有很强毒害作用,如镉中毒导致“痛痛病”等.同时,Pb、Cd也是各国废物焚烧标准及水泥窑处置危险废物标准中重点限排的重金属.因此,对Pb、Cd化合物在水泥窑协同处置过程中的挥发动力学特性进行研究尤为重要.
危险废物中Pb和Cd的主要存在形式有氧化物、氯化物、硫化物等,在前期对水泥窑协同处置过程中Pb和Cd的氧化物挥发特性的研究基础上(崔敬轩等,2013),本文继续对Pb和Cd的氯化物和硫化物的挥发特性进行研究.影响重金属挥发特性的关键参数为温度、时间和气氛(Barton et al., 1990;王学涛等,2006),本实验所采用的温度、时间和气氛与新型干法水泥窑一致,因此,实验结果基本可以反映实际水泥窑协同处置危险废物过程中的重金属挥发特性.本研究采用热重分析仪和高温管式炉,首先通过热重分析法确定PbCl2、PbS、CdCl2、CdS加热过程中的质量变化温度区间,然后结合水泥窑煅烧温度,开展等温挥发实验研究,得出等温挥发动力学参数,建立等温挥发动力学模型,以期为预测水泥窑协同处置过程中Pb、Cd的释放提供依据.
2 材料与方法(Materials and methods) 2.1 实验材料实验中所用到的试剂均为优级纯(GR),测定所用电感耦合等离子体质谱仪(ICP-MS)型号为Agilent 7500a,为美国Agilent公司产品.SDT Q600(Simultaneous Differential Technique)同步热分析仪,测温范围为室温至1500 ℃,为美国TA公司产品.
生料取自河北金隅红树林环保技术有限责任公司生料均化库,烧失量为35.02%,石灰饱和系数(KH)为0.9645,硅率(SM)为3.256,铝率(AM)为1.448.生料具体化学组成及配比见表 1.
| 表1 生料化学组成及配比 Table 1 Chemical composition and the ratio of raw materials |
称取5~15 mg粉末状试剂,放入热重分析专用坩埚,以空气作为载气进行热分析.气体流量设定为100 mL · min-1,实验升温速率为20 ℃ · min-1.
2.2.2 熟料煅烧实验利用新型干法水泥窑处置危险废物时,需要对重金属含量进行限定,确保重金属的添加对熟料品质不产生明显影响,同时,又要保证煅烧后的烟气及熟料中重金属含量高于相关精密仪器的检测限.基于此,本研究利用化学试剂模拟危险废物,将Pb、Cd在生料中的质量分数定为1%.将PbCl2、PbS、CdCl2 · 2.5H2O、CdS按计算值和生料均匀混合,备用.
准确称取分别混合有PbCl2、PbS、CdCl2 · 2.5H2O 、CdS的生料30 g,置于瓷舟中,然后推入升温到设定温度的高温管式炉中进行煅烧,每3 min取一次气体样,每个温度下煅烧40 min,取出瓷舟冷却至室温,保留煅烧熟料并研磨,过100目筛备用(经查阅文献可知,影响水泥窑协同处置危险废物过程中重金属挥发特性的关键因素为:温度、时间、气氛,因此,只要干法水泥窑协同处置危险废物过程中这3个条件与本实验一致,就可以预测该过程中重金属的挥发).
2.2.3 消解实验称取0.5 g研磨好的煅烧熟料,置于100 mL聚四氟乙烯烧杯中,加入王水和浓HF各20 mL,将烧杯置于预热至130~150 ℃的电热板上加热,蒸发至近干,用去离子水冲洗烧杯壁,再次加热蒸发至近干.然后将烧杯从电热板上移下,冷却至室温,加入1 mL浓硝酸和20 mL去离子水,在预热至90~100 ℃的电热板上持续加热,直至样品全部溶解.取下烧杯冷却至室温,过滤并转移至100 mL容量瓶定容,取样至聚乙烯瓶用ICP-MS测定重金属的浓度,计算其含量.
3 结果与分析(Results and analysis) 3.1 热重实验结果分析由图 1可见,PbCl2的失重主要发生在500~700 ℃,失重速率峰值出现在606 ℃,约为1.157% ℃-1.PbCl2的熔点为501 ℃,这与PbCl2开始发生失重的温度相符;PbS挥发的主要温度区间为800~1300 ℃,最大挥发速率出现在约1155 ℃,约为0.767% ℃-1.CdCl2 · 2.5H2O在失去结晶水(19.7%)后挥发的主要温度区间为550~700 ℃,最大挥发速率出现在约650 ℃;CdS在1155 ℃时挥发速率最大,主要挥发温度区间为800~1200 ℃.
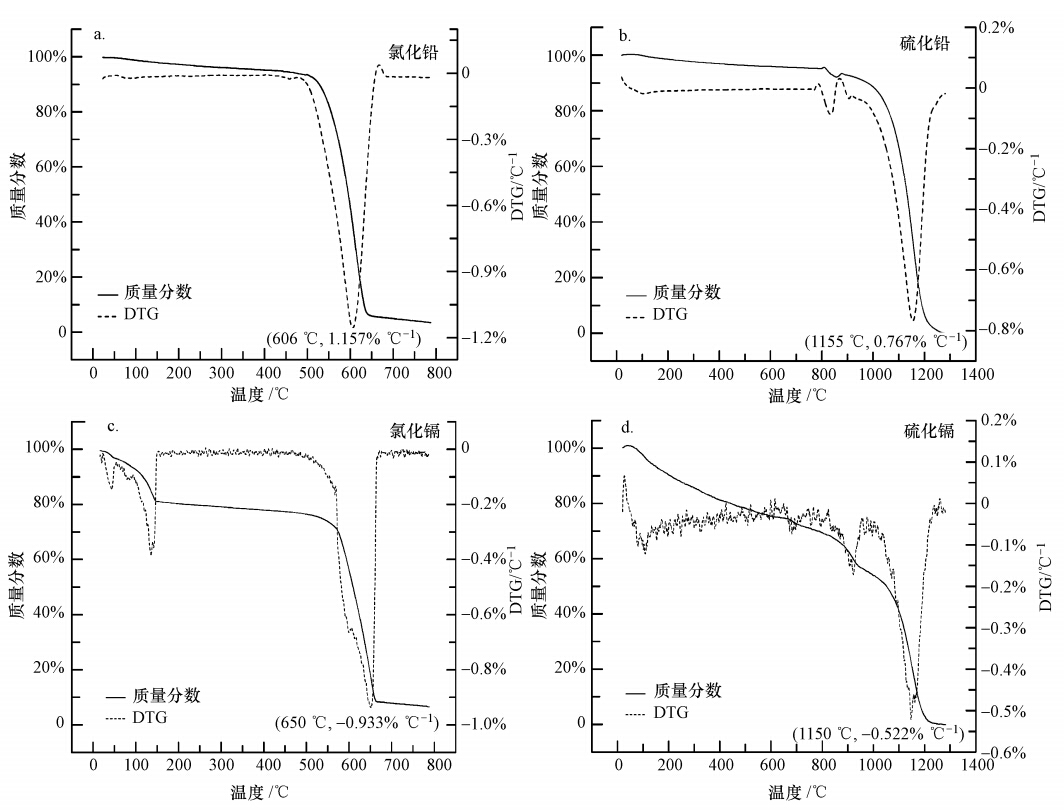 |
| 图 1 Pb、Cd的氯盐和硫化物的热重曲线 Fig. 1 Thermogravimetric curves of Pb and Cd |
目前,研究重金属挥发的资料大多是通过测定熟料中的量来推算挥发比例(王雷,2011c),为了避免熟料冷却过程中重金属持续挥发导致的误差,本实验直接采烟气样(采样及测样方法参照EPA method 29),测量不同时刻的Pb,Cd释放量.定义挥发率α为:
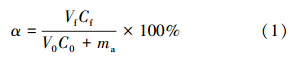
图 2给出了不同温度下加入Pb、Cd化合物的生料在煅烧过程中Pb、Cd的挥发率随时间的变化情况.氯化铅和硫化铅中铅的挥发率均随温度的升高、时间的增加而增大,煅烧25 min后基本不再挥发.氯化铅在500 ℃时开始挥发,1450 ℃时的最大挥发率为97.5%;硫化铅在800 ℃时开始挥发,1450 ℃时的最大挥发率为94%.由热重实验确定的氯化镉(CdCl2 · 2.5H2O)的主要挥发温度区间为500~1450 ℃,但实验过程中发现,氯化镉中镉从900~1000 ℃开始挥发.图 2c给出了水泥窑协同处置条件下CdCl2 · 2.5H2O的挥发规律,随着温度的升高、时间的增加,Cd的挥发率呈增大趋势,且在1450 ℃时,Cd在25 min时的挥发率达到了94%;硫化镉(CdS)的煅烧实验中,选择动力学模拟的温度为800~1450 ℃,但实验过程中发现,硫化镉中镉从1100~1150 ℃开始挥发.图 2d给出了水泥窑协同处置条件下CdS的挥发规律,随着温度的升高、时间的增加,Cd的挥发率呈增大趋势,且在1450 ℃时,Cd在25 min时的挥发率达到了92%.铅的氯化物的挥发率较之前研究的氧化物(崔敬轩等,2013)的挥发率要高.
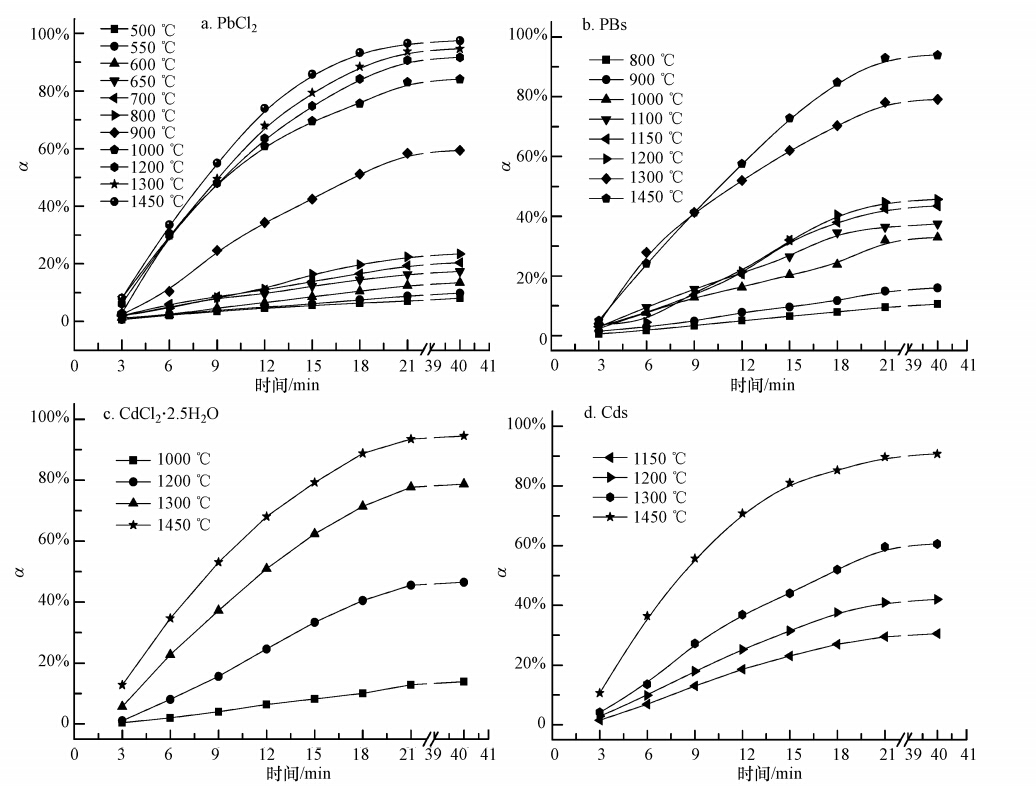 |
| 图 2 温度和时间对Pb、Cd元素挥发特性的影响 Fig. 2 Effect of temperature and time on the volatilization characteristics of Pb and Cd |
实验室煅烧熟料时重金属主要有3个去向:一是煅烧过程中随烟尘进入吸收液,一是固化在熟料中,一是通过在管壁冷凝等损失.这里把吸收液中和冷凝在管壁上的重金属均视为挥发部分的重金属.定义熟料中固化率=熟料中重金属含量/总进量,将煅烧后的熟料消解测定重金属含量.表 2给出了铅、镉的氯化物和硫化物经煅烧后在熟料中的固化率.
| 表2 铅、镉在熟料中的固化率 Table 2 Solidification ratios of Pb and Cd in clinker |
铅、镉的氯化物和硫化物中铅、镉的固化率呈现随温度升高而降低的规律,与挥发规律呼应.温度在1000 ℃以上时,氯化物的固化率要小于相应温度下硫化物和之前研究的氧化物的固化率(崔敬轩等,2013),这表明氯元素可能促进了铅、镉的挥发.
3.4 挥发动力学研究本文对Pb、Cd的挥发特性进行动力学研究,所涉及的挥发反应动力学属于等温、非均相反应动力学范畴,所采用的反应动力学方程是根据热力学原理推测的Arrhenius方程:
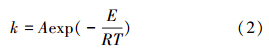
将式(2)等号两边取对数:
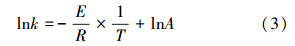
重金属的挥发速率可表示为如下形式:

为了减小误差,本文选用积分形式动力学机理函数G(α)= -ln(1-α),它与微分形式机理函数f(α)之间关系见如下公式:
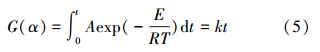
通过数据处理得到表观活化能E和指前因子A,代入式(2),再代入式(5)得到挥发率α与温度T和时间t的关系,即重金属随温度、时间变化的动力学方程.
对于氯化铅,n=1时,机理函数G(α)= -ln(1-α),因此,以-ln(1-α)对时间t做图,得到一直线(说明假设一级动力学是正确的),斜率即为k.图 3给出了各温度下氯化铅的挥发率积分函数G(α)对时间t的拟合曲线.对于不同的温度T,k值不同,于是再利用温度T与k的关系来求出E和A.
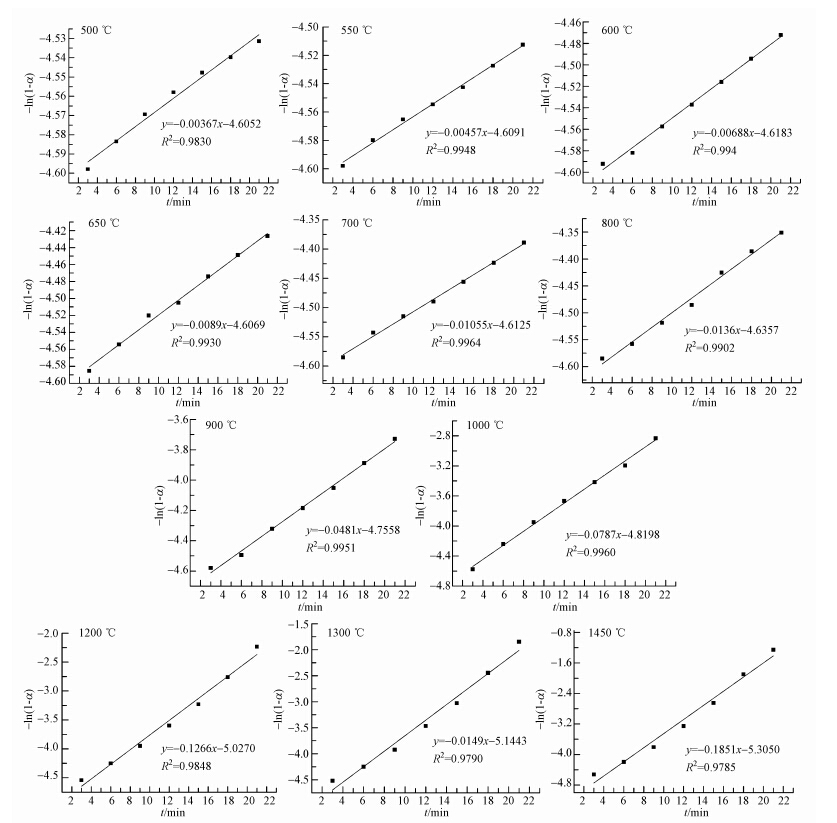 |
| 图 3 PbCl2中铅挥发率的G(α)-t的线性拟合 Fig. 3 G(α)versus t plots for linear fitting of PbCl2 |
图 4给出了PbCl2中铅的lnk-T-1的关系,由图 4a可以清晰地看到,在水泥窑协同处置过程中氯化铅的挥发规律可以分为两部分:900 ℃以上和900 ℃以下.900 ℃以上时,PbCl2的lnk-T-1的线性拟合如图 4b所示,把所得斜率和截距带入式(3),求得协同处置过程中氯化铅中铅挥发反应的表观活化能E为40.24 kJ · mol-1,指前因子A为3.23 min-1,得到煅烧过程中氯化铅中铅的挥发动力学方程:α=1-exp(-3.23exp(-4048.4/T)t).900 ℃以下时,PbCl2的lnk-T-1的线性拟合如图 4c所示,把所得斜率和截距带入式(3),求得协同处置过程中氯化铅中铅挥发反应的表观活化能E为31.37 kJ · mol-1,指前因子A为0.49 min-1,进而得到煅烧过程中氯化铅中铅的挥发动力学方程:α=1-exp(-0.49exp(-3772.6/T)t).
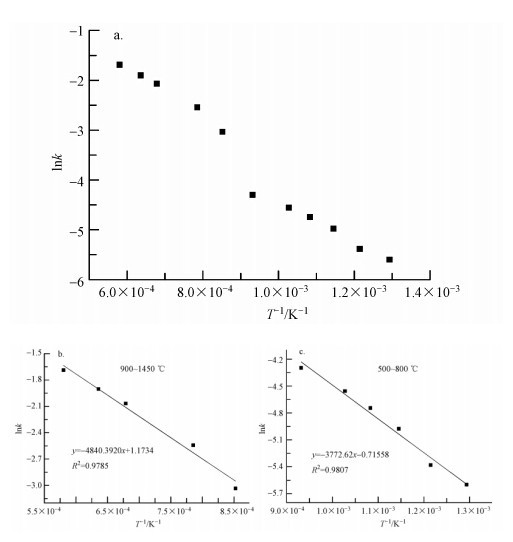 |
| 图 4 PbCl2的lnk-T-1的线性拟合效果图 Fig. 4 lnk versus T-1 plots for linear fitting of PbCl2 |
对于硫化铅,将铅的挥发率积分函数G(α)对时间t进行线性拟合,结果见表 3.将各温度下速率常数k取对数值,对温度的倒数(T-1)作图,结果如图 5所示.
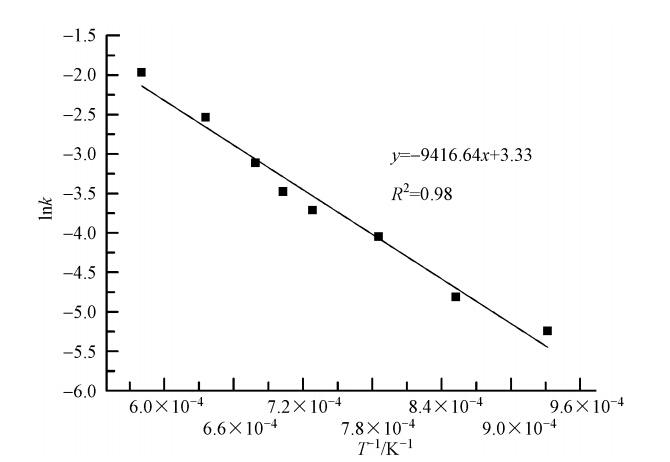 |
| 图 5 硫化铅中铅的lnk-T-1的线性拟合效果图 Fig. 5 lnk versus T-1 plots for linear fitting of lead sulfide |
把图 5中所得斜率和截距带入式(3),求得协同处置过程中硫化铅中铅挥发反应的表观活化能E为78.29 kJ · mol-1,指前因子A为27.9 min-1,进而得到煅烧过程中硫化铅中铅的挥发动力学方程:α=1-exp(-27.9exp(-9416.6/T)t).
| 表3 硫化铅中铅的G(α)-t的线性拟合汇总 Table 3 G(α)versus t plots for linear fitting of lead sulfide |
对于氯化镉,将镉的挥发率积分函数-ln(1-α)和时间t进行线性拟合,结果见表 4.将各温度下速率常数k取对数值,对温度的倒数(T-1)作图,结果如图 6所示.
| 表4 氯化镉中镉的G(α)-t的线性拟合汇总 Table 4 G(α)versus t plots for linear fitting of cadmium chloride |
把图 6中所得斜率和截距带入式(3),求得协同处置过程中氯化镉中Cd的挥发反应的表观活化能E为124 kJ · mol-1,指前因子A为898 min-1,进而得到煅烧过程中氯化镉中Cd的挥发动力学方程:α=1-exp(-898exp(-14901/T)t).
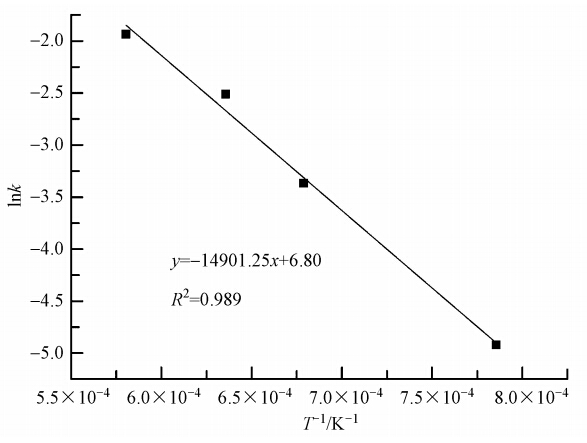 |
| 图 6 氯化镉中镉的lnk-T-1的线性拟合效果图 Fig. 6 lnk versus T-1 plots for linear fitting of cadmium chloride |
对于硫化镉,将镉的挥发率的积分函数-ln(1-α)对时间t进行线性拟合,结果见表 5.将各温度下的反应速率常数k取对数值,对温度倒数(T-1)作图,结果如图 7所示.
| 表5 硫化镉中镉的G(α)-t的线性拟合汇总 Table 5 G(α)versus t plots for linear fitting of cadmium sulfide |
把图 7中所得斜率和截距带入式(3),求得协同处置过程中硫化镉中Cd的挥发反应的表观活化能E为129 kJ · mol-1,指前因子A为1032 min-1,进而得到煅烧过程中硫化镉中Cd的挥发动力学方程:α=1-exp(-1032exp(-15518/T)t).
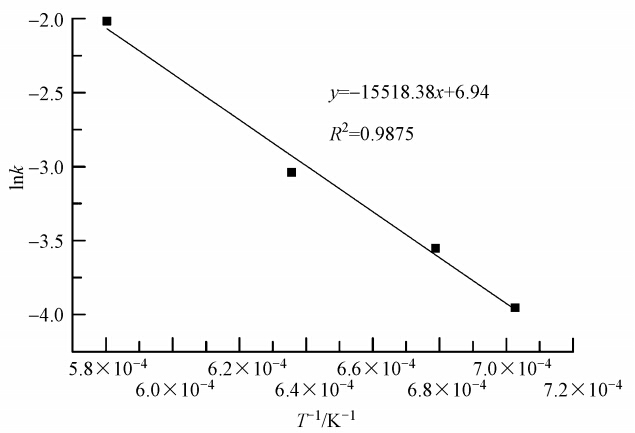 |
| 图 7 硫化镉中镉的lnk-T-1的线性拟合效果图 Fig. 7 lnk versus T-1 plots for linear fitting of cadmium sulfide |
从表观活化能的角度判断,水泥窑协同处置过程中两种重金属的挥发性排序为Pb>Cd;铅的不同化学形态的挥发性为PbCl2 > PbS> PbO(崔敬轩等,2013),镉的不同化学形态的挥发性为CdCl2 > CdS > CdO.
通过实验中得到的挥发动力学方程式,可以预测水泥窑协同处置危险废物过程中以硫化物和氯化物形态存在的Pb和Cd在任何温度和任何停留时间时的挥发率,进而可以筛选适合水泥窑协同处置的危险废物类别,确定适宜的危险废物投加位置,控制危险废物的掺加量,有效控制水泥窑协同处置危险废物过程中的环境风险.
4 结论(Conclusions)1)热重实验表明,Pb、Cd的氯化物和硫化物在加热到一定温度时具有较高的挥发性,且氯化物的挥发温度比硫化物低.
2)水泥窑协同处置过程中,以氯化物和硫化物形态存在的Pb、Cd的挥发率均随温度的升高、时间的增加而增大,煅烧25 min后基本不再挥发.
3)实验结果证明,挥发速率函数G(α)= -ln(1-α)与时间t呈很好的线性关系,挥发规律符合一级动力学方程,共处置过程中Pb、Cd的挥发动力学方程为: PbCl2:500~800 ℃, α=1-exp(-0.49exp(-3772.6/T)t); 900~1450 ℃, α=1-exp(-3.23exp(-4048.4/T)t); PbS:800~1450 ℃, α=1-exp(-27.9exp(-9416.6/T)t); CdCl2·2.5 H2O:1000~1450 ℃, α=1-exp(-898exp(-14901/T)t); CdS:1150~1450 ℃, α=1-exp(-1032exp(-15518/T)t).
4)从表观活化能的角度判断,水泥窑协同处置过程中,两种重金属的挥发性排序为Pb>Cd;铅的不同化学形态的挥发性为PbCl2 > PbS > PbO,镉的不同化学形态的挥发性为CdCl2 > CdS > CdO.
| [1] | Barton R G,Clark W D,Seeker W R.1990.Fate of metals in waste combustion systems[J].Combustion Science and Technology,74(1/6):327-342 |
| [2] | 崔敬轩,闫大海,李丽,等.2013.水泥窑协同处置过程中Pb、Cd的挥发特性[J].环境工程学报,7(12):5001-5006 |
| [3] | De Ladebat H,Lemarchand D.2000.Waste manage-ment solution[J].World Cement,31(3):70-78 |
| [4] | Eckert J J O,Guo Q Z.1998.Heavy metals in cement and cement kiln dust from kilns co-fired with hazardous waste-derived fuel:application of EPA leaching and acid-digestion procedures[J].Journal of Hazardous Materials,59(1):55-93 |
| [5] | 方伟.2000.水泥回转窑处置危险废物的技术研究[J].水泥技术,7(6):8-11 |
| [6] | Guo Q Z,Eckert Jr J O.1996.Heavy metal outputs from a cement kiln co-fired with hazardous waste fuels[J].Journal of Hazardous Materials,51(1):47-65 |
| [7] | Jakob A,Stucki S,Kuhn P.1995.Evaporation of heavy metals during the heat treatment of municipal solid waste incinerator fly ash[J].Environmental Science & Technology,29(9):2429-2436 |
| [8] | 李飞.2011.共处置废弃物生产水泥过程中重金属的迁移与固化机理研究 .焦作:河南理工大学 |
| [9] | Siddique R,Rajor A.2012.Use of cement kiln dust in cement concrete and its leachate characteristics[J].Resources,Conservation and Recycling,61:59-68 |
| [10] | Sinyoung S,Songsiriritthigul P,Asavapisit S,et al. 2011.Chromium behavior during cement-production processes:a clinkerization,hydration,and leaching study[J].Journal of Hazardous Materials,191 (1/3):296-305 |
| [11] | 唐艳冬,陈坤,王树堂,等.2012.水泥窑共处置应用的国际经验[J].环境保护,40(14):68-71 |
| [12] | 王雷,金宜英,李润东,等.2011a.危险废物水泥窑共处置过程Pb的热力学平衡[J].燃烧科学与技术,17(3):224-230 |
| [13] | 王雷,金宜英,聂永丰,等.2011b.焚烧飞灰水泥窑共处置过程As的迁移特征[J].环境科学学报,31(2):407-413 |
| [14] | 王雷,金宜英,李润东,等.2011c.废物水泥窑共处置过程砷的固定特性及产物的环境安全性[J].化工学报,62(3):816-822 |
| [15] | 王学涛,金保升,仲兆平.2006.气氛对焚烧飞灰熔融过程中重金属行为的影响[J].中国电机工程学报,26(7):47-52 |
| [16] | 杨玉飞,杨昱,汪群慧,等.2011.间歇浸取对废物水泥窑共处置产品中 Cr 和 As 释放的影响[J].环境工程学报,5(2):419-424 |
| [17] | 张俊丽,刘建国,李橙,等.2008.水泥窑协同处置与水泥固化/稳定化对重金属的固定效果比较[J].环境科学,29(4):1138-1142 |
| [18] | 张霞,花明,黄启飞,等.2007.固体废物水泥窑共处置技术的现状及发展[J].再生资源研究,28(4):37-40 |
| [19] | 中华人民共和国环境保护部.2014 工业固体废物 .2014-03-20.http://zls.mep.gov.cn/hjtj/nb/2012tjnb/201312/t20131225_265549.htm |
| [20] | 朱桂珍.2000a.利用水泥回转窑焚烧处置危险废物的评价研究[J].环境科学学报,20(6):810-812 |
| [21] | 朱桂珍.2000b.利用水泥回转窑焚烧处理危险废物的评价研究[J].环境保护,28(3):14-16 |
| [22] | 朱雪梅,刘建国,黄启飞,等.2006.固体废物水泥窑共处置技术应用及存在问题[J].中国水泥,21(4):45-49 |
 2014, Vol. 34
2014, Vol. 34


