2. 特拉华大学土木与环境工程系,美国特拉华纽瓦克 19716
2. Department of Civil and Environmental Engineering,University of Delaware,Newark,USA 19716
垃圾填埋气体主要包含CO2和CH4,两者均是主要的温室气体,其中,甲烷因更强的红外吸收能力和更短的大气层滞留时间,其温室气体潜力在100年尺度上是等质量CO2的25倍(IPCC,2007a;I2007b).垃圾填埋气体是我国大气甲烷的主要排放源之一,估计到2020年来自于垃圾填埋场的甲烷排放量将占总排放量的31.6%(赵玉杰等,2004).生物覆盖(Biocover)是政府间气候变化专门委员会(IPCC)推荐用于减少垃圾填埋场甲烷排放的一种低成本技术(IPCC,2007a),其主要原理是通过优化环境条件,强化填充介质中的微生物消耗甲烷过程来实现甲烷排放的减量化(Huber-Humer et al., 2009).
甲烷的氧化(或微生物活动)主要受制于温度、水分、pH和营养供给等因素(Humer et al., 1999).在实际工程应用中,季节交替引起的温度变化、大气降水和干旱等都将直接影响到生物覆盖层中温度和含水率的变化,这种变化易引起覆盖层中甲烷氧化性能变化.研究表明,嗜甲烷菌生长的最佳适宜温度约为30 ℃(Boeckx et al., 1996;Scheutz et al., 2009;Stein et al., 2001;Whalen et al., 1990),随着温度升高微生物活动逐步降低,直到临界值~55 ℃(Spokas et al., 2011).介质含水率是影响微生物氧化甲烷的决定性条件之一(Humer et al., 1999),主要原因在于适宜的含水率可以使嗜甲烷菌、水、氧气和甲烷有充分的接触时间.另一方面,过高的含水率会阻碍氧气扩散进入覆盖层,如Cabral等(2004)认为当水饱和度>85%时扩散系数将骤减一个数量级,液相可用的CH4和O2将急剧减少,从而导致氧化效率下降(Scheutz et al., 2009).相反地,在干燥条件下介质颗粒周围水膜厚度变薄会导致微生物活动减弱,当含水率低于10%时,甲烷的氧化效率将变得非常低(Abichou et al., 2011).此外,Boeckx等(1996)的研究表明,当含水率低于5%时,甲烷的氧化效率急剧下降.
目前,有关生物覆盖在工程应用和野外条件下的研究仍然较少,大部分研究主要集中在利用不同测量手段(如同位素等)检验生物覆盖层对甲烷的氧化性能等方面,长期野外观察仍然较少.在野外条件下,含水率和温度作为控制生物覆盖层介质中微生物生长的两个重要影响因子,两者会随季节、降水过程等的变化而改变.因此,本文利用实验室模型验证温度和含水率在野外条件下对不同有机质含量(38%和61%)的生物覆盖单元甲烷氧化率的单因素和综合影响.一方面验证已有的关于温度和含水率对生物覆盖层甲烷氧化率预测模型在野外条件下(如季节变化)的有效性,以期为利用模型预测生物覆盖技术在实际工程中甲烷的氧化效能提供指导作用.另一方面,充分理解含水率和温度在野外条件下对生物覆盖层中微生物活动的条件控制,即含水率和温度与微生物氧化甲烷的相互关系,将有助于通过其他物理措施优化生物覆盖层中温度和含水率以达到最优性能.
2 试验设计和方法(Experiments and methods) 2.1 实验设计2 009年,将两种不同有机质含量的庭院垃圾用于美国加利福尼亚州YOLO郡垃圾填埋场一填埋单元旁的两个生物覆盖单元(2.4 m ×1.8 m ×1.2m)建设,分别标记为1# 单元(有机质含量38%的陈旧绿色废物放置在垃圾填埋场填埋单元斜坡上,熟化时间超过1年)和2#单元(垃圾填埋场新接收的有机质含量为61%的新鲜绿色废物,熟化时间为约2个月),并对两个单元进行为期为15个月的实验和观测).Yolo郡为典型的地中海气候,常年少雨,生物覆盖单元的剖面示意图如图 1所示.体积比为59%:40% 的CH4/CO2混合气体经过粗砾层后均匀地导入初始厚度为0.9 m的生物覆盖层.2010年4月测得1#和2#单元的甲烷进气量分别为(251±4)g · m-2 · d-1和(207±3)g · m-2 · d-1.2010年4月7日测得1#和2#单元生物覆盖层厚度因为物理沉降和生物降解分别减少为76 cm和62 cm.根据厚度变化估计1#和2#单元填埋平均干密度分别从初期0.29和0.25 g · cm-3增加为0.34和0.36 g · cm-3.2009年6月完成的填料分析表明,两种填料的区别主要在于pH(5.1和5.7,建议值6.5~8.5)、有机质(38%和61%,建议值>15%)及氨氮(21和103 mg · kg-1,建议值<400 mg · kg-1),除此之外,其它建议项(Huber-Humer et al., 2009)均为细微差别.此外,2010年7月测得所取两个单元样品的总体孔隙度均为0.73.
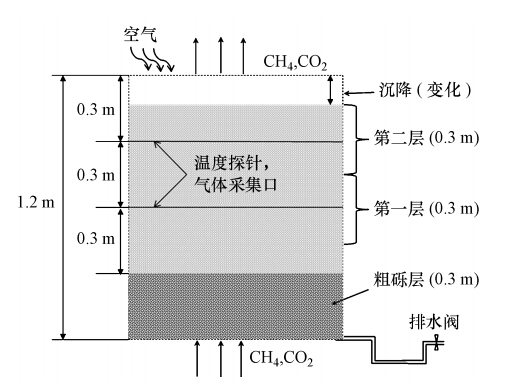 |
| 图 1 生物覆盖单元示意图 Fig. 1 Sketch map of biocover cell |
微生物对甲烷的氧化反应方程可用式(1)表示,其氧化动力学方程可用式(2)表示.
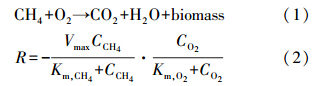
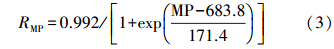
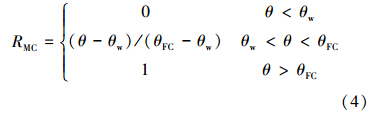
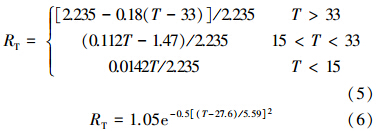
本研究中,分别通过悬挂法(0~10 kPa)和露点水势仪(10 kPa以上数据,型号:WP4,DECAGON,美国)测量水势,样品烘干后转换为体积含水率绘制持水曲线.为得到其它非测量点水势用于计算,两种材料的持水曲线均通过悬挂法测得的数据基于双孔模型(Dual Porosity Model,DPM)(Gerke et al., 1993)进行拟合,拟合所得参数见表 1.
| 表1 双孔模型拟合参数 Table 1 Fitting of parameters of dual porosity model |
相对氧化率的测量和计算是在实验室内完成的.25 ℃条件下,野外采集的样品分成8个约42 g的小样加入到25 mL蒸馏水中,在体积为250 mL的试管内培育.期间每0.5 h测量一次CH4浓度的变化,进而通过拟合获取Vmax,完成测试后在105 ℃下烘烤24 h,通过换算得到甲烷消耗率(g · g-1,以干样计),并以测得的最大甲烷消耗量作为参考值将测得数据归一化得到相对氧化率.
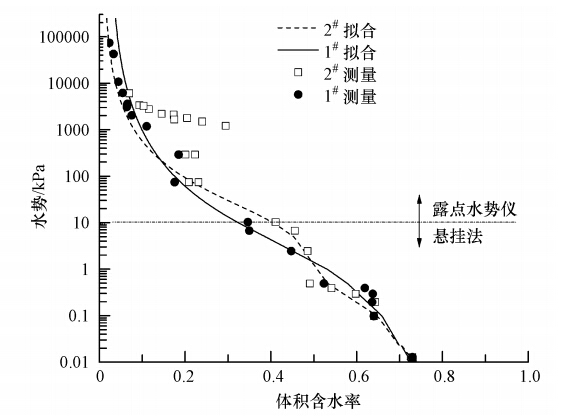 |
| 图 2 模拟数据与测量结果的比较 Fig. 2 Simulated data versus measured value |
采用地螺钻采样,并用烘干法测得两个单元样品的含水率,结果如图 3所示.需要说明的是,不同日期的样品并不是取至相同深度,其深度变化如表 2所示.从图 3可以看出,2010年春季,1#单元第2层(0~30 cm)样品的含水率都明显高于第1层(30~60 cm),这可能与生物覆盖单元所在地区降雨集中在冬、春季有关(图 6),降水量在11月至次年2月较为集中.2#单元样品的含水率明显高于1#单元,这与2#单元更强的持水能力保持一致.研究表明,每增加1%的有机质含量,介质持水能力将增加3.7%(Hudson,1994).
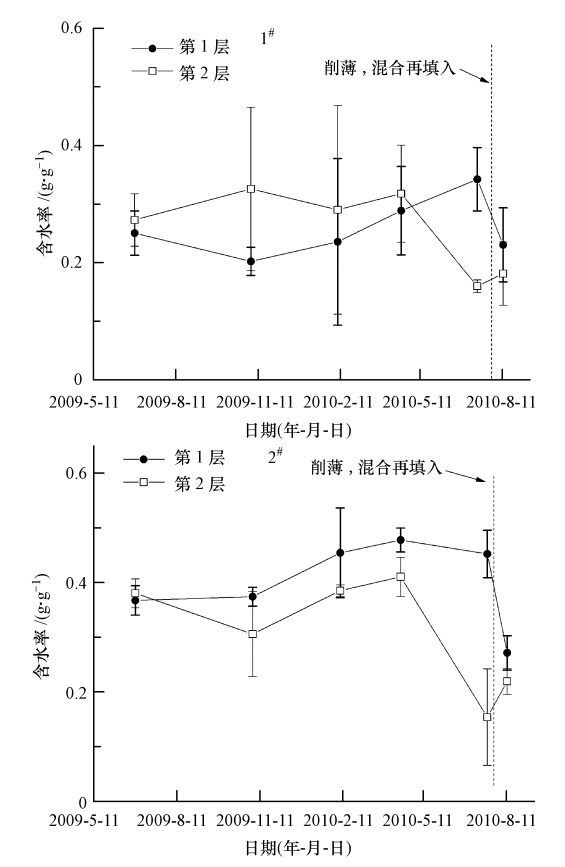 |
| 图 3 1#和2#单元两层样品的含水率 Fig. 3 Measured moisture content in two layers of 1# cell and 2# cell |
| 表2 含水率测量深度 Table 2 Depth of moisture content measurement |
据式(3)得到水势的相对氧化率(拟合数据)与2010年2月实验室实测含水率转化成相对氧化率的对比如图 4所示.从图 4可以看出,预测结果与两个模型的拟合结果保持一致,即两个模型均能较好地预测水势对甲烷氧化效率的影响.
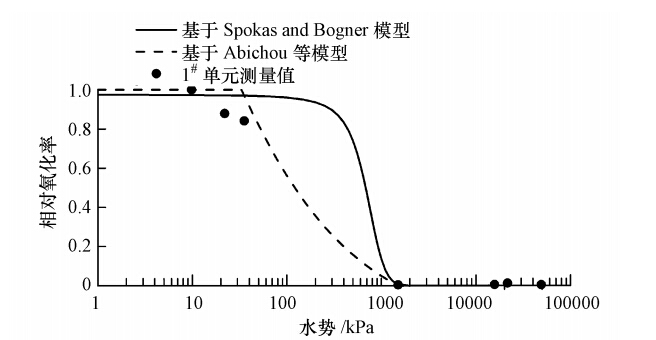 |
| 图 4 基于模型的预测值与测量值间的比较 Fig. 4 Comparison of predicted result by models and measured data |
一般地,甲烷在覆盖层中的氧化主要发生0~30 cm深处,将不同日期测得的含水率(图 3)通过双孔模型转换成水势,得到两个单元第2层(0~30 cm)的甲烷相对氧化率如图 5所示,误差棒代表 95%置信区间.从图 5可以看出,在2#单元中,第2层含水率在约0.3~0.4(实线)之间变化,仍保持在0.9以上的相对氧化率.与此相反,在1#单元第2层,含水率的波动(虚线)对甲烷的相对氧化率影响较大,相对氧化率在约0.4~0.7范围内大幅度波动. 2010年7月底,将两个单元的顶层剥除后再混合填入覆盖单元后含水率均达到0.2左右,此时甲烷的相对氧化率变得非常小,随后伴随含水率的增加两个单元的甲烷相对氧化率又恢复到较高水平(>0.6).总体上,2#单元因含水率相对较高,含水率的小幅波动对甲烷氧化率影响不大.
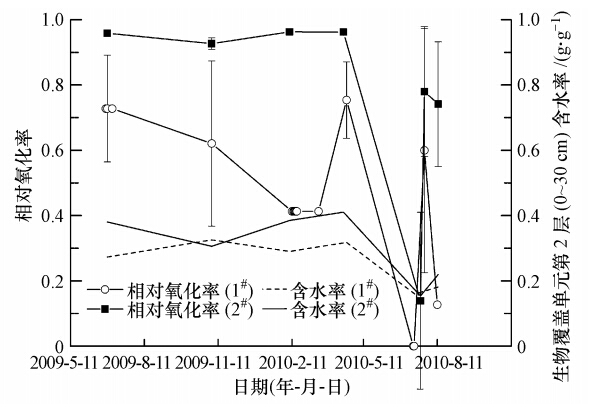 |
| 图 5 含水率对甲烷氧化的影响 Fig. 5 Impact of moisture content on methane oxidation |
图 6分别描述了传感器日均温度随季节交替而变化的规律.2009年夏季生物覆盖层建设初期,因典型的厚度差异(传感器固定在生物覆盖层支撑龙骨上,分别位于初始表面下方30、60 cm处)使得环境温度与处于不同深度间传感器温度差异明显,但伴随生物覆盖层厚度的减少和温度的降低,这种温度差异逐渐变小(图 6),在11月至次年3月中旬,温度差异不明显,随着夏季到来,温度逐步回升.总体上保持了冬、春季低温,夏、秋季高温的趋势.
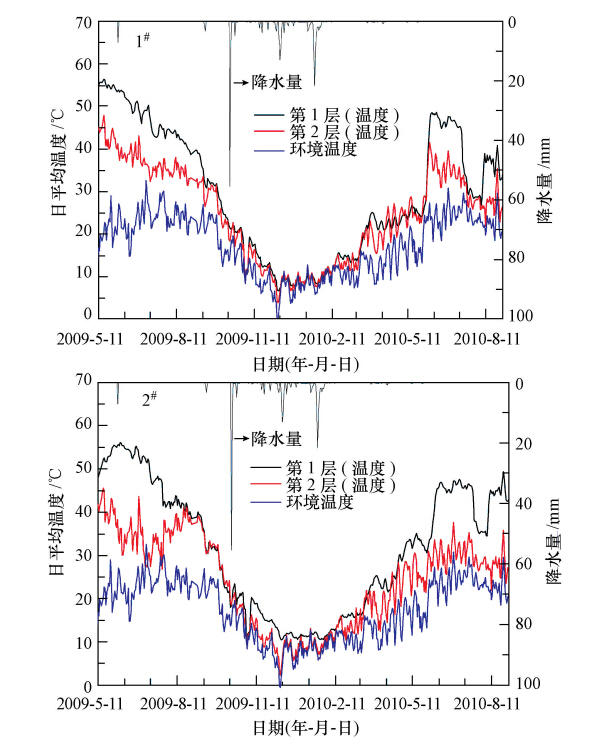 |
| 图 6 1#和2#单元不同层温度测量值 Fig. 6 Measured temperature in different layers of 1# cell and 2# cell |
图 7展示的是采集样品分别在15、25和35 ℃条件下完成微生物培养实验所得数据.结果表明,模型预测值与实验室培养结果总体一致.
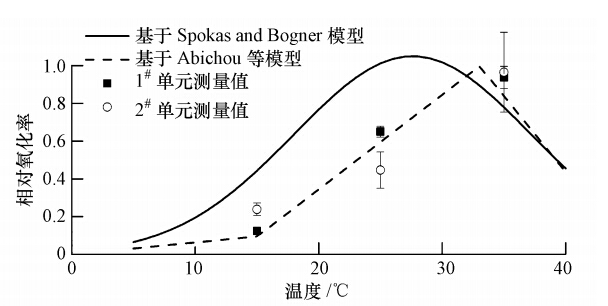 |
| 图 7 基于模型的预测值与测量值间的比较 Fig. 7 Comparison of predicted result by models and measured data |
温度对甲烷相对氧化率的影响如图 8所示,结果表明,在1#单元第2层,甲烷相对氧化率随季节变化而波动明显:从2009年夏季的约0.6降至2010年春季的最低点0.3,2010年夏季回升至0.9以上,说明温度对1#单元的甲烷氧化有明显影响.相比之下,2#单元第2层的甲烷相对氧化率在测试点上总能保持在0.7以上,说明在2#单元温度对甲烷相对氧化率的影响相对比较稳定.
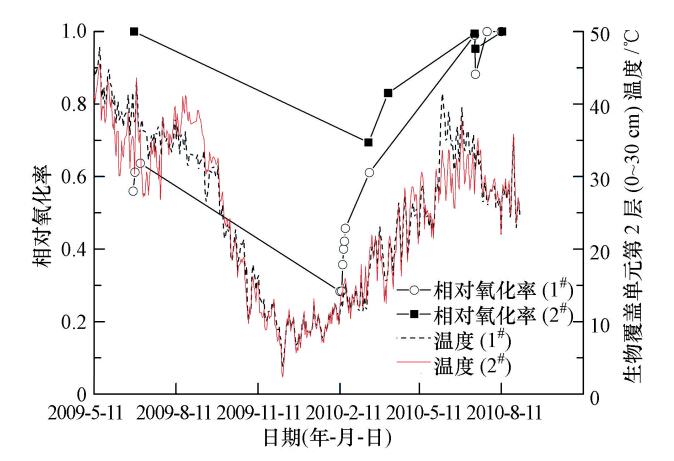 |
| 图 8 温度对甲烷氧化率的影响 Fig. 8 Impact of temperature on methane oxidation |
为更好地理解含水率和温度对甲烷氧化效率的综合影响(RMP、RT),本文进行了模型预测值(Spokas et al., 2011)与实测氧化率间的比较.相关性分析结果表明,1#单元中测量值与模型预测值呈现出明显的关联性(皮尔森相关系数r=0.71).此外,回归分析结果表明,1#模型能较准确地预测1#单元生物覆盖层中甲烷氧化率与温度和含水率间的关系(校正R2=0.46,图 9),即温度和含水率共同影响着甲烷的氧化.但2#单元并未显示出明显的线性关系,表明除温度和含水率之外,其它因子的影响不能忽略.
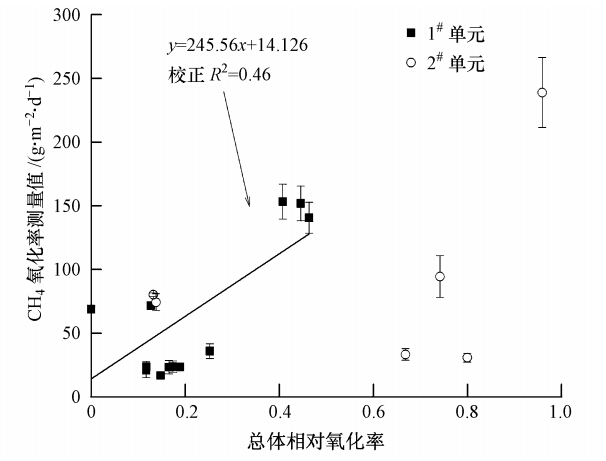 |
| 图 9 总体相对氧化率与测量值 Fig. 9 Total relative oxidation and measured oxidation |
根据温度和含水率影响下的甲烷相对氧化率之比可得出对甲烷氧化起主导作用的因子.整个实验期间的限制因子如表 3所示.需要说明的是,在表 3中限制项仅表示一种相对性,如2009年6月25日,2#单元2种因素下的甲烷相对氧化率分别为1.00、0.96,结果显示为含水率为限制因子,但实际上两者比值接近1,即表明两者对甲烷的氧化贡献率很接近.生物覆盖层建设初期(约3个月后,即2009年夏季),温度和含水率相对氧化率比值表明,1#单元受到温度和含水率的共同影响且两者的贡献率较为接近,在2010年,随降水量减少和温度回升,含水率限制了生物覆盖层的氧化性能.2#单元也显示出相似的规律,这与实验现场所处的气候条件(地中海气候,夏季降水较少)保持一致.尽管在2010年8月没有降水,通过再混合填入,两个填埋单元的含水率各自变得相对均匀,但结果表明1#单元仍是含水率限制了甲烷的氧化.在2#单元,含水率和温度相对氧化率间的比例明显变小,从图 3和图 4可以看出,2#单元在混合前后的含水率变化明显大于1#单元,这与表 3中8月份所得相对氧化率比值是一致的.
| 表3 相对氧化率与限制因子 Table 3 Relative oxidation and limited factor |
本文运用已有的预测模型验证了野外条件下温度和含水率对生物覆盖层甲烷氧化性能的影响,结果表明,两个模型单因素预测值与实验室测量值保持一致,即模型均能预测温度和含水率(水势)对生物覆盖层中甲烷氧化性能的影响.在预测含水率和温度对其性能的综合影响时,相对较低有机质含量(38%)单元的预测值与测量值呈现出明显的线性关系,说明在本实验中温度和含水率对生物覆盖层的甲烷氧化效率起主导作用.然而这种关系在高有机质含量(61%)单元中表现并不明显,说明除温度和含水率之外,其他因子对生物覆盖层的氧化性能起到了重要作用.另一方面,高有机质含量会明显改变多孔介质,如结构、比表面、持水能力和营养供给等物化特性,这也可能是导致本实验2#单元中预测的不确定性的原因之一.
| [1] | Abichou T,Chanton J,Powelson D,et al. 2006.Methane flux and oxidation at two types of intermediate landfill covers[J].Waste Manage-ment,26(11):1305-1312 |
| [2] | Boeckx P,vanCleemput O,Villaralvo I.1996.Methane emission from a landfill and the methane oxidising capacity of its covering soil[J].Soil Biology and Biochemistry,28:1397-1405 |
| [3] | Cabral A R,Tremblay P,Lefebvre G.2004.Determination of the diffusion coefficient of oxygen for a cover system including a pulp and paper by-product[J].Geotechnical Testing Journal,27(2):184-197 |
| [4] | Gerke H H, Van Genuchten M T.1993.A dual-porosity model for simulating the preferential movement of water and solutes in structured porous-media[J]. Water Resources Research,29(2):305-319 |
| [5] | Huber-Humer M,Rder S,Lechner P.2009.Approaches to assess biocover performance on landfills[J]. Waste Management,29(7):2092-2104 |
| [6] | Hudson B D.1994.Soil organic-matter and available water capacity[J].Journal of Soil and Water Conserva-tion 49(2):189-194 |
| [7] | Humer M,Lechner P.1999.Alternative approach to the elimination of greenhouse gases from old landfills[J].Waste Manage-ment Research,17:443-452 |
| [8] | IPCC.2007a.Climate Change 2007:Mitigation.Contribution of Working Group III to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change [M].Cambridge,United Kingdom and New York,NY,USA:Cambridge University Press |
| [9] | IPCC.2007b.Cli-mate Change 2007:The Physical Science Basis.Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change [M].Cambridge,United Kingdom and New York,NY,USA:Cambridge University Press |
| [10] | Scheutz C,Kjeldsen P,Bogner J E,et al. 2009.Microbial methane oxidation processes and technologies for mitigation of landfill gas emissions[J].Waste Management Research,27 (5):409-455 |
| [11] | Spokas K A,Bogner J E.2011.Limits and dynamics of methane oxidation in landfill cover soils[J].Waste Management,31(5):823- 832 |
| [12] | Stein V B,Hettiaratchi J P A.2001.Methane oxidation in three Alberta soils:Influence of soil parameters and methane flux rates[J]. Environmental Technology,22(1):101-111 |
| [13] | Whalen S C,Reeburgh W S,Sandbeck K A.1990.Rapid methane oxidation in a landfill cover soil [J].Applied and Environmental Microbiology,56(11):3405-3411 |
| [14] | 赵玉杰,王伟.2004.垃圾填埋场甲烷气的排放及减排措施[J].环境卫生工程,12(4): 217-219 |
 2014, Vol. 34
2014, Vol. 34


