2. 中国环境科学研究院, 城市水环境科技创新基地, 北京 100012;
3. 东北大学, 材料与冶金学院, 沈阳 110004
2. Department of Urban Water Environmental Research, Chinese Research Academy of Environmental Sciences, Beijing 100012;
3. College of Material and Metallurgy, Northeast University, Shenyang 110004
溶解有机质(DOM)是天然水体中重要的组成部分,它可以通过各种物理化学过程,与水体中的颗粒物以及污染物,如矿物颗粒、金属离子、有机污染物等相互作用,从而影响水体的特性以及污染物的分布、迁移转化、生物可降解性以及生物毒性(Ravichandran, 2004; Leenheer and Croué,2003).由于溶解有机质对水体生态系统和生物化学过程产生的重要影响,因而受到越来越多研究者的关注(Al-Reasi et al., 2013; Hudson et al., 2007; Stutter et al., 2013).
水体中溶解有机质主要包括腐殖质、富里酸、各种亲水性有机酸、氨基酸、碳水化合物和一些人类活动产生的有机污染物等(Baker,2002a),来源不同的溶解性有机物具有不同的荧光基团.荧光基团主要分为类蛋白和类腐殖质两大类,这些基团的荧光特性包含了与其结构、官能团、构型、非均质性、分子内与分子间的动力学特征等相关的信息.来源不同的溶解性有机物的荧光峰的位置和荧光强度不尽相同(Coble,2002; Mayer et al., 1999; Murphy et al., 2008).目前,三维荧光技术,作为高灵敏度、高选择性、高信息量、快速准确的光谱指纹技术,已被广泛应用于天然水体中溶解有机质的研究(Chen et al., 2013; Mostofa et al., 2005; Pagano et al., 2012),它是通过同时扫描激发和发射波长而获得荧光强度的三维坐标矩阵光谱分析,并对复杂体系中荧光光谱进行光谱识别和表证,从而获得水体中溶解有机质荧光组分的组成和浓度信息,并解析溶解有机质在各种水体中的来源、分布及生物活动,由此判断水体的水质状况.
辽河流域是全国著名的老工业基地,传统的工业产业发展有近60年的历史,辽河流域集中了以化工、石化、制药、冶金、印染等为核心的产业集群,同时也是都市密集区;英国中部城市伯明翰是英国第二大城市,工业革命时期,伯明翰的工业发展非常迅速,以重工业为主,是当时世界最大的金属加工地区之一,其中包括黑色冶金、有色冶金(铜、锌、黄铜、铝、镍)、机床、化工等行业,目前经济已经向第三产业转移.从历史的角度,这两个区域的水资源都受到重工业活动的严重影响.随着工业的发展和人口的增长,人类对流域水资源的需求量增大,其水质状况对人类的生产、生活有着重要的影响.因此,本研究通过对辽河流域水体中溶解有机质荧光特性的分析,揭示各研究断面水中溶解有机质的荧光组分类型和性质的差异,并将荧光特性的定量化指标与河流的自然特性相结合,对溶解有机质来源进行解析;同时将其与英国中部河湖水体中溶解有机质荧光特性进行对比分析,以期借鉴英国中部河流水体治理经验,为辽河流域的水质改善提供参考.
2 材料与方法(Materials and methods) 2.1 采样点描述辽河流域主要包括两大水系:辽河水系和大辽河水系.大辽河水系由发源于抚顺的浑河、本溪的太子河汇合而成,于营口入海,而蒲河和海城河是浑河和太子河的重要支流.另外,辽河流域污染源主要集中在浑河和太子河的大辽河水系,因此,本研究根据辽河水系和流域污染源的分布情况,2013年5月至6月枯水期,分别采集了浑河中下游、太子河下游(浑河与太子河汇合之前)、蒲河下游(入浑河之前)以及海城河中游(海城市段)的水样,这些水体基本反映了辽河流域受典型行业污染的水质特性.采样点分布见图 1a.
水样采集于玻璃瓶中,使用前先用表面活性剂浸泡48 h,依次用自来水、超纯水洗净,晾干待用.取样时,先用采集水样冲洗3次,装满,不留气泡,放入装有冰块的保温箱避光低温保存,立即运回实验室,用0.7 μm的GF/F Whatman 玻璃纤维滤膜(马弗炉中于500 ℃灼烧4 h)进行过滤,滤液保存至PET瓶中,并于-20 ℃冰箱冷冻保存,1周内完成测定.
River Trent是英国最重要河流之一,位于英国中部,River Tame是River Trent的重要支流,同时是英国西米德兰郡的最主要河流,也是典型的城市河流;River Cole是River Tame的支流,流经农村区域和伯明翰城市市区后,与River Blythe汇合,不久便与River Tame交汇;River Tern是一个典型的市郊河流,位于伯明翰市区的西北部;Vale lake是人工湖,位于伯明翰市区的西南部.2010年2月至5月,分别采集了Vale lake、River Tame、River Tern和River Cole的水样,为了使采样点具有代表性,本文所选的采样点是英国环境署的检测断面.采样点分布见图 1b.采集各断面表层水样于预先处理过的棕色玻璃瓶中,冰块保护下立刻运回实验室,过0.7 μm的玻璃微孔膜(Whatman,使用前在500 ℃马氟炉中灼烧5 h)后进行相关测试(Liu et al., 2013).
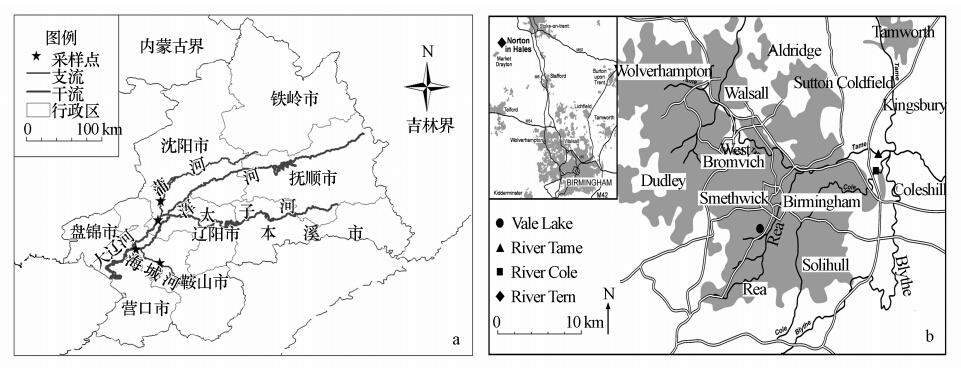 |
| 图 1 辽河流域和英国中部河湖的采样点分布 Fig. 1 Sampling sites of Liaohe Basin and Midl and Watershed of UK |
辽河水样经解冻并放置到室温后进行荧光光谱测量和分析,分析仪器用日立(Hitachi)F-7000荧光光谱分析仪,配以1 cm石英比色皿,以Mill-Q 水为空白,进行荧光扫描,150 W氙灯为激发光源,PMT电压为700 V,激发波长扫描范围为200~450 nm,发射波长扫描范围为250~550 nm,激发波长和发射波长增量均设为5 nm,狭缝宽度为10 nm,扫描速度为1200 nm · min-1.
英国河湖水样的三维荧光光谱测定是在美国的Cary Eclipse荧光光谱仪上进行,激发和发射波长的狭缝宽度均为5 nm,扫描波长范围为250~400 nm(激发波长)和300~500 nm(发射波长),扫描速度设为1200 nm · min-1,扫描光谱进行仪器自动校正.水样在装入1 cm石英荧光样品池,测定过程保持温度恒定(Liu et al., 2013; 2007).
为了保证各水样荧光光谱特性的可比性,所得到的荧光光谱均是经过扣除超纯水空白后的矫正结果,以减少仪器条件和拉曼散射对荧光光谱的影响.
3 结果与讨论(Results and discussion) 3.1 各河湖及水质特性浑河源于抚顺的清原县滚马岭,流经抚顺、沈阳等辽宁中部城市群,基本上成为沿岸城市废水排放的主要渠道.太子河流贯本溪境内,流经辽阳等市县,除了人类活动的影响外,主要受纳排放的工业废水,太子河与浑河在海城三岔河湿地自然保护区附近交汇形成大辽河.蒲河是浑河右岸主要支流,发源于铁岭县横道河子乡想儿山,从东北流向西南,它受到工业和农业活动的共同影响,在浑河干流北道沟大桥下游汇入浑河.海城河是太子河的支流,主要接纳印染行业的排放废水,在太子河干流小姐庙附近流入太子河(付保荣等,2011;马溪平等,2011).
Vale Lake是人工湖,主要受到伯明翰市区人类生活的影响;River Cole位于英格兰中部,全长大约40 km,起源于伯明翰西南部高原,流向东北部,流经农村区域和城市市区后,与River Blythe汇合,本研究采集了在汇合点前River Cole的水样,River Blythe不久便与River Tame交汇;River Tame是英格兰西米德兰郡的主要河流,位于伯明翰北部,它是英国重要河流River Trent的主要支流,起源于西米德兰郡的东北部,全长共93 km,是一个典型的城市河流,历史上,它是英国最脏的河流之一,主要受钢铁冶炼、煤矿开采等工业活动的严重污染;River Tern是一个典型的乡村集水区,没有受到明显的人类生活影响,并且沿岸有众多的天然湿地,是重要的补充地下水的河流(Liu et al., 2007).
表 1列出了各采样点水质的基本特性.由表 1可见,辽河水体中溶解氧饱和度普遍较低(低于18.6%),除了蒲河下游断面,TOC含量均低于3.4 mg · L-1.通常,溶解氧含量越低,表明有机污染程度越严重.尽管辽河各采样断面的TOC含量较低,但有相当一部分可能来自于有机污染物(后续的荧光光谱特性将说明这一点),这与沿河的污染源分布和排放相一致,辽河各采样断面较低的溶解氧含量(小于23%)也证明了这一点.在英国河湖各采样断面中,Vale Lake中的溶解氧含量最低(51.5%),这与它的地理位置(位于市区)是分不开的,由于人类和动物的活动,很容易受到固体废弃物的污染以及其它人为因素的影响.
| 表1 各采样点水质特性 Table 1 Chemical parameters of the freshwaters from each sampling site |
荧光光谱特性是表征天然水体中DOM以及评估其来源的重要参数,三维荧光光谱(EEM)可以用于检测DOM的荧光光谱组成.图 2所示为不同采样点水体中DOM的三维荧光光谱图,不同来源的DOM,三维荧光光谱存在一定差异,辽河各采样点水样的EEM均显示4个荧光特征峰,即:两个类蛋白峰Peak A(色氨酸,λex/λem = 220~240/325~360 nm)和Peak B(酪氨酸,λex/λem = 270~300/325~360 nm)、一个可见光区的类腐殖质Peak C(λex/λem = 290~350/390~460 nm)和一个紫外光区的类腐殖质Peak D(λex/λem =230~270/385~460 nm).一般认为,Peak C和Peak D反映的是外源输入的腐殖酸和富里酸形成的荧光峰值,而Peak A和Peak B则反映的是生物降解来源形成的荧光峰值(Coble,1996).在英国河湖各监测断面,除River Tame水体明显显示上述4个荧光特征峰之外,River Cole和Vale Lake水体的DOM清晰显示了3个特征峰(即Peak A、Peak C和Peak D),而River Tern只表现类腐殖酸和类富里酸的荧光特性.
另外,由于类蛋白物质和类腐殖酸或类富里酸物质的相互干扰,使得各荧光组分出峰位置发生不同程度的位移,其荧光峰的位置和强度见表 2.由图 2和表 2可知,本文所研究的河湖水体与众多的天然水体一样,DOM的荧光基团主要为类蛋白和类腐殖质两大类,类蛋白荧光主要是由微生物和浮游植物的作用所产生,包括外源输入的生活污水和工业废水等携带的微生物和水体中自身的微生物的生命过程;类腐殖质荧光由外源输入的沿岸土壤溶解到水中的腐殖质以及内源中浮游动植物释放的有机物经由细菌进一步降解后产生(Coble,1996; Murphy et al., 2008; Nelson et al., 2004).在辽河各研究断面的水体中,类蛋白物质(Peak A和Peak B)的荧光强度顺序为太子河下游 > 蒲河下游 > 浑河中游 > 海城河中游,太子河下游较高的类蛋白物质与沿途接纳本溪、辽阳和鞍山3个城市大量的工业及生活污水有着密切关系.在类蛋白荧光组分中,英国河湖中几乎没有发现类酪氨酸蛋白物质,即表现在EEM的荧光图谱中没有明显的Peak B出现,即使在River Tame的水体中存在酪氨酸类组分,其荧光强度也低于辽河各研究水体,这种差异主要由于水环境条件及污染程度不同导致水体中蛋白质的组成和降解情况不同;与其它水体相比,River Cole河水表现了极强的荧光特性,导致各组分荧光强度较高,这与它的起源、流经路线以及历史和地质条件有着密切关系.
| 表2 不同来源DOM的三维荧光光谱峰 Table.2 Fluorescence peak position and intensity of each component in DOM from all sampling sites |
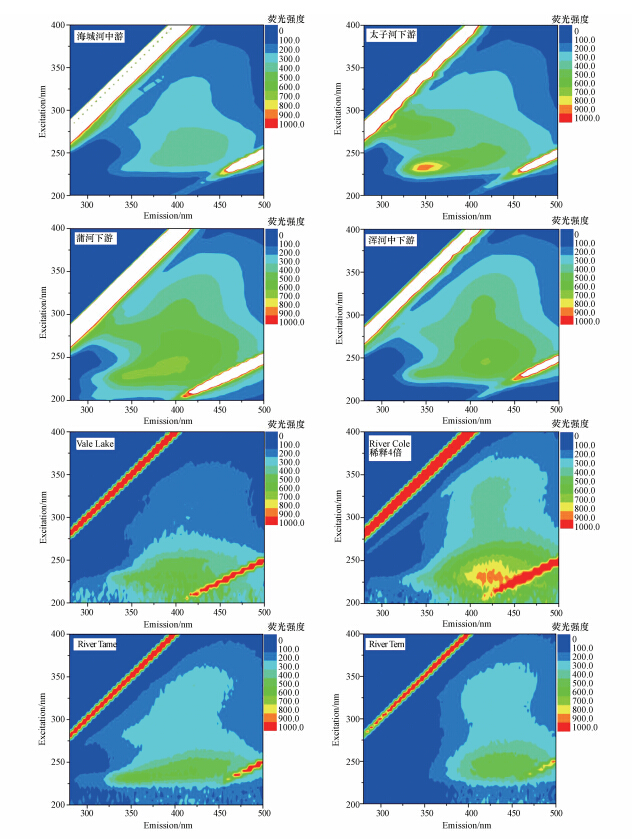 |
| 图 2 各采样断面的三维荧光图谱(荧光强度单位:a.u.) Fig. 2 Fluorescence EEMs of the freshwater from each sampling site(unit of fluorescence intensity: a.u.) |
荧光指数(FI)、生物源指数(也有称为自身生产力指标,BIX)、腐殖化指数(HIX)和类蛋白(Peak A)与类腐殖质(Peak C)荧光峰强度比值(RA/C)是定量描述和区分DOM荧光特性的常用指标.不同河湖水样的荧光定量指标见表 3.
| 表3 不同河湖的荧光定量指标 Table.3 Quantitative parameters of fluorescence characteristics for each freshwater sample |
荧光指数是在370 nm激发波处,450 nm与500 nm发射波长下的荧光强度比值,可用来表征溶解有机质中腐殖质的来源,大于1.9说明主要来源于微生物代谢等过程,小于1.4说明陆源占主要贡献(McKnight et al., 2001).如表 3所示,各河流水体的荧光指数范围为1.8~1.3,表明这些水体中DOM是混合来源,即细菌和藻类的胞外释放的内源以及陆生植物和土壤有机质的外源输入的综合影响,其中,辽河流域各断面的荧光指数没有很大差别,均接近1.8,表明内源作用大于陆源,而英国河流水体均小于1.6,River Tern的荧光指数甚至低至1.3,表明以陆源影响为主.
生物源指数是310 nm激发波长下380发射波长处荧光强度与420~435 nm区间最大荧光强度的比值,这个参数反映了新产生的DOM在整体DOM中所占的比例,生物源指数越高,说明DOM降解程度增加、内源碳产物越容易生成(Parlanti et al., 2000; Huguet et al., 2009).由表 3可知,在所有调查的河流中,生物源指数范围是0.6~0.99,其中,辽河流域中太子河下游断面的生物源指数最高(0.99),浑河下游断面最低(0.73).将Huguet等提出的BIX溯源方法与本文结果相结合(Huguet et al., 2009),得出太子河下游、蒲河下游、海城河中游具有较强的新近自生源特征,而浑河下游显示出中度的新近自生源特征,这种特征与水体中类蛋白物质的荧光强度有着密切的内在关系.与之相比较,英国中部河湖中River Tern和River Cole水体(BIX: 0.6~0.7)具有较少的新近自生源组分,Vale Lake水体(BIX: 0.7~0.8)显示出中度的新近自生源特征,而典型城市河流River Tame(BIX > 0.8)具有较强的新近自生源特征.
腐殖化指数是254 nm波长激发光下435~480 nm间最高荧光值除以300~345 nm间最高荧光强度与435~480 nm间最高荧光强度之和(Ohno,2002).如表 3所示,辽河流域各河流水体腐殖化指数的顺序为浑河中游 > 海城河中游 > 蒲河下游 > 太子河下游,腐殖化指数越高则DOM腐殖化程度越高,由此可见太子河下游断面DOM表现出相对较强的生物或水生细菌来源,这与生物源指数的结果是一致的.英国中部河湖水体腐殖化指数的顺序为:River Tern > River Cole > Vale Lake > River Tame,表明River Tern表现出较高的腐殖质特性,这与其本身的地质和环境条件有着密切关系.
类蛋白(Peak A)与类腐殖质(Peak C)荧光峰强度比值可以作为判断受污染河流水体中DOM来源的指标(Baker,2002b).本研究中的各河流由于受污染程度的差异,其类蛋白与类腐殖质荧光峰强度比值分布范围相对较宽,在0~3.27之间,辽河流域的各断面水体类蛋白与类腐殖质平均比值为1.75.通常,受污染河流DOM的三维荧光光谱图中类蛋白荧光强度较高,如:太子河的类蛋白与类腐殖质的比值高达3.27,表明该水体受外源污染严重.英国各河湖水体的平均值为1.25,表明水体受污染程度较低.未受污染的水体中类腐殖质荧光强度较高,有时甚至只有类腐殖质荧光(如River Tern).
3.4 DOM及污染来源分析通常,天然河流中类蛋白质荧光组分含量较低,而在受到污染(如工业废水和生活污水)的河流中类蛋白荧光组分的比例会显著增高(Baker,2002a; 2002b).太子河、蒲河、浑河和海城河受到沿岸城镇工业废水和生活污水的点源污染较重,因此,表现出较强的类蛋白荧光特性.太子河流经本溪、辽阳、鞍山等市县,这3个市是辽宁省工业较发达地区,以钢铁和化工等行业为主,人类生活和工业活动对水质的影响较为显著,因此太子河下游较高的类蛋白物质应该与沿途接纳本溪、辽阳和鞍山3个城市大量的工业及生活污水有着密切关系.蒲河是受城市扩展区和乡镇排污影响严重的天然河流,每年接纳的污水主要来自于蒲河新城和于洪区中上游段,尤其是蒲河新城东部的工业区、中部的虎石台镇和西部大学城区的快速建设和排污量的增长,导致了蒲河全河段的水质恶化.浑河主要接纳抚顺和沈阳市城区生活污水和工业废水,同时支流河道两侧固体生活垃圾堆积严重,遇有雨水冲刷最后都汇入浑河,这些都会加剧浑河水质的污染.海城河是辽宁省印染行业重点排污河段,河两岸分布了几十家印染企业,同时也接纳海城市的生活污水,与其他研究河流相比,海城河水样表现为类蛋白物质的荧光强度相对较弱.各河道除了受到外来点源污染之外,分布在河道两侧的养殖业的废弃物、沿岸生活垃圾和作物秸秆等流入河道,使得河水荧光光谱特性发生变化,同时加剧河水污染.研究表明(何小松等,2010),垃圾渗滤液中微生物活跃,其水溶性有机物中含有大量的微生物降解产物及不同腐殖化程度的腐殖质类物质,由于堆放的方式和时间不同,使得荧光光谱峰的数目、类型和峰的位置发生变化.由辽河流域各水体荧光光谱分析可知,各河流中的DOM,一方面,来自于浮游植物释放后经细菌进一步分解产生的荧光腐殖质,另一方面,由于污染物质的大量输入会加剧水体中微生物的生命活动,因而造成了严重的内源污染,导致类蛋白物质的含量增加.
River Tern是未受到明显污染的河流,因而DOM仅表现出类腐殖质荧光特性,由于河流远离城市市区,水体中的DOM主要来源于农村地区土壤、天然湿地和腐烂植物中的腐殖质,进而随雨水进入河流. River Tame是典型的城市河流,River Cole综合了城市与农村河流的特点,尽管历史上River Tame受到工业活动的严重影响,曾经是钢铁冶炼、煤矿开采等废水的受纳河流,但经过后来产业结构的调整、污染企业的关闭及河道的整治,河流水质得到明显改善,目前这两条河流主要接纳来自英国第二大城市伯明翰市区处理后排放的生活污水,水体中的DOM主要受到类腐殖质的控制,同时,除了水体中本身的浮游动植物之外,排入河流的生活污水中也携带有微生物,其代谢活动产生的类蛋白物质也是不容忽略的.因此,DOM中类腐殖质不仅来源于微生物等代谢过程,同时陆源的输入也是主要来源.由于Vale Lake是市区的人工湖,其DOM主要来自于水体本身存在的大量微生物以及浮游植物的活动,同时也与人类和动物活动产生的固体废弃物的污染有关,此外,土壤经雨水的冲刷流入湖体也会使得DOM含量增加,因此,DOM的来源既有外源的输入,也有内源贡献.
4 结论(Conclusions)1)辽河流域和英国中部河湖水体中,DOM荧光组分的种类以及各组分的相对荧光强度都存在明显的差异,这种差异源自于河流自身的水文条件、水质特点以及人类活动带来的污染程度和污染物种类.辽河流域各研究断面水中DOM的来源相对比较复杂,除了自然过程产生的有机质外,人类活动产生大量污染物质的输入,加剧了水体中微生物的生命活动,因而造成了严重的内源污染,导致DOM含量增加;英国各河湖断面其DOM主要来自于水体本身存在的大量微生物以及浮游植物的活动,土壤有机质经雨水的冲刷流入水体也是DOM的重要来源.
2)通过DOM荧光特性比较可知,辽河流域水体的污染程度相对较高,尤其是太子河,英国河湖污染程度较低.尽管历史上英国中部各河湖受污染程度严重,尤其是River Tame,曾被称为英国最脏的河流之一,但通过后来的污染企业的关停、河道的整治、废水排放及水资源的有效管理,使得各河流水质得到彻底改善.因此,为控制辽河流域水体中的DOM,借鉴英国河流的管理和治理经验,应以控制入河污水排放为主,即通过产业结构的调整和生产工艺的改进以降低和控制工业排放源、通过污水厂的提标改造和扩建以及有效行政管理制度的制定实现城市污水的达标排放、将控污截污与河道治理技术有机结合开展污染河道的综合整治和生态修复,从而实现辽河流域水质的全面改善.
| [1] | Al-Reasi H A, Wood C M, Smith D S. 2013. Characterization of freshwater natural dissolved organic matter(DOM): Mechanistic explanations for protective effects against metal toxicity and direct effects on organisms[J]. Environment International, 59: 201-207 |
| [2] | Baker A. 2002a. Fluorescence properties of some farm wastes: implications for water quality monitoring[J]. Water Research, 36(1): 189-195 |
| [3] | Baker A. 2002b. Fluorescence excitation-emission matrix characterization of river waters impacted by a tissue mill effluent[J]. Environmental Science and Technology, 36(7): 1377-1382 |
| [4] | Chen H, Meng W, Zheng B H, et al. 2013. Optical signatures of dissolved organic matter in the watershed of a globally large river (Yangtze River, China)[J]. Limnologica-Ecology and Management of Inland Waters, 43(6): 482-491 |
| [5] | Coble P G. 1996. Characterization of marine and terrestrial dissolved organic matter in seawater using excitation–emission matrix spectroscopy[J]. Marine Chemistry, 51(4): 325-346 |
| [6] | 付保荣, 苏杰, 吴丹, 等. 2011. 辽河流域水环境时空差异性评价[J]. 水资源保护, 27(6): 5-8 |
| [7] | 何小松, 席北斗, 魏自民, 等. 2010. 垃圾堆放渗滤液水溶性有机物的荧光特性[J]. 中国环境科学, 30(6): 752-757 |
| [8] | Hudson N, Baker A, Reynolds D. 2007. Fluorescence analysis of dissolved organic matter in natural, waste and polluted waters-a review[J]. River Research and Applications, 23(6): 631-649 |
| [9] | Huguet A, Vacherl L, Relexans S, et al. 2009. Properties of fluorescent dissolved organic matter in the Gironde Estuary[J]. Organic Geochemistry, 40(6): 706-719 |
| [10] | Leenheer J A, Croué J P. 2003. Characterizing aquatic dissolved organic matter[J]. Environmental Science and Technology, 37(1): 19-26 |
| [11] | Liu R X, Lead J R, Baker A. 2007. Fluorescence characterization of cross flow ultrafiltration derived freshwater colloidal and dissolved organic matter[J]. Chemosphere, 68(7): 1304-1311 |
| [12] | Liu R, Lead J R, Zhang H. 2013. Combining cross flow ultrafiltration and diffusion gradients in thin-films approaches to determine trace metal speciation in freshwaters[J]. Geochimica et Cosmochimica Acta, 109: 14-26 |
| [13] | 马溪平, 吕晓飞, 张利红, 等. 2011. 辽河流域水质现状评价及其污染源解析[J]. 水资源保护, 27(4): 1-4, 73 |
| [14] | Mayer L M, Schick L L, Loder Ⅲ T C. 1999. Dissolved protein fluorescence in two maine estuaries[J]. Marine Chemistry, 64(3): 171-179 |
| [15] | McKnight D M, Boyer E W, Westerhoff P K, et al. 2001. Spectrofluorometric characterization of dissolved organic matter for indication of precursor organic material and aromaticity[J]. Limnology and Oceanography, 46(1): 38-48 |
| [16] | Mostofa K M G, Yoshioka T, Konohira E, et al. 2005. Three-dimensional fluorescence as a tool for investigating the dynamics of dissolved organic matter in the Lake Biwa watershed[J]. Limnology, 6(2): 101-115 |
| [17] | Murphy K R, Stedmon C A, Waite T D, et al. 2008. Distinguishing between terrestrial and autochthonous organic matter sources in marine environments using fluorescence spectroscopy[J]. Marine Chemistry, 108(1/2): 40-58 |
| [18] | Nelson N B, Carlson C A, Steinberg D K. 2004. Production of chromophoric dissolved organic matter by Sargasso Sea microbes[J]. Marine Chemistry, 89(1/4): 273-287 |
| [19] | Ohno T. 2002. Fluorescence inner-filtering correction for determining the humification index of dissolved organic matter[J]. Environmental Science and Technology, 38(4): 742-746 |
| [20] | Pagano T, Ross A D, Chiarelli J, et al. 2012. Multidimensional fluorescence studies of the phenolic content of dissolved organic carbon in humic substances[J]. Journal of Environmental Monitoring, 14(3): 937-943 |
| [21] | Parlanti E, Worz K, Geoffroy L, et al. 2000. Dissolved organic matter fluorescence spectroscopy as a tool to estimate biological activity in a coastal zone submitted to anthropogenic inputs[J]. Organic Geochemistry, 31(12): 1765-1781 |
| [22] | Ravichandran M. 2004. Interactions between mercury and dissolved organic matter a review[J]. Chemosphere, 55(3): 319-331 |
| [23] | Stutter M I, Richards S, Dawson J J C. 2013. Biodegradability of natural dissolved organic matter collected from a UK moorland stream[J]. Water Research, 47(3): 1169-1180 |
 2014, Vol. 34
2014, Vol. 34


