2. 中国科学院城市环境研究所, 厦门 361021
2. Institute of Urban Environment, Chinese Academy of Sciences, Xiamen 361021
近年来,环境污染日益严重,其中有毒、有害污染物质的残留问题尤为突出.如农产品中水果(刘长武等,2003)和茶叶(Cajka et al., 2012)表面残留的农药,水产养殖中非法添加的孔雀石绿(Afkhami et al., 2010)和结晶紫(Long et al., 2009)等,都严重威胁人类的健康.因此,迫切需要发展一种简单和低成本的污染物快速检测方法.
表面增强拉曼散射(SERS)不仅具有超高的灵敏度和选择性,同时具备水干扰性小和无损分析等优点,在痕量物质检测方面展现了巨大的应用前景(Pieczonka et al., 2008).SERS的高灵敏度主要取决于SERS基底的增强效应(Chen et al., 2009),因此制备重现性好、增强因子高的SERS基底是当前的研究热点之一.然而,由于目前大部分SERS都是硬基底且不透光,因此一般需要应用溶剂从被检测物体表面萃取污染物质,然后滴加到SERS基底上进行检测,整个过程复杂且耗时.因此,发展一种可以直接在物体表面原位检测污染物的SERS方法迫在眉睫,而实现原位快速SERS检测的关键是柔性、透光SERS基底的制备.
本文以乙醇为诱导因子,诱导水溶液中的金纳米粒子上浮到水和聚甲基丙烯酸甲酯甲苯溶液界面,并自组装成有序的金纳米层结构.待甲苯挥发后,甲苯溶液中具有柔韧性和透光性的PMMA把已组装有序的纳米粒子固定住,形成具有柔韧性和透光性的AuNPs/PMMA薄膜表面增强拉曼基底.因该表面增强拉曼基底具有良好的柔韧性和透光性,可将该表面增强拉曼基底直接放在各种形状物体表面,快速、原位检测物体表面的污染物,弥补了传统表面增强拉曼硬基底缺乏柔性和透光性的不足.由于金纳米粒子组装有序,该拉曼基底具有很好的重现性和高拉曼活性.
本文选取孔雀石绿作为模拟环境污染物.孔雀石绿是一种广泛应用于水产养殖业中的杀菌剂、驱虫剂,其残留对人体具有“致癌、致畸和致突变”的危害(Manjanatha et al., 2004; Alderman,2002; Rao,1995),已经被中国等许多国家禁止使用.但是,因其价格低廉且药效好,在水产养殖中仍被非法使用(An et al., 2010).目前,虽然孔雀石绿的检测方法很多,如高效液相色谱法(Zheng et al., 2012)、液相色谱-串联质谱法(Lopez-Gutierrez et al., 2013)等,但是这些检测手段耗时耗力、样品制备复杂、检测周期长、成本昂贵,给环保和食品监管等部门带来了许多不便.
本文成功制备了柔韧性和透光性的AuNPs/PMMA薄膜,并以此为SERS基底,对鱼表面残留的孔雀石绿进行了原位检测,建立了利用SERS实现原位、快速而准确地定量检测环境中污染物的方法.
2 实验部分(Experimental section) 2.1 仪器与试剂仪器:TU-1810紫外可见分光光度计(北京普析通用仪器有限责任公司,中国);LabRAM Aramis激光共聚焦拉曼光谱仪(HORIBA Jobin Yvon,法国);S-4800场发射扫描电子显微镜(SEM,HITACHI,日本);LSP04-1A型注射泵(保定兰格恒流泵有限公司,中国).
试剂:氯金酸(HAuCl4·4H2O)、柠檬酸三钠(C6H5Na3O7·2H2O,≥99.0%)、无水乙醇(C2H5OH,≥99.7%)、甲苯(C7H8,≥99.5%)、孔雀石绿(C23H25CIN2,BC).以上药品均为分析纯,购于国药集团化学试剂有限公司. 甲基对硫磷标准溶液(1 mg · mL-1)购于阿拉丁试剂有限公司.异硫氰基孔雀石绿(MGITC)购买于Invitrogen Corporation,Carlsbad,CA.聚甲基丙烯酸甲酯(分子量1.2×105)购买于Sigma-Aldrich公司.实验用鱼购于当地超市,实验用水均为超纯水,电阻率不小于18.2 MΩ · cm-1.所有玻璃器皿使用前均用王水浸泡,超纯水清洗,60 ℃烘干.
2.2 金纳米粒子合成金纳米粒子(AuNPs)制备参考Frens法(Frens,1973)并加以改进,通过改变氯金酸和柠檬酸三钠的加入量,合成不同粒径的金纳米微粒.方法简述如下:首先,向99 mL沸腾的质量体积分数为1% 的HAuCl4·4H2O水溶液中迅速加入质量体积分数为1%的柠檬酸三钠水溶液1 mL,保持3 min,溶液颜色由无色变为酒红色;接着,依次添加柠檬酸三钠和氯金酸各1 mL,重复数次,每次添加时间间隔30秒;最后,停止加热和搅拌,冷却至室温,得到纳米金溶胶,4 ℃保存备用.
2.3 AuNPs/PMMA薄膜的制备首先,移取纳米金溶液15 mL于烧杯中;接着,将含有20 mg PMMA的甲苯溶液加入装有纳米金溶液的烧杯中,混合溶液分为上下两层;然后,向下层纳米金溶液中缓慢注入无水乙醇.随着乙醇的加入,纳米金粒子逐渐上浮到界面,并自组装成纳米金层;最后,待甲苯彻底挥发后,取出AuNPs/PMMA薄膜,于60 ℃烘干备用.
2.4 拉曼增强因子样品制备在AuNPs/PMMA薄膜的增强因子计算实验中,我们选用MGITC作为染料分子.主要基于以下两个原因:第一,因为MGITC具有异硫氰基官能团,能与AuNPs形成牢固的化学键(Qian et al., 2008),在经过数次乙醇清洗后,能确保在AuNPs/PMMA薄膜上只形成单分子层的MGITC.第二,因为MGITC与水中污染物孔雀石绿分子相似,对检测孔雀石绿更有说服力.具体实验步骤为:将AuNPs/PMMA薄膜在10 μmol · L-1的MGITC溶液中浸泡20 min,然后用乙醇清洗数次,去除游离的MGITC分子,使AuNPs/PMMA薄膜上只吸附上单分子层的MGITC,室温下避光干燥.
2.5 原位检测鱼表面残留的孔雀石绿首先,以水为溶剂,配制1 mmol · L-1、100 μmol · L-1、 10 μmol · L-1、1 μmol · L-1和0.1 μmol · L-1一系列浓度的孔雀石绿溶液;接着,将鱼分别浸泡于不同浓度的孔雀石绿溶液中 3 min;然后,把AuNPs/PMMA薄膜暴露纳米金的一面直接贴于浸泡过孔雀石绿的鱼表面,并进行拉曼光谱扫描,得到鱼表面残留不同浓度的孔雀石绿的SERS图谱.
2.6 原位检测苹果表面的农药甲基对硫磷首先,用喷壶把甲基对硫磷标准溶液喷洒在洁净的苹果表面;接着,把AuNPs/PMMA薄膜暴露纳米金的一面直接贴于喷洒过甲基对硫磷的苹果表面,并进行拉曼光谱扫描,得到苹果表面残留甲基对硫磷的SERS图谱.
3 结果与讨论(Results and discussion) 3.1 金纳米粒子图 1a为A、B、C和D 4组纳米金溶液的紫外可见吸收光谱.结果显示,随着氯金酸和柠檬酸三钠重复添加次数的增加,其最大吸收波长逐渐红移,纳米金溶液颜色也由酒红色逐渐变为砖黄色,说明纳米金粒子的粒径逐渐变大.因SERS信号强度与纳米金粒子的粒径和均一性密切相关(Prashant et al., 2006),本文选择粒径为60 nm 的B组金纳米粒子作为拉曼活性粒子.从图 1b的SEM照片,可以看出B组金纳米粒子的粒径和形貌较均一,适于作为拉曼活性粒子.
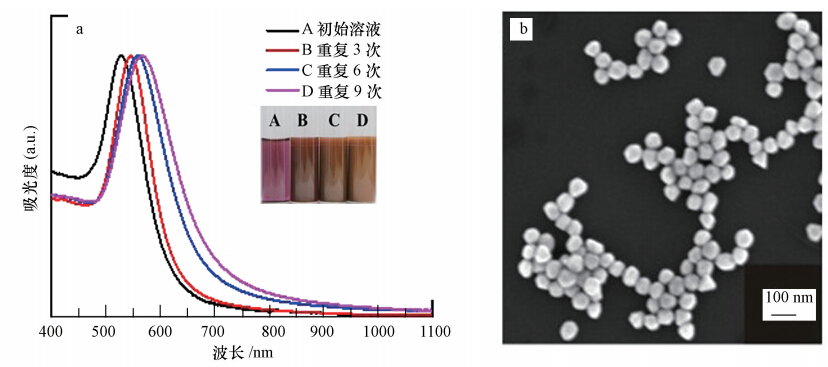 |
| 图 1 a)纳米金粒子的紫外吸收光谱及其溶液颜色变化图;b)B组金纳米粒子SEM照片 Fig. 1 a)UV-Vis absorption spectra of AuNPs solutions; inset is the corresponding optical images of the solutions; b)SEM image of AuNPs in group B from Fig. 1a) |
图 2a为AuNPs/PMMA薄膜的紫外吸收光谱图,图中显示AuNPs/PMMA薄膜有两个明显的吸收峰.位于550 nm附近的峰较弱,该峰与纳米金溶液的吸收峰(图 1 B组)位置相近,而位于900 nm附近的峰较强,该峰是由于PMMA模板上相邻纳米金粒子间的等离子共振耦合作用所产生(Jiang et al., 2003),这暗示PMMA模板上的纳米金粒子是密集的组装结构. AuNPs/PMMA薄膜的SEM照片(图 2b)进一步证实了我们的猜想,从图中可以看到PMMA模板上的金纳米粒子紧密地排列成有序的组装体.该纳米金组装体能含有无数的拉曼热点,这些热点对于吸附在其附近的分子具有很强的拉曼增强效果.图 2a的内插图为AuNPs/PMMA薄膜弯曲时的照片,说明AuNPs/PMMA薄膜具有良好的柔韧性.因此,可以贴附在不同形貌的物体表面,克服了硬性SERS基底无法原位检测形状不规则样品的难题.此外,由于PMMA具有很好的透光性,因此激光可以透光PMMA层,到达纳米金层,激发其等离子共振,使纳米金层产生巨大的电磁场增强,从而放大纳米金层附近分子的拉曼信号.
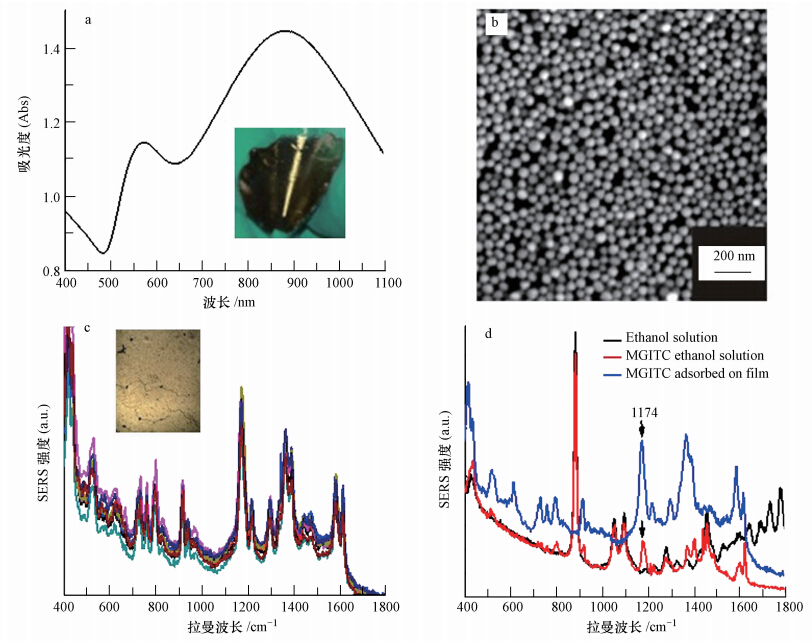 |
| 图 2 a)AuNPs/PMMA薄膜的紫外吸收光谱(插入图为AuNPs/PMMA薄膜的光学照片);b)AuNPs/PMMA薄膜的SEM照片;c)MGTIC在AuNPs/PMMA薄膜8个随机位置的拉曼光谱图(插入图为拉曼仪器下获得的AuNPs/PMMA薄膜光学图);d)乙醇,1 mmol-1 MGITC乙醇溶液和MGITC在AuNPs/PMMA薄膜上的拉曼光谱图(乙醇和1 mmol · L-1 MGITC乙醇溶液的拉曼测试条件为:激光波长785 nm,激光能量20 mW,信号采集时间20 s. MGITC在AuNPs/PMMA薄膜的拉曼测试条件为:激光波长785 nm,激光能量0.2 mW,信号采集时间5 s) Fig. 2 a)UV-Vis adsorption spectra of AuNPs/PMMA film(inset is the optical image of AuNPs/PMMA film); b)SEM image of AuNPs/PMMA film; c)Raman spectra of MGITC on AuNPs/PMMA film in eight r and om spots(inset is the corresponding Raman image of AuNPs/PMMA film); d)Raman spectra of ethanol solution,1 mmol · L-1 MGITC in ethanol solution, and MGITC on AuNPs/PMMA film(The Raman spectra of ethanol and 1 mmol · L-1 MGITC ethanol solution were recorded with 20 mW of 785 nm excitation and an acquisition time of 20 s,while the SERS spectra of MGITC on AuNPs/PMMA film was recorded with 0.2 mW of 785 nm excitation and an acquisition time of 5 s) |
SERS信号的可重现性是SERS原位检测的一个至关重要因素,其取决于SERS基底的均一性.我们以10 μmol · L-1的MGITC作为信号分子,表征AuNPs/PMMA薄膜的均一性.实验结果表明,在AuNPs/PMMA薄膜随机选取8个点的MGITC拉曼信号强度基本一致(图 2c),说明AuNPs/PMMA薄膜具有较好的均一性,其作为SERS基底有良好的可重现性.另外,从拉曼仪器下获得的AuNPs/PMMA薄膜光学图中,也可以看出AuNPs/PMMA薄膜是一张完整而且均一的膜(图 2c中的插入图).
图 2d给出了乙醇、1 mmol · L-1 MGITC乙醇溶液和吸附在AuNPs/PMMA薄膜上MGITC的SERS图谱.通过图谱比较,我们选择MGITC在1174 cm-1处的拉曼峰强度,作为计算AuNPs/PMMA薄膜增强因子EF的依据,计算公式如下(Souza et al., 2006):
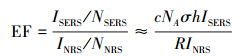
式中,ISERS为基底表面吸附物质的SERS强度,INRS为溶液中该物质的常规拉曼光谱强度,NSERS为基底表面聚焦光斑区域内的分子数,NNRS为溶液中采样区内的分子数,c为溶液中探针分子的浓度,NA是阿弗加德罗常数,σ为单个吸附分子所占的表面积,h为激光腰束,R为SERS基底的表面粗糙因子.按照上述方法,计算8组数据,得出AuNPs/PMMA薄膜的增强因子高达(2.4±0.3)×107,说明AuNPs/PMMA薄膜具有很强的拉曼增强效果.
3.3 鱼表面残留孔雀石绿的原位检测为了验证AuNPs/PMMA薄膜作为SERS基底应用于实际环境污染物的原位检测的可行性,我们以鱼表面残留的孔雀石绿作为模拟污染物研究对象.由于PMMA具有很好的柔韧性和透光性,将AuNPs/PMMA薄膜暴露纳米金的一面紧贴在浸泡过不同浓度孔雀石绿的鱼表面,金纳米粒子将直接与鱼表面残留的孔雀石绿接触.当激光照射在AuNPs/PMMA薄膜上时,激光会透光PMMA层,到达组装的纳米金层,从而激发纳米金层等离子共振,使纳米金层产生巨大的电磁场增强,显著地放大了鱼表面残留的孔雀石绿拉曼信号.图 3a拉曼光谱显示,即使鱼泡在孔雀石绿浓度只有0.1 μmol · L-1的水溶液里,以AuNPs/PMMA薄膜为SERS基底也能原位检测到鱼表面残留的孔雀石绿在797 cm-1、1174 cm-1、1366 cm-1、1392 cm-1和1616 cm-1处的拉曼特征峰(He et al., 2008).
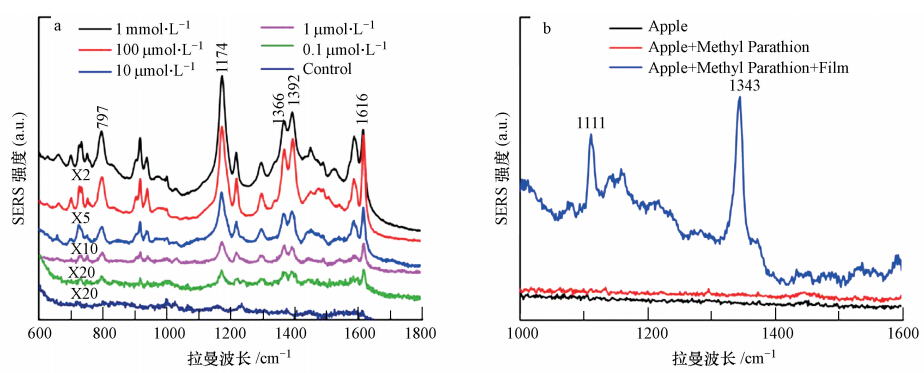 |
| 图 3 a) 浸泡过不同浓度孔雀石绿的鱼表面拉曼光谱(对照样品为没有AuNPs/PMMA薄膜时浸泡过1 mmol · L-1孔雀石绿鱼表面的拉曼光谱);b)苹果表面拉曼光谱(拉曼测试条件:激光波长785 nm,激光能量0.2 mW,信号采集时间20 s) Fig. 3 a)Raman spectra of fish surface soaked under different concentrations of malachite green(the control spectra was obtained from fish surface immersed in 1 mmol · L-1 malachite green with no attachment of AuNPs/PMMA film); b)Raman spectra of apple surface(Laser wavelength is 785 nm,laser energy is 0.2 mW,acquisition time is 20 s |
此外,本文也用AuNPs/PMMA薄膜尝试了原位检测苹果表面残留的农药甲基对硫磷. 初步结果显示在没有AuNPs/PMMA薄膜的情况下,即使苹果表面喷有甲基对硫磷,也检测不到任何拉曼信号.相反,当把AuNPs/PMMA薄膜贴在喷洒过甲基对硫磷的苹果表面后,却可以清晰地观察到甲基对硫磷的拉曼特征峰(1111 cm-1和1343 cm-1)(Li et al., 2010),说明AuNPs/PMMA基底显著放大了苹果表面甲基对硫磷的拉曼信号.
4 结论(Conclusions)本文成功制备了具有柔韧性和透光性的AuNPs/PMMA表面增强拉曼基底,该SERS基底具有良好的重现性和高的拉曼活性,其增强因子高达(2.4±0.3)×107;利用该柔韧和透光的SERS基底,成功实现鱼表面残留孔雀石绿的原位检测,检测下限达到0.1 μmol · L-1.该检测方法简便、快捷、成本低,为SERS检测技术的应用提供了新的思路,开阔了SERS的应用前景.
| [1] | Afkhami A, Moosavi R, Madrakian T. 2010. Preconcentration and spectrophotometric determination of low concentrations of malachite green and leuco-malachite green in water samples by high performance solid phase extraction using maghemite nanoparticles [J]. Talanta, 82(2): 785-789 |
| [2] | Alderman D J. 2002. Trends in therapy and prophylaxis 1991—2001. The 10th International Conference of the European Association of Fish Pathologists. Dublin, Ireland. 117-125 |
| [3] | An L, Deng J, Zhou L, et al. 2010. Simultaneous spectrophotometric determination of trace amount of malachite green and crystal violet in water after cloud point extraction using partial least squares regression [J]. Journal of Hazardous Materials, 175(1/3): 883-888 |
| [4] | Cajka T, Sandy C, Bachanova V, et al. 2012. Streamlining sample preparation and gas chromatography-tandem mass spectrometry analysis of multiple pesticide residues in tea [J]. Analytica Chemica Acta, 743: 51-60 |
| [5] | Chen C, Hutchison J A, Clemente F, et al. 2009. Direct evidence of high spatial localization of hot spots in surface enhanced Raman scattering [J]. Angewandte Chemie International Edition, 48(52): 9932-9935 |
| [6] | Frens G. 1973. Controlled nucleation for the regulation of the particle size in monodisperse gold suspension [J]. Nature Physical Science, 241(105): 20-21 |
| [7] | He L L, Kim N J, Li H, et al. 2008. Use of a fractal-like gold nanostructure in surface-enhanced Raman spectroscopy for detection of selected food contaminants [J]. Journal of Agricultural and Food Chemistry, 56(21): 9843-9847 |
| [8] | Jiang J, Bosnick K, Maillard M, et al. 2003. Single molecule Raman spectroscopy at the junctions of large Ag nanocrystals [J]. Journal of Physical Chemistry B, 107(37): 9964-9972 |
| [9] | Li J F, Huang Y F, Ding Y, et al. 2010. Shell-isolated nanoparticle-enhanced Raman spectroscopy [J]. Nature, 464(7278): 392-395 |
| [10] | 刘长武, 刘凤枝, 翟广书, 等. 2003. 蔬菜水果中25 种有机氯农药残留快速检测方法[J]. 环境科学学报, 23(4): 499-502 |
| [11] | Long C Y, Mai Z B, Yang Y F, et al. 2009. Determination of multi-residue for malachite green, gentian violet and their metabolites in aquatic products by high-performance liquid chromatography coupled with molecularly imprinted solid-phase extraction [J]. Journal of Chromatography A, 1216 (12): 2275-2281 |
| [12] | Lopez-Gutierrez N, Romero-Gonzalez R, Plaza-Bolanos P, et al. 2013. Simultaneous and fast determination of malachite green, leucomalachite green, crystal violet, and brilliant green in seafood by ultrahigh performance liquid chromatography-tandem mass spectrometry [J]. Food Analytical Methods, 6(2): 406-414 |
| [13] | Manjanatha M G, Shelton S D, Bishop M, et al. 2004. Analysis of mutations and bone marrow micronuclei in Big Blue rats fed leucomalachite green [J]. Mutation Research, 547(1/2): 5-18 |
| [14] | Pieczonka N P W, Aroca R F. 2008. Single molecule analysis by surfaced-enhanced Raman scattering [J]. Chemical Society Reviews, 37(5): 946-954 |
| [15] | Prashant K J, Kyeong S L, Ivan H S, et al. 2006. Calculated absorption and scattering properties of gold nanoparticles of different size, shape, and composition: applications in biological imaging and biomedicine [J]. Journal of Physical Chemistry B, 110(14): 7238-7248 |
| [16] | Qian X M, Peng X H, Ansari D O, et al. 2008. In vivo tumor targeting and spectroscopic detection with surface-enhanced Raman nanoparticle tags [J]. Nature Biotechnology, 26(1): 83-90 |
| [17] | Rao K V K. 1995. Inhibition of DNA synthesis in primary rat hepatocyte cultures by malachite green: a new liver tumor promoter [J]. Toxicology Letters, 81(2/3): 107-113 |
| [18] | Souza G R, Levin C S, Hajitou A, et al. 2006. In vivo detection of gold-imidazole self-assembly complexes: NIR-SERS signal reporters [J]. Analytical Chemistry, 78(17): 6232-6237 |
| [19] | Zheng Z, Zhou K, Bu Y Q, et al. 2012. Determination of malachite green and crystal violet in environmental water using temperature-controlled ionic liquid dispersive liquid-liquid microextraction coupled with high performance liquid chromatography [J]. Analytical Methods, 4(2): 429-433 |
 2014, Vol. 34
2014, Vol. 34


