金属硫蛋白(Metallothionein,MT)是一类广泛存在于生物界、低分子量(6000~7000 Da)、富含半胱氨酸而无芳香族氨基酸和组氨酸、热稳定性良好、可被金属诱导、功能独特的非酶类蛋白质(Hamer,1986;Kagi et al., 1988).自从1957年哈佛大学的Margoshes和Vallee在研究马肾脏蓄积镉的过程中首次发现并分离出MT以来(Margoshes and Vallee, 1957),在真核微生物、高等植物、原核生物中陆续发现有MT的存在(Carpenè et al., 2007).研究表明,MT主要与重金属的解毒有关,重金属进入机体可特异性诱导MT的高水平表达,进而螯合一定的重金属形成重金属-MT复合物,或者夺取与其他功能蛋白结合的重金属离子来降低功能蛋白的损伤,减少重金属对组织的损害(Bremner,1987),这是生物体重要的解毒机制之一.由于水生生物体内的MT与水环境和体内组织中的重金属具有显著的相关性,因此,MT可作为水环境重金属暴露和毒性效应早期警报的主要生物标志物,为水环境污染程度提供客观和全面的指标(Amiard et al., 2006).目前,关于MT作为生物标志物的相关报道主要集中在鱼类、贻贝和牡蛎等软体动物中(Ma et al., 2008),而蟹类中、特别是与淡水蟹类相关的研究国内外鲜见报道.同时,由于定量检测方法的限制,MT作为生物标志物在环境监测方面的应用还未能进一步开发.目前,MT含量的测定方法主要有金属结合法、电化学法、色谱分析法等,因MT蛋白的特殊性,上述测定方法无一不受MT结合金属种类、MT同形体多态性等因素的影响而对结果产生偏差.而酶联免疫吸附测定(ELISA)以其灵敏性高、特异性好、操作简单、费用低廉且可准确、特异、高通量地实现MT的定量测定,正逐步应用于环境监测、医疗检验等方面(Nakajima et al., 2010; Yudkovski et al., 2008; Apostolova et al., 1998).而建立ELISA方法的关键是高效价、高特异性抗体的制备.
河南华溪蟹(Sinopotamon henanense)由海洋蟹多元转化而成,属于甲壳纲、十足目中一个特殊分支.作为生活于水体基底层的低等生物,溪蟹直接面对沉积在水体的金属离子,是一种较为理想的水环境监测指示生物,其组织中的MT含量作为一种监测水体重金属暴露的生物标志物,客观反应水体污染水平(Ma et al., 2008).因此,本研究在制备功能性重组河南华溪蟹MT的基础上,利用纯化的融合蛋白SUMO-MT免疫小鼠,获得抗华溪蟹MT抗血清,以期为深入研究MT的重金属解毒机制及进一步建立快速、敏感的ELISA 检测方法奠定基础.
2 材料与方法(Materials and methods) 2.1 材料重组工程菌PET-28a-SUMO-MT/BL21(DE3)由本实验室构建、保存,健康雌性BALB/c小鼠购自北京维通利华实验动物技术有限公司,BCA蛋白浓度测定试剂盒购自碧云天生物技术有限公司,羟自由基测定试剂盒购自南京建成生物工程研究所,PVDF 膜(0.22 μm)购自Bio-Rad公司,Quick Antibody-Mouse5W免疫佐剂购自北京康碧泉生物技术公司,HRP标记的羊抗鼠IgG购自GeneTex公司,AP标记的羊抗鼠IgG购自生工生物工程(上海)股份有限公司,邻苯二胺(OPD)和NBT/BCIP 显色剂购自Amresco公司,DAB染色试剂盒购自北京康为世纪生物科技有限公司,其余常规试剂均为国产分析纯.
2.2 方法 2.2.1 重组MT蛋白的制备及鉴定根据本实验室之前建立的方法,IPTG诱导重组工程菌PET-28a-SUMO-MT/ BL21(DE3)表达河南华溪蟹MT蛋白,经Ni 离子螯合柱分离纯化,制备重组华溪蟹MT(He et al., 2014).纯化获得的重组融合蛋白SUMO-MT经超滤浓缩交换至储存液(0.01 mol · L-1 Tris-HCl,0.2 mmol · L-1 PMSF,10 mmol · L-1 DTT,pH=7.8)后,SDS-PAGE分析其纯度.采用UNICO UV-2102 PC型紫外可见分光光度计在190~300 nm波长下进行紫外光谱扫描分析鉴定重组MT.
2.2.2 重组SUMO-MT与金属离子的结合能力分析根据Yang等(2007)建立的方法略加改良测定重组SUMO-MT的金属结合能力.利用BCA蛋白浓度测定试剂盒,以牛血清白蛋白BSA为标准,测定重组MT蛋白浓度;同时取1 mL重组蛋白纯化样品置于硝化瓶中,加入硝酸/高氯酸(1 ∶ 3)后置于电热板上消化完全,火焰原子吸收分光光度计(日本SH IMDZU AA26300)测定重组蛋白中的Zn含量.重组蛋白SUMO-MT分子量以26000 Da计,SUMO-MT分子与Zn原子的物质的量比RMT/Zn利用以下公式计算:
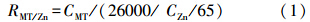
式中,RMT/Zn为SUMO-MT分子与Zn原子的物质的量比,CMT为重组SUMO-MT蛋白浓度(mg · mL-1),CZn为重组蛋白中Zn浓度(mg · mL-1).
2.2.3 重组SUMO-MT清除自由基能力分析羟基自由基(· OH)是体内最活泼的活性氧,而Fenton反应是最常见的产生羟基自由基的化学反应,H2O2的量和Fenton反应产生的· OH量成正比,当给予电子受体后,用griess试剂显色,形成红色物质,其呈色与· OH的量呈正比(Lindsey et al., 2000).分别在反应体系中加入不同浓度的重组SUMO-MT,检测其清除羟自由基能力.实验方法按照羟自由基测定试剂盒操作说明,在550 nm波长下,用双蒸水调零,测定各管吸光度.羟自由基清除率SRMT按照以下公式计算:
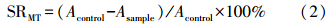
式中,SRMT为羟自由基清除率,Acontrol为空白对照的吸光度值,Asample为样品的吸光度值.
2.2.4 SUMO-MT抗血清的制备按照Quick Antibody-Mouse5W免疫佐剂说明书进行小鼠免疫.选择6~8周龄雌性BALB/c小鼠5只,取纯化后的重组SUMO-MT蛋白免疫小鼠.首次免疫每只小鼠取0.5 mL目的蛋白(50 μg · mL-1)与等体积Quick Antibody-Mouse5W水溶性免疫佐剂迅速混合后,于小鼠后腿小腿肌肉注射免疫,每只小鼠注射100 μL,免疫前尾部静脉取血作为阴性对照.3周后按照同样的方式加强免疫一针.5周后,小鼠摘除眼球取血,室温静置1 h后3000 r · min-1离心5 min.上清置于4 ℃冰箱内过夜,待血液凝固后,4 ℃、4000 r · min-1下离心10 min.取上清,加入0.02% NaN3,无菌分装于-80 ℃保存.
2.2.5 抗血清效价的测定根据Kim等(2011)建立的间接ELISA法测定SUMO-MT抗血清的效价.选取96孔酶标板,每孔用碳酸盐缓冲液(0.5 mol · L-1 Na2CO3/NaHCO3,pH=9.6)包被重组SUMO-MT(10 μg · mL-1,100 μL · 孔-1),留空白对照孔,4 ℃保存过夜;次日取出,弃去孔内液体,洗涤液PBST(0.01 mol · L-1 PBS,0.1% Tween,pH=7.4)洗3次,每次5 min;加入BSA封闭液(10 g · L-1)100 μL · 孔-1,37 ℃封闭2 h;洗涤3次后,加入pH =7.4、0.01 mol · L-1 PBS倍比稀释的免疫后小鼠血清及免疫前血清(稀释倍数为200~204800),100 μL · 孔-1,37 ℃作用1 h;洗涤3次,加入1 ∶ 5000 PBSTB(0.01 mol · L-1 PBS,1% BSA,0.1% Tween,pH=7.4)稀释的HRP标记的羊抗鼠IgG,37 ℃反应1 h;洗涤3次,加入底物邻苯二胺(OPD)溶液100 μL · 孔-1,暗处显色30 min,加入2 mol · L-1 H2SO4,30 μL · 孔-1,终止反应.492 nm处酶标仪测定.每块酶标板同时设空白对照、阴性对照和阳性对照.以P/N≥2.1的最高血清稀释倍数表示抗体效价.
2.2.6 Western blot和免疫组化鉴定抗血清的特异性重组SUMO-MT蛋白纯化样和重组TF(阴性对照)经15% SDS-PAGE电泳分析后,用电转仪(Bio-Rad)将SDS-PAGE 胶中的蛋白转至PVDF 膜上,用封闭液(PBST+ 5%脱脂奶粉)封闭过夜,PBST 洗膜4次,10 min · 次-1,加入1 ∶ 500稀释的自制抗血清作为一抗,4 ℃过夜,PBST 洗膜4次后,加入1 ∶ 5000稀释的AP标记的羊抗鼠 IgG,室温反应2 h,用PBST 洗膜4次后,最后用BCIP/NBT 显色试剂盒避光显色并拍照.
免疫组化实验按照DAB染色试剂盒说明书进行.经不同镉浓度(5.8、11.6 mg · L-1)处理1 d的河南华溪蟹石蜡包埋鳃组织经脱蜡、水化后用柠檬酸缓冲液高压修复抗原,自然冷却后蒸馏水淋洗,再用PBS漂洗2次,每次3 min;滴加内源性过氧化物酶封闭液,室温10 min,PBS充分淋洗;滴加封闭用正常羊血清工作液,室温10 min,甩干;滴加所制备的抗MT血清50 μL,4℃过夜,过夜后37 ℃复温40 min,然后PBS充分淋洗;滴加生物素标记的羊抗鼠IgG,室温10 min,PBS充分淋洗;滴加HRP标记的链霉素亲和素,室温10 min,PBS充分淋洗;DAB显色时间为1~5 min,显色后复染2 min,盐酸酒精分化,PBS充分淋洗,脱水、透明、封片、镜检.
3 结果(Results) 3.1 重组MT的表达、纯化及紫外光谱扫描鉴定利用本实验之前建立的方法制备了重组河南华溪蟹MT融合蛋白.纯化获得的重组融合蛋白SUMO-MT经 SDS-PAGE检测(图 1),其分子量约为26 kD,且纯度较高,可以用于特异性抗血清的制备.重组SUMO-MT经超滤交换至储存液后,在190~300 nm波长下进行紫外光谱扫描(图 2),结果显示,重组蛋白分别在216 nm和285 nm处出现两个特征吸收峰,分析其216 nm处为Zn-MT特征吸收峰,而285 nm处为SUMO标签的特征吸收峰,与预期结果一致.
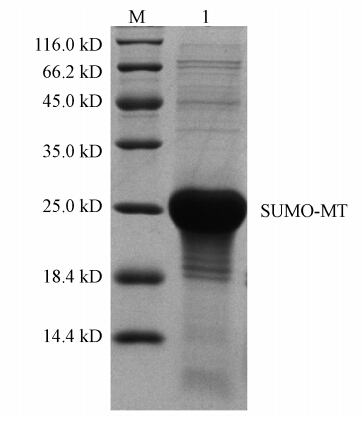 |
| 图 1 SDS-PAGE分析SUMO-MT纯化样品(1:SUMO-MT纯化样品;M:蛋白质Marker) Fig. 1 SDS-PAGE analysis of the purified SUMO-MT(1:the purified SUMO-MT;M:Marker protein) |
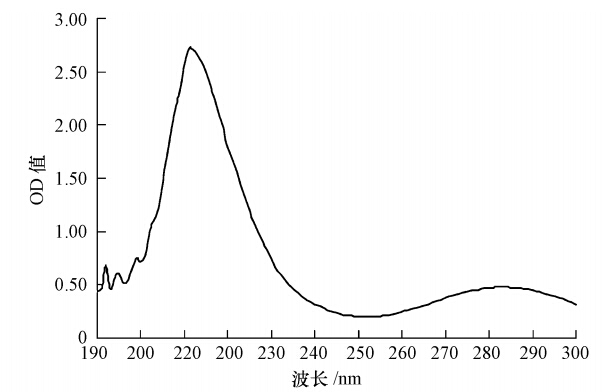 |
| 图 2 重组MT纯化样紫外扫描光谱分析 Fig. 2 UV absorbance spectrometry analysis of recombinant SUMO-MT |
利用BCA蛋白浓度测定试剂盒,以牛血清白蛋白BSA为标准,测定重组SUMO-MT蛋白浓度CMT为0.827 mg · mL-1,重组蛋白经硝化、定容后,测定其Zn含量为0.012 mg · mL-1,根据公式(1)计算其物质的量比为1 ∶ 6,与天然华溪蟹MT蛋白一致,证明重组SUMO-MT仍具有较强的金属结合能力.
3.3 重组SUMO-MT羟基自由基清除率的测定利用羟基自由基测定试剂盒,分别在反应体系中加入不同浓度的重组SUMO-MT,检测其清除羟基自由基能力.结果如图 3所示,当重组SUMO-MT浓度为16 μmol · L-1时,羟基自由基清除率达51%,当浓度为64 μmol · L-1时,羟基自由基清除率达95%,证明重组SUMO-MT具有较强的清除自由基的能力(图 3).
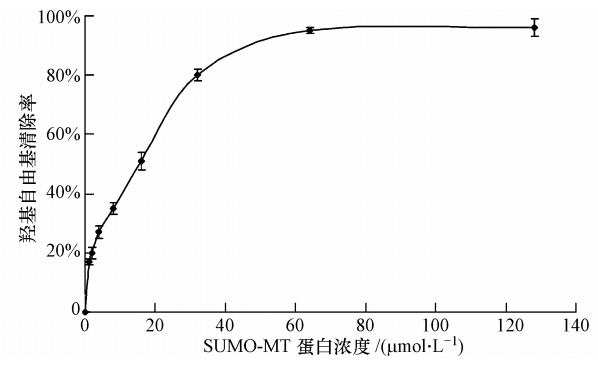 |
| 图 3 重组SUMO-MT蛋白清除羟基自由基能力测定 Fig. 3 Hydroxyl radical scavenging ability of recombinant SUMO-MT protein |
采用间接ELISA法测定SUMO-MT抗血清的效价(表 1),结果表明,以SUMO-MT免疫小鼠,均可获得较高效价的抗血清.其中,3#小鼠血清效价最高,当最大稀释度至102400时,其OD492为0.47,且P/N≥2.1,抗血清的效价高达1 ∶ 102400.
| 表 1 小鼠血清效价检测 Table 1 Results of indirect ELISA to determine antibody activities of anti-SUMO-MT serum |
以1 ∶ 500稀释的自制抗血清作为一抗,对重组SUMO-MT纯化样、经IPTG诱导的工程菌组织全蛋白和重组TF(阴性对照)进行Western blot分析,结果显示,自制抗血清可以识别重组SUMO-MT而与重组TF无特异性结合(图 4).
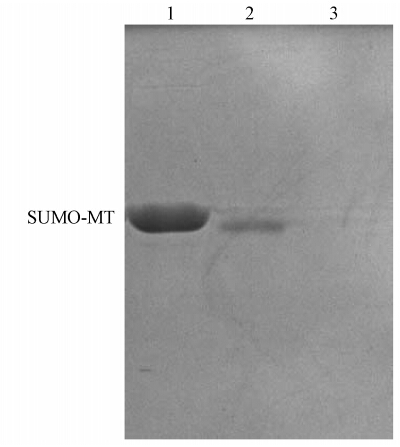 |
| 图 4 抗血清的Western blot鉴定(1:SUMO-MT纯化样品;2:经IPTG诱导的重组工程菌PET-28a-SUMO-MT/BL21(DE3)全菌样;3:重组TF蛋白对照) Fig. 4 Western blot of recombined SUMO-MT fusion protein with anti-SUMO-MT serum(1:the purified SUMO-MT;2:induced cell extract by 1 mM IPTG;3:recombinant TF protein) |
以制备的SUMO-MT抗血清检测了经不同镉浓度(5.8、11.6 mg · L-1)处理的河南华溪蟹鳃组织,结果显示,所制备的抗血清可以与组织中的MT特异性结合.免疫组化染色结果表明,组织中的MT主要定位于细胞质中,呈棕褐色,且随着镉处理浓度的增加,MT的表达量也在升高(图 5).
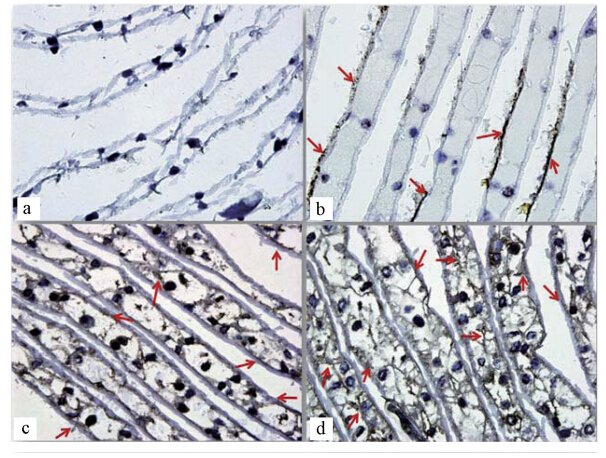 |
| 图 5 DAB 染色法检测MT蛋白在镉处理河南华溪蟹鳃组织中的表达(a.阴性对照(PBS替代一抗);b.正常对照组华溪蟹鳃组织;c.5.8 mg · L-1 CdCl2染毒1 d华溪蟹鳃组织;d.11.6 mg · L-1 CdCl2染毒1 d华溪蟹鳃组织;→表示MT;×600倍) Fig. 5 Light micrographs of gill tissue of S. henanense(a.Negative control;b.Control group;c.Exposure to 5.8 mg · L-1 CdCl2 for 1 d; d.Exposure to 11.06 mg · L-1CdCl2 for 1 d; →st and s for MT;×600) |
MT是自然界中广泛存在的一种可诱导的应急蛋白质.研究表明,MT具有重金属解毒、清除自由基及防止细胞癌变等功能(Eckschlager et al., 2009).MT因其独特的功能和作用,已成为一种具有广阔应用前景的医药蛋白资源,也是一种理想的保健品、化妆品的添加剂.目前,已有多种来源的MT获得了重组表达(Jie et al., 2005; Sauge-Merle et al., 2012; 曹晓敏等,2007),但依然存在表达量较低、易降解、极易形成包涵体等诸多问题.这主要是由于MT分子量较小,半衰期短,在大肠杆菌体内不稳定且易被酶降解;且MT富含半胱氨酸,极易形成无生物活性的包涵体.同时,由于MT在大肠杆菌内极不稳定,脱金属硫蛋白对细胞的毒性及细胞对金属离子的耐受性差等问题,一直难以获得比较高的产率(Mejáre et al., 2001).课题组在前期研究中,利用SUMO融合表达系统实现了河南华溪蟹MT的可溶表达.在此基础上,本研究对重组制备的SUMO-MT进行了金属结合能力和自由基清除能力的测定,进一步证实了重组SUMO-MT具有和天然MT蛋白一致的生物学功能.
由于定量检测方法的限制,MT作为生物标志物在环境监测方面的应用还未能进一步开发.目前,国内外许多学者通过免疫学方法(ELISA或免疫组化)对MT进行定量和定位分析测定,但建立该方法的关键是特异性的抗体的制备.而华溪蟹组织MT蛋白分子量仅有7 kD左右,蛋白免疫原性较弱(Kim et al.,2001),因此,本研究利用分子量为26 kD的功能性重组华溪蟹SUMO-MT蛋白作为抗原.同时,抗血清制备实验中,利用新型的水溶性佐剂Quick Antibody替代传统的福氏佐剂,该佐剂具有免疫针次少、抗原用量低、抗体产生快、抗体滴度高、不需乳化等诸多特点.结果表明,利用SUMO-MT和Quick Antibody佐剂制备了效价较高、特异性好的华溪蟹MT抗血清.该MT抗血清应用于不同镉染毒处理的河南华溪蟹鳃组织免疫组化实验,可特异性识别组织中的MT.MT抗血清的制备,为进一步建立快速、敏感的ELISA 测定方法及MT重金属解毒机制的深入研究奠定了基础.
5 结论(Conclusions)1)利用SUMO融合表达系统完成了河南华溪蟹MT的重组制备,经SDS-PAGE及紫外光谱扫描鉴定后,检测其仍具有与金属离子结合和清除自由基的生物学功能.
2)以功能性重组河南华溪蟹MT为抗原,制备了小鼠抗血清.该抗血清效价经间接ELISA法测定最高达1 ∶ 102400,Western blot分析其具有良好的特异性,并可特异性识别河南华溪蟹组织中的MT,可应用于免疫组化定位及定性检测.
| [1] | Amiard J C, Amiard-Triquet C, Barka S, et al. 2006. Metallothioneins in aquatic invertebrates: their role in metal detoxification and their use as biomarkers[J]. Aquatic Toxicology, 76(2): 160-202 |
| [2] | Apostolova M, Nachev C, Koleva M, et al. 1998. New competitive enzyme-linked immunosorbent assay for determination of metallothionein in tissue and sera[J]. Talanta, 46(2): 325-333 |
| [3] | Bremner I. 1987. Nutritional and physiological significance of metallothionein[J]. Experientia Supplementum, 52: 81-107 |
| [4] | 曹晓敏, 李冰, 陈祯, 等. 2007. 中华绒螯蟹重组金属硫蛋白的原核表达与分离纯化[J]. 生物医学工程学杂志, 24(2): 409-412 |
| [5] | Carpenè E, Andreani G, Isani G. 2007. Metallothionein functions and structural characteristics[J]. Journal of Trace Elements in Medicine and Biology, 21: 35-39 |
| [6] | Eckschlager T, Adam V, Hrabeta J, et al. 2009. Metallothioneins and cancer[J]. Current Protein & Peptide Science, 10(4): 360-375 |
| [7] | Hamer D H. 1986. Metallothionein[J]. Annual Neview of Biochemistry, 55(1): 913-951 |
| [8] | He Y, Ma W, Li Y, et al. 2014. Expression of metallothionein of freshwater Crab (Sinopotamon henanense) in Escherichia coli enhances tolerance and accumulation of zinc, copper and cadmium[J]. Ecotoxicology, 23(1): 56-64 |
| [9] | Jie L, Kaifeng S, Dian Y, et al. 2005. Chracterization of expression and stability of recombinant cystein-rich protein MT1A from yeast[J]. Protein & Peptide Letters, 12(6): 567-571 |
| [10] | Kagi J H R, Schaffer A. 1988. Biochemistry of metallothionein[J]. Biochemistry, 27(23): 8509-8515 |
| [11] | Kim N, Shon S H, Kim, C T, et al. 2011. Responses of label-free metallothionein sensor immobilized with thiolated antibody[J]. Current Applied Physics, 11(5): 1210-1214 |
| [12] | Lindsey M E, Tarr M A. 2000. Quantitation of hydroxyl radical during Fenton oxidation following a single addition of iron and peroxide[J]. Chemosphere, 41(3): 409-417 |
| [13] | Ma W, Wang L, He Y, et al. 2008. Tissue-specific cadmium and metallothionein levels in freshwater crab Sinopotamon henanense during acute exposure to waterborne cadmium[J]. Environmental Toxicology, 23(3): 393-400 |
| [14] | Margoshes M, Vallee B L. 1957. A cadmium protein from equine kidney cortex[J]. Journal of the American Chemical Society, 79(17): 4813-4818 |
| [15] | Mejáre M, Bülow L. 2001. Metal-binding proteins and peptides in bioremediation and phytoremediation of heavy metals[J]. Trends in Biotechnology, 19(2): 67-73 |
| [16] | Nakajima K, Kodaira T, Kato M, et al. 2010. Development of an enzyme-linked immunosorbent assay for metallothionein-I and -Ⅱ in plasma of humams and experimental animals[J]. Clinica Chimica Acta, 411(9/10): 758-761 |
| [17] | Sauge-Merle S, Lecomte-Pradines C, Carrier P, et al. 2012. Heavy metal accumulation by recombinant mammalian metallothionein within Escherichia coli protects against elevated metal exposure[J]. Chemosphere, 88(8): 918-924 |
| [18] | Yang F, Zhou M, He Z, et al. 2007. High-yield expression in Escherichia coli of soluble human MT2A with native functions[J]. Protein Expression and Purification, 53(1): 186-194 |
| [19] | Yudkovski Y, Rogowska-Wrzesinska A, Yankelevich I, et al. 2008. Quantitative immunochemical evaluation of fish metallothionein upon exposure to cadmium[J]. Marine Environmental Research, 65(5): 427-436 |
 2014, Vol. 34
2014, Vol. 34


