2. 西北农林科技大学 黄土高原土壤侵蚀与旱地农业国家重点实验室, 杨凌 712100
2. State Key Laboratory of Soil Erosion and Dryland Farming on Loess Plateau, Northwest A&F University, Yangling 712100
土壤是植物赖以生存的基础,植被是生态系统物质循环和能量交换的枢纽,是防止生态退化的物质基础.在植被-土壤系统中,土壤微生物作为土壤分解系统的重要组分,和其他土壤生物发生相互作用,通过营养元素的周转调节养分供应,影响植物的生长、资源分配和化学组成,既是土壤中营养元素的“源”,又是营养元素的“库”,因此,土壤微生物对植物的生长及发育、群落结构演替具有重要的作用(Hooper et al., 2000; Loreau,2010).土壤微生物活性和群落结构不仅可以敏感地指示气候和土壤环境条件的变化,而且能够反映出土壤生态系统的质量和健康状况(李晶等,2013),在监测土壤质量变化和胁迫中起着重要的作用.同时,土壤微生物种类、结构及功能与土壤矿化有密切的关系.Waldrop等(2000)研究发现,林地转化为耕地的过程中,有机氮含量显著下降,微生物种类和数量发生明显的改变.具体到各类微生物,它们对于氮素改变的响应不尽一致.Maithani等(1998)研究发现,氮矿化作用与细菌数量显著正相关;张琴等(2011)研究发现,真菌、好气性纤维素分解菌和厌氧纤维素分解菌与全氮含量之间极显著相关;顾明华等(2009)发现,铵态氮与氨化细菌、亚硝化细菌和反硝化细菌正相关程度高.因此,研究土壤矿化过程中的微生物群落结构特性,对维持土壤肥力、提高土壤质量、促进土地可持续利用具有重要意义.
磷脂脂肪酸(Phospholipid fatty acid,PLFA)是活体微生物细胞膜的重要组分,不同类群的土壤微生物可通过不同的生物化学途径合成不同的PLFA,它对环境因素极为敏感,不同微生物群落结构的样品具有独特的PLFA谱图,因而可以通过分析PLFA种类及组成比例的变化来评价微生物的结构多样性.目前,由于PLFA 生物标记法具有能够快速、直接、有效地提供较为客观可靠的土壤微生物含量、组成及群落信息等优点,而被广泛运用于土壤微生物分析中(白震等,2006;颜慧等,2006).
宁夏南部山区地处内陆,气候干旱,地面多山,下垫面复杂,生态环境脆弱.20世纪末随着退耕还林工程的实施,宁南山区的生态环境得到了明显改善,山桃和柠条因适应性广、抗性强、耐瘠薄,成为当地生态造林的主要树种之一.目前对黄土丘陵区不同植被类型下土壤养分、微生物量及土壤微生物功能多样性的研究并不少见(安韶山等,2003;2011;胡婵娟等,2009),但基于野外长期定位试验,研究土壤微生物群落结构及土壤理化性质对植被类型及季节变化响应的报道较少,同时有关以柠条和山桃为主的人工灌木林土壤矿化过程中微生物群落的组成和结构尚不清楚,土壤微生物活性变化的研究仍然相对薄弱.因此,本文选择宁南山区人工灌木林中的柠条和山桃林土壤作为研究对象,采用PVC顶盖埋管法进行1年的原位矿化实验,探究土壤矿化过程中林木类型及季节变化对微生物群落结构及与其密切相关的土壤理化性质的影响,以期为宁南山区生态系统的保护、恢复及重建工作提供理论依据.
2 材料与方法(Materials and methods) 2.1 研究区概况研究区位于宁夏南部山区中国科学院水土保持研究所固原生态站上黄试验区(35°59′~36°03′N,106°26′~106°30′E,海拔1534~1822 m).该地区属于半干旱中温带向暖温带过渡季风气候,年均气温6.9 ℃,年均降水量420 mm,降水集中在7月,多年平均蒸发量1400 mm,无霜期140 d.上黄试验区由小川河分为东、西两部分,东部为梁状丘陵,地形起伏较大,西部自东向西依次为台、坪、梁,较为开阔(刘梦云等,2007).地带性土壤为黑垆土,主要分布在台、坪,有深厚的有机质层;丘陵区主要为黄绵土.主要植被类型为人工草地(主要种植苜蓿,作为该区养殖业的饲料供给)、人工灌木林(主要有柠条、山桃等)、撂荒地(主要有长芒草、百里香、茭蒿等)和坡耕地(主要种植小麦、燕麦、荞麦、玉米等).
2.2 实验方案及土样采集于2012年4月在上黄试验区选择1983年种植的柠条(Caragana korshinskii Kom,C.K)和山桃(Prunus davidiana,P.D)林地,即30年生人工灌木林作为研究对象,各样地具体情况如表 1所示.
| 表 1 样地概况 Table 1 Status of the sampling sites |
在每种林地中设置3个样方(5 m×5 m)作为野外3个重复,各样方均按 “S”形多点采样0~15 cm,混合后作为各样地背景土样.同时,采用PVC顶盖埋管法进行野外原位培养矿化试验,在每个选定的样方内,按照梅花形布点方法,一次性选择5个采样点,在每个选定的采样点,除去土壤腐殖质层凋落物后,打入PVC管(高15 cm,内径6 cm),然后取出含有原状土柱的PVC管,上端用不透水的塑料薄膜封口,下端用透气的脱脂棉封口后放回原位.经过不同时间段的培养后,分别于2012年4、6、8、10、12月和2013年4月在各样方内的5个采样点里,每次随机取出1个原状土柱带回实验室进行土壤碳氮及微生物多样性的分析.因为每个林地有3个样方,且每次采样时每个样方内都各取1个,因此,每次每个林地都有3个野外重复的样品.6次土样所对应的土壤矿化时间分别为0、60、120、180、240和360 d.
2.3 分析方法 2.3.1 理化性质测定土壤有机碳采用重铬酸钾-外加热法测定;全氮采用半微量凯氏法测定,土壤铵态氮、硝态氮采用1 mol · L-1 KCl浸提新鲜土样,浸提液通过AA3连续流动分析仪测定;土壤含水率用烘干法测定,pH用DELTA320酸度计测定(鲁如坤,2001).
2.3.2 PLFA测定磷脂脂肪酸的提取使用Bligh和Dyer法,并结合其他学者(Bligh et al., 1959;White et al., 1979;Petersen et al., 1994)在此基础上的改进方法.提取过程为:称取过2 mm筛的鲜土约3.0 g,加入1.5 mL柠檬酸缓冲液、1.9 mL氯仿、3.7 mL甲醇和2 mL柠檬酸缓冲液/氯仿/甲醇(体积比为0.8∶1∶2)混合液,2次浸提,离心,取上清液;于上清液中加入3.1 mL柠檬酸缓冲液和3.1 mL氯仿,离心,取下层氯仿相,高纯N2吹干;分别用氯仿、丙酮和甲醇过活性硅胶柱,收集甲醇相,高纯N2吹干;加0.1 mL 19∶0内标(正十九烷脂肪酸甲酯,N-nonadecanoic Acid Methyl Ester),1 mL甲醇/甲苯(体积比为1∶1)混合液和1 mL 氢氧化钾甲醇溶液(0.2 mol · L-1),37 ℃保温15 min;加2 mL氯仿/正己烷(体积比为1∶4)混合液、0.3 mL冰醋酸(1 mol · L-1,调pH值至中性)和2 mL超纯水,离心,取上层有机相,高纯N2吹干.测定前用异辛烷溶解样品,GC/MS测定.
气相色谱仪型号为Thermo Fisher Trace 2000 DSQⅡ,Aɡilent Sule HP-5MS(MSD)毛细管柱(50 m×0.2 mm×0.33 μm);载气用氦气,流速1.3 mL · min-1;检测器为质谱检测器,进样口和检测器温度分别维持在280 ℃和300 ℃左右;柱温采用程序升温法.脂肪酸的种类通过细菌脂肪酸甲酯混标(Bacterial Acid Methyl Esters Mix)和37种脂肪酸甲酯混标(SupelcoTM 37 Component FAME Mix)与质谱图库确定,而含量则由19∶0内标确定.脂肪酸的命名常规写法为X∶YωZ,其中,X代表链上的碳原子数,Y代表不饱和双键的数目,Z代表不饱和双键距离分子的甲基末端的碳原子数.前缀a和i分别表示有支链反异构脂肪酸和支链异构脂肪酸分支;c、t分别表示顺式和反式脂肪酸,cy表示具环状结构的脂肪酸;Me表示甲基团离羧端的位置,如10Me表示第10 个碳原子的甲基(从羟基端算起)(Frostegård et al., 1993;夏志超等,2012).上述标准品均购自Supelco公司.不同微生物相对应的磷脂脂肪酸标记见表 2.
| 表 2 检验土壤微生物种群的磷酸脂肪酸标志物 Table 2 Assignment of signature phospholipid fatty acids(PLFAs)to soil microbial groups |
数据经过Excel 2010整理和作图后,采用SPSS 18.0软件进行统计分析.不同处理间用单因素方差分析(One-Way ANOVA)和最小显著差异法(LSD)进行分析比较,应用SPSS 18.0软件对不同土壤样品的微生物群落结构做主成分分析(Principal component analysis,PCA),所有数据均为3次重复的平均值.
3 结果与分析(Results and analysis) 3.1 土壤基本理化性质的变化如表 3所示,总体上,柠条林地土壤有机碳、全氮、硝态氮、铵态氮和土壤含水率在矿化过程中显著高于山桃林地(p<0.05).两种灌木林地土壤有机碳、硝态氮和铵态氮随时间均呈现出显著变化,全氮随时间变化不显著,其中,柠条和山桃林地有机碳含量在矿化240 d和360 d时较低,显著小于其他矿化时期(p<0.05),硝态氮、铵态氮含量均在矿化240 d时最低,显著小于其他矿化时期(p<0.05).两种灌木林地土壤含水率皆在矿化240 d时有最大值,显著高于其他矿化时期(p<0.05),而其他矿化时期土壤含水率变化不大.两种灌木林地间的土壤pH值均无显著差异.由此可见,柠条相较于山桃,更利于改善土壤水分和养分状况.
| 表 3 土壤理化性质 Table 3 Soil physiochemical characteristics |
由图 1可以看出,两种灌木林地土壤矿化过程中的总PLFA、细菌PLFA、真菌PLFA、放线菌PLFA、GP PLFA和GN PLFA随着矿化时间存在显著差异,并呈现出相似的变化规律.总体来说,柠条林土壤各菌群PLFA在矿化过程中要高于山桃林土壤,并且在某些矿化时间存在显著差异;柠条和山桃林土壤各菌群PLFA随矿化时间大体呈现出120 d>0、60、180 d和360 d>240 d的趋势,且差异显著(p<0.05).其中,柠条林土壤总PLFA、细菌PLFA、真菌PLFA、放线菌PLFA、GP PLFA和GN PLFA均在矿化120 d后最大,分别为31.86、15.50、5.39、1.04、6.66和3.76 nmol · g-1;在矿化240 d后最小,分别为14.97、6.04、3.30、0.37、2.03和0.89 nmol · g-1.山桃林土壤总PLFA、细菌PLFA、真菌PLFA、放线菌PLFA、GP PLFA和GN PLFA也均在矿化120d后最大,分别为24.82、10.03、4.65、0.85、5.91和2.68 nmol · g-1;在矿化240 d后最小,分别为13.83、3.68、2.79、0.36、2.28和0.91 nmol · g-1.说明柠条和山桃林土壤微生物数量随矿化时间变化明显,并在矿化120 d后最大,矿化240 d后最小.
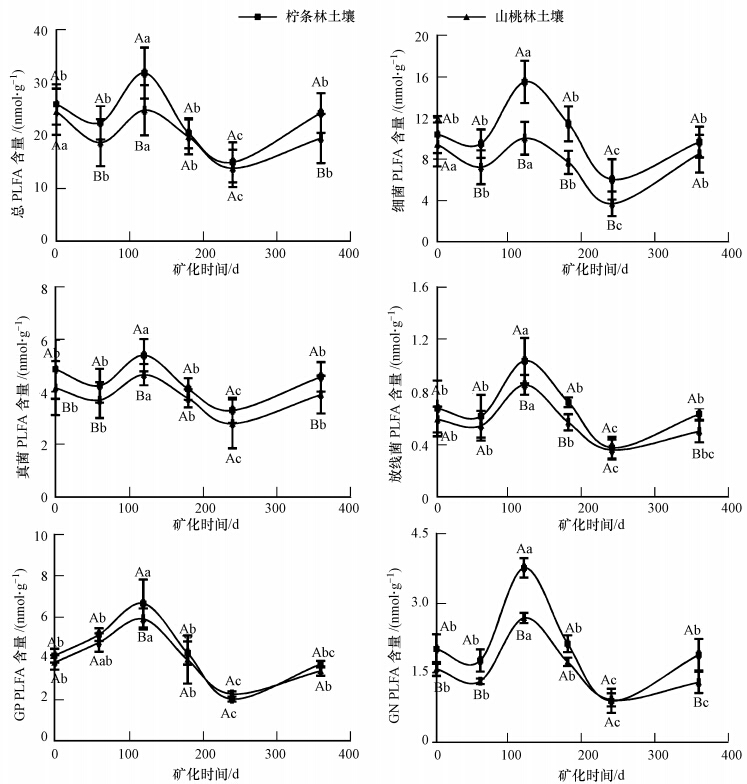 |
| 图 1 灌木林土壤矿化过程中微生物磷脂脂肪酸变化(不同小写字母代表相同植被类型不同时间下的差异显著(p < 0. 05),不同大写字母代表不同植被类型相同时间下的差异显著(p < 0. 05)) Fig. 1 The change of microbial phospholipid fatty acid of shrub l and during soil mineralization |
由图 2可以看出,2种灌木林地土壤细菌与真菌PLFA含量比随着矿化时间延长呈现出不同的变化趋势.其中,柠条林土壤细菌与真菌的PLFA比值介于1.83~2.87之间,随着矿化时间延长该比值呈现120 d和180 d>0、60、240和360 d的趋势,且差异显著(p<0.05);山桃林土壤细菌与真菌的PLFA比值介于1.32~2.27之间,在矿化240 d后有最小值1.32,显著低于其他矿化时间(p<0.05).同时,柠条林土壤矿化60、120、180和240 d时的细菌与真菌的PLFA比值显著高于山桃林地(p<0.05).两种灌木林地土壤革兰氏阳性和阴性菌 PLFA含量比随着矿化时间呈现出相似的变化趋势.其中,柠条林土壤革兰氏阳性和阴性菌PLFA比值介于1.77~2.92之间,在矿化60 d后有最大值2.92,显著高于其他矿化时间(p<0.05);山桃林土壤革兰氏阳性和阴性菌PLFA比值介于2.21~3.63之间,也在矿化60 d后有最大值3.63,显著高于其他矿化时间(p<0.05).同时,柠条林土壤矿化过程中的革兰氏阳性和阴性菌PLFA比值低于山桃林地,并在矿化0、60、120和360 d时差异显著(p<0.05).
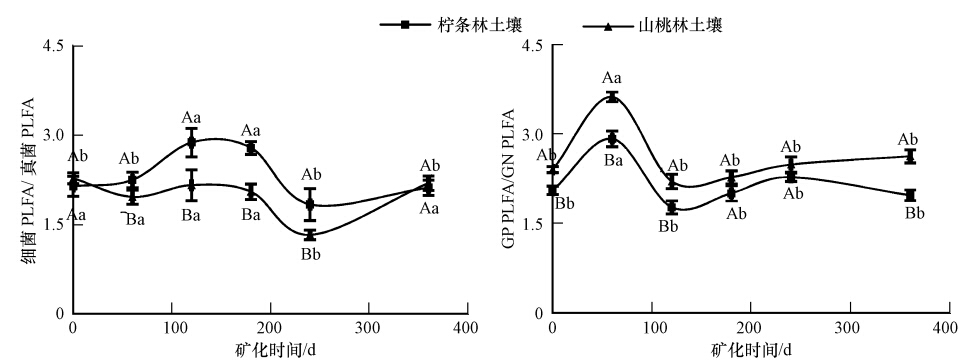 |
| 图 2 灌木林土壤矿化过程中微生物磷脂脂肪酸比值变化 Fig. 2 The ratio change of microbial phospholipid fatty acid of shrub l and during soil mineralization |
为进一步分析不同灌木类型土壤微生物群落结构差异,对柠条和山桃林地土壤样品中检测出的21种典型磷脂脂肪酸进行主成分分析发现,第一主成分(PC1)对PLFA 数据变异的贡献率为71.93%,权重最大,第二主成分(PC2)对总PLFA数据变异的贡献率是14.08%,累积贡献率达到了86.01%.对第1主成分起主要作用的磷脂脂肪酸为16∶0、16∶1ω9c、16∶1ω9t、17∶0、18∶0、18∶2ω9,12c、10Me18∶0和cy19∶0,而对第 2 主成分起主要作用的脂肪酸为a15∶0,i15∶0,i16∶0,i17∶0、18∶1ω9c和20∶0(图 3a).可以看出,第1主成分主要由以16∶ 、16 ∶1ω9c、16∶1ω9t、17∶0、10Me18∶0和cy19∶0所代表的细菌及以18∶2ω9,12c所代表的真菌构成;第2主成分主要由以a15∶0、i15 ∶ 0、i16∶0、i17∶0所代表的GP及以18∶1ω9c所代表的真菌构成.
柠条和山桃林不同矿化时期的土壤微生物群落分布在排序空间的不同位置,矿化0、60、120、180、240和360 d的柠条和山桃林地土壤位于第1象限,矿化240 d的柠条和山桃林地土壤位于第4象限(图 3b).对主成分得分系数进行方差分析发现,两种灌木林地土壤春、秋季与夏季和冬季在主成分上的得分系数差异显著(p<0.05),表明柠条和山桃林地土壤微生物群落结构具有明显的季节性变化规律.其中,春、秋季土壤微生物群落结构未发生明显变化,夏季和冬季土壤微生物群落结构变化显著.土壤矿化过程中,柠条林土壤在主成分上的得分系数显著高于山桃林地土壤(p<0.05),表明两种灌木林地土壤微生物群落结构不同,并且柠条林土壤微生物群落结构受第1和第2主成分的影响更为显著.
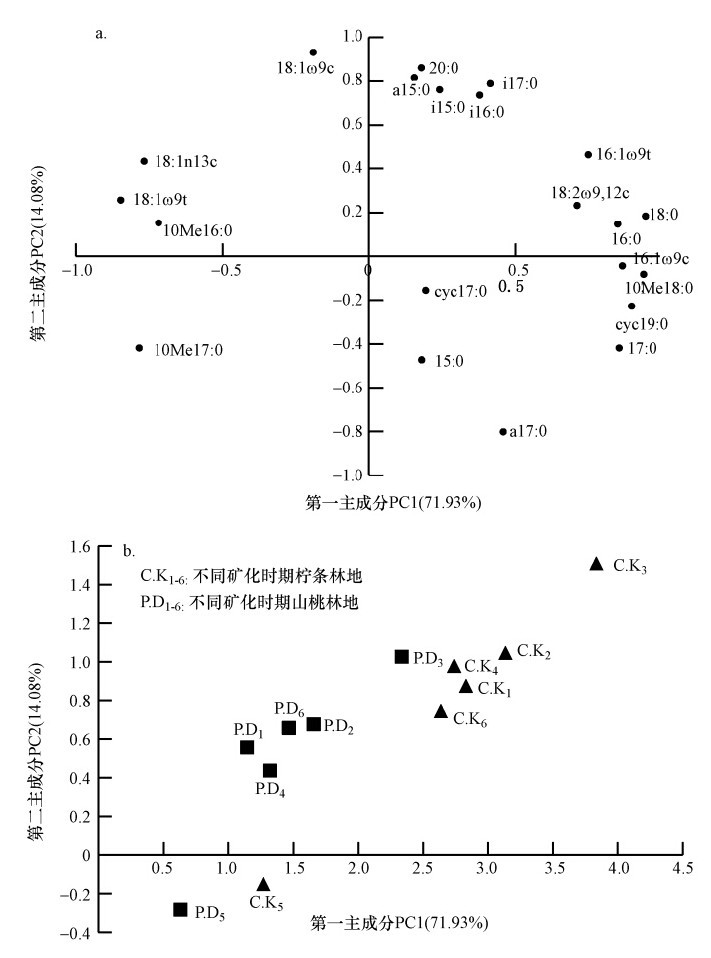 |
| 图 3 灌木林土壤矿化过程中微生物磷脂脂肪酸结构主成分分析(a. 因子载荷图,b. 成分得分图) Fig. 3 The ratio change of microbial phospholipid fatty acid of shrub l and during soil mineralization(a. component loadings,b.0 component scores) |
如表 4所示,土壤总PLFA和细菌PLFA均与有机碳、硝态氮和土壤含水率显著正相关;真菌PLFA与有机碳、硝态氮和土壤含水率显著正相关;放线菌PLFA、GP PLFA和GN PLFA均与有机碳和土壤含水率显著正相关(p<0.01).除总PLFA外,各菌群PLFA与全氮和铵态氮未达到显著相关,除总PLFA外,各菌群PLFA与土壤pH不相关.这说明土壤各菌群PLFA与土壤理化性质联系紧密.
| 表 4 土壤各菌群PLFA与土壤性质的相关性分析 Table 4 Correlation between PLFAs content and soil properties |
土壤微生物是林地生态系统的重要组成部分,影响着凋落物分解、土壤肥力形成与维持、物质循环和能量转化等生态过程(Schloter et al., 2003).研究土壤微生物对了解土壤肥力、土壤养分的转化和循环及环境变化具有重要意义(Kandeler et al., 1999).
4.1 土壤矿化过程中微生物群落结构的季节变化PLFA是活体微生物细胞膜的恒定组分,对环境因素敏感,在生物体外迅速降解,因此,特定菌群PLFA数量变化可反映出原位土壤微生物活体生物量与菌群结构(Zelles,1999;Liu et al., 2006).本研究中柠条和山桃林土壤各菌群PLFA随矿化时间大体呈现出夏季>春、秋季>冬季的趋势,这与微生物活性随温度和水分的变化趋势相一致.Srivastava(1992)研究发现,微生物生物量与有机物的供应、植物生长状况及温度、湿度等环境因素有关.土壤温度在0~35 ℃范围内,随着温度的升高,微生物活动明显增强.在干旱缺水的情况下,水分状况将成为影响土壤微生物量的重要因素,水分的可利用性直接影响微生物的活性.李世清等(2004)通过培养试验发现,在4~36 ℃范围内,微生物体氮与温度呈线性相关,并通过田间试验证实,土壤微生物体氮总的变化规律是夏季最高,冬季最低,其它时期居中.本实验中原位培养土样由PVC管和外界隔离,因此,土壤温度和湿度等环境因素对微生物的影响尤为明显.夏季土壤温度较高,含水率较大,土壤微生物活动较强;而冬季土壤温度低,极大地限制了微生物的活性.
本研究中柠条林土壤细菌与真菌PLFA含量比随矿化时间呈现出夏、秋季>春、冬季的趋势,而山桃林土壤细菌与真菌PLFA含量比在冬季最低.这是因为冬季土壤微生物活性在低温环境下受到了极大的限制,而土壤细菌相较于真菌而言,对环境因素更为敏感(何寻阳等,2008),从而表现出了较低的土壤细菌与真菌PLFA含量比.本研究中柠条和山桃林土壤革兰氏阳性和阴性菌PLFA含量比在春季最大.这是因为春季土壤养分含量较高,土壤微生物所受的环境胁迫较小,土壤中较多的化能营养群落(许多是革兰氏阴性细菌)向较多的异养群落转变(Tscherkoa et al., 2004).两种灌木类型微生物群落结构随季节的变化与细菌和真菌的变化联系紧密.本研究的PLFA主成分分析表明,主成分1和主成分2共解释了变异的86.01%,第1主成分主要由以16 ∶ 0、16 ∶ 1ω9c、16 ∶ 1ω9t、17 ∶ 0、10Me18 ∶ 0和cy19 ∶ 0所代表的细菌及以18 ∶ 2ω9,12c所代表的真菌构成;第2主成分主要由以a15 ∶ 0、i15 ∶ 0、i16 ∶ 0和i17 ∶ 0所代表的GP及以18 ∶ 1ω9c所代表的真菌构成.这说明柠条和山桃土壤微生物群落结构的变化主要由细菌及真菌的相对变化引起,而细菌相较于真菌而言,对微生物群落结构变化的贡献最大.
4.2 两种灌木植被土壤矿化过程中微生物群落结构的差异有研究表明,土壤微生物PLFA含量大小与植被、土壤养分密切相关,而土壤有机碳含量对土壤微生物生物量起到关键作用(Yoshitake et al., 2006;张地等,2012).在本研究中,土壤矿化过程中柠条林土壤各菌群PLFA含量高于山桃林土壤,这是由于不同灌木类型输入到土壤的碳、氮含量明显不同,柠条林土壤有机碳、全氮等土壤养分含量高于山桃林地,其土壤微环境较优异,土壤微生物的繁殖代谢相对较强,更利于微生物量的累积和固持.
本研究表明,柠条和山桃林土壤细菌与真菌的PLFA比值分别介于1.83~2.87和1.32~2.27之间,略低于夏志超等(2012)的研究结果2.13~4.34.细菌与真菌PLFA比可反映细菌和真菌相对含量的变化和两个种群的相对丰富程度.土壤细菌与真菌脂肪酸比值越低,土壤生态系统越持续稳定(Thiet et al., 2006; Devries et al., 2006).这与本研究结果不完全相同,本研究显示,柠条林土壤细菌与真菌的PLFA比值明显高于山桃林,但是柠条林相较于山桃林,土壤微生物PLFA含量及养分含量均较高,显示出了更加稳定的状态.这可能是由于柠条为豆科固氮植物,其土壤微生物区系中氨化细菌、自生固氮菌、硝化细菌等数量较多,真菌和细菌的结构组成受固氮微生物的影响较大(刘岳燕等,2006),因此土壤细菌与真菌的PLFA比值较高.革兰氏阳性细菌和革兰氏阴性细菌的PLFA比值的增加,意味着在生态体系中革兰氏阴性细菌向革兰氏阳性细菌的转变,也说明随着碳源的增加,土壤中较多的化能营养群落(许多是革兰氏阴性细菌)向较多的异养群落转变或者由营养丰富的状态向营养不足的状态转变(Bartelt-Ryser et al., 2005).本研究中柠条和山桃林地革兰氏阳性与革兰氏阴性菌PLFA比值的变化范围分别为1.77~2.92和2.21~3.63,与赵帅等(2011)0.87~6.29的研究结果相符.柠条林土壤矿化过程中的革兰氏阳性与革兰氏阴性菌PLFA比值显著低于山桃林,说明柠条和山桃林土壤细菌结构不同,山桃林土壤细菌中具有较多的异养细菌,其土壤处于营养不足的状态,这也从另一个侧面解释了山桃林地土壤养分含量偏低的原因.
4.2 土壤矿化过程中土壤性质与微生物PLFA的关系两种灌木类型土壤微生物PLFA含量与有机碳和硝态氮显著相关,与全氮和铵态氮无显著相关性,这与赵帅等(2011)的研究结果基本一致.但Kong等(2011)研究发现,土壤微生物在进行自身合成与代谢过程时,除了碳源,还要吸收一定量的氮,氮的增加会提高微生物分解有机质的速率,因此,土壤微生物生物量与土壤全氮呈正相关.陈晓娟等(2013)也指出,不同耕地利用方式下土壤微生物类群与全氮存在显著的相关关系,然而在本研究中土壤微生物PLFA含量与全氮无显著相关性,这可能是由于原位矿化实验中,土壤中无外源氮源的输入,土壤全氮在整个矿化过程中没有显著性变化的原因.土壤中有机氮的矿化实质上是一种微生物学过程,因此,土壤微生物群落的组成与活性在很大程度上决定了土壤氮素的矿化过程,而硝态氮作为土壤矿化过程的产物,与土壤微生物联系紧密,体现出了较好的相关性.但Puri和Ashman(1998)研究表明,微生物生物量对氮素的矿化只有一小部分影响,而土壤湿度和土壤温度是影响氮素矿化的最重要因子,这可能是本研究中土壤微生物PLFA含量与铵态氮无显著相关性的原因.相关性分析还表明,两种灌木类型土壤微生物PLFA含量与土壤含水率显著相关,与pH值不相关.土壤含水量与土壤微生物活性联系紧密,在良好的土壤水分条件下,土壤微生物各类群活性较强,其中,细菌的竞争优势更明显(Hackl et al., 2005),说明土壤水分条件越好,越有利于土壤微生物的生长和分解作用.而土壤 pH 是影响微生物生长和活性的一个重要因素,对微生物生物量及土壤微生物群落结构有显著影响(Rousk et al., 2010).本研究中土壤pH在8.0~8.5之间,变化幅度较小,属于偏碱性土壤,尽管土壤微生物通常可在一个较宽pH范围内生长,但它们对pH变化的耐受性也有一定限度,较低或较高的土壤pH值都不利于微生物的生长(Kemmitt et al., 2006).
5 结论(Conclusions)宁南山区两种灌木类型土壤各菌群PLFA含量随矿化时间差异显著,其中,柠条林土壤各菌群PLFA含量均高于山桃林;土壤矿化过程中,柠条和山桃林土壤的微生物群落结构具有明显的季节性变化规律,微生物结构的变化主要由以16∶0、16∶1ω9c、16∶1ω9t、17∶0、10Me18∶0和cy19∶0所代表的细菌及以18∶2ω9、12c所代表的真菌引起.土壤微生物PLFA与土壤有机碳、硝态氮和土壤含水率显著相关,与土壤pH不相关,说明土壤微生物PLFA与土壤理化性质联系紧密.
| [1] | 安韶山,刘梦云,李壁成,等. 2003.宁南山区不同植被恢复措施的土壤养分效应研究[J].西北植物学报, 23(8): 1429-1432 |
| [2] | 安韶山,李国辉,陈利顶. 2011.宁南山区典型植物根际与非根际土壤微生物功能多样性[J].生态学报, 31(18): 5225-5234 |
| [3] | 白震,何红波,张威,等. 2006.磷脂脂肪酸技术及其在土壤微生物研究中的应用[J].生态学报, 26(7): 2387-2394 |
| [4] | Bartelt-Ryser J, Joshi J, Schmid B, et al. 2005. Soil feedbacks of plant diversity on soil microbial communities and subsequent plant growth[J]. Perspectives in Plant Ecology, Evolution and Systematics, 7(1): 27-49 |
| [5] | Bligh E G, Dyer W J. 1959. A rapid method of total lipid extraction and purification[J]. Canadian Journal of Biochemistry and Physiology, 37(8): 911-917 |
| [6] | 陈晓娟,吴小红,刘守龙,等. 2013.不同耕地利用方式下土壤微生物活性及群落结构特性分析:基于PLFA和MicroResp-(TM)方法[J].环境科学, 34(6): 2375-2382 |
| [7] | Devries F T, Hoffland E, van Eekeren N, et al. 2006. Fungal/bacterial ratios in grasslands with contrasting nitrogen management[J]. Soil Biology and Biochemistry, 38(8): 2092-2103 |
| [8] | Frostegård , Tunlid Å, Bååth E. 1993. Phospholipid fatty acid composition, biomass, and activity of microbial communities from two soil types experimentally exposed to different heavy metals[J]. Applied and Environmental Microbiology, 59(11): 3605-3617 |
| [9] | Grayston S J, Prescott C E. 2005. Microbial communities in forest floors under four tree species in coastal British Columbia[J]. Soil Biology and Biochemistry, 37(6): 1157-1167 |
| [10] | 顾明华,区惠平,刘昔辉,等. 2009.不同耕作方式下稻田土壤的氮素形态及氮素转化菌特征[J].应用生态学报, 20(6): 1362-1368 |
| [11] | Hackl E, Pfeffer M, Donat C, et al. 2005. Composition of the microbial communities in the mineral soil under different types of natural forest[J]. Soil Biology and Biochemistry, 37(4): 661-671 |
| [12] | 何寻阳,王克林,徐丽丽,等. 2008.喀斯特地区植被不同演替阶段土壤细菌代谢多样性及其季节变化[J].环境科学学报, 28(12): 2590-2596 |
| [13] | Hooper D U, Bignell D E, Brown V K, et al. 2000. Interactions between aboveground and belowground biodiversity interrestrial ecosystems[J]. Bioscience, 50(12): 1049-1061 |
| [14] | 胡婵娟, 傅伯杰, 靳甜甜, 等. 2009. 黄土丘陵沟壑区植被恢复对土壤微生物生物量碳和氮的影响[J]. 应用生态学报, 20(1): 45-50 |
| [15] | Kandeler E, Tscherko D, Spiegel H. 1999. Long-term monitoring of microbial biomass, N mineralisation and enzyme activities of a Chernozem under different tillage management[J]. Biology and Fertility of Soils, 28(4): 343-351 |
| [16] | Kemmitt S J, Wright D, Goulding K W, et al. 2006. pH regulation of carbon and nitrogen dynamics in two agricultural soils[J]. Soil Biology and Biochemistry, 38(5): 898-911 |
| [17] | Kong A Y Y, Scow K M, Córdova-Kreylos A L, et al. 2011. Microbial community composition and carbon cycling within soil microenvironments of conventional, low-input, and organic cropping systems[J]. Soil Biology and Biochemistry, 43(1): 20-30 |
| [18] | 李晶,刘玉荣,贺纪正,等. 2013.土壤微生物对环境胁迫的响应机制[J].环境科学学报, 33(4): 959-967 |
| [19] | 李世清,任书杰,李生秀. 2004.土壤微生物体氮的季节性变化及其与土壤水分和温度的关系[J]. 植物营养与肥料学报, 10(1): 18-23 |
| [20] | Liu B R, Jia G M, Chen J A, et al. 2006. A review of methods for studying microbial diversity in soils[J]. Pedosphere, 16(1): 18-24 |
| [21] | 刘梦云,常庆瑞,岳庆玲,等. 2007. 宁南山区不同利用方式土壤颗粒分形特征[J].干旱地区农业研究, 25(6): 201-206 |
| [22] | 刘岳燕,姚槐应,黄昌勇. 2006. 水分条件对水稻土微生物群落多样性及活性的影响[J].土壤学报, 43(5): 828-834 |
| [23] | Loreau M. 2010. Linking biodiversity and ecosystems: towards a unifying ecological theory [J]. Philosophical Transactions of the Royal Society (B: Biological Sciences), 365(1537): 49-60 |
| [24] | 鲁如坤. 2001.土壤农业化学分析方法[M].北京:科学出版社. 176-179 |
| [25] | Maithani K, Arunachalam A, Tripathi R S, et al. 1998. Nitrogen mineralization as influenced by climate, soil and vegetation in a subtropical humid forest in northeast India[J]. Forest Ecology and Management, 109(1/3): 91-101 |
| [26] | Petersen S O, Klug M J. 1994. Effects of sieving, storage, and incubation temperature on the phospholipid fatty acid profile of a soil microbial community[J]. Applied and Environmental Microbiology, 60(7): 2421-2430 |
| [27] | Potthoff M, Steenwerth K L, Jackson L E, et al. 2006. Soil microbial community composition as affected by restoration practices in California grassland[J]. Soil Biology and Biochemistry, 38(7): 1851-1860 |
| [28] | Puri G, Ashman M R. 1998. Relationship between soil microbial biomass and gross N mineralization[J]. Soil Biol Biochem, 30(2): 251-256 |
| [29] | Rousk J, Brookes P C, Bth E. 2010. The microbial PLFA composition as affected by pH in an arable soil[J]. Soil Biology and Biochemistry, 42(3): 516-520 |
| [30] | Schloter M, Dilly O, Munch J. 2003. Indicators for evaluating soil quality[J]. Agriculture, Ecosystems and Environment, 98(1/3): 255-262 |
| [31] | Srivastava S C. 1992. Microbial C, N and P in dry tropical soils: seasonal changes and influence of soil moisture[J]. Soil Biology and Biochemistry, 24(7): 711-714 |
| [32] | Thiet R K, Frey S D, Six J. 2006. Do growth yield efficiencies differ between soil microbial communities differing in fungal: bacterial ratios? Reality check and methodological issues[J]. Soil Biology and Biochemistry, 38(4): 837-844 |
| [33] | Treonis A M, Cook R, Dawson L, et al. 2007. Effects of a plant parasitic nematode (Heterodera trifolii) on clover roots and soil microbial communities[J]. Biology and Fertility of Soils, 43(5): 541-548 |
| [34] | Tscherkoa D, Hammesfahra D, Marxb M C, et al. 2004. Shifts in rhizosphere microbial communities and enzyme activity of Poa alpina across an alpine chronosequence[J]. Soil Biology & Biochemistry, 36(10): 1685-1698 |
| [35] | Waldrop M P, Balser T C, Firestone M K. 2000. Linking microbial community composition to function in a tropical soil[J]. Soil Biology and Biochemistry, 32(13): 1837-1864 |
| [36] | White D C, Davis W M, Nickels J S, et al. 1979. Determination of the sedimentary microbial biomass by extractible lipid phosphate[J]. Oecologia, 40(1): 51-62 |
| [37] | 夏志超, 孔垂华, 王朋, 等. 2012. 杉木人工林土壤微生物群落结构特征[J].应用生态学报, 23(8): 2135-2140 |
| [38] | 颜慧, 蔡祖聪, 钟文辉. 2006. 磷脂脂肪酸分析方法及其在土壤微生物多样性研究中的应用[J].土壤学报, 43(5): 851-859 |
| [39] | Yoshitake S, Uchida M, Nakatsubo T, et al. 2006. Characterization of soil microflora on a successional glacier foreland in the High Arctic on Ellesmere Island, Nunavut, Canada using phospholipid fatty acid analysis[J]. Polar Bioscience, 19: 73-84 |
| [40] | Zelles L.1999.Fatty acid patterns of phospholipids and lipopoly saccharides in the characterization of microbial communities in soil: A review[J]. Biology and Fertility of Soils, 29(2): 111-129 |
| [41] | 张地,张育新,曲来叶,等. 2012. 海拔对辽东栎林地土壤微生物群落的影响[J].应用生态学报, 23(8): 2041-2048 |
| [42] | 张琴,李艳宾,何智慧. 2011. 胡杨林地土壤微生物主要类群的动态及与土壤碳氮变化的关系[J].江苏农业科学, 39(4): 444-446 |
| [43] | 赵帅, 张静妮, 赖欣, 等. 2011. 放牧与围栏内蒙古针茅草原土壤微生物生物量碳, 氮变化及微生物群落结构 PLFA分析[J]. 农业环境科学学报, 30(6): 1126-1134 |
 2014, Vol. 34
2014, Vol. 34


