疏水性有机污染物在土壤系统中多以吸附态或液态形式存在,在水中不溶或微溶,不易被土壤微生物利用并降解.多环芳烃(PAHs)是常见的一类疏水性有机化合物(HOCs),由于具有致癌、致畸、致突变作用其迁移转化和控制治理一直备受关注,受其污染土壤的修复问题也成为研究热点(Zhao et al., 2011;Chen et al., 2012;Kobayashi et al., 2012;Li et al., 2012). 当前,土壤有机污染修复方法主要有物理修复、化学修复和生物修复(朱利中,1999;陈怀满,2005). 其中,表面活性剂增效修复(SER)技术是众多修复方式中颇具潜力的实用化学修复技术(Park et al., 2005;Bandala et al., 2010),其原理是利用表面活性剂等增效试剂对憎水性污染物的增溶和增流作用,洗脱土壤中的污染物,增大水相中有机物的浓度,提高有机物污染的生物可利用性,加速其生物降解过程,从而达到修复的目的. 为提高增效修复能力,各种表面活性剂及类表面活性物质已被用于增溶修复土壤有机污染物的研究(Zhu et al., 2003;Conte et al., 2005; Zhao et al., 2007;郭利果等,2009;吴应琴等,2009).
N-烷(酰)基乙二胺三乙酸盐(ED3A)类表面活性剂是近年来为解决三聚磷酸钠所引起的环境问题而发展起来的新型螯合型表面活性剂,已在合成洗涤剂、化学工业及农牧业中广泛应用(王军,2009). 它是以优良螯合剂ED3A为母体,引入一个脂肪酰基或烷基合成的系列衍生物(Parker et al., 1996;牛瑞霞等,2011),分子中含有几个相邻的离子型亲水基(螯合部分)和一个长链烷(酰)基亲油基,具有表面活性、螯合性、耐硬水、易于生物降解等优越性能. 将其用于土壤污染化学修复,有望实现单一试剂对土壤有机污染物和重金属的同时去除,并可减少自身对土壤的污染.
近年来,关于表面活性剂对疏水性有机污染物的增溶已有许多定量描述(Kurt et al., 1997;Sailaja et al., 2003),但用新型螯合型表面活性剂作增效试剂增溶疏水性有机物的研究国内外鲜有报道.因此,本文选用N-十二酰基乙二胺三乙酸钠(以下简称N-LED3A)为增效试剂,以菲为研究对象,探讨菲在N-LED3A溶液中的增溶性能及其热力学和动力学特征,以期为今后开展螯合型表面活性剂修复土壤有机污染的研究工作提供理论参考.
2 实验部分(Experimental section) 2.1 试剂与仪器试剂:螯合型表面活性剂N-LED3A(摩尔质量为482 g · mol-1,纯度为95%)购自杭州生物科技有限公司,菲(摩尔质量178 g · mol-1,分析纯)购自美国Aldrich Chemical Co.,甲醇为HPLC级,超纯水.
仪器:Thermo Fisher LCQ Advantage 4000型液质联用仪的Surveyor高效液相色谱系统,SHZ-82气浴恒温振荡器,Anke TDL80-2B离心机,FA2004N分析天平,DG超声波清洗器.
2.2 实验方法 2.2.1 增溶平衡实验分别移取20mL一系列浓度的N-LED3A溶液于50 mL磨口碘量瓶中,然后加入稍过量的菲晶体,同时以去离子水代替表面活性剂做空白试样,盖紧塞子,在一定温度(15、25、35、45 ℃)和150 r · min-1转速条件下振荡24 h(预实验表明24 h已足够)平衡后,将溶液转入10 mL离心管中,加盖密封后以4000 r · min-1离心30 min,完全分离未溶解的菲.移取一定量的上清液于25 mL比色管中,往其中加入10 mL甲醇后用去离子水定容,定容后的待测液过0.22 μm的注射器滤膜到进样瓶中,用HPLC分析水溶液中菲的浓度.同时做2组平行样,根据工作曲线算出溶质的表观溶解度求平均值.绘制菲的表观溶解度和表面活性剂浓度关系曲线.
液相色谱分析条件:AT-LICHROM ODS2 C18反相色谱柱(250 mm×4.6 mm×5 μm),流动相为甲醇 ∶ 水(80 ∶ 20),流速0.2 mL · min-1,柱温40 ℃,进样量10 μL,检测波长250 nm.
2.2.2 增溶动力学实验在初始浓度为6.224 mmol · L-1的N-LED3A溶液中加入稍过量的菲晶体,用上述方法进行增溶实验,增溶温度为(25±1)℃,分别在1、2、4、6、10、12、16、20、24、30、40 h时取相应振荡时间试样测定菲的浓度. 同时做2组平行样,求平均值. 绘制菲的表观溶解度与振荡时间的关系曲线,拟合增溶动力学方程,计算表观增溶速率常数.
3 结果与讨论(Results and discussion) 3.1 温度对N-LED3A增溶菲的影响 3.1.1 菲在N-LED3A溶液中的增溶在一定浓度的N-LED3A溶液中,试验了不同温度下N-LED3A对菲的增溶作用,结果见图 1.由图可知,菲在表面活性剂溶液中的表观溶解度随表面活性剂浓度的升高而增加。增溶曲线可分段描述如下:当表面活性剂浓度较低时,菲的表观溶解度随着表面活性剂浓度的增加呈线性增加但增加量较小且不明显;随表面活性剂浓度的不断增加,达到临界胶束浓度CMC后,由于溶液中出现了胶团,根据相似相容原理,疏水性有机物菲很快在胶团相和水相之间进行分配而进入胶团,导致表面活性剂浓度大于CMC时,菲的表观溶解度与N-LED3A溶液浓度也呈线性关系。可见,菲的增溶曲线与表面活性剂浓度呈现双线性变化关系,曲线上的转折点对应的浓度值即为表面活性剂的CMC值,由溶解度法计算得到不同温度下的CMC值(赵喆等,2010)列于表 1.
 |
| 图 1 不同温度下N-LED3A对菲的增溶曲线 Fig. 1 Effects of temperature on solubility enhancement of phenanthrene by N-LED3A solution |
| 表1 LED3A对菲增溶曲线的线性回归数据及CMC、Sw、Kmn、 Kmc值 Table 1 Linear regression data of solubility enhancement of phenanthrene by N-LED3A at different temperatures and their corresponding CMC,Sw,Kmn,Kmc values |
表面活性剂对有机物增溶作用的程度与表面 活性剂单体、胶束浓度和溶质在单体/水、胶束/水 介质间的分配系数有关,具体表达如下(Kile et al., 1989):

式中,S*w是表面活性剂浓度为X(X=Xmn+Xmc)时菲的表观溶解度(mmol · L-1);Sw是菲在纯水中的溶解度(mmol · L-1);Xmn是表面活性剂单体的浓度(mmol · L-1);Xmc是以胶束形式存在的表面活性剂浓度(mmol · L-1);Kmn是溶质在表面活性剂单体和水之间的分配系数(mL · mol-1);Kmc是溶质在在表面活性剂胶束与水之间的分配系数(mL · mol-1).Kmn和Kmc与增溶曲线的线性斜率K1和K2的关系如下:
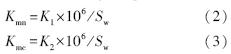
式中,K1、K2分别为表面活性剂浓度在CMC前、后增溶曲线线性回归方程的斜率.
根据溶解度法,由N-LED3A在CMC前后的增溶曲线线性回归方程可求出不同温度下N-LED3A的CMC值;由式(2)和式(3)可计算得到Kmn、Kmc,结果列于表 1.
由表 1可见,随着温度的升高,N-LED3A溶液对菲的增溶能力(Kmn和Kmc)增大,而相应温度下的CMC值呈现先减小后增大的趋势.15、25、35和45 ℃时的Kmn分别为4.95×105、6.43×105、6.81×105和1.08×106 mL · mol-1,Kmc分别为1.51×106、1.67×106、2.12×106和2.48×106 mL · mol-1.由此可见,菲在水中表观溶解度S*w的增大是由于其在表面活性剂N-LED3A单体或胶束中分配作用所致,分配系数随温度升高而增大,使得相同初始表面活性剂浓度下菲的S*w随温度的升高而增大,虽然温度升高使菲的疏水性减弱,Sw也有所增加,但其增加量很小.总体来说,N-LED3A单体及胶束作为菲的增溶介质,使菲的增溶量(S*w-Sw)和增溶程度S*w/Sw随着温度的升高而增大.例如,在N-LED3A浓度为3.320 mmol · L-1时,不同实验温度下(15、25、35和45 ℃),S*w-Sw分别为0.013、0.022、0.031和0.047 mmol · L-1,S*w/Sw分别为4.25、4.90、5.97和6.54. 表 1显示,15、25、35和45 ℃下,N-LED3A的CMC分别为1.54、1.42、1.36和1.89 mmol · L-1,CMC随温度的升高呈现先减小后增大的趋势,但变化范围不大. 这是因为温度对表面活性剂亲水基和疏水基有不同的影响,温度升高削弱了亲水基的水合作用,有利于胶团的形成,促使临界胶团浓度降低;而温度升高又引起疏水基周围水的结构破坏,这不利于胶团形成,促使临界胶团浓度升高.表面活性剂临界胶团浓度随温度变化情况是这两个因素综合作用的结果,温度对亲水基的影响在较低温度时起主要作用,而它对疏水基的影响在较高温度时起主要作用。说明N-LED3A的CMC最低点出现在温度35 ℃附近.
3.1.2 菲在N-LED3A溶液中的增溶热力学从热力学角度说,增溶现象是一种溶解平衡,在一定的温度、压力下,菲在水中的溶解焓及菲在N-LED3A单体和胶束中的溶解焓变化可以用克劳修斯-克拉佩龙方程来计算(陈宝梁等,2006):
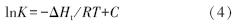
式中,R为气体摩尔常数,取值为8.314 J · K-1 · mol-1;T为热力学温度(K);C为常数;ΔHt为表观摩尔溶解焓(J · mol-1);K为菲的表观溶解平衡常数,分为以下3种情况:①当K 为菲在水中的溶解平衡常数Kw时,ΔHt用ΔHw表示;②当K 为菲在N-LED3A单体中表观增溶平衡常数时(表 1中CMC以下拟合直线斜率K1),ΔHt用ΔHmn表示;③当K为菲在N-LED3A胶束中表观增溶平衡常数时(表 1中CMC以上拟合直线斜率K2),其表观摩尔溶解焓变则用ΔHmc表示. 若不考虑温度对ΔHt的影响,将式(4)的lnK(K分别取Kw、K1 、K2)与1/T作图,由线性回归方程的斜率可求出相应的ΔHt(ΔHw、ΔHmn、ΔHmc)值,数据如表 2所示.
| 表2 温度对菲在水中、N-LED3A单体和胶束中平衡溶解系数影响曲线的线性回归数据及ΔHw、 ΔHmn、ΔHmc值 Table 2 Linear regression data of equilibrium solubilization coefficients of phenanthrene in aqueous solution and N-LED3A solution at different temperatures and their corresponding ΔHw,ΔHmn,ΔHmc values |
表 2中菲在纯水中的表观摩尔溶解焓ΔHw= 18.87 kJ · mol-1,菲在N-LED3A单体和胶束中的表观摩尔溶解焓变ΔHmn= 37.17 kJ · mol-1,ΔHmc= 31.99 kJ · mol-1. ΔHw>0、ΔHmn >0、ΔHmc >0,溶解热均为正,证明菲在N-LED3A溶液中的增溶过程为吸热过程,可见温度升高有利于菲在水、N-LED3A单体和胶束中的溶解. 菲在N-LED3A单体和胶束中的表观摩尔分配焓变可表示为:

经计算,ΔH*mn=18.3 kJ · mol-1,ΔH*mc=13.12 kJ · mol-1,表明均为吸热过程.因此,温度升高有利于菲在N-LED3A单体和胶束中的分配作用.另外,不同温度下菲的lnKmn或lnKmc与lnSw之间呈现较好的线性关系,回归方程分别为lnKmn=0.9597lnSw+18.386(R2=0.9226,n=4)和lnKmc=0.6404ln Sw+17.753(R2=0.8656,n=4). 说明随温度升高,菲在水中溶解度的增大对菲在N-LED3A溶液中增溶能力的增强有一定的促进作用,但并非主因,这在3.1.1节中已有所讨论.
3.2 菲在N-LED3A溶液中的增溶动力学在温度(25±1)℃下,6.224 mmol · L-1N-LED3A溶液增溶菲的动力曲线如图 2所示. 结果表明,开始阶段增溶很快,2 h时菲的表观溶解度已达到0.044 mmol · L-1,随后的增加幅度逐渐变慢,20 h基本达到增溶平衡,增溶过程趋于平稳.因此,将20 h确定为菲的最佳增溶平衡时间.
 |
| 图 2 N-LED3A对菲的增溶动力学曲线 Fig. 2 Solubilization kinetics of phenanthrene in N-LED3A solution |
将菲在N-LED3A溶液中的增溶动力学过程分别用动力学一级方程(7)、Elovich 方程(8)、双常数方程(9)进行拟合,结果见表 3.由表 3可知,一级动力学方程最适合描述N-LED3A对菲的增溶过程,由方程斜率确定其表观增溶速率常数为0.1023 h-1(25℃,N-LED3A浓度6.224 mmol · L-1).

式中,t为反应时间(h);S是t时间内菲在N-LED3A溶液中的表观溶解度(mmol · L-1);Sm是菲在N-LED3A溶液中的最大表观溶解度(mmol · L-1);k为表观增溶速率常数(h-1);a、b为常数.
| 表3 菲在N-LED3A溶液中的增溶动力学方程参数 Table 3 Kinetics parameters for solubilization of phenanthrene in N-LED3A solution |
1)螯合型表面活性剂N-LED3A可有效增溶菲,菲的表观溶解度随表面活性剂浓度的升高而增加,这是由于菲在N-LED3A单体或胶体中分配所致,Kmn和Kmc均随温度升高增大,增溶能力随温度升高而增强.
2)N-LED3A的CMC随温度的升高(15、25、35和45 ℃)呈现先减小后增大的趋势,但变化范围并不大,其值分别为1.54、1.42、1.36、1.89 mmol · L-1.
3)菲在N-LED3A单体/水和胶束/水的摩尔分配焓变分别为18.30 kJ · mol-1和13.12 kJ · mol-1,温度升高有利于菲在N-LED3A单体和胶束中的分配作用;菲在水、N-LED3A单体和胶束中的表观摩尔溶解热分别为18.87、37.17和31.99 kJ · mol-1均为吸热过程,故温度升高菲在水、N-LED3A单体和胶束中的溶解量增大.
4)动力学方程拟合结果表明,一级动力学方程最适合描述N-LED3A对菲的增溶过程,其表观增溶速率常数为0.1023 h-1,最佳增溶平衡时间为20 h.
| [1] | Bandala E R, Aguila F, Torres L G. 2010. Surfactant-enhanced soil washing for the remediation of sites contaminated with pesticides[J]. Land Contamination and Reclamation, 18(2): 151-159 |
| [2] | 陈宝梁, 李菱, 朱利中. 2006. 温度和离子强度对SDBS增溶菲的影响及机理 [J]. 环境化学, 25(6): 697-700 |
| [3] | Chen B L, Yuan M X, Qian L B. 2012. Enhanced bioremediation of PAH-contaminated soil by immobilized bacteria with plant residue and biochar as carriers [J]. Journal of Soils and Sediments, 12(9): 1350-1359 |
| [4] | 陈怀满. 2005. 环境土壤学[M]. 北京:科学出版社. 397-441 |
| [5] | Conte P, Agretto A, Spaccini R, et al. 2005. Soil remediation: humic acids as natural surfactants in the washings of highly contaminated soils[J]. Environmental Pollution, 135(3): 515-522 |
| [6] | 郭利果, 苏荣国, 梁生康, 等. 2009. 鼠李糖脂生物表面活性剂对多环芳烃的增溶作用[J]. 环境化学, 28(4): 510-514 |
| [7] | Kile D E, Chiou C T. 1989. Water solubility enhancements of DDT and trichlorobenzene by some surfactants below and above the critical micelle concentration[J]. Environmental Science and Technology, 23(7): 832-838 |
| [8] | Kobayashi T, Kaminaga H, Navarro R R, et al. 2012. Application of aqueous saponin on the remediation of polycyclic aromatic hydrocarbons-contaminated soil[J]. Journal of Environmental Science and Health (Part A: Toxic/Hazardous Substances and Environmental Engineering), 47(8): 1138-1145 |
| [9] | Kurt D P,Andrew M A,Linda M A, et al. 1997. Solubilization of dodecane,tetrachloroethylene and 1,2-dichloo-benzene in micellar solutions of ethoxylated nonionic surfactants [J]. Environmental Science and Technology, 31(5):1382-1389 |
| [10] | Li F M, Guo S H, Hartog N. 2012. Electrokinetics-enhanced biodegradation of heavy polycyclic aromatic hydrocarbons in soil around iron and steel industries[J]. Electrochimica Acta, 85: 228-234 |
| [11] | 牛瑞霞, 龙彪, 李柏林, 等. 2011. 螯合型表面活性剂NaLED3A的合成及性能[J]. 精细石油化工, 28(1): 45-49 |
| [12] | Park S K, Bielefeldt A R. 2005. Non-ionic surfactant flushing of pentachlorophenol from NAPL-contaminated soil[J]. Water Research, 39(7): 1388-1396 |
| [13] | Parker B A, Crudden J J. 1996. The commercial synthesis and characterization of novel multifunctional surfactant chelates. 4th World Surfactant Conference. Barcelona. 446-460 |
| [14] | Sailaja D, Suhasini K L, Kumar S, et al. 2003. Theory of rate of solubilization into surfactant solutions[J]. Langmuir, 19(9): 4014-4026 |
| [15] | 王军. 2009. 功能性表面活性剂制备与应用[M]. 北京: 化学工业出版社 |
| [16] | 吴应琴, 陈慧, 王永莉, 等. 2009. 腐殖酸对蒽的增溶作用及其影响因素[J]. 环境化学, 28(4): 515-518 |
| [17] | Zhao B W, Jiang B. 2011. Aqueous dissolution of phenanthrene from loess soil using Triton X-100 and sodium dodecylbenzene sulfonate[J]. Asian Journal of Chemistry, 23(9): 3859-3864 |
| [18] | Zhao B W, Zhu K, Zhang C L. 2007. Solubility enhancements of trichloroethene and perchloroethene by mixed surfactant[J]. Journal of the Chemical Society of Pakistan, 29(5): 421-426 |
| [19] | 赵喆, 王齐放. 2010. 表面活性剂临界胶束浓度测定方法的研究进展[J]. 实用药物与临床, 13(2): 140-144 |
| [20] | 朱利中. 1999. 土壤及地下水有机污染的化学与生物修复[J]. 环境科学进展, 7(2): 65-71 |
| [21] | Zhu L Z, Feng S L. 2003. Synergistic solubilization of polycyclic aromatic hydrocarbons by mixed anionic-nonionic surfactants[J]. Chemosphere, 53(5): 459-467 |
 2014, Vol. 34
2014, Vol. 34


