随着集约化畜牧业的发展,畜禽疾病越来越多样化,兽药种类及用量也与日俱增,由此引发的生态环境问题及对人类健康所造成的危害也越来越严重(陈杖榴,2005).磺胺类药物是一种具有对氨基苯磺酰胺结构的人工合成化学药物,主要用于预防和治疗细菌感染性疾病,是国家允许使用的广谱抗菌药物,其作为畜禽饲料药物添加剂被广泛应用于防治畜禽疾病.近年来,我国磺胺类药物的产量一直呈持续增长趋势,2003年已突破2万t,由于磺胺类药物在土壤中降解缓慢,可以使其在土壤中有不同程度的残留.已有研究证实,磺胺类药物对人体健康有较大危害(Baran et al., 2006),但目前国内外有关磺胺类药物在土壤中环境行为的研究报道仍较少.
根-土界面是土壤与植物根系的交界面,其范围一般只有0.1~5 mm.在植物根系分泌和吸收动态过程的作用下,根-土界面的pH、Eh、根系分泌物、酶活性都不同于土体,形成一个有别于土体的特殊微域环境(Bertin et al., 2003; Bais et al., 2006;Hartmann et al., 2008).研究表明,植物-微生物联合作用的微域环境能够加速有机物降解,一方面是因为植物根系巨大的表面积为微生物提供了寄宿之处,使植物根际微生物数量明显多于周围土壤(Nichols,1997);另一方面是由于植物向根系输送氧气和释放根系分泌物,使根际微域中土壤养分、土壤湿度及酶活性等产生相应的变化(Paterson et al., 1990; Hinsinger et al., 2003),这种根与土壤理化性质的相互作用,对有机污染物在土壤中的迁移滞留行为产生了极大的影响.然而对于这种根际效应,其作用范围也存在具体条件上的差异,根际效应范围与植物种类、土壤类型、土壤含水量、根系的特定分布、根系分泌物、根瘤菌的存在与否及根毛多少等因素有关(Jay et al., 1995).目前关于植物根际效应对土壤养分作用的研究报道较多,但针对兽药降解的根际效应方面的报道则较少,开展相关方面的研究可为兽药的根际修复提供理论指导和借鉴.
因此,本试验以黄潮土为研究对象,玉米为供试作物,采用多隔层根箱法,通过尼龙网插片的控制,实现对不同距离根际微域土样的分离采集,研究磺胺嘧啶(SD)在根际土壤的降解动态及根系分泌有机酸的梯度变化,旨在揭示SD在距根不同距离的根际土壤中的降解规律及伴随根系分泌物梯度递减效应的响应趋势.
2 材料与方法(Materials and methods) 2.1 试验材料 2.1.1 供试土壤土壤采自河南师范大学生物园,土壤理化性质如下:pH=6.31,阳离子交换量12.26 cmol · kg-1,TP 0.04 mg · kg-1,TK 0.18 mg · kg-1,有机质1.65%,粘粒13.4%,粉粒24.2%.土壤风干研磨,过2 mm筛备用.
2.1.2 药品与试剂SD标准品(白色结晶,纯度为99.0%,美国Sigma公司),甲醇(色谱纯,美国Fisher公司),重蒸水(二次蒸馏水),草酸、苹果酸、乙酸和柠檬酸均为色谱纯,乙腈为色谱纯,实验用水为超纯水,磷酸为国产分析纯,水相针式过滤器,孔径0.45 μm.
2.2 试验方法 2.2.1 试验设计根际箱方法参照文献(Moritsuka et al., 2000).根际箱为不透明的聚乙烯方盒,长、宽、高都是10 cm,盒壁厚4 mm.根-土界面被分成多个不同的空间,具体为:种植玉米的中央区域为5 mm,以此为中心,每层之间距离为1 mm,两侧被均匀分隔成5层,隔板是覆盖300目尼龙网的有机玻璃框,框的厚度为0.18 mm.
参照目前禽畜粪便中SD残留量的相关研究(Elena et al., 2007),按照厩肥的大致用量,将土壤中SD的剂量设为1 mg · kg-1和5 mg · kg-1.称取一定量上述土壤于盆中,拌入尿素和磷酸二氢钾作底肥,基肥量为N 0.15 g · kg-1、P2O5 0.15 g · kg-1、K2O 0.1 g · kg-1,混匀后放置3 d.量取一定体积SD甲醇溶液与少量土先混匀,放置24 h,待甲醇挥发后,再拌到剩余土中充分搅拌、混匀,得到初始含量为1 mg · kg-1和5 mg · kg-1的试验土壤.种子浸于0.5%的次氯酸钠溶液中消毒20 min,用去离子水冲洗干净,放入恒温培养箱,于25 ℃下催芽24 h.每箱播种20粒,出苗后,每箱保苗10株.培养期间保持土壤含水量在田间最大持水量的60%,每组设3次重复.根际箱放于恒温光照培养箱(LRH-250-A,3000 lx)内,光照时间14 h,无光照时间10 h,对应温度分别为25 ℃和20 ℃.采用破坏法取样,分别在出苗后第20、40和60 d取两侧不同剖面土样,混匀,测定其残留SD含量,同时分别取植株地上部和根,测定其不同部位SD含量.
2.2.2 SD测定方法称取5 g样品(土样或植物样)于锥形瓶中,加入25 mL甲醇-1%(质量分数),乙酸提取液(甲醇 ∶ 1%乙酸=30 ∶ 70,V/V),涡旋振荡2 h,倒入离心管中于4000 r · min-1下离心10 min,移取上清液;向沉淀物中再加入25 mL提取液,重复提取2次,合并提取液,用0.45 μm有机微孔滤膜过滤,高效液相色谱(HPLC)分析测定.每组试验重复3次.在0.5~10 mg · kg-1范围内测得SD回收率为90.36%~94.21%,变异系数为1.6%~3.1%,检测限为0.05 mg · kg-1.说明该方法灵敏度高、稳定,能够满足对土壤样品SD残留分析检测的需求.
HPLC操作条件如下:Waters高效液相色谱仪,Waters 2998 二极管阵列检测器(Waters,Singapore),Waters 1525 Binary溶剂输送泵(Waters,Singapore),SunFire C18分析柱(150 mm×4.6 mm,5 μm),保护柱(C18,4.6 mm×20 mm,5 μm);流动相为甲醇-1%乙酸(体积比为30 ∶ 70),检测波长 270 nm,进样量20 μL,流速1 mL · min-1,柱温 35 ℃.
2.2.3 有机酸的测定方法称取土壤样品2 g于25 mL离心管中,加入0.1% H3PO4 10 mL,振荡3min,5000 r · min-1下离心5 min,过水相0.45 μm滤膜,供HPLC测定.测定条件为:SunFire C18分析柱(150 mm×4.6 mm,5 μm),保护柱(C18,4.6 mm×20 mm,5 μm),流动相为0.1% 磷酸和乙腈(体积比为98 ∶ 2),检测波长 210 nm,进样量20 μL,流速 1 mL · min-1,柱温 35 ℃.每组试验均设3次重复.该方法的回收率在98.5%~110.3%之间,检测限在0.2~1.0 μg · kg-1之间,能较好地分离甲酸、苹果酸、乙酸、柠檬酸4种有机酸,能够满足土壤中有机酸mg · kg-1级痕量检测的要求.
2.3 数据处理与分析采用SPSS17.0和Origin7.5数据处理软件对数据进行方差分析和线性拟合.
3 结果与分析(Results and analysis) 3.1 各毫米级根际微域SD降解动态变化本研究分析了在2个SD污染水平胁迫下,种植/未种植玉米土壤SD降解的空间变化和时间变化(图 1).由图 1可知,在玉米生长20 d后,2个SD处理水平下(1、5 mg · kg-1),种植玉米根际土壤的SD降解率显著高于未种植玉米土壤.在1 mg · kg-1的SD作用下,种植玉米处理微域土壤的平均总降解率为4.32%,而未种植玉米处理的平均总降解率仅为1.34%;同样,5 mg · kg-1处理种植玉米各毫米级根际的平均总降解率为5.76%,显著高于未种植玉米(1.41%).从图 1可以看出,不同剂量SD处理下,种植玉米的各毫米级微域降解动态存在明显差异.当土壤中SD为1 mg · kg-1时,SD总降解趋势为:根中心区>近根区>远根区(T>5),具体为:T-0>T-2>T-1> T-3> T-4>T-5>远根区.当土壤中SD为5 mg · kg-1,近根区的平均总降解率为6.13%,明显高于根中心区与远根区,而根中心区(4.72%)与远根区(4.65%)两者之间差异不显著,对于近根区SD的降解高低顺序依次为:T-3>T-2>T-4>T-1>T-5.
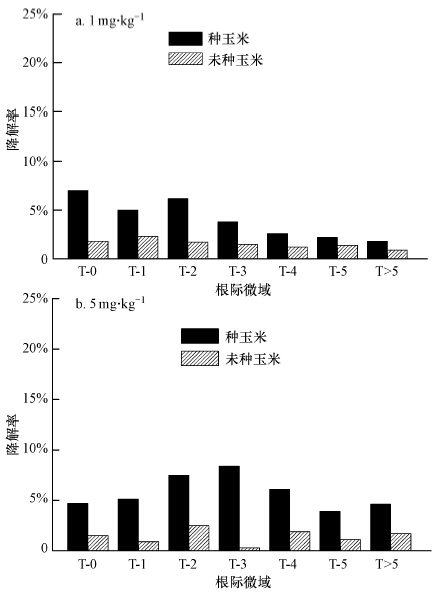 |
| 图 1 20 d时不同根-土界面SD降解率的变化(T-0:根中心区;T-1~T-5:近根区;T>5:远根区;数字编码表示距根中心区的距离(mm)) Fig.1 Sulfadiazine degradation rate on different rooT-soil interfaces(20 d) |
图 2为40 d时,种植/未种植玉米处理各毫米级根际微域土壤SD降解率.由图 2可知,当培养时间为40 d时,2个处理水平下,种植/未种植玉米各毫米级根际微域土壤SD的降解率均比第1次采样时有所提高.在实验第40 d,未种植玉米土壤对SD的平均降解率分别增加到4.37%(1 mg · kg-1)和3.94%(5 mg · kg-1).不过,从图 2可以看出,种植玉米处理的降解率仍显著高于未种植玉米处理.1 mg · kg-1 SD作用下,种植玉米处理各根际土壤对SD的平均降解率为12.06%,显著高于第1次采样时的降解率(4.32%),其中,距根中心区3 mm处(T-3)降解率最高,达到16.84%,总的降解趋势为:T-3> T-2> T-4> T-1> T-5> T-0>远根区(T>5).在5 mg · kg-1 SD作用下,SD在种植玉米各根际土壤的平均降解率为8.76%,低于低剂量SD胁迫下的降解率,说明在低剂量SD处理下,根际效应显著加速了SD的降解速度.与第1次采样结果相同,近根区的降解率要远高于根中心区和远根区,根中心区与远根区差异不显著,且近根区3 mm处(T-3)SD降解率最高(11.32%),SD在近根区降解率的具体高低顺序为:T-3> T-2> T-4> T-5> T-1.这与何艳等(2005)研究PCP在根际微域中的降解规律一致,其研究结果表明,PCP降解得到最大程度激发区域是距根中心区3 mm处,而不是根中心区和近根面1 mm或2 mm处,这与传统的植物营养研究中所揭示的营养因子根际梯度递减效应明显不同.
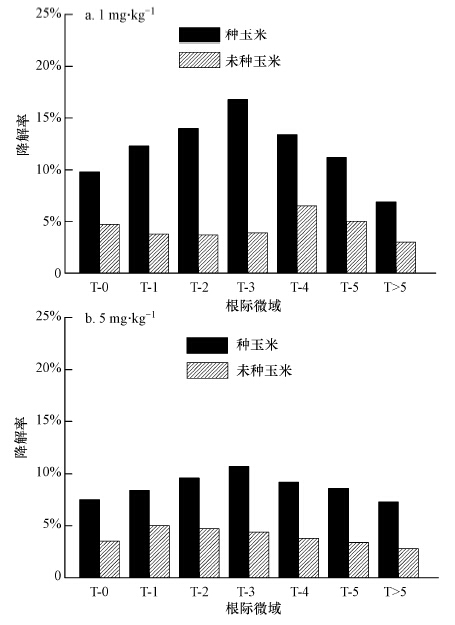 |
| 图 2 40 d时不同根-土界面SD降解率的变化 Fig.2 Sulfadiazine degradation rate on different rooT-soil interfaces at 40th day |
由图 3可知,当玉米生长到60 d时,无论是种植玉米还是未种植玉米处理各根际/非根际土壤对SD的降解率均达到最高.1 mg · kg-1 SD处理下,种植玉米各根际土壤的平均降解率为18.97%,T-3的SD降解率最高(24.1%),各根际土壤降解率差异减小,总的降解趋势为:T-3> T-2> T-0>T-1> T-4> T-5>远根区(T>5).5 mg · kg-1 SD作用下,各根际土壤SD平均降解率为13.97%,同样T-3的SD降解率最高(18.15%),各根际土壤降解率差异不显著.这可能是因为本试验采用恒温培养箱培养,当第3次采样时,高剂量的SD对玉米表现出一定的胁迫效应,导致植物根际效应对各根际土壤作用较小,因此,不同剂量水平对污染物降解差异不明显,各根际土壤之间的降解率差异亦不显著.由图 3可见,未种植玉米处理下,SD在各根际土壤的平均降解率分别提高至8.63%(1 mg · kg-1)和6.61%(5 mg · kg-1).
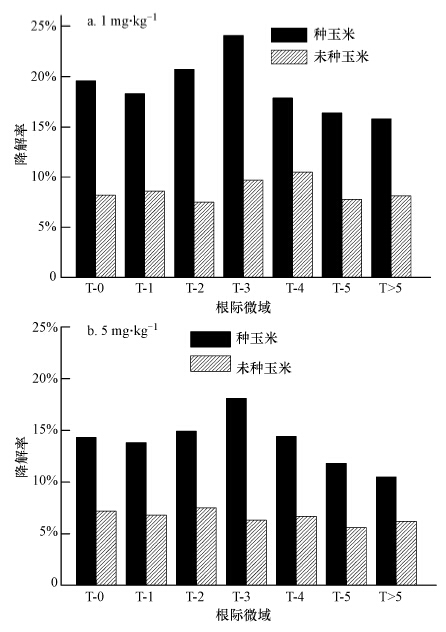 |
| 图 3 60 d时不同根-土界面SD降解率的变化 Fig.3 Sulfadiazine degradation rate on different rooT-soil interfaces at 60th day |
如图 4所示,1 mg · kg-1 SD污染胁迫下,随着培养时间的增加,各毫米级微域土壤4种有机酸总量呈增大趋势.低剂量SD作用下,土壤甲酸含量总体上均较少,其含量随着培养时间的延长而增多.根中心区甲酸含量最高(玉米生长20 d除外),在距根中心区1~5 mm的近根区,甲酸含量随距离增加而减少.1 mg · kg-1 SD污染胁迫下,玉米生长40 d、60 d时,土壤乙酸总量分别约为生长20 d时的4倍和6倍.在玉米生长20 d时,根中心区乙酸含量最高,距根中心区1~2 mm范围次之,在距根中心区3~5 mm范围内乙酸含量较少,且含量差异不显著.在玉米生长到第40 d和60 d时,各根际土壤中乙酸含量明显高于20 d时乙酸含量,且在1~5 mm近根区范围内随着距离的增加均呈先增加后降低的趋势,即T-3处土壤乙酸含量最高,分别为8.25 mg · kg-1和10.57 mg · kg-1.与乙酸相同,在玉米生长20 d时,苹果酸在根中心区含量最高,且在距根中心区3~5 mm范围内苹果酸含量没有显著差异(p>0.05).在玉米生长第40 d和60 d时,T-3处的苹果酸含量最高,在距根中心区1~3 mm范围内其含量随距离增加而增加,而3~5 mm范围内随距离增加而减少.不同培养时间之间,各根际土壤苹果酸差异显著(p<0.05),但与乙酸含量变化趋势不同的是,随着时间的增加,根际苹果酸的含量呈先增大后减小的趋势,即在玉米生长40 d时,苹果酸在各根际土壤中含量最高.
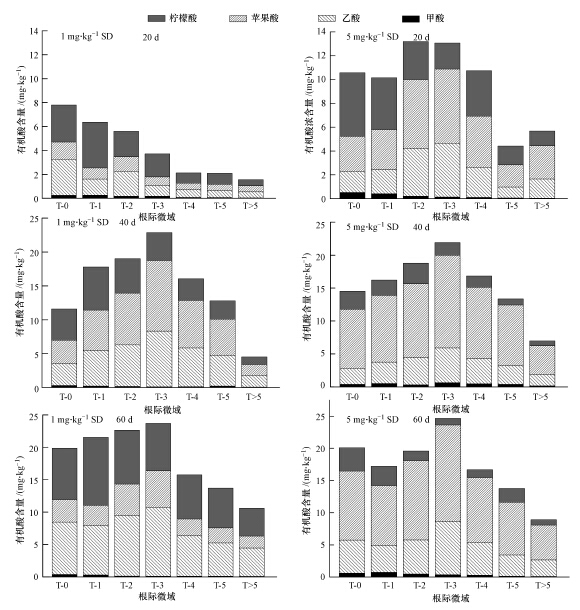 |
| 图 4 1 mg · kg-1和5 mg · kg-1 SD污染胁迫下有机酸动态变化 Fig.4 The concentration of organic acids in various sampling zones affected by 1 mg · kg-1 and 5 mg · kg-1 SD |
相对甲酸来说,玉米各根际微域土壤柠檬酸含量相对较高,最高达到10.47 mg · kg-1.从图 4可以看出,玉米根际土壤柠檬酸含量随着玉米生长时间的增加而增高.从生长20 d至60 d期间,各毫米级微域土壤中柠檬酸含量差异显著(p<0.05),且T-1处土壤柠檬酸含量最高,在1~5 mm近根区随着距离的增加其含量均呈降低趋势.
在2个SD处理水平下,玉米各毫米级根际微域土壤4种有机酸含量差异较大,且在高剂量SD胁迫下,不同时间、不同剖面4种有机酸变化趋势也不尽相同.5 mg · kg-1 SD处理下,各毫米级微域土壤中甲酸的含量亦较少,随着玉米生长时间的延长呈增加趋势(图 4).在玉米生长20 d时,根中心区的甲酸含量最高,随着距离的增加,其含量逐渐降低.当玉米生长到40 d和60 d时,距离根中心区5 mm处土壤中甲酸的含量升至最高,显著高出20 d时的含量.同样地,在5 mg · kg-1 SD污染胁迫下,玉米生长60 d时,其根际土壤中乙酸总量达到最高,约为生长40 d和20 d时的2倍和1.5倍,且均在T-3处含量最高,在距根中心区1~3 mm范围内其含量随距离增加而增加,而3~5 mm范围内随距离增加而减少.苹果酸变化趋势与乙酸相同,不同的是在生长40 d至60 d期间,距根中心区1~5 mm范围内苹果酸变化差异不显著.有别于其它3种有机酸,在高剂量SD胁迫下,柠檬酸在玉米根际土壤中总量随着培养时间的增加逐渐降低,由21.75 mg · kg-1(20 d)降至13.33 mg · kg-1(60 d).从玉米生长20 d至60 d整个培养周期,均是根中心区的柠檬酸含量最高,且其含量随着距离增加而逐渐降低.
将2个SD处理水平下,SD降解率对4种有机酸含量做图(图 5),并进行了回归分析(表 1).从表 1的R2值可以看出,在2个SD污染水平胁迫下,20 d、40 d和60 d时,SD降解率与乙酸和苹果酸之间有很好的拟合关系.这说明苹果酸和乙酸可能是影响SD在根际土壤中降解的关键因素之一.
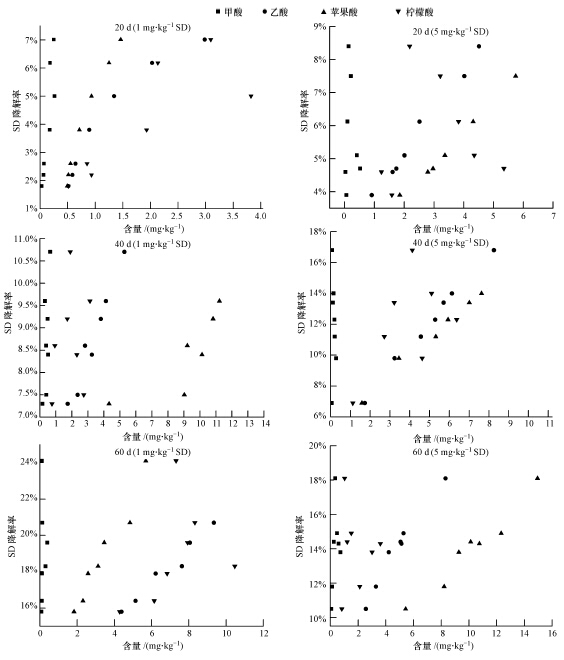 |
| 图 5 不同采样时期SD降解率与有机酸含量相关性分析 Fig.5 Correlation between degradation rate of sulfadiazine and concentrations of organic acids |
| 表 1 SD降解率与有机酸含量线性关系(y=ax+b) Table 1 The linear regression analysis between degradation rate of sulfadiazine and concentrations of organic acids(y=ax+b) |
玉米植株SD含量随时间的变化见图 6.在整个培养周期内,不同剂量SD胁迫下,其在地上部分的积累量低于检测限,说明进入土壤的SD主要被微生物降解,这与Bellin等(1990)研究一致.而根部SD含量在第40 d有所下降,而后又升高.这可能是由于从20 d到40 d,玉米生长旺盛,虽吸收的SD有所增加,但玉米根系生物量增加大于SD吸收量,所以对SD起到了稀释作用.而后又升高是因为随着时间的延长,吸收SD量增加,而玉米根系生物量的增加进入缓慢期,此时,玉米根系生物量增加小于SD的增加量,因此,在一定意义上,对SD含量起到了浓缩作用(Benizri et al., 2002).由图可知,SD在玉米不同部位含量极低(根部吸收SD量占土壤中SD量可以忽略不计),这说明土壤中SD含量的降低主要是由降解引起的,而非作物吸收.
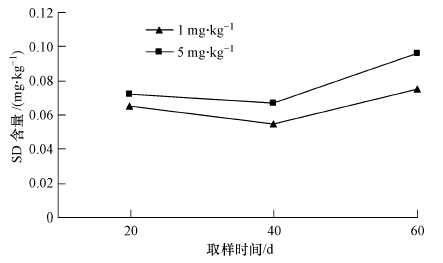 |
| 图 6 污染胁迫下玉米植株地下部SD含量(地上部分(芽、茎)SD含量未检出) Fig.6 The contamination of sulfadiazine in plant roots of the two spiked level treatments |
研究表明,根系分泌物在SD降解过程中起重要作用.试验期间,在2个剂量水平SD污染胁迫下,特别是玉米生长到40 d和60 d时,近根区SD降解速度最快.植物修复污染土壤是建立在根际效应和微生物活性基础上.在根际效应作用下,土壤本身的各种特性,包括土壤理化性状、微生物组成及活性等均会发生变化.诱导这些变化的根本原因在于根际环境中含有大量可利用碳源,而这些碳源是以根系分泌物等形式存在的(Anderson et al., 1993; Li et al., 2013),因根系分泌物作用的强弱及微生物生长及消耗,这些可利用碳源在土壤根际周围就会产生浓度梯度效应.这种效应对于诱导外源污染物在土壤根际快速消减过程的可能性,可作为污染土壤植物修复特别是根际修复的基本理论基础.
相关研究表明,种植植物可有效促进有机污染物的降解.陈波等(2006)采用根际袋实验研究了异丙甲草胺在根际与非根际土壤的降解特性,研究发现,根际丰富的微生物对异丙甲草胺的降解具有一定的促进作用,种植植物可有效促进异丙甲草胺的降解.Liste等(2006)选用9种植物进行根际修复芘的研究,结果发现,培养8周后,根际土壤中74%芘被降解,而非根际土壤中降解率不到40%.本研究也发现,在整个培养周期内,2个污染水平胁迫下,SD在种植玉米处理中的降解率均显著高于未种植玉米处理.这可能是由于植物根际分泌了大量碳水化合物、氨基酸、维生素等有机物,为微生物代谢提供了丰富的优良碳源,从而对微生物生长具有刺激作用(Singh et al., 2004),促进了微生物生长.因此,根际微域环境往往聚集着大量的具有高活性的微生物群落(Kidd et al., 2008),增强了被截留的有机污染物的微生物降解效应.
在本研究中发现,SD的最大消减水平发生在距离根室3 mm的近根区,而不是在距根系表面最近的根室或者1~2 mm处,这和有机酸在此区域达到最大丰度一致.这种外源性有机污染物消减的根际效应明显与传统植物营养中揭示的营养因子根际梯度递减效应(通常距根表距离大于2 mm以上的区域,含量随着距离的增加呈下降趋势)不同(Joner et al., 1995),这可能与根系分泌物主动营造并优化的环境密切相关.根系分泌物组成及数量的变化对外源污染物降解存在显著影响,其作用机制主要表现在根系分泌物对根际微生物的生物有效性方面.在根际土壤中,根系生长会诱导产生大量根系分泌物,这些分泌物可作为微生物生长的碳源.而这种碳源对有机物降解存在两种相反作用:一方面,根系分泌物可以作为微生物生长的基质供其代谢所用,从而激发微生物的活性并促进有机物在土壤中的消减;另一方面,作为与有机物相互竞争的另一种碳源,根系分泌物的微生物可利用性更大,在提供微生物生长代谢所需能源方面表现出强于有机物的竞争性,由此又抑制有机物在土壤中的消减(He et al., 2005; Ding et al., 2009).因此,根系分泌物和有机物对微生物的生物有效性及其强弱差异,是引起近根际各毫米级微域土壤内有机物降解过程产生变异的重要原因之一.本研究中,在距离根室3 mm的近根际微域内,可能存在最利于SD降解的根系分泌物水平,在这种水平微生物活性得到最大程度激发同时又使其本身SD的竞争效应降到最低.相反,根系分泌物水平不足或过量,都会导致SD降解率降低.如果根系分泌物水平不足(4 mm或5 mm处),微生物活性不能达到最大,影响SD降解.如果根系分泌物水平过量(1 mm或2 mm处),SD的竞争效应就会加强,亦不利于其自身降解.
5 结论(Conclusions)1)根际效应在一定程度上可促进SD消减,且距根系距离不同,SD消减水平存在差异,在2个SD污染水平下趋势一致,即近根际>根室>远根际;SD的最大消减水平发生在距根室3 mm的近根区.
2)在整个培养周期内,不同剂量SD胁迫下,其在地上部分的积累量低于检测限,而根部对SD吸收量在第40 d有所下降,而后又升高.
3)通过对不同剂量SD胁迫下有机酸响应的相关分析得出,苹果酸和乙酸是影响SD在根际土壤中降解的关键因素之一.
| [1] | Ande rson T A, Guthrie E A, Walton B T. 1993. Bioremediation in the rhizosphere[J]. Environment Science and Technology, 27(13): 2630-2636 |
| [2] | Bais H P, Weir T L, Perry L G, et al. 2006. The role of root exudates in rhizosphere interactions with plants and other organisms[J]. Annual Review of Plant Biology, 57: 233-266 |
| [3] | Baran W, Sochacka J, Wardas W. 2006. Toxicity and biodegradability of sulfonamides and products of their photo catalytic degradation in aqueous solutions[J]. Chemosphere, 65(8): 1295-1299 |
| [4] | Bellin C A, O'Connor G A. 1990. Plant uptake of pentachlorophenol from sludge-amended soils[J]. Journal of Environmental Quality, 19(3): 598-602 |
| [5] | Benizri E, Dedourge O, Dibattista L C, et al. 2002. Effect of maize rhizodeposits on soil microbial community structure[J]. Applied Soil Ecology, 21(3): 261-265 |
| [6] | Bertin C, Yang X H, Weston L A. 2003. The role of root exudates and allelochemicals in the rhizosphere[J]. Plant and Soil, 256(1): 67-83 |
| [7] | 陈波, 徐冬梅, 吴军林, 等. 2006. 异丙甲草胺对根际土壤微生物数量的影响及其在根际环境中的降解研究[J]. 农业环境科学学报, 25(4): 898-902 |
| [8] | 陈杖榴. 2005. 兽用化学药物研发动向[J]. 中国牧业通讯, (8): 26-31 |
| [9] | Ding N, Guo H C, Hayat T, et al. 2009. Microbial community structure changes during Aroclor 1242 degradation in the rhizosphere of ryegrass (Lolium multiflorum L.) [J]. FEMS Microbiology Ecology, 70(2): 305-314 |
| [10] | Elena M C, Carmen G B, Scharf S, et al. 2007. Environment monitoring study of selected veterinary antibiotics in animal manure and soils in Austria[J]. Environmental Pollution, 148(2): 570-579 |
| [11] | Hartmann A, Rothballer M, Schmid M. 2008. Lorenz Hiltner, a pioneer in rhizophere microbial ecology and soil bacteriology research[J]. Plant and Soil, 312(1/2): 7-14 |
| [12] | He Y, Xu J M, Tang C X, et al. 2005. Facilitation of pentachlorophenol degradation in the rhizosphere of ryegrass[J]. Soil Biology and Biochemmistry, 37(11): 2017-2024 |
| [13] | Hinsinger P, Plassard C, Tang C X, et al. 2003. Origins of root-mediated PH changes in the rhizosphere and their responses to environmental constraints: A review[J]. Plant and Soil, 248(1/2): 43-59 |
| [14] | Jay J B, Jodi R S. 1995. Biodegradation of phenol, 2,4-DCP, 2,4-D, and 2,4,5-T in field-collected rhizosphere and nonrhizosphere soils[J]. Journal of Environmental Quality, 24(4): 782-785 |
| [15] | 金彩霞, 周启星, 樊静, 等. 2007. 镉与豆磺隆复合胁迫下小麦根—土界面镉形态的变化[J]. 应用生态学报, 18(7): 1498-1504 |
| [16] | Joner E J, Magid J, Gahoonia T S, et al. 1995. P depletion and activity of phosphatases in the rhizosphere of mycorrhizal and non-mycorrhizal cucumber (Cucumis sativus L.) [J]. Soil Biology and Biochemistry, 27(9): 1145-1151 |
| [17] | Kidd P S, Prieto-Fernández A, Monterroso C, et al. 2008. Rhizosphere microbial community and hexachlorocyclohexane degradative potential in contrasting plant species[J]. Plant and Soil, 302(1/2): 233-247 |
| [18] | Li T Q, Liang C F, Han X, et al. 2013. Mobilization of cadmium by dissolved organic matter in the rhizosphere of hyperaccumulator Sedum alfredii[J]. Chemosphere, 91(7): 970-976 |
| [19] | Liste H H, Felgentreu D. 2006. Crop growth, culturable bacteria, and degradation of Petrol hydrocarbons (PHCs) in a long-term contaminated field soil[J]. Applied Soil Ecology, 31(1/2)1: 43-52 |
| [20] | Moritsuka N, Yanai J, Kosaki T. 2000. Effect of plant growth on the distribution and forms of soil nutrients in the rhizosphere[J]. Soil Science and Plant Nutrition, 46(2): 439-447 |
| [21] | Nichols T D, Wolf D C, Rogers H B, et al. 1997. Rhizosphere microbial populations in contaminated soils[J]. Water, Air and Soil Pollution, 95(1/4): 165-176 |
| [22] | Paterson S, Mackay D, Tam D, et al. 1990. Uptake of organic chemicals by plants: A review of processes, correlations and models[J]. Chemosphere, 21(3): 297-331 |
| [23] | Singh B K, Millard P, Whiteley A S, et al. 2004. Unravelling rhizosphere-microbial interactions: opportunities and limitations[J]. Trends in Microbiology, 12(8): 386-393 |
 2014, Vol. 34
2014, Vol. 34


