2. 长沙矿冶研究院, 长沙 410012;
3. 湖南省发展和改革委员会, 长沙 410004
2. Changsha Research Institute of Mining and Metallurgy, Changsha 410012;
3. Development and Reform Commission of Hunan Province, Changsha 410004
均相Fenton和类Fenton反应可有效降解水中的多种难降解有机污染,但也存在一定的不足(Fernandez et al., 1999; Feng et al., 2004),尤其是出水中含有大量的铁离子,不仅造成水中色度增加,还产生了大量的铁泥渣,且催化剂不能重复使用.而多相Fenton和多相类Fenton能够克服以上缺点,近年来成为人们研究Fenton反应的热点.这些研究主要关注2类类Fenton催化剂:一是铁、锰、铈等具有可变价态的金属氧化物;二是通过载体材料负载铁化合物,载体材料主要包括Nafion 膜(Parra et al., 2004)、聚乙烯膜(Dhananjeyan et al., 2001)、树脂(Cheng et al., 2004; 赵超等,2007; Zhao et al., 2008)、多孔硅(Martínez et al., 2005)、粘土(Chen et al., 2006)、氧化铝(Muthukumari et al., 2009)、碳(Ramirez et al., 2007)等.在这些多相Fenton和多相类Fenton反应中,有机污染物能够被有效降解,催化剂可在较宽的pH值范围内重复使用,但仍存在催化活性较低等不足.纳米材料由于比表面积大、表面能高而表现更高的催化活性,而粒径均一、分散性的纳米颗粒催化活性和选择性更高.为了克服多相Fenton催化剂活性较低的缺点,近年来,纳米多相Fenton催化剂已引起了人们的极大兴趣,特别是磁性纳米四氧化三铁因价格相对便宜,有磁性容易分离而受到了特别关注.但纳米四氧化三铁存在磁偶极之间的相互作用,容易因团聚而导致活性降低.因此,研究与建立稳定化磁性纳米粒子的策略与方法具有十分重要的理论与实际意义.碳纳米管具有耐水性、中空管状结构、高比表面积、良好的化学稳定性、特殊的电子结构,是理想的催化剂载体材料(Deng et al., 2012).本课题组与其他一些研究均表明,碳纳米管作为载体,具有协同效应,能增强催化剂的活性(Planeix et al., 1994; Juan et al., 2007; Deng et al., 2012).
染料与印染废水因其含有残余染料、水量大、浓度变化大、种类多、污染组分复杂且色度、化学需氧量和生化需氧量均较高等特点,成为国内外难处理的工业废水之一.因此,本研究在课题组前期研究的基础上,利用溶剂热合成方法合成碳纳米管负载纳米四氧化三铁复合物(Fe3O4/MWCNTs),以此作为催化剂,以染料亚甲基蓝(MB)为降解对象,研究该催化剂对亚甲基蓝溶液的催化降解特性及其影响因素,以期为该新型催化剂的应用奠定基础.
2 材料与方法(Materials and methods) 2.1 仪器及材料仪器:不锈钢反应釜(80 mL),DF-101S焦热式恒温加热磁力搅拌器,SHB-Ⅲ 循环式多用真空泵,2XZ(S)-2型旋片式真空干燥箱,PB-10普及型玻璃膜电极pH测量计,KQ-250DE型数控超声波清洗器,JES-FA200波谱仪(JEOL),UV-2401PC紫外可见分光光度计(日本,岛津).
试剂:乙二醇、亚甲基蓝、30%过氧化氢购自国药集团化学试剂有限公司,乙酰丙酮铁购自Alfa Aesar 公司,以上试剂均为分析纯试剂;多壁碳纳米管(MWCNTs)(纯度>95%,长度10~20 μm,外径30~50 nm,内径 5~12 μm,比表面积>60 m2 · g-1,中国科学院成都有机化学有限公司);其它试剂均为分析纯试剂(北京化学试剂公司生产).
2.2 试验方法Fe3O4/MWCNTs由实验室自制.合成具体步骤如下:称取0.1 g酸处理后的MWCNTs、0.2 g乙酰丙酮铁,并与乙二醇和水的混合溶剂混合,之后加入到不锈钢反应釜中,通入氮气排除氧气,封盖.然后将其放在油浴锅中,加热到200 ℃,保温30 min,再继续加热到260 ℃,保温30 min.反应完成后,从油浴锅中取出反应釜自然冷却至室温,加入乙醇洗涤4~5次,80 ℃真空干燥24 h备用.
MB降解试验:将一定量的Fe3O4/MWCNTs催化剂加到MB溶液中,先搅拌20 min,然后加入一定量的H2O2启动降解反应,每隔5 min取样,于665 nm波长处测定吸光度.分别考察溶液pH、H2O2浓度、催化剂用量、反应温度、MB溶液浓度等因素对降解率的影响,并按照公式(1)计算MB的降解率D.
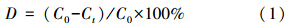
式中,C0为MB初始浓度(mmol · L-1),Ct为t时刻的MB的浓度(mmol · L-1).
MB降解的UV-Vis光谱变化:MB降解过程中不同时刻的UV-Vis光谱变化采用UV-2401PC紫外可见分光光度计(日本,岛津)测量.
重复性试验:催化剂每次降解MB后利用磁铁收集,洗涤、干燥,再次用于降解试验.
2.3 Fe3O4/MWCNTs样品的表征采用JSM-6301F型扫描电镜(SEM)表征微观形貌,X-射线衍射采用D/MAX-TTRIII型衍射仪(日本).
3 结果与分析(Results and analysis) 3.1 Fe3O4/MWCNTs表征负载铁氧化物后MWCNTs的特征峰(2θ=26.0°)仍然存在.图 1为Fe3O4/MWCNTs样品的XRD图.从图中可以看出,负载铁氧化物后MWCNTs的特征峰仍然存在,说明硝酸氧化处理后的MWCNTs的石墨结构没有被破坏;而在2θ=18.3°、30.1°、35.4°、37.2°、43.1°、53.3°、56.9°和62.5°处出现衍射峰,其分别归属于立方晶Fe3O4的(111)、(220)、(311)、(222)、(400)、(422)、(511)和(440)晶面的衍射(JCPDS 19-0629);乙酰丙酮铁被乙二醇和水的混合溶剂还原得到纳米Fe3O4.
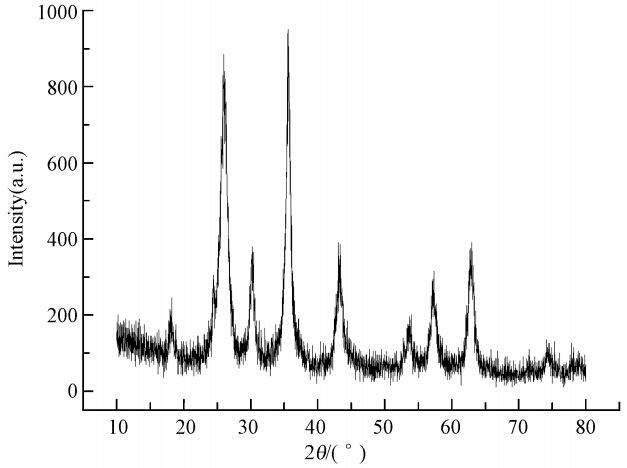 |
| 图 1 Fe3O4/MWCNTs纳米复合物的XRD图 Fig. 1 XRD patterns of Fe3O4/MWCNTs compositions |
图 2为Fe3O4/MWCNTs的SEM图.从图中可以看出,Fe3O4纳米颗粒能够均匀地分散在碳纳米管上而没有团聚,说明碳纳米管载体能很好地分散具有磁性的Fe3O4,增加纳米Fe3O4的比表面积,从而有利于增加Fe3O4/MWCNTs的催化活性.
 |
| 图 2 Fe3O4/MWCNTs的SEM图 Fig. 2 SEM image of Fe3O4/MWCNTs |
研究发现,溶液pH会影响催化剂表面电荷特性、吸附行为和电子转移能力等(Kim et al., 2012),从而影响其催化降解率.图 3为在催化剂投量500 mg · L-1、H2O2浓度10 mmol · L-1、反应温度25 ℃、反应时间30 min的条件下,0.2 mmol · L-1 的MB在不同pH值下的降解率.从图中可明显看到,pH对MB的降解率有一定影响.当溶液pH=3.0时,MB降解率为98.9%;pH=3.5时,MB降解率为99.1%;随溶液pH的进一步增加,MB的降解率逐渐降低,但都维持在较高水平,如当溶液pH=4.5时,MB的降解率为87.2%,pH=8.0时,MB的降解率为64.2%.据文献报道(Si et al., 2010),在pH值高于4的情况下,纳米Fe3O4由于形成水合铁和水合亚铁配合物,其催化能力明显减弱.Fe3O4通过MWCNTs负载以后,一方面,MWCNTs充当快速电子转移通道,有利于增强Fe3O4/MWCNTs催化活性(Yu et al., 2011);另一方面,载体MWCNTs表面电势发生了改变,对阳离子型的染料MB容易接近催化活性位.因此,即使溶液的pH为8的条件下,催化剂也展示较高的催化活性.
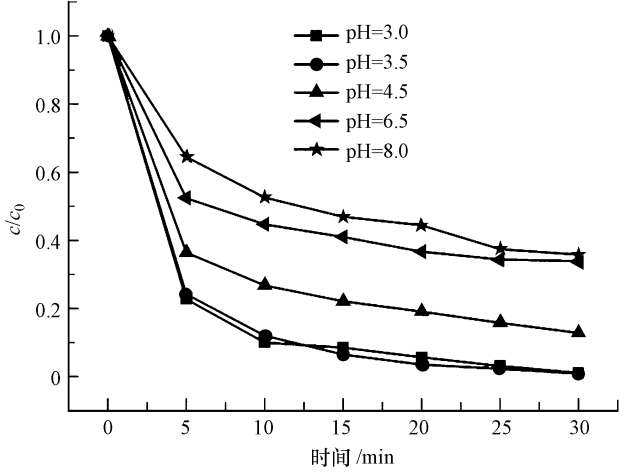 |
| 图 3 MB降解率随不同pH值的变化关系 Fig. 3 Variation of degradation efficiency of MB with different pH values |
图 4为催化剂投量500 mg · L-1、反应时间30 min、反应温度25 ℃、溶液pH=3.5的条件下,0.2 mmol · L-1 MB溶液的降解率随H2O2浓度变化的曲线.从图中可以看出,H2O2的浓度从4 mmol · L-1 增加到10 mmol · L-1时,MB的降解率从74.3%增加到99.1%,表明MB的降解率随着H2O2浓度的增大而增大;当H2O2的浓度超过10 mmol · L-1时,MB的降解率不再增加反而略有下降,但仍维持在较高的水平(H2O2浓度为12 mmol · L-1时,降解率为97.3%).这可能是因为H2O2浓度较低时,催化反应产生· OH自由基的量随H2O2浓度的增加而增加;但当H2O2的浓度高于临界值时,由于产生的· OH能被过量的H2O2捕获生成氧化还原电位更低的过氧自由基HO2 ·(式(2)~(4),Buxton et al., 1988),反而减少了· OH自由基的数目.虽然反应生成的HO2 · 自由基(氧化还原电位1.7 V)也是一种氧化自由基,但它的氧化能力大大低于· OH 自由基,从而影响了MB的降解率.因此,在本实验条件下,最佳的H2O2浓度为10 mmol · L-1.
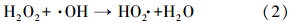
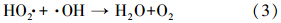
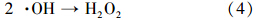
 |
| 图 4 H2O2浓度对MB降解率的影响 Fig. 4 Effect of H2O2 dosages on the degradation of MB |
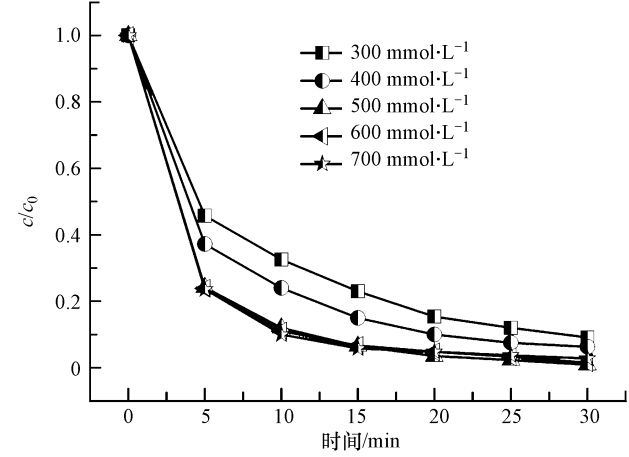
图 5为在pH=3.5、H2O2浓度10 mmol · L-1、反应温度25 ℃、反应时间30 min的条件下,0.2 mmol · L-1 MB降解率随不同催化剂用量的变化关系.从图可以看出,催化剂用量为300 mg · L-1时,MB的降解率为90.9%;催化剂用量为400 mg · L-1时,MB降解率上升到93.7%;催化剂质量为500 mg · L-1时,MB降解率上升到99.1%;表明MB的降解率随着催化剂用量的增加而提高.但再增加催化剂的用量(大于500 mg · L-1),MB的降解率变化不大甚至有所下降,如催化剂用量为600 mg · L-1时,MB的降解率为98.5%,低于500 mg · L-1时的降解率.本实验确定的催化剂最佳用量为500 mg · L-1.一方面可能由于催化剂的用量增加,催化活性位增加,降解速度提高;但另一方面由于催化剂的用量增加,催化活性位也相应增加,产生了大量的· OH,而· OH自由基的寿命不足1 ns,且活性高,来不及与溶液中的MB反应,· OH与· OH之间会很快发生反应而淬灭,从而减少了反应体系中· OH的浓度,这样反而不利于MB的降解.其主要反应如下(Lei et al., 2007):
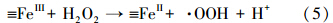
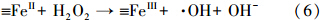
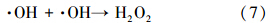
 |
| 图 5 催化剂用量对MB降解率的影响 Fig. 5 Effect of catalyst dosage on the degradation of MB |
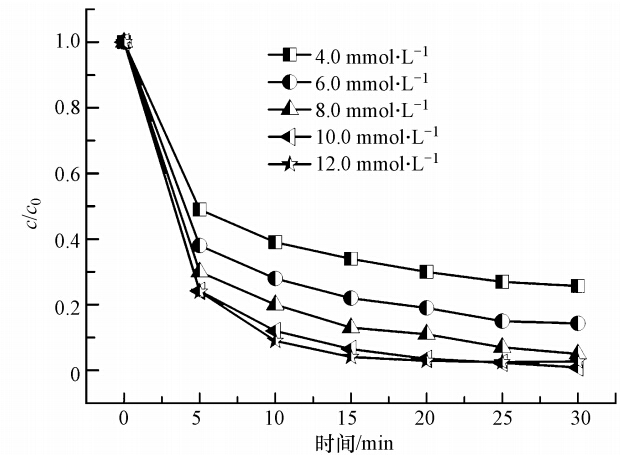
在催化剂用量500 mg · L-1、H2O2浓度10 mmol · L-1、溶液pH=3.5、反应温度25 ℃、反应时间30 min的条件下,研究了不同浓度MB的降解情况,结果见图 6.可见,催化剂对于0.15~0.50 mmol · L-1的MB染料均有较高的降解率,随着降解时间的增加,MB的降解率也不断增加.但当MB浓度从0.15 mmol · L-1增加为0.50 mmol · L-1时,MB在5 min时的降解率从79.0%下降为54.4%,表明MB的降解率随着MB染料浓度的升高而下降.这可能是因为在催化剂量及H2O2一定的情况下,可近似认为水溶液中产生的羟基自由基的量是一定的,因此,随着反应物总量的提高,用于进攻发色基团的· OH自由基的量不足以完全打断MB染料的发色基团;另一方面,由于染料的脱色反应主要发生在催化剂表面区域,随着染料浓度的升高,MB占据的催化剂表面的活性位越多,不利于催化剂催化活化H2O2,从而使得体系中羟基自由基的产率降低,导致MB降解率降低.
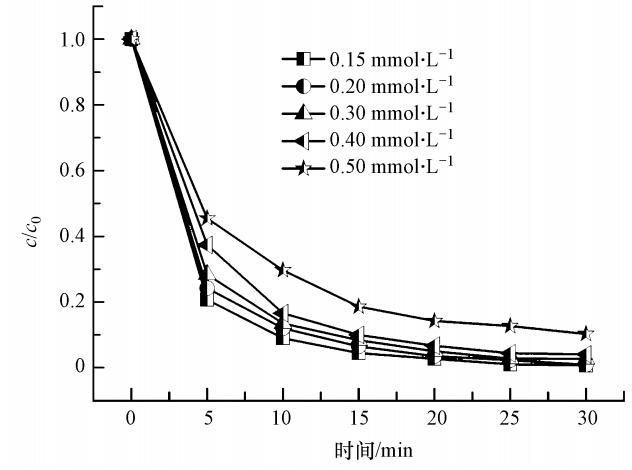 |
| 图 6 初始浓度对MB降解率的影响 Fig. 6 Effect of initial concentration of dye on the degradation of MB |
一些研究表明,Fenton反应温度是影响有机物降解的重要因素,一方面温度升高会增加产生· OH的速率,从而加快对有机物的降解;另一方面,升高温度也会加快H2O2自分解为氧气和水的速率(Wu et al., 2010).为此,本文在催化剂用量500 mg · L-1、H2O2浓度10 mmol · L-1、MB溶液浓度0.2 mmol · L-1,pH=3.5、反应时间30 min的条件下,选择了20~35 ℃的温度范围来研究反应温度对降解率的影响,结果见图 7.由图 7可见,随着反应温度的增加,Fe3O4/MWCNTs降解MB的降解率也不断地增加.反应5 min时,20 ℃条件下MB的降解率为72.0%,而35 ℃条件下MB的降解率增加到91.05%.这说明反应温度对MB降解率的影响非常明显.Guedes等(2003)采用Fenton试剂处理焦化废水,发现降解率最佳的温度为30 ℃.在本实验条件下,温度升高有利于Fe3O4/MWCNTs催化H2O2产生羟基自由基,从而加快MB的降解.
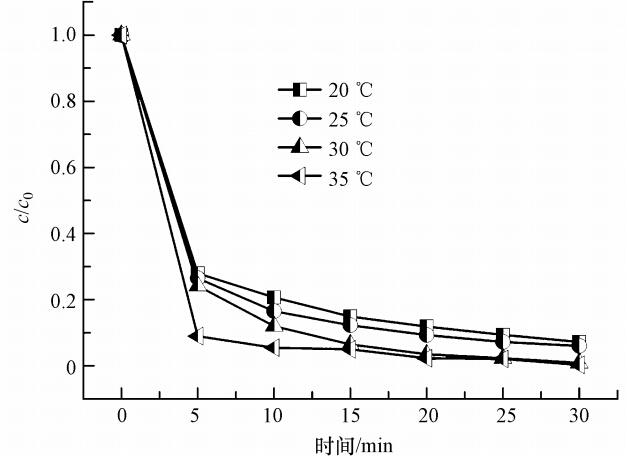 |
| 图 7 温度对MB降解率的影响 Fig. 7 Effect of temperature on the degradation of MB |
印染废水中普遍存在着许多无机阴离子,如Cl-、SO2-4和CO2-3等.由于羟基自由基具有无选择性,阴离子能俘获羟基自由基从而影响对染料的降解.为了研究无机阴离子对MB降解的影响,在MB中分别添加5 mmol · L-1 的NaNO3、NaCl、Na2SO4、Na2CO3,由于Na+对Fenton反应没有影响,因此,这些化合物对降解MB的影响可以归因于相应的无机阴离子.
图 8为保持MB浓度0.2 mmol · L-1、pH=3.5、反应温度25 ℃、H2O2和催化剂用量分别为10 mmol · L-1和500 mg · L-1的条件不变,分别添加5 mmol · L-1的NaNO3、NaCl、Na2SO4、Na2CO3,反应30 min后MB的降解率.从图中可以看出,加入NO-3和Cl-后,MB的降解效率分别为94.3%和93.2%,而不加NO-3和Cl-的条件下,MB的降解率为99.1%,说明其它降解条件不变的情况下,加入NO-3和Cl-后,MB的降解率分别下降了4.8%和5.9%.而SO2-4和CO2-3对MB的降解影响相对较大,MB的降解率分别为85.6%和81.6%,分别下降13.5%和17.3%.究其原因,主要是由于Cl-、NO-3、SO2-4和CO2-3都能与羟基自由基发生如式(8)~(11)所示的反应,可以消耗羟基自由基,同时产生相应的自由基.而对于氯离子来说,E0(Cl ·/Cl-)= 2.5 V,而对CO2-3来说,E0(CO· -3/CO32-)= 1.85 V,可能形成的CO· -3不足以氧化有机底物.
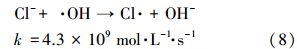
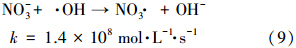
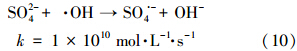
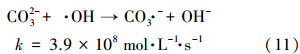
 |
| 图 8 加入NO-3、Cl-、SO2-4、CO2-3对MB降解的影响 Fig. 8 Effect of NO-3,Cl-,SO2-4 and CO2-3 on the degradation of MB |
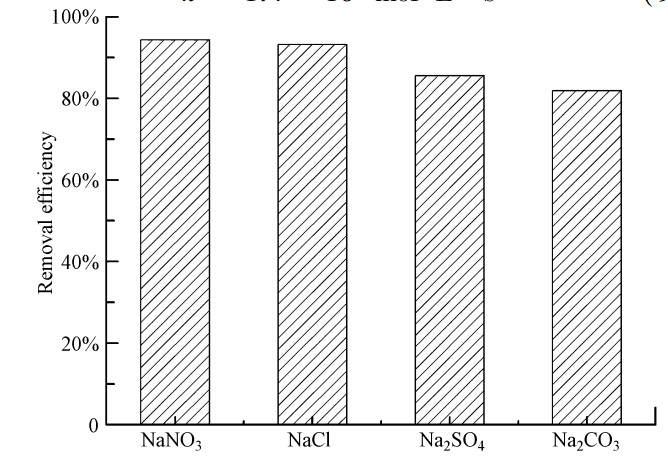
亚甲基蓝为高共轭的阳离子染料,化学性质稳定很难被降解.图 9显示了催化剂为500 mg · L-1,H2O2为10 mmol · L-1,MB为0.2 mmol · L-1,溶液pH值为3.5,反应温度为25 ℃的条件下,降解过程中MB的UV-Vis光谱变化图.可见,MB的紫外可见吸收光谱分别在246、292、610、665 nm处有4个特征吸收峰.随着反应的进行,亚甲基蓝在246、292、610、665 nm处的特征吸收峰强度逐渐减弱,但峰型和位置基本不变,当反应30 min后所有的特征峰都基本消失,同时也没有出现新的吸收峰.吸附剂表面的颜色消失,由蓝色恢复为原来颜色,说明MB的降解并不是被吸附而是由于MB发色基团被破坏发生降解.
 |
| 图 9 Fe3O4/MWCNTs降解亚甲基蓝的UV-Vis图 Fig. 9 The UV-Vis spectral changes of MB during the degradation process |
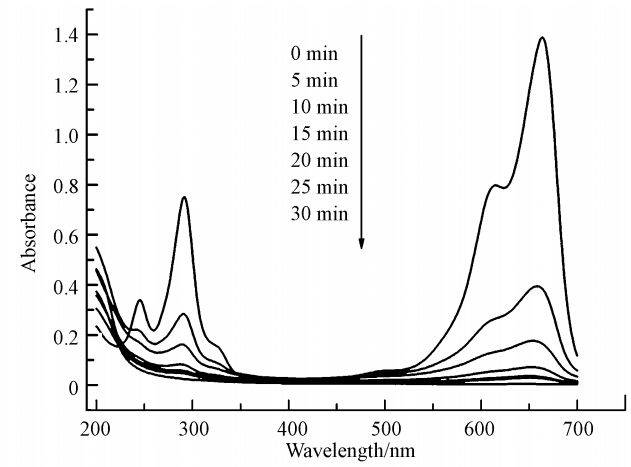
采用固定化催化剂与多相催化体系的主要目的之一是便于反应后催化剂的回收与再利用.本研究合成的Fe3O4/MWCNTs是磁性催化剂,很容易利用磁性而分离.在溶液中催化剂质量500 mg · L-1、MB浓度0.2 mmol · L-1、pH=3.5、H2O2浓度10 mmol · L-1、反应温度25 ℃、反应时间30 min的条件下,研究催化剂的重复使用情况,结果如图 10所示.从图中可以看出,使用第1次时的降解率为99.1%,到第8次时降解率仍达80.9%,在重复使用8次后活性没有明显降低.说明Fe3O4/MWCNTs作为多相Fenton-like催化剂具有良好的重复使用效果.
 |
| 图 10 重复使用过程中催化降解MB的降解率 Fig. 10 Degradation efficiency of MB catalyzed by recycled Fe3O4/MWCNTs |
Fenton反应的实质是能否产生· OH自由基,测定· OH 的方法一般可以通过电子自旋共振(ESR)仪直接测定.ESR是测定短寿命自由基的一种非常有效的现代分析技术.将不饱和抗磁性物质(自旋捕捉剂)DMPO加入到Fe3O4/MWCNTs与H2O2体系中,生成寿命较长的自旋加合物而进行自由基的测定(式(2)).
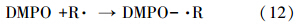
图 11显示了自旋捕获DMPO-· OH加合物的ESR波谱.从图中可以看出,反应体系中不加Fe3O4/MWCNTs时,EPR谱图没有信号出现;而有催化剂存在的条件下,EPR谱图显示有1个四重峰,其强度1∶2∶2∶1,其明显的特征峰为DMPO-· OH加合物的ESR波谱的特征信号峰.这说明Fe3O4/MWCNTs能活化H2O2产生羟基自由基(Jiang et al., 1993),该反应体系涉及到· OH自由基的产生和参与反应,· OH为该体系催化反应的主要氧化中间体.
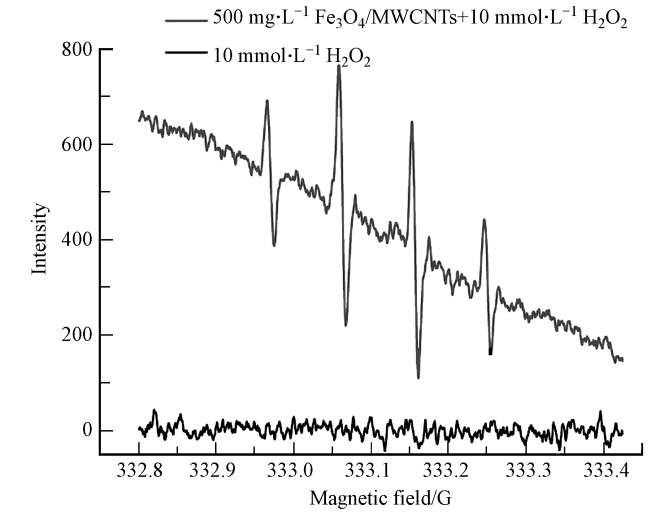 |
| 图 11 DMPO捕获羟基自由基ESR谱图 Fig. 11 DMPO spin-trapping ESR spectra of hydroxyl radicals |
1)在pH值3~8的范围内,以碳纳米管(MWCNTs)为载体制备的Fe3O4/MWCNTs催化剂都能有效催化降解MB,最佳pH值为3.5.
2)过氧化氢的初始浓度越高,反应速率越快,但在本实验条件下,达到10 mmol · L-1时,MB降解率最高,随着H2O2的增加,MB降解率略有下降.
3)当反应温度为25 ℃时,Fe3O4/MWCNTs催化剂对0.2 mmol · L-1 MB染料降解的最佳条件为:pH=3.5,催化剂用量为500 mg · L-1,H2O2浓度为10 mmol · L-1.
4)催化剂重复使用后仍然具有较好的催化活性,说明Fe3O4在MWCNTs表面负载比较牢固,催化剂具有良好的反复使用性能.
| [1] | Buxton G V,Greenstock C L,Helman W P,et al.1988.Critical Review of rate constants for reactions of hydrated electrons,hydrogen atoms and hydroxyl radicals (·OH/·O-) in Aqueous Solution[J].Journal of Physical and Chemical Reference Data,17(2):513-886 |
| [2] | Chen J X,Zhu L Z.2006.Catalytic degradation of Orange II by UV-Fenton with hydroxyl-Fe-pillared bentonite in water[J].Chemosphere,65(7):1249-1255 |
| [3] | Cheng M M,Ma W H,Li J,et al.2004.Visible-light-assisted degradation of dye pollutants over Fe(III)-loaded resin in the presence of H2O2 at neutral pH values[J].Environmental Science & Technology,38(5):1569-1575 |
| [4] | Deng J H,Wen X H,Wang Q L.2012.Solvothermal in situ synthesis of Fe3O4-multi-walled carbon nanotubes with enhanced heterogeneous Fenton-like activity[J].Materials Research Bulletin,47(11):3369-3376 |
| [5] | Dhananjeyan M R,Mielczarski E,Thampi K R,et al.2001.Photodynamics and surface characterization of TiO2 and Fe2O3 photocatalysts immobilized on modified polyethylene films[J].The Journal of Physical Chemistry B,105(48):12046-12055 |
| [6] | Feng J,Hu X,Yue P L.2004.Novel bentonite clay-based Fe-nanocomposite as a heterogeneous catalyst for photo-Fenton discoloration and mineralization of Orange II[J].Environmental Science & Technology,38(1):269-275 |
| [7] | Fernandez J,Bandara J,Lopez A,et al.1999.Photoassisted Fenton degradation of nonbiodegradable azo dye (Orange II) in Fe-free solutions mediated by cation transfer membranes[J].Langmuir,15(1):185-192 |
| [8] | Guedes A M F M,Madeira L M P,Boaventura R A R,et al.2003.Fenton oxidation of cork cooking wastewater-overall kinetic analysis[J].Water Research,37(13):3061-3069 |
| [9] | Jiang J J,Bank J F,Scholes C P.1993.Subsecond time-resolved spin trapping followed by stopped-flow EPR of Fenton reaction products[J].Journal of the American Chemical Society,115(11):4742-4746 |
| [10] | Juan J C,Jiang Y J,Meng X J,et al.2007.Supported zirconium sulfate on carbon nanotubes as water-tolerant solid acid catalyst[J].Materials Research Bulletin,42(7):1278-1285 |
| [11] | Kim H J,Phenrat T,Tilton R D,et al.2012.Effect of kaolinite,silica fines and pH on transport of polymer-modified zero valent iron nano-particles in heterogeneous porous media[J].Journal of Colloid and Interface Science,370(1):1-10 |
| [12] | Lei L C,Hao X L,Zhang X W,et al.2007.Wastewater treatment using a heterogeneous magnetite (Fe3O4) non-thermal plasma process[J].Plasma Processes and Polymers,4(4):455-462 |
| [13] | Martínez F,Calleja G,Melero J A,et al.2005.Heterogeneous photo-Fenton degradation of phenolic aqueous solutions over iron-containing SBA-15 catalyst[J].Applied Catalysis (B:Environmental),60(3/4):181-190 |
| [14] | Muthukumari B,Selvam K,Muthuvel I,et al.2009.Photoassisted hetero-Fenton mineralisation of azo dyes by Fe(II)-Al2O3 catalyst[J].Chemical Engineering Journal,153(1/3):9-15 |
| [15] | Parra S,Nadtotechenko V,Albers P,et al.2004.Discoloration of azo-dyes at biocompatible pH-values through an Fe-histidine complex immobilized on nafion via Fenton-like processes[J].The Journal of Physical Chemistry B,108(14):4439-4448 |
| [16] | Planeix J M,Coustel N,Coq B,et al.1994.Application of carbon nanotubes as supports in heterogeneous catalysis[J].Journal of the American Chemical Society,116(17):7935-7936 |
| [17] | Ramirez J H,Maldonado-Hódar F J,Pérez-Cadenas A F,et al.2007.Azo-dye orange II degradation by heterogeneous Fenton-like reaction using carbon-Fe catalysts[J].Applied Catalysis (B:Environmental),75(3/4):312-323 |
| [18] | Si Y B,Fang G D,Zhou J,et al.2010.Reductive transformation of 2,4-dichlorophenoxyacetic acid by nanoscale and microscale Fe3O4 particles[J].Journal of Environmental Science and Health,Part B,45(3):233-241 |
| [19] | Wu Y Y,Zhou S Q,Qin F H,et al.2010.Modeling the oxidation kinetics of Fenton's process on the degradation of humic acid[J].Journal of Hazardous Materials,179(1/3):533-539 |
| [20] | Yang S J,He H P,Wu D Q,et al.2009.Degradation of methylene blue by heterogeneous fenton reaction using titanomagnetite at neutral pH values:Process and affecting factors[J].Industrial & Engineering Chemistry Research,48(22):9915-9921 |
| [21] | Yu J G,Ma T T,Liu S W.2011.Enhanced photocatalytic activity of mesoporous TiO2 aggregates by embedding carbon nanotubes as electron-transfer channel[J].Physical Chemistry Chemical Physics,13(8):3491-3501 |
| [22] | 赵超,姜利荣,黄应平.2007.Fenton及Photo-Fenton非均相体系降解有机污染物的研究进展[J].分析科学学报,23(3):355-360 |
| [23] | Zhao Y P,Hu J Y,Jin W.2008.Transformation of oxidation products and reduction of estrogenic activity of 17β-estradiol by a heterogeneous photo-Fenton reaction[J].Environmental Science & Technology,42(14):5277-5284 |
 2014, Vol. 34
2014, Vol. 34


