节球藻毒素是泡沫节球藻(Nodularia spumigena)的次生代谢产物,广泛存在于水华爆发的水体中,其在水中的浓度最高可达95 μg · L-1(Mazur-Marzec et al., 2006). 作为一类环状五肽化合物,节球藻毒素(Nodularin,NOD)与被广泛报道的微囊藻毒素(MCs)具有相似的分子结构,均能够抑制真核生物蛋白丝/苏氨酸PP1和PP2A活性(Žegura et al., 2011),造成过磷酸化作用,导致细胞凋亡(Gehringer,2004). 研究发现,NOD可通过食物链最终在比目鱼、鲟鱼、三刺鱼、青鱼和大马哈鱼等体内累积并产生毒性效应,致使鱼类大量死亡(Sipiä et al., 2001;Karjalainen et al., 2007).暴露在NOD中的水生生物可出现酶活性改变、胚胎发育畸形和幼体死亡率增加等现象(Ojaveer et al., 2003). 此外,NOD还具有致使哺乳类动物细胞发生粘连,进而损害其免疫系统等免疫毒效应(Hernández et al., 2000).
巨噬细胞是一类吞噬细胞,直接参与细胞特异性免疫和非特异性免疫,可识别病原体,通过呈递抗原或者直接杀死病原体参与细胞免疫应答过程(Babior,2000),并已被用于鱼类免疫毒性的评价(Secombes et al., 1992).NOD可以通过多种途径侵入鱼体,作为第一道防线,免疫系统较易受到藻毒素的攻击(Datta et al., 2009).目前关于藻毒素诱导细胞凋亡的途径主要分为:线粒体通路和死亡受体通路.Ding等(2003)报道,进入细胞内的藻毒素,可以破坏线粒体的电子传递链,诱发ROS大量生成,引起线粒体膜电位崩溃,最后导致细胞凋亡.Mikhailov等(2003)研究发现,藻毒素能够结合三磷酸腺苷合成酶(ATP)的亚基结构导致酶失活,而该合成酶是线粒体电子传递链上的重要成分,当ATP酶钝化后,电子传递链活动中止,揭示藻毒素使细胞线粒体的电子传递链失活的机理.然而,目前仍未有关于NOD对鱼类巨噬细胞毒性效应的研究报道.因此,本研究选用藻食性鲤科鲫鱼(Carassius auratus)为材料,采用体外离体培养诱导方法,从细胞凋亡线粒体通路相关角度,探讨NOD诱导鱼体巨噬细胞凋亡的机理.
2 材料与方法(Materials and methods) 2.1 试剂和毒素节球藻毒素标准品购自美国Sigma公司,分子式C41H60N8O10,相对分子量824.96;Leibovitz′s-15培养基购自Life Technologies公司;胎牛血清购自杭州科易生物有限公司;34%/51%(V/V)Percoll分离液购自上海卒瑞生物科技有限公司;碘化丙啶(PI)染料、核糖核酸酶(RNase)、钙荧光探针(Fluo-3 AM)、二氯二氢荧光素双醋酸盐(DCFH-DA)、罗丹明123(Rh123)、Caspase-3/8/9活性检测试剂盒均购自碧云天生物技术研究所;其它试剂为分析纯.
2.2 主要仪器流式细胞仪(Guava easyCyte 8HT),Sigma高速冷冻离心机,酶标仪,细胞培养箱,超净工作台.
2.3 试验鱼种试验选用体重400~500 g鲫鱼50条,购自浙江省水产研究所. 实验室驯养1周后进行实验.
2.4 巨噬细胞的分离与诱导鲫鱼头肾巨噬细胞的分离参照文献(Tumbol et al., 2009)方法.在无菌条件下取出鲫鱼头肾,置于磷酸盐(PBS)缓冲液中用眼科剪剪碎,过100目不锈钢细胞网筛,应用Percoll细胞分离液收集巨噬细胞,置于Leibovitz′s-15培养基(含10%胎牛血清)中培养,温度维持在27 ℃.实验用细胞密度控制在106 cells · mL-1.试验分为空白对照与诱导组,空白组(CK)经PBS处理,空白组和诱导组均设置6个平行组,实验诱导时间为12 h;诱导组分3个不同浓度NOD暴露,分别为1 μg · L-1、10 μg · L-1和100 μg · L-1.
2.5 流式细胞仪细胞凋亡和细胞周期检测空白组和诱导组的巨噬细胞(1×106个)离心收集(3000 r · min-1,5min),70%乙醇冰浴过夜,过40 μm细胞网筛,用50 μg · mL-1 PI、100 μg · mL-1 RNase和0.1% TrionX-100在室温避光孵育30 min后,用Guava easyCyte 8HT流式细胞仪Incyte模块检测分析.检测激发波长488 nm,发射波长630 nm.
2.6 胞内钙离子浓度的测定巨噬细胞内钙离子浓度测定参照文献(Merritt et al., 1990)方法.空白组和诱导组的巨噬细胞(1×106个)离心收集(3000 r · min-1,5 min),重悬于预冷的PBS中,加入Fluo-3AM至终浓度为5 μg · mL-1,室温避光孵育40 min.上机前过40 μm细胞网筛,用流式细胞仪Incyte模块检测相应荧光强度变化,以此显示胞内钙离子的变化规律.检测激发波长488 nm,发射波长525 nm.
2.7 胞内活性氧(ROS)的测定空白组和诱导组的巨噬细胞(1×106个)离心收集(3000 r · min-1,5min),重悬于预冷的PBS中,加入DCFH-DA至终浓度为10 μmol · L-1,室温避光孵育20 min.上机前过40 μm细胞网筛,用流式细胞仪Incyte模块检测相应荧光强度变化,以此显示细胞内ROS的变化规律.检测激发波长488 nm,发射波长525 nm.
2.8 微量丙二醛(MDA)的测定微量丙二醛检测依据Ohkawa等(1979)的方法,过氧化脂质降解产物中丙二醛(MDA)可与硫代巴比妥酸(TBA)缩合,形成红色产物,在532 nm处有最大吸收峰.空白组和诱导组的巨噬细胞(1×106个)离心收集(3000 r · min-1,5 min),重悬于预冷的PBS中,采用超声破碎细胞,按试剂盒说明书操作步骤进行测定.
2.9 线粒体膜电位测定空白组和诱导组的巨噬细胞(1×106个)离心收集(3000 r · min-1,5 min),重悬于预冷的PBS中,加入Rh123至终浓度为5 μg · mL-1,室温避光孵育30 min.上机前过40 μm细胞网筛,用流式细胞仪Incyte模块检测相应荧光强度变化,以此显示线粒体膜电位的变化规律.检测激发波长507 nm,发射波长529 nm.
2.10 Caspase-3/8/9酶活性的测定空白组和诱导组细胞(1×106个)样品,4 ℃条件下离心收集(600 r · min-1,5 min),小心吸除上清液,同时确保尽量没有细胞被吸除,PBS漂洗1次.同前吸尽上清后,按照每2×106个细胞加入200 μL裂解液的比例加入裂解液,重悬沉淀,冰浴裂解15 min.4 ℃下离心(16000 r · min-1,15 min).把上清转移到冰浴预冷的离心管中待测.Caspase3/8/9可分别催化底物Ac-X-pNA(Caspase3:X=DEVD;Caspase8:X=IETD;Caspase9: X=LEHD)产生黄色的pNA,可根据pNA在405 nm附近有强吸收来检测Caspase3/8/9的活性.按照试剂盒说明书的实验步骤进行操作.
2.11 数据分析用Original 8.0 分析软件进行统计,数据处理结果用平均值±标准差表示.组间差异用One-way ANOVA分析,*p<0.05被认为有显著性差异,* *p<0.01被认为有极显著性差异.
3 结果(Results) 3.1 流式细胞仪的测定结果经流式细胞仪分析,鲫鱼巨噬细胞经节球藻毒素(1、10、100 μg · L-1)处理12 h后,均出现了典型的细胞凋亡特征(亚二倍体峰).如图 1所示,细胞凋亡率分别达到17.37%、27.59%、61.64%,而空白组的仅为3.72%. 与空白组和不同诱导组相比,节球藻毒素诱导鲫鱼巨噬细胞凋亡率的变化呈现明显的剂量-效应特征.
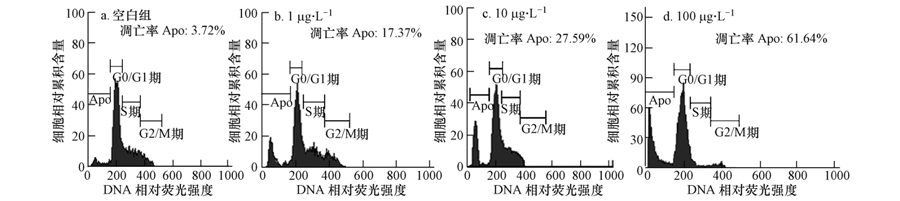 |
| 图 1 节球藻毒素诱导鲫鱼巨噬细胞凋亡的流式检测结果 Fig. 1 Macrophages apoptosis induced by nodularin detected by flow cytometry |
细胞周期的改变是DNA损伤诱发细胞凋亡的关键因素(Kruman et al., 2004).细胞周期通常分为G0/G1期(DNA复制前期),该期主要合成RNA和核糖体;S期(DNA合成期)有DNA和蛋白合成;G2/M期为DNA合成后期.如表 1所示,随着节球藻毒素暴露剂量的不断增加,G0/G1期明显减少,S期也明显减少.与空白组相比,100 μg · L-1的节球藻毒素诱导组导致上述细胞周期分别减少了14.65%、10.65%.
| 表1 节球藻毒素对鲫鱼巨噬细胞周期的影响 Table 1 Effects of nodularin on cell cycles of C. auratus macrophages |
钙离子是细胞内信号通路的第二信使,在凋亡中起关键作用(Goll et al., 2003).由图 2可见,随着节球藻毒素浓度的增加,细胞内钙离子水平不断提高,呈现明显的剂量效应关系.较低剂量(1 μg · L-1)NOD诱导组中钙离子浓度升高,和空白组相比无差异性.与空白组相比,10、100 μg · L-1节球藻毒素处理组中胞内钙离子分别提高了44.75%、76.9%,差异极显著,呈现明显剂效关系.
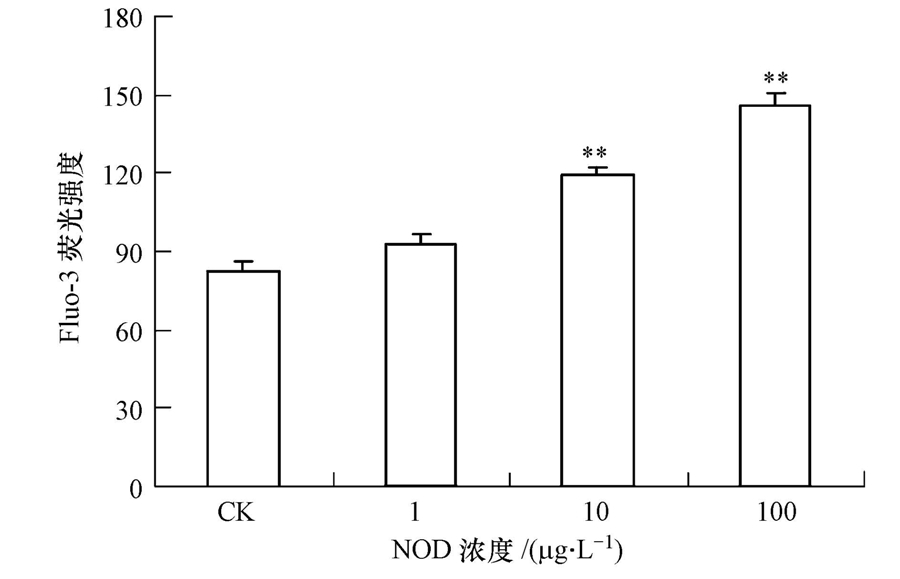 |
| 图 2 节球藻毒素诱导鲫鱼巨噬细胞内钙离子变化情况 Fig. 2 Intracellular Ca2+ changes in C. auratus macrophages induced by nodularin |
ROS是细胞凋亡诱导过程中的关键信号(Ježek et al., 2005).采用流式细胞仪检测NOD作用12 h后,鲫鱼巨噬细胞中的ROS水平,结果如图 3所示.由图可知,与空白组相比,1 μg · L-1节球藻毒素处理组中巨噬细胞内ROS水平升高了29.1%,差异显著. 而10、100 μg · L-1处理组的ROS水平则分别为空白组的1.56、1.86倍,差异极显著.节球藻毒素诱导鲫鱼巨噬细胞ROS强烈的剂量-效应变化说明氧化应激是NOD诱导巨噬细胞毒性的主要原因.
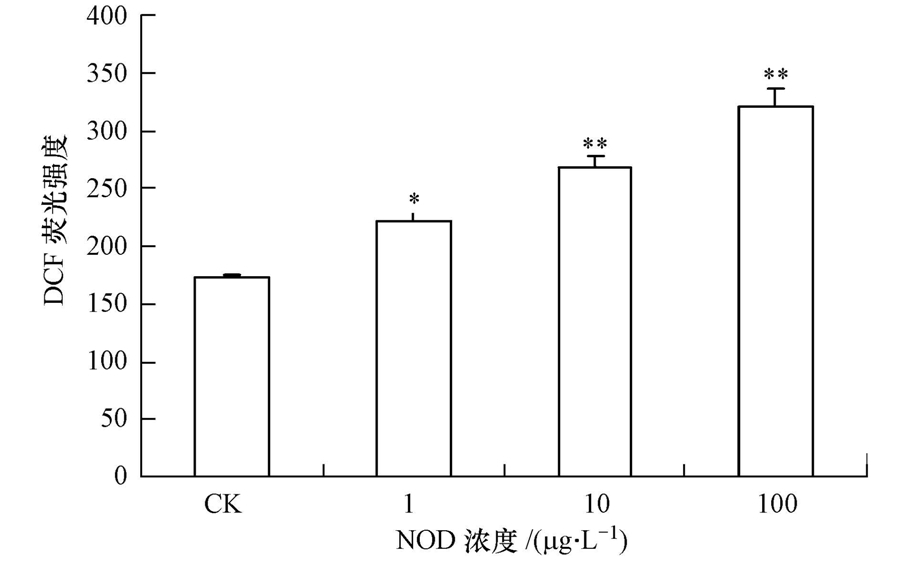 |
| 图 3 节球藻毒素诱导鲫鱼巨噬细胞内ROS变化情况 Fig. 3 Intracellular ROS changes in C. auratus macrophages induced by nodularin |
MDA是氧自由基攻击细胞膜上的不饱和脂肪酸后,生成的脂质过氧化产物,也是氧化应激的重要指标(Ates et al., 2007). 图 4为NOD暴露后的细胞内MDA含量,从图中可以看出,随着NOD浓度的升高,胞内MDA含量明显增加. 与空白组相比,1 μg · L-1处理组的MDA含量上升了65.9%,差异显著;而10、100 μg · L-1 NOD处理组的MDA含量分别为空白组的2.23、2.94倍,差异极显著.这和ROS的实验结果具有一致性,也呈现了明显的剂量-效应关系.
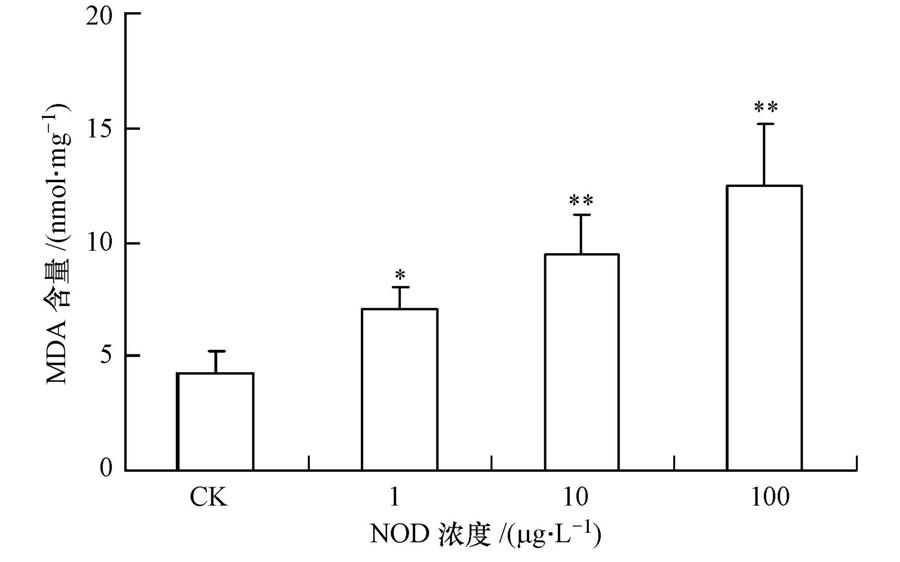 |
| 图 4 节球藻毒素诱导鲫鱼巨噬细胞内MDA含量变化 Fig. 4 Intracellular MDA changes in C.auratus macrophages induced by nodularin |
线粒体上存在电子呼吸链,可形成跨膜电位,当受到刺激后,线粒体膜电位发生崩溃,被认为是细胞凋亡的早期事件(Desagher et al., 2000).Rh123可以用来检测胞内线粒体膜电位的变化情况,该物质的荧光强度可以直接表示线粒体膜电位变化. 如图 5所示,与空白组相比,1、10、100 μg · L-1 NOD诱导组中线粒体膜电位均呈现下降趋势,分别下降了14.8%、23.5%、35.8%,剂量-效应变化极显著.该结果表明线粒体可能是NOD攻击巨噬细胞的靶器官.
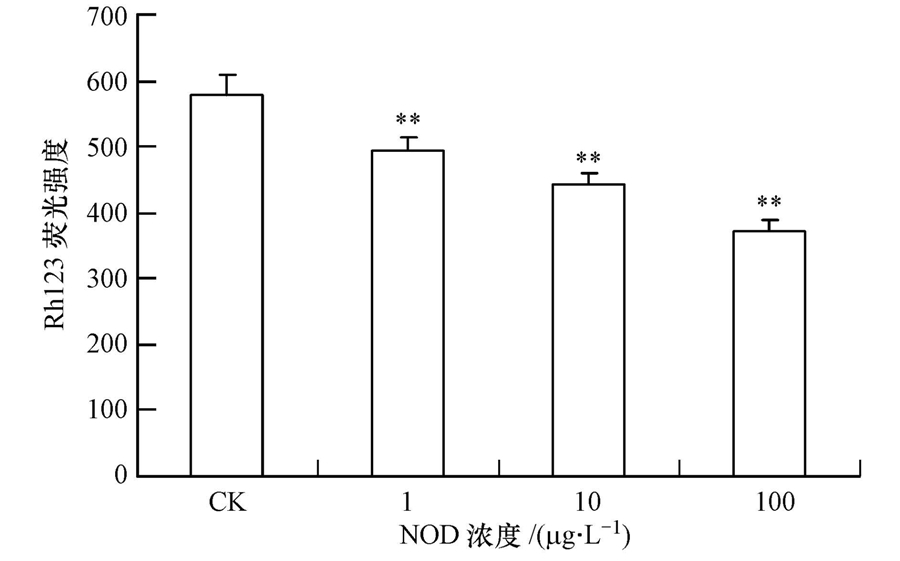 |
| 图 5 节球藻毒素诱导鲫鱼巨噬细胞内线粒体膜电位变化情况 Fig. 5 Intracellular MMP changes in C. auratus macrophages induced by nodularin |
Caspase-3是细胞凋亡过程后期的主要执行者(Lockshin,2005),而Caspase-8/9则为起始Caspases,能够激活下游Caspase-3反应.Caspase-3/8/9的酶活性可以通过pNA在405 nm处有强吸收而进行表征.由图 6可知,10、100 μg · L-1 NOD处理组中,Caspase-3的酶活性分别为空白组的1.92、2.89倍,差异极显著.与空白组相比,1 μg · L-1 NOD诱导组的Caspase-9酶活性上升了43%,10、100 μg · L-1 NOD处理组的Caspase-9酶活性则为空白组2.40、3.73倍,差异极显著.而Caspase-8的酶活性也表现为升高,与空白组相比,NOD诱导组中的酶活性分别升高13.5%、22.9%、33.3%,不同诱导组差异极显著,呈现明显剂量-效应特征.
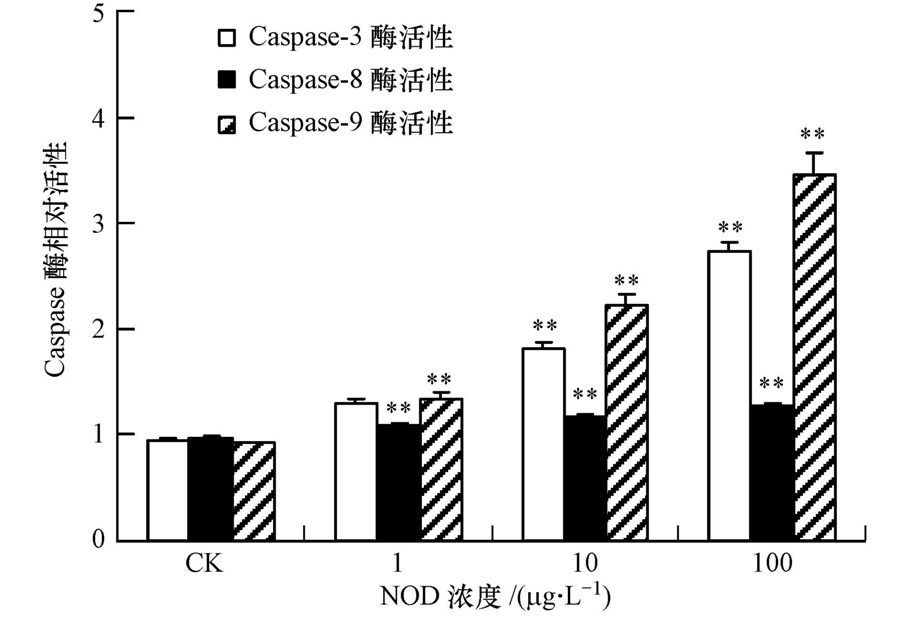 |
| 图 6 节球藻毒素诱导鲫鱼巨噬细胞内Caspase-3/8/9酶活性变化情况 Fig. 6 Caspase activities in C. auratus macrophages induced by nodularin |
细胞凋亡是指细胞受到胞外环境或者胞内环境刺激而发生的程序性死亡,涉及特殊的半胱氨酸蛋白酶Caspases的激活,引起一系列形态学上的改变(Fan et al., 2005).实验结果表明,1~100 μg · L-1剂量水平的NOD处理鲫鱼巨噬细胞12 h后可检测到凋亡亚二倍体峰,并呈现明显的剂量-效应特征.类似地,Lankoff等(2002)在对HepG2细胞的研究中也发现NOD能诱导细胞凋亡,发生由ROS介导的DNA损伤.细胞周期分析中发现,NOD暴露下鲫鱼巨噬细胞G0/G1期和S期均明显受到阻滞,意味着RNA和DNA合成与复制受到影响,并发生减弱,这可能是NOD导致鲫鱼巨噬细胞毒性的重要原因.类似地,在40 mg · mL-1藻毒素暴露下,动物的淋巴细胞增殖也受到明显的抑制(Rymuszka et al., 2007).
钙离子稳态在细胞凋亡诱导中起关键作用(Goll et al., 2003).钙离子可参与到细胞免疫活动,如白介素-1β可以影响硬骨鱼白细胞中的钙离子浓度(Benedetti et al., 2006).本研究也发现,NOD可以提高细胞内钙离子浓度,表明钙离子相关信号通路可能存在于NOD诱导的鱼体巨噬细胞免疫毒性机理中.报道称,胞内钙离子浓度升高可引起线粒体对钙离子的过量摄入,造成线粒体膜崩溃,诱导ROS生成(Halliwell et al., 1999).ROS是细胞有氧呼吸作用的产物,线粒体电子传递过程中可导致ROS产生,正常过程中,线粒体中能产生少量的ROS,但当线粒体受到应激后,ROS可大量产生(Fleury et al., 2002).如图 3所示,NOD诱发鱼体巨噬细胞内ROS升高,线粒体是细胞凋亡过程中重要的参与者,可以调节胞内钙离子稳态(Hail et al., 2004). NOD可以通过降低欧洲比目鱼(Platichthys flesus)体内GST和CAT的酶活性使细胞更容易遭受ROS的攻击,形成的ROS可以调节胞内GSH水平并使细胞膜脂质过氧化(Persson et al., 2009).如图 4所示,NOD可以升高巨噬细胞内MDA水平,Bouaïcha等(2004)和Davies等(2005)分别报道称NOD可以增加大鼠、贻贝体内的MDA水平.研究发现,细胞死亡过程可以通过消除胞内上升的钙离子和ROS而被抑制,内质网可以释放钙离子,诱发线粒体处形成ROS(Prasad et al., 2010).线粒体膜电位崩溃,膜的完整性丧失,线粒体内容物泄露.如图 5所示,NOD可以诱使鱼体巨噬细胞内线粒体膜电位下降,表明线粒体是NOD毒效应的作用靶细胞器.
细胞凋亡主要有两条途径:内源性线粒体通路和外源性TNF介导的死亡受体通路.死亡受体通路中,Caspase-8被诱导激活,线粒体通路中Caspase-9被激活,Caspase-3属于效应Caspase,它存在于死亡受体和线粒体这两条通路中(Shi,2002);在线粒体通路中,Caspase-9可以被线粒体内容物激活,进而切割下游的Caspase-3,激活后的Caspase-3可以执行细胞凋亡程序(Garrido et al., 2006).外源性污染物可以诱发鱼类形成Caspase依赖型凋亡.外毒素AIP56可以通过激活Caspase-8和Caspase-9诱导黑鲈鱼(Dicentrarchus labrax)巨噬细胞和嗜中性粒细胞发生凋亡,表明内源性和外源性凋亡途径均存在(Costa-Ramos et al., 2011).图 6结果表明,NOD可以激活鲫鱼巨噬细胞中Caspase-3/8/9酶活性,其中,Caspase-9的表达量远高于空白组,表明NOD诱导鱼类巨噬细胞凋亡的通路主要为线粒体途径.研究发现,藻毒素可以引起鲫鱼的淋巴细胞和肝细胞发生凋亡,造成ROS上升,线粒体功能紊乱,线粒体膜电位崩溃,ATP耗损等现象(Li et al., 2007).而水生微生物亦可以诱发鱼类细胞线粒体功能改变,线粒体膜电位下降,Caspase-3和Capsase-9激活(Chen et al., 2010).本研究中μg · L-1剂量水平的节球藻毒素即可引起一系列细胞内的变化,包括胞内钙离子水平升高,ROS累积,MDA含量增加,线粒体膜电位下降及Caspase-3/8/9的激活.据报道,脂多糖也可诱导鱼类细胞发生线粒体依赖型凋亡(Xiang et al., 2008).这些结果表明,NOD诱导鲫鱼巨噬细胞凋亡通路主要为线粒体依赖型.
5 结论(Conclusions)节球藻毒素NOD能够在1~100 μg · L-1的低剂量暴露下,体外诱导鲫鱼巨噬细胞发生典型的细胞凋亡,其表现为细胞G0/G1期和S期减少,细胞周期紊乱,胞内钙离子水平升高,ROS累积,MDA含量增加,线粒体膜电位下降及Caspase-3/8/9的激活.研究结果显示,NOD诱导鲫鱼巨噬细胞凋亡通路主要为线粒体依赖型,因此,推断节球藻毒素很可能是通过诱导鱼体免疫细胞凋亡进而影响鱼体的免疫功能.
| [1] | Ates O, Cayli S, Altinoz E, et al. 2007. Neuroprotection by resveratrol against traumatic brain injury in rats [J]. Molecular and Cellular Biochemistry, 294(1/2): 137-144 |
| [2] | Babior B M. 2000. Phagocytes and oxidative stress [J]. The American Journal of Medicine, 109(1): 33-44 |
| [3] | Benedetti S, Randelli E, Buonocore F, et al. 2006. Evolution of cytokine responses: IL-1b directly affects intracellular Ca2+ concentration of teleost fish leukocytes through a receptor-mediated mechanism [J]. Cytokine, 34(1/2): 9-16 |
| [4] | Bouaïcha N, Maatouk I. 2004. Microcystin-LR and nodularin induce intracellular glutathione alteration, reactive oxygen species production and lipid peroxidation in primary cultured rat hepatocytes [J]. Toxicology Letters, 148(1/2): 53-63 |
| [5] | Chen P C, Wu J L, Her G M, et al. 2010. Aquatic birnavirus induces necrotic cell death via the mitochondria-mediated caspase pathway [J]. Fish & Shellfish Immunology, 28(2): 344-353 |
| [6] | Costa-Ramos C, do Vale A, Ludovico P, et al. 2011. The bacterial exotoxin AIP56 induces fish macrophage and neutrophil apoptosis using mechanisms of the extrinsic and intrinsic pathways [J]. Fish & Shellfish Immunology, 30(1): 173-181 |
| [7] | Datta S, Ghosh D, Saha D R, et al. 2009. Chronic exposure to low concentration of arsenic is immunotoxic to fish: role of head kidney macrophages as biomarkers of arsenic toxicity to Clarias batrachus[J]. Aquatic Toxicology, 92(2): 86-94 |
| [8] | Davies W R, Siu W H L, Jack R W, et al. 2005. Comparative effects of the blue green algae Nodularia spumigena and a lysed extract on detoxification and antioxidant enzymes in the green lipped mussel (Perna viridis) [J]. Marine Pollution Bulletin, 51(8/12): 1026-1033 |
| [9] | Desagher S, Martinou J C. 2000. Mitochondria as the central control point of apoptosis [J]. Trends in Cell Biology, 10(9): 369-377 |
| [10] | Ding W X, Ong C N. 2003. Role of oxidative stress and mitochondrial changes in cyanobacteria-induced apoptosis and hepatotoxicity [J]. FEMS Microbiology Letters, 220(1): 1-7 |
| [11] | Fan T J, Han L H, Cong R S, et al. 2005. Caspase family proteases and apoptosis [J]. Acta Biochimica et Biophysica Sinica, 37(11): 719-727 |
| [12] | Fleury C, Mignotte B, Vayssière J L. 2002. Mitochondrial reactive oxygen species in cell death signaling [J]. Biochimie, 84(2/3): 131-141 |
| [13] | Garrido C, Galluzzi L, Brunet M, et al. 2006. Mechanisms of cytochrome c release from mitochondria [J]. Cell Death and Differentiation, 13(9): 1423-1433 |
| [14] | Gehringer M M. 2004. Microcystin-LR and okadaic acid-induced cellular effects: a dualistic response [J]. FEBS Letters, 557(1/3): 1-8 |
| [15] | Goll D E, Thompson V F, Li H, et al. 2003. The calpain system [J]. Physiological Reviews, 83(3): 731-801 |
| [16] | Hail N Jr, Konopleva M, Sporn M, et al. 2004. Evidence supporting a role for calcium in apoptosis induction by the synthetic triterpenoid 2-cyano-3, 12-dioxooleana-1, 9-dien-28-oic zcid (CDDO) [J]. The Journal of Biological Chemistry, 279(12): 11179-11187 |
| [17] | Hernández M, Macia M, Padilla C, et al. 2000. Modulation of human polymorphonuclear leukocyte adherence by cyanopeptide toxins [J]. Environmental Research, 84(1): 64-68 |
| [18] | Ježek P, Hlavatá L. 2005. Mitochondria in homeostasis of reactive oxygen species in cell, tissues, and organism [J]. The International Journal of Biochemistry & Cell Biology, 37(12): 2478-2503 |
| [19] | Karjalainen M, Engström-Öst J, Korpinen S, et al. 2007. Ecosystem consequences of cyanobacteria in the northern Baltic sea [J]. AMBIO: A Journal of the Human Environment, 36(2): 195-202 |
| [20] | Kruman I I, Wersto R P, Cardozo-Pelaez F, et al. 2004. Cell cycle activation linked to neuronal cell death initiated by DNA damage [J]. Neuron, 41(4): 549-561 |
| [21] | Lankoff A, Banasik A, Nowak M. 2002. Protective effect of melatonin against nodularin-induced oxidative stress in mouse liver [J]. Archives of Toxicology, 76(3): 158-165 |
| [22] | Li X Y, Wang J, Liang J B, et al. 2007. Toxicity of microcystins in the isolated hepatocytes of common carp (Cyprinus carpio L.) [J]. Ecotoxicology and Environmental Safety, 67(3): 447-451 |
| [23] | Lockshin R A. 2005. Programmed cell death: history and future of a concept [J]. Journal de la Société de Biologie, 199(3): 169-173 |
| [24] | Mazur-Marzec H, Kre el A, Kobos J, et al. 2006. Toxic Nodularia spumigena blooms in the coastal waters of the Gulf of Gdańsk: a ten-year survey [J]. Oceanologia, 48(2): 255-273 |
| [25] | Merritt J E, McCarthy S A, Davies M P, et al. 1990. Use of fluo-3 to measure cytosolic Ca2+ in platelets and neutrophils. Loading cells with the dye, calibration of traces, measurements in the presence of plasma, and buffering of cytosolic Ca2+ [J]. Biochemical Journal, 269(2): 513-519 |
| [26] | Mikhailov A, Härmälä-Braskén A S, Hellman J, et al. 2003. Identification of ATP-synthase as a novel intracellular target for microcystin-LR [J]. Chemico-Biological Interactions, 142(3): 223-237 |
| [27] | Ohkawa H, Ohishi N, Yagi K. 1979. Assay for lipid peroxides in animal tissues by thiobarbituric reaction [J]. Analytical Biochemistry, 95(2): 351-358 |
| [28] | Ojaveer E, Simm M, Balode M, et al. 2003. Effect of Microcystis aeruginosa and Nodularia spumigena on survival of Eurytemora affinis and the embryonic and larval development of the Baltic herring Clupea harengus membras [J]. Environmental Toxicology, 18(4): 236-242 |
| [29] | Persson K J, Legrand C, Olsson T. 2009. Detection of nodularin in European flounder (Platichthys flesus) in the west coast of Sweden: evidence of nodularin mediated oxidative stress[J]. Harmful Algae, 8(6): 832-838 |
| [30] | Prasad A, Bloom M S, Carpenter D O. 2010. Role of calcium and ROS in cell death induced by polyunsaturated fatty acids in murine thymocytes [J]. Journal of Cellular Physiology, 225(3): 829-836 |
| [31] | Rymuszka A, Sierosawska A, Bownik A, et al. 2007. In vitro effects of pure microcystin-LR on the lymphocyte proliferation in rainbow trout (Oncorhynchus mykiss) [J]. Fish & Shellfish Immunology, 22(3): 289-292 |
| [32] | Secombes C J, Fletcher T C. 1992. The role of phagocytes in the protective mechanisms of fish [J]. Annual Review of Fish Diseases, 24: 53-71 |
| [33] | Shi Y G. 2002. Mechanisms of caspase activation and inhibition during apoptosis [J]. Molecular Cell, 9(3): 459-470 |
| [34] | Sipiä V O, Kankaanpää H T, Lahti K, et al. 2001. Detection of nodularin in flounders and cod from the Baltic Sea [J]. Environmental Toxicology, 16(2): 121-126 |
| [35] | Tumbol R A, Baiano J C F, Barnes A C. 2009. Differing cell population structure reflects differing activity of Percoll-separated pronephros and peritoneal leucocytes from barramundi (Lates calcarifer) [J]. Aquaculture, 292(3/4): 180-188 |
| [36] | Xiang LX, Peng B, Dong W R, et al. 2008. Lipopolysaccharide induces apoptosis in Carassius auratus lymphocytes, a possible role in pathogenesis of bacterial infection in fish [J]. Developmental & Comparative Immunology, 32(8): 992-1001 |
| [37] | Žegura B, Štraser A, Filipi č M. 2011. Genotoxicity and potential carcinogenicity of cyanobacterial toxins-a review [J]. Mutation Research-Reviews in Mutation Research, 727(1/2): 16-41 |
 2014, Vol. 34
2014, Vol. 34


