2. 天津大学环境科学与工程学院, 天津 300072
2. College of Environmental Science and Engineering, Tianjin University, Tianjin 300072
污水厌氧生化处理过程是指在无分子氧参与的条件下,有机物通过厌氧污泥中多种微生物的生化作用,分解为有机酸、CH4、CO2、H2等产物的过程.由于其具有处理负荷高、剩余污泥少、可产生沼气等特征,因而在有机固体废物(剩余污泥、厨余、农业废弃物)减量、高浓度有机废水、难降解废水等处理中广泛应用(Fernandez et al., 2001; Gunaseelan,2004; Neves et al., 2004; Raposo et al., 2006).影响厌氧处理过程的因子包括基础因素(厌氧污泥组成、浓度、污泥负荷等)和环境因素(pH、ORP、抑制性物质等)两大类,其中,厌氧污泥的生物相组成和代谢活性对厌氧生化处理的过程进展发挥着重要的作用.当采用不同的接种厌氧污泥时,由于微生物构成、对基质的适应性和接种量的不同,厌氧污泥产CH4活性存在较大差异(Raposo et al., 2011; Labatut et al., 2011).对厌氧污泥的产CH4活性进行系统地对比与研究,确定厌氧污泥产CH4生成势,一方面可对厌氧污泥的厌氧净化性能和产CH4活性进行评价,同时也能为厌氧工艺的关键操作参数优化提供依据(Lesteur et al., 2010).
末端限制性片段多态性(Terminal-Restriction fragment length polymorphism,T-RFLP)分析方法由RFLP发展而来,又称为16S rRNA基因的末端限制性片段分析技术,是目前微生物分子生物学研究中有效的研究手段之一.该方法将PCR引物中的一条加以荧光标记,对扩增产物用限制性内切酶进行切割并电泳,根据片断的大小不同及标记片断种类和数量的不同来分析群落的结构及组成.Marsh等(1998)采用T-RFLP分析了活性污泥、生物反应器、沙质、地下水及白蚁消化道中的细菌组成,比较了这些群落结构的相似性,并将6种已知菌混和在一起组成模拟的群落进行了分析.Lüdemann等(2000)采用该技术分析了水稻种植区土壤中沿着氧垂直梯度上的细菌群落组成变化,同时结合16S rDNA克隆文库的构建和测序分析,获得了与氧垂直梯度相关的不同深度细菌群落组成情况.当前该技术已成功应用于微生物群落组成和结构及微生物系统发育等研究,在产CH4菌和CH4氧化菌的群落结构、动态变化的检测中发挥着重要的作用.
本研究采用厌氧污泥生化产CH4生成势(Biological methane potential,BMP)的测试方法(Owen et al., 1979;Angelidaki et al., 2009),对AP、DH两污水处理厂的厌氧污泥进行批次实验,并对两厂厌氧污泥的产气速率与基质浓度进行回归,得出产CH4的关键参数,评价不同厌氧污泥的产CH4生成势.同时,对批次实验前后的水质变化进行分析,结合厌氧污泥的T-RFLP与SEM分析结果,对两种厌氧污泥产CH4生成势的差异进行解析.
2 材料与方法(Materials and methods) 2.1 厌氧污泥来源与特征本研究所用的两种厌氧污泥分别来自于AP和DH两污水处理厂的污泥厌氧消化池,AP污水处理厂采用合流制明渠排水沟进水,进水水质易受降雨影响,且泥沙等无机颗粒含量较高;DH污水处理厂配套管网设施完善,进水为完整的下水管网收集的城市生活污水.污水厂长期的监测数据表明,AP厌氧污泥的VSS/TSS值多在0.5以下,而DH厌氧污泥的VSS/TSS值维持在0.6以上.
2.2 BMP实验设计AP-BMP、DH-BMP共设置5组不同的食微比S/X(0、0.1、0.2、0.4、0.6)进行BMP实验,实测S/X如表 1所示.依据测试基质浓度在120 mL的血清瓶中加入定量储备NaAc溶液,基质体积为60 mL.厌氧微量元素溶液采用Owen等(1979)提出的配方,其中,CaCl2 · 2H2O、NH4Cl、MgCl2 · 6H2O、KCl、MnCl2 · 4H2O、CoCl2 · 6H2O、H3BO3、CuCl2 · 2H2O、Na2MoO4 · 2H2O、ZnCl2的浓度分别为16.7、26.6、120、86.7、1.33、2、0.38、0.18、0.17、0.14 g · L-1.每个血清瓶加入27 mL的微量元素液体和5.4 mL的(NH4)2HPO4(26.7 g · L-1),之后接种同量的厌氧污泥后,盖上胶盖并用铝箔封口.在35 ℃下旋转培养箱内进行实验,实验过程中以玻璃注射筒(50 mL)测量总产气量,并利用GC-ECD测定CH4、CO2和H2的比例.AP-BMP、DH-BMP分别设置两组平行实验,产气量测量可精确到0.1 mL.
| 表 1 BMP实验实测S/X比 Table 1 Measured S/X in BMP test |
常规水质指标包括pH(Suntex Ion Analyzer 3000A)、SS(Sartorius Analytic Oven)、VSS(Sartorius Analytic Furnace)、NH3-N(Autotitrator AT-400KYOTO)、TKN(Autotitrator AT-400KYOTO)、COD(回流加热滴定)等,均依照美国EPA规定的标准方法(APHA,1999)进行.实验过程中气体成分(CH4、CO2和H2)的测量采用气相色谱(China Chromatography GC8900T)进行.厌氧污泥SEM镜检用Hitachi-2500 SEM进行.
2.3.2 T-RFLP分析本文参照了Tillmann等(2000)建立的T-RFLP方法对实验前后厌氧污泥的生物多样性进行分析,步骤如下:①通过PCR来复制DNA样品中的目标基因,引物为在5′的尾端上带有荧光的Ar 109f和Ar 912r*,首先在94 ℃预变性5 min,扩增循环阶段包括94 ℃变性1 min,52 ℃退火1 min,72 ℃延伸1.5 min,共循环28次,最后在72 ℃条件下延伸6 min;②在8.5 μL的PCR产物中加入0.5 μL Taq I和1.5 μL的缓冲溶液,在65 ℃条件下消化切割2 h;③将切割后的片段利用电泳分离并以荧光侦测器(全自动遗传分析仪,ABI PRISM 3100 Genetic Analyzer)检测片段上所带的荧光强度.Tillmann等(2000)成功分离、克隆出产CH4髦毛菌Methanosaeta spp.、产CH4微菌Methanomicrobiaceae、RC-I和产CH4杆菌Methanobacteriaceae,未能定性的菌种归入Diverse类.
2.3.3 数据分析BMP实验中的累积CH4产气量采用改进的Gompertz模型回归分析(Zwietering et al., 1990):
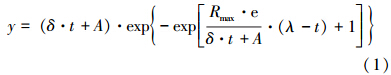
式中,y为累积产气量(mL),δ为产气末期校正斜率(mL · h-1),t为反应时间(h),A为平衡产气量(mL),Rmax为最大产气速率(mL · h-1),λ为迟滞期(h).
底物的厌氧代谢过程实质上是一系列的酶促反应,因此,采用Michaelis-Menten模型描述基质浓度与比产气速率的关系:
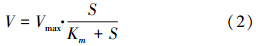
式中,Vmax为最大比产气速率(mL · g-1 · d-1,以VSS计),V为比产气速率(mL · g-1 · d-1,以VSS计),Km为半饱和常数(mg · L-1,以COD计),S为基质浓度(mg · L-1,以COD计).
3 结果与讨论(Results and discussion) 3.1 BMP产气结果分析AP-BMP、DH-BMP批次实验持续时间分别为239 h、286 h,由图 1可知,5组不同投配比条件下的累积产气量存在着明显的差异.实验初期,累积产气量差异不明显,后期逐步增大.气体成分以CH4(80%)、CO2(20%)为主,同时存在少量的H2(不足1%).以NaAc为基质的实验,由于不经历酸化水解的限速阶段,产气速度较快,但高浓度的NaAc对厌氧污泥也存在着一定的抑制作用,例如,DH-BMP实验中,S/X值最高的4#样品产CH4量在170 h后才超过3#样品.AP-BMP实验中,4#样品的产CH4量最高,达到了166 mL,DH-BMP中最高的产CH4量达到了201 mL.
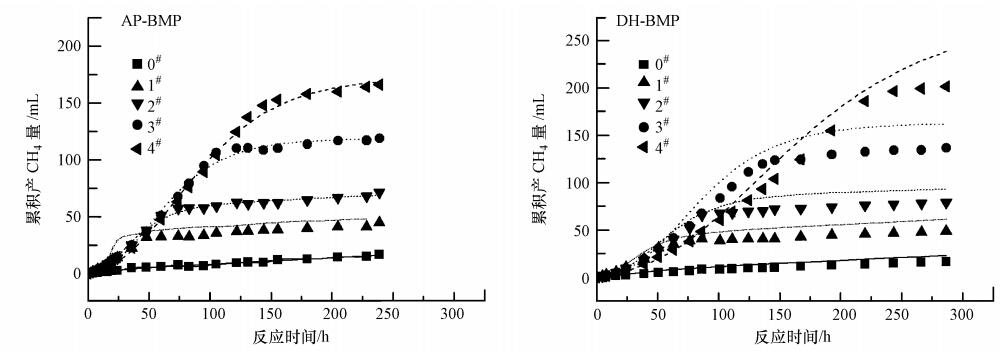 |
| 图 1 实测CH4累积产气量与回归曲线 Fig. 1 Measured cumulative volume of CH4 and regression curve |
应用改进的Gompertz模型对AP-BMP、DH-BMP产气进行回归后的参数如表 2所示.两厂的厌氧污泥产气数据与改进的Gompertz模型拟合较好(R2>0.99).通常厌氧消化过程中的限速步骤为水解破壁过程(Noike et al., 1985),在无添加外来基质的0#样品中,AP、DH厌氧污泥的迟滞期分别为13.56、0 h,表明DH厌氧污泥的活性较高.投加基质NaAc对厌氧污泥具有一定的抑制作用,且抑制作用随基质浓度的提高而提升.DH厌氧污泥4#条件下迟滞期达到48.80 h,可能与4#样品中S/X最高(0.67)有关.Prashanth等(2006)指出,较高的S/X比造成的氨氮和挥发酸的积累,对厌氧菌群产生一定的抑制作用,通常较低S/X值下的迟滞期较短(Chen et al., 1996).而在AP-BMP实验中,无添加基质的0#的迟滞期达到了13.56 h,高于添加添加基质的1#、2#.这可能是由于AP厌氧污泥的反应活性较差,在无基质添加条件下需调整造成的.
| 表 2 改进Gompertz模型回归BMP实验参数 Table 2 Regression results in BMP test with modified Gompertz model |
采用Michaelis-Menten模型对两个批次实验的基质浓度、比产气速率进行回归分析后的结果如图 2所示(R2>0.99).由图可知,AP、DH厌氧污泥的最大比产气速率差距不大,分别为67.93、62.65 mL · g-1 · d-1(以VSS计),但两厂厌氧污泥的Km存 在着显著的差异,DH厌氧污泥的Km为801 mg · L-1,而AP厌氧污泥的Km高达1517 mg · L-1.Km是表征底物亲和力的常数,表明AP厌氧污泥对基质NaAc的适应性差,需要在较高的基质浓度下才能表现出较好的产CH4性能.
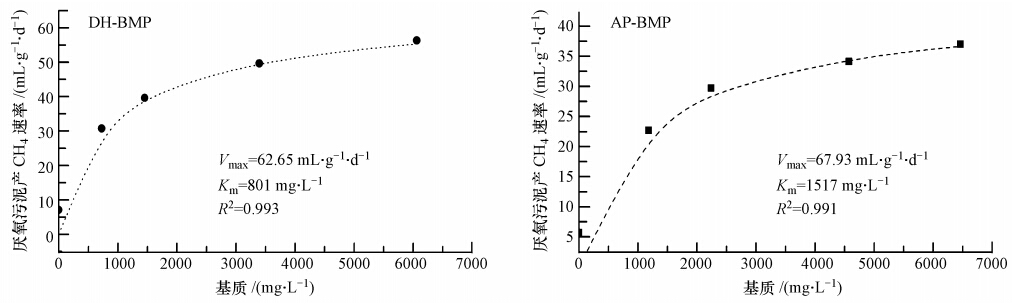 |
| 图 2 Michaelis-Menten模型回归BMP产CH4速率参数 Fig. 2 Regression results of methane production rate curve in BMP test with Michaelis-Menten model |
AP-BMP、DH-BMP两个批次实验结束时,不同S/X条件下的水质状况如表 3所示.两个批次实验中随着S/X增大,pH由弱酸性渐变为弱碱性,分别位于在6.5~7.8、6.7~7.8范围内.0#呈弱酸性,可能由未添加基质、厌氧污泥自身的水解造成.DH-BMP与AP-BMP实验结束时,ORP值分别位于-245~-327 mV与-310~-373 mV范围内.随着S/X比的增大,两个批次实验的ORP值都呈下降的趋势.厌氧环境的主要标志是发酵液具有低的ORP,不同的厌氧消化体系和不同的厌氧微生物对ORP的要求不同.通常中温厌氧消化系统要求的ORP应位于-300~-380 mV之间,产CH4菌最适宜的ORP为-350 mV或更低.DH-BMP实验样品的ORP明显低于对应的AP-BMP实验样品值,表明DH-BMP中形成了良好的厌氧生化条件,厌氧污泥的活性高.
| 表 3 BMP实验末期不同S/X条件下主要水质 Table 3 Main water quality of different S/Xs at the end of BMP test |
两批次实验中在高S/X条件下溶解性COD(CODs)显著下降,实验结束时CODs基本相同,而未添加外来基质的0#样品中CODs有所提高,可能是厌氧微生物内源代谢导致酸化水解从而造成CODs的提高.批次实验前后,NH3-N浓度均有提高,不同S/X条件下NH3-N变化差异不大,其原因为有机氮的氨化作用造成NH3-N含量的提高,而外来基质NaAc的添加对有机氮的降解影响不大.在低S/X条件下(0#),两厌氧污泥实验结束后VSS/TSS降低,原因可能为厌氧污泥进行内源代谢,导致VSS/TSS降低.而在高S/X比条件下,VSS/TSS略有提高这可能是由于厌氧微生物生长缓慢,而实验持续时间较短造成.
CH4回收率表示该实验中生成CH4的COD还原值与实验前后COD降低值的比值.AP-BMP中随着S/X的增大,CH4回收率也随之提高,但最高回收率只有52%.其原因推测为AP厌氧污泥中产CH4菌的浓度低、活性差,基质以其它的形式代谢.DH-BMP中1#、2#样品的CH4回收率接近100%,可能由DH厌氧污泥中产CH4菌代谢活跃造成,0#样品由于未添加基质,CH4回收率为43%,主要进行微生物的内源代谢,3#、4#样品中CH4回收率在80%以上,均高于AP-BMP实验中的对应回收率.
3.3 厌氧污泥生物多样性分析如图 3所示,两厂的厌氧污泥中产CH4菌的组成存在着一定的差异.AP厂厌氧消化池中的厌氧污泥Diverse菌群相对丰度达45%,产CH4功能菌主要以产CH4髦毛菌Methanosaeta spp.(280 bps)为主,同时存有少量的产CH4微菌Methanomicrobiaceae(80 bps)、RC-I(389 bps)和产CH4杆菌Methanobacteriaceae(88 bps).同时,DH厌氧消化池中的厌氧污泥产CH4功能菌相对丰度高,Diverse菌群相对丰度仅为7%.产CH4功能菌主要以产CH4髦毛菌Methanosaeta spp.(280 bps)为主,同时存在产CH4微菌Methanomicrobiaceae(80 bps)、RC-I(389 bps)和产CH4杆菌Methanobacteriacea(88 bps).DH污水厂的进水是由完整的市政下水道收集的生活污水,污水中有机含量高,可生化降解性能强,为厌氧消化提供了良好的条件,从而造成了DH厌氧消化池中厌氧污泥产CH4功能菌群丰度较高.
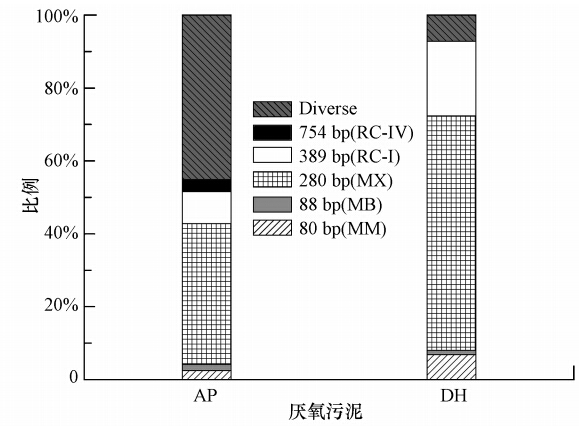 |
| 图 3 AP、DH厌氧污泥中主要T-RFs丰度对比 Fig. 3 Comparison of relative abundance of major T-RFs in AP and DH anaerobic sludges |
SEM镜检AP、DH厌氧污泥结果如图 4所示.AP厌氧污泥镜检中发现了较为稀疏的髦毛菌,同时还存在着1~2 μm的短杆菌、7~10 μm的长杆菌和直径为2 μm的产CH4微粒菌.这些菌群较为分散,菌群间的协同作用不强.DH厌氧污泥菌群与AP污泥相比丰富多样,在基质上依附着大量的髦毛菌,与T-RFLP检测的结果较为吻合.同时还存在着1~2 μm的短杆菌、7~10 μm的长杆菌和双叠球菌等常见的产CH4菌.这些产CH4菌互相交错、依赖形成了丰度较高的产CH4菌群,与DH厌氧污泥实验的较佳的产CH4活性相吻合.
 |
| 图 4 AP和DH厌氧污泥SEM镜检 Fig. 4 Scanning electron micrographs of microbial communities in AP and DH anaerobic sludge |
1)AP、DH两厌氧污泥采用改进的Gompertz模型回归的最大比产气速率数值接近,分别达到了67.93、62.65 mL · g-1 · d-1(以VSS计),但对基质NaAc的半饱和常数Km差异较大,分别为1517和801 mg · L-1,DH厌氧污泥对基质的亲和力高.
2)BMP实验最终的水质变化表明,DH-BMP厌氧污泥中的ORP位于-310~-373 mV之间,低于AP-BMP样品中对应的ORP.在投加基质的条件下,DH厌氧污泥的CH4回收率高于80%,高于AP厌氧污泥的CH4回收率.在高S/X条件下,BMP实验结束后VSS/TSS略有提高.
3)两厌氧污泥T-RFLP和SEM镜检结果与其生化产CH4势较为吻合,AP厌氧污泥中产CH4功能菌菌群稀疏且Diverse菌群相对丰度达45%,而DH厌氧污泥中产CH4功能菌种群密集,Diverse菌群丰度仅为7%.DH厌氧污泥中产CH4功能菌以产CH4髦毛菌Methanosaeta spp.(280 bps)为主,同时存在产CH4微菌Methanomicrobiaceae(80 bps)、RC-I(389 bps)和产CH4杆菌Methanobacteriacea(88 bps).
4)大量剩余污泥的产生是活性污泥工艺面临的一个重要问题.后续可采用剩余污泥为基质,采用BMP的实验方法,考察污泥消化减量过程中产气性能、产甲烷功能菌群的动态变化及水质变化情况,为剩余污泥厌氧消化工艺性能优化提供基础数据.
| [1] | Angelidaki I, Alves M, Bolzonella D, et al.2009. Defining the biomethane potential (BMP) of solid organic wastes and energy crops: a proposed protocol for batch assays [J]. Water Science and Technology,59(5): 927-934 |
| [2] | APHA.1999.Standard Methods for the Examination of Waste and Wastewater(19th edition)[M].Washington, DC:America Public Health Assoc |
| [3] | Chen T H, Hashimoto A G.1996. Effects of pH and substrate:inoculum ratio on batch methane fermentation[J].Bioresource Technology, 56(2/3): 179-186 |
| [4] | Collins G, Woods A, McHugh S,et al.2003.Microbial community structure and methanogenic activity during start-up of psychrophilic anaerobic digesters treating synthetic industrial wastewater [J]. FEMS Microbiology Ecology, 46(2): 159-170 |
| [5] | Elbeshbishy E,Nakhla G,Hafez H.2012.Biochemical methane potential (BMP) of food waste and primary sludge: Influence of inoculum pre-incubation and inoculum source [J]. Bioresource Technology, 110(4): 18-25 |
| [6] | Fernandez B,Porrier P,Chamy R.2001.Effect of inoculum-substrate ratio on the start up of solid waste anaerobic digesters[J]. Water Science and Technology, 44 (4): 103-108 |
| [7] | Gunaseelan V N.2004.Biochemical methane potential of fruits and vegetable solid waste feedstocks[J]. Biomass Bioenergy, 26 (4): 389-399 |
| [8] | Labatut R A, Angenent L T, Scott N R.2011. Biochemical methane potential and biodegradability of complex organic substrates[J]. Bioresource Technology, 102(3): 2255-2264 |
| [9] | Lesteur M, Bellon-Maurel V, Gonzalez C, et al.2010. Alternative methods for determining anaerobic biodegradability: a review[J]. Process Biochemistry, 45(4): 431-440 |
| [10] | Lüdemann H, Arth I, Liesack W. 2000. Spatial changes in the bacterial community structure along a vertical oxygen gradient in flooded patty soil cores [J]. Applied and Environmental Microbiology, 66(2): 754-762 |
| [11] | Marsh T L, Liu W T, Forney L J, et al.1998. Beginning a molecular analysis of the eukaryal community in activated sludge[J]. Water Science and Technology, 37(4/5): 455-460 |
| [12] | Neves L, Oliveira R, Alves M M.2004. Influence of inoculum activity on the biomethanization of a kitchen waste under different waste/inoculum ratios [J]. Process Biochemistry,39(12): 2019-2024 |
| [13] | Noike T, Endo G, Chang J E, et al.1985. Characteristics of carbohydrate degradation and the rate-limiting step in anaerobic digestion [J]. Biotechnology and Bioengineering, 27(10): 1482-1489 |
| [14] | Owen W F, Stuckey D C, Healy Jr J B, et al. 1979. Bioassay for monitoring biochemical methane potential andanaerobic toxicity[J]. Water Research, 13(6): 485-492 |
| [15] | Prashanth S, Kumar P, Mehrotra I.2006. Anaerobic degradability: effect of particulate COD[J]. Journal of Environmental Engineering-ASCE, 132(4): 488-496 |
| [16] | Raposo F, Banks C J, Siegert I, et al. 2006. Influence of inoculum to substrate ratio on the biochemical methane potential of maize in batch tests[J]. Process Biochemistry,41(6): 1444-1450 |
| [17] | Raposo F, Fernandez-Cegri V, De la Rubia M A, et al.2011. Biochemical methane potential (BMP) of solid organic substrates: evaluation of anaerobic biodegradability using data from an international interlaboratory study[J].Journal of Chemical Technology and Biotechnology, 86(8): 1088-1098 |
| [18] | Tillmann L, Michael F.2000. Archaeal polulation dynamics during sequential reduction processes in rice field soil [J]. Applied and Environmental Microbiology, 66(7): 2732-2742 |
| [19] | Zwietering M H, Jongenburger I, Rombouts F M, et al. 1990. Modeling of the bacterial growth curve [J]. Applied and Environmental Microbiology, 56(6): 1875-1881 |
 2014, Vol. 34
2014, Vol. 34


