2. 东华大学 环境科学与工程学院, 上海 201620
2. College of Environmental Science and Engineering, Donghua University, Shanghai 201620
软骨藻酸是赤潮毒素的一种,由海洋硅藻产生的兴奋性神经毒素氨基酸,可在贝类中富集,因最早从红藻属的树枝软骨藻(Chondria armata)中分离出来并确定其结构被命名为软骨藻酸(Fire et al., 2009),人类和海洋哺乳动物误食含有DA的鱼虾贝类后会引起中毒,主要表现在干扰中枢神经系统,发生暂时性失去记忆甚至死亡(Smith et al., 2006;Costa et al., 2010;Jeffery et al., 2004;Mafra et al., 2009).在免疫学的基础上得到快速发展的酶联免疫分析法,以其特异性高、灵敏度高、操作简便、检测迅速和分析成本低的优点被广泛应用于环境中污染物的分析(刘仁沿等,2009;Yu et al., 2009).间接竞争ELISA法是检测抗体常用的方法,其优点是只要变换包被抗原就可利用同一酶标抗体建立检测相应的抗体(Guo et al., 2010).
目前,国内还没有开发出成熟的ELISA 试剂盒,国外已经有商品化的 ELISA检测试剂盒,但价格昂贵.由于以ELISA为基础的免疫学检测方法具有快速、简便、灵敏与经济的特点,适用于大批样品的筛查,因而越来越受到人们的青睐和重视.本实验在课题组对软骨藻酸快速检测技术研究的基础上(王茜等,2012;高利利,2011;刘元嫄等,2011),进一步优化和建立了利用单抗快速检测DA的间接竞争ELISA方法,并对其线性检测范围、检测限、回收率及稳定性等参数进行了研究.同时也利用该方法对部分贝类实际样品进行了初步检测,为最终形成商品化的检测试剂盒奠定了良好基础.
2 材料和方法(Materials and methods) 2.1 试剂与仪器辣根过氧化物酶标记的羊抗鼠(酶标二抗,HRP-IgG)购于上海生工,软骨藻酸单克隆抗体为本实验室自制.常用化学试剂购自中国国药集团,分析纯.其它实验所用仪器和试剂均与文献(王茜,2012)相同.
2.2 试验方法 2.2.1 包被抗原的制备采用碳化二亚胺法合成包被抗原DA-BSA,反应完成后取少量混合物稀释,用紫外可见分光光度计在200~400 nm进行扫描,用以判断DA是否与载体蛋白BSA偶联成功.
2.2.2 抗原及单抗最佳稀释度的选择采用方阵滴定的方法:将包被抗原DA-BSA用碳酸盐缓冲液(pH为9.6)做1∶200、1∶400、1∶800、1∶1600、1 ∶3200、1∶6400、1:12800、1:25600倍稀释,每孔100 μL,4 ℃包被12 h;用PBST洗涤3次,每次3 min,拍干;用1%PVA-PBS做封闭液,37 ℃封闭2 h;一抗用0.1%BSA-PBS做1:200、1:400、1∶800、1∶1600、1∶3200、1∶6400倍稀释,每孔100 μL,每块板同时设有空白和阴性对照,37 ℃温育1 h;用PBST洗涤、拍干;将酶标二抗用0.1% BSA-PBS稀释至1:3000,每孔100 μL,37 ℃温育1 h;洗涤、拍干;每孔加TMB底物液100 μL,室温显色15 min,用2 mol · L-1的浓硫酸每孔50 μL终止反应;在450 nm及630 nm处测定OD值,实际值为OD450-OD630,依据OD值和P/N值筛选抗原和一抗最佳稀释倍数.
在确定的最佳包被抗原和单抗稀释度下,酶标二抗做1:2000、1:3000、1:4000、1:5000和1:6000 倍稀释,进行ELISA测定,依据OD值和P/N值筛选最佳酶标二抗稀释度.
2.2.4 最佳抗原包被条件的选择以包被抗原最佳稀释度包被,设置37 ℃包被1 h后转入4 ℃包被12 h、37 ℃包被2 h转入后4 ℃包被12 h、37 ℃包被3 h后转入4 ℃包被12 h、4 ℃包被12 h、37 ℃包被1 h、37 ℃包被2 h和37 ℃包被3 h等7个包被条件,进行ELISA测定,依据其OD值和P/N值筛选最佳包被条件.
2.2.5 抗原、单抗最佳作用时间和温度的选择在上述最佳条件下,选择在25 ℃、37 ℃和43 ℃ 3个温育温度,抗原和一抗作用30 min、45 min、60 min、90 min,进行ELISA测定,依据其OD值和P/N值筛选抗原、单抗最佳作用温度和时间.
2.2.6 酶标二抗最佳作用时间和温度的选择在上述最佳条件下,选择在25 ℃、37 ℃和43 ℃ 3个温育温度,二抗温育30 min、45 min、60 min、90 min,进行ELISA测定,依据其OD值和P/N值筛选酶标二抗最佳作用时间和温度.
2.2.7 最佳显色条件的选择在上述最佳条件下进行ELISA测定,于室温和37 ℃条件下,避光和不避光显色5 min、10 min、15 min、20 min、30 min,依据其OD值和P/N值筛选最佳显色条件.
2.2.8 标准曲线的制作利用上述建立的最佳条件包被抗原,洗涤;一抗稀释至最佳稀释度,每孔加入50 μL;将DA用PBS配成100 ng · mL-1、50 ng · mL-1 、20 ng · mL-1、10 ng · mL-1、4 ng · mL-1、2 ng · mL-1、0 ng · mL-1系列浓度,每孔加入50 μL.按之前建立的最佳条件进行ELISA测定.
2.2.9 重复性试验将DA稀释为0、20、50和100 ng · mL-1 4个不同浓度,按上述建立的间接竞争ELISA法操作步骤,同一浓度在同一板内、不同时间、相同条件下重复检测5次,同一浓度在不同板内、同一时间、相同条件下重复5次计算板内精密度和板间精密度.
2.2.10 加标回收率的测定在阴性样品中分别添加 10、20和50 ng · mL-1 的DA,按照本文建立的间接竞争ELISA 方法测定,计算加标回收率.
3 结果与讨论(Results and discussion) 3.1 包被抗原的制备与鉴定软骨藻酸为小分子化合物,属于半抗原类物质,可以与抗体发生反应,具有抗原性,但是无法与有机体产生免疫应答反应.为使软骨藻酸具有免疫原性,需将它与大分子载体偶联形成包被抗原.本研究选择载体蛋白BSA对DA进行偶联.反应完成后,将合成完的偶联物DA-BSA和DA、BSA稀释,用紫外光谱仪进行扫描,所获得的紫外吸收谱如图 1所示.
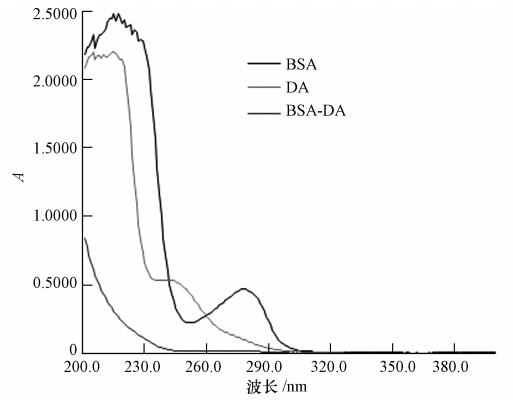 |
| 图 1 DA、BSA、DA-BSA紫外吸收图谱 Fig. 1 UV absorption spectrums of DA,BSA and DA-BSA |
由图 1可以看出,DA的UV特征吸收峰在242 nm处,载体蛋白BSA在215 nm和278 nm处各有一个吸收峰,而合成的偶联物的紫外吸收图谱与DA和BSA图谱的峰型及最大吸收峰有明显的区别,因此推断DA成功偶联到BSA上,成功制得包被抗原DA-BSA.
3.2 包被抗原和一抗的最佳稀释度的确定试验采用方阵滴定法,筛选出抗原和一抗最佳稀释度,从而使抗体与抗原充分结合,提高了反应的灵敏度.由表 1可见:随着一抗稀释倍数的增加OD逐渐降低.当抗原稀释12800倍、一抗稀释400倍数时,OD值为1.031,P/N值为21.6.因此确定抗原和一抗的最佳稀释度为1:12800倍和1:400倍.
| 表1 包被抗原和一抗最佳稀释度的确定 Table.1 Optimization of the coating antigen and antibody concentrations |
将酶标羊抗小鼠二抗分别稀释2000、3000、4000、5000和6000倍,分别测其OD值并计算出P/N值,结果如表 2所示.
| 表2 二抗使用浓度与P/N值变化 Table.2 Variations between P/N value and HRP-IgG concentration |
当酶标二抗稀释度为1:3000时,OD值为1.006,P/N值为17.9,故酶标二抗最佳稀释度为1:3000倍.
3.4 抗原包被条件的确定将最佳稀释度的抗原在不同包被条件下进行ELISA测定,结果如表 3所示.当抗原在4 ℃包被12 h时OD值为0.9820,P/N最大,故最佳包被条件为4 ℃包被12 h.
| 表3 抗原最适包被条件的确定 Table.3 Conditional optimization of antigen coating |
分别选择25 ℃、37 ℃和43 ℃为反应温度,抗原和一抗作用30 min、45 min、60 min、90 min.研究结果显示:在37 ℃反应60 min时OD值为0.987,P/N值为16.8,因此抗原抗体最佳反应温度为37 ℃,反应时间 60 min.
3.6 酶标二抗最佳作用时间和温度的确定分别选择25 ℃、37 ℃和43 ℃为反应温度,二抗反应30 min、45 min、60 min和90 min.研究结果显示:在43 ℃反应30 min时OD值为0.963,P/N值为49.6,因此酶标二抗最佳反应温度为43 ℃,反应时间30 min.
3.7 最佳显色条件的选择与确定以避光和不避光为反应条件,分别在室温和37 ℃反应5 min、10 min、15 min、20 min和30 min.结果显示:在室温不避光条件下,反应20 min时OD值为0.977,P/N值为8.8,因此最佳显色条件为室温不避光显色20 min.
3.8 标准曲线的绘制以不同浓度标准品的对数值为横坐标,以B/B0值为纵坐标绘制标准曲线,计算曲线的回归方程和可决系数,B/B0=1.2时对应的DA浓度值即为最 低检测限.所获标准曲线如图 2所示,曲线方程为y=-0.0896x+0.975,R2 = 0.9943.利用回归方程计算出该间接ELISA法的最低检测限为4.86 ng · mL-1.
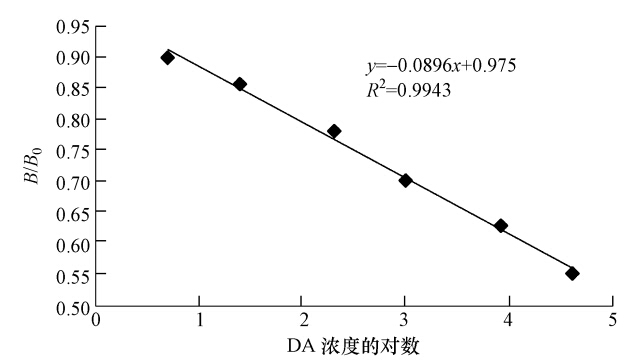 |
| 图 2 间接竞争ELISA标准工作曲线 Fig. 2 St and ard working curve of ic-ELISA |
间接竞争ELISA标准曲线的孔间差异如表 4所示.间接竞争ELISA标准曲线的板间差异如表 5所示.由表 4和表 5计算出OD值的孔间变异系数为2.81%~7.08%,板间变异系数为2.46%~5.96%,均小于15.00%,表明本方法具有良好的重现性.
| 表4 间接竞争ELISA标准曲线的孔间差异 Table.4 The variation among holes in st and ard curve of ic-ELISA |
| 表5 间接竞争ELISA标准曲线的板间差异 Table.5 The variation between-assay in st and ard curve of ic-ELISA |
取阴性样本添加一定浓度的DA,其回收率如表 6所示.可以看出,该法的添加回收率在85%~115%范围内,可见本研究建立的间接竞争ELISA法能够满足一般检测要求.
| 表6 间接竞争ELISA加标回收率 Table.6 Sample recovery ofic-ELISA |
本文建立的间接竞争ELISA法快速、灵敏、重现性好.不仅能满足国际规定的20 ng · mL-1 DA安全限值的测定要求,而且也适合应用于现场对大批量样本的检测.
| [1] | Costa L G, Giordano G, Faustman E M. 2010.Domoic acid as a developmental neurotoxin[J]. Neuro Toxicology, 31(5):409-423 |
| [2] | Fire S E, Wang Z H, Leighfield T A, et al.2009.Domoic acid exposure in pygmy and dwarf sperm whales (Kogia spp.) from southeastern and mid-Atlantic US waters[J]. Harmful Algae, 8(5): 658-664 |
| [3] | 高利利, 程金平, 刘元嫄, 等. 2011.软骨藻酸胶体金免疫层析检测试纸条的研制[J].环境科学, 32(8):2492-2496 |
| [4] | Guo D, Wang B, Han F, et al.2010.RNA interference therapy for glioblastoma[J]. Expert Opin Biol Ther, 10(6): 927-936 |
| [5] | Jeffery B, Barlow T, Moizer K, et al.2004.Amnesic shellfish poison[J]. Food and Chemical Toxicology, 42(4): 545-557 |
| [6] | 刘仁沿, 许道艳, 董玉华, 等. 2009.海水和贝类中软骨藻酸的酶联免疫吸附分析方法研究[J]. 卫生研究, 38 (5 ): 622-624 |
| [7] | 刘元嫄, 高利利, 程金平, 等. 2011.软骨藻酸间接竞争ELISA检测方法的研究[J].环境化学, 30(6):1192-1196 |
| [8] | Mafra L L, Legar C, Bates S S, et al. 2009.Analysis of trace levels of domoic acid in seawater and plankton by liquid chromatography without derivatization using UV or mass spectrometry detection[J]. Journal of Chromatography A, 1216 (32 ): 6003-6011 |
| [9] | Smith E A, Papapanagiotou E P, Brown N A, et al.2006.Effect of storage on amnesic shellfish poisoning (ASP ) toxins inking scallops (Pecten maximus )[J]. Harmful Algae, 5 (1):9-19 |
| [10] | 王茜. 2012.抗软骨藻酸单克隆抗体直接竞争ELISA方法的建立及试剂盒的组装[D].上海:上海交通大学 |
| [11] | 王茜, 程金平, 高利利, 等. 2012.软骨藻酸直接竞争ELISA方法的建立及优化[J].环境科学, 33(2):647-651 |
| [12] | Yu Z, Feng G P, Yan S L, et al. 2009.Colloidal gold probe-based immunochromatographic assay for the rapid detection of brevetoxins in fishery product samples[J]. Biosensors and Bioelectronics, 24(8): 2744-2747 |
 2014, Vol. 34
2014, Vol. 34


