2. 临沂大学生命科学院, 临沂 276000
2. School of Life Science, Linyi University, Linyi 276000
汞(Hg)是一种可生物积累的有毒有害重金属,在土壤中积累会对环境及人类健康产生危害(王梅等,2011).从1956年日本“水俣病”爆发开始,Hg污染问题就已引起人们的关注和重视(Thomas et al., 1999).Hg的天然释放和人为污染都是土壤中Hg的重要来源,Hg进入土壤后由于土壤矿物对Hg具有强烈的吸附作用,因此,各类土壤中90%以上的矿物组成对Hg的吸持特性是决定土壤中Hg环境活性的重要因素.
土壤重金属污染的修复方式有很多种,近年来,从化学修复中逐渐分出来的矿物修复被誉为继物理修复和化学修复尤其是生物修复方法之后的第四类污染治理方法(杭小帅等,2013).天然矿物材料由于其独特的结构和优异的性质,对环境中重金属元素有较强的吸附能力,进而会影响它们在环境中的浓度和迁移能力(Chang et al., 2010).铁锰氧化物和铁铝氧化物是土壤中两种常见的氧化物,自然界中存在的天然铁锰矿物材料具有稳定的电荷零点,比表面积大、表面活性强,其对环境中重金属元素的吸附、固定控制着它们在环境中的浓度、存在形态和化学行为.近年来,有关氧化物在环境重金属修复中的应用也受到越来越多的关注(Miyata et al., 2007;张林静等,2013).有研究表明,MnO2、Fe2O3等矿物材料对Hg 有较大的吸附容量,且固持能力强(姚爱军等,2004).
因此,本试验通过在重金属Hg污染土壤中添加铁锰和铁铝氧化矿物,探讨两种氧化物对土壤Hg的吸附作用,阐明两种氧化物对土壤Hg有效性的影响,为寻求各类土壤中Hg环境活性规律及制定相应的调控措施提供理论依据.
2 材料与方法(Materials and methods) 2.1 复合氧化物的制备铁锰复合氧化物的合成(Chang et al., 2010):将一定体积1 mol · L-1的NaOH溶液加入到0.025 mol · L-1的KMnO4溶液中,在缓慢搅拌下,以5 mL · min-1的速度向溶液中滴加0.045 mol · L-1 FeCl2溶液,直至悬液pH达到8.0;然后储于塑料容器中,在60 ℃恒温箱中老化48 h,离心分离得到沉淀物,用去离子水冲洗干净,将沉淀物在60 ℃下真空干燥,即铁锰复合氧化物.
铁铝复合氧化物的合成(Basu et al., 2012):将三氯化铁(FeCl3 · 6H2O)和三氯化铝(AlCl3 · 6H2O)配成混合溶液,置于烧杯中,在不断搅拌的情况下,向溶液中滴加3 mol · L-1 NaOH溶液,调节溶液的pH为7.4继续搅拌均匀,储于塑料容器中,在60 ℃恒温箱中老化48 h;然后离心分离得到沉淀物,用去离子水冲洗干净,将沉淀物在60℃下真空干燥,得到铁铝复合氧化物.
2.2 土壤采集于临沂市区内进行土样采集,并采用GPS定位,每种土样取10个点的表层(0~20 cm)土壤制成混合样品.土样1取自临沂市滨河大道沿岸(118°34′E,35°06′N),土样2取自临沂市青年路与沂水路交汇处(118°35′E,35°05′N).
土壤基本理化性质为,土样1:pH=7.81,速效磷 0.45 mg · kg-1,速效钾 189.09 mg · kg-1,有效态Hg 3.58 mg · kg-1,全Hg 17.62mg · kg-1;土样2: pH=7.60,速效磷 0.49 mg · kg-1,速效钾 170.84 mg · kg-1,有效态Hg 2.10 mg · kg-1,全Hg 13.75 mg · kg-1.
2.3 试验设计实验采用土培的方法,土壤风干磨碎过20目筛,装入塑料盆中,每盆装入500 g土壤.实验设计4个处理,分别为铁铝氧化物+土样1、铁铝氧化物+土样2、铁锰氧化物+土样1、铁锰氧化物+土样2,每个处理重复16次.其中,氧化物的加入量均为5 g · 盆-1,将氧化物与土壤充分混匀后,向塑料盆中加入适量去离子水,保持土壤湿润,将塑料盆放在室温下进行培养,期间定期添加去离子水.分别在土样培养后的第3、5、7、14 d取样.每次每个处理取4个重复,样品风干后,磨碎用作Hg含量的测定.
2.4 测定方法有效态汞含量的测定(Tessier et al., 1979):分别称取2.0 g过20目筛的土壤样品于50 mL 离心管中,准确加入20 mL浓度为1 mol · L-1 的氯化镁溶液(pH=7.0),摇匀,盖上盖子,于(25±2)℃下在振荡器上振荡2 h,取下,离心15 min;将清液过滤,滤液用等离子体发射光谱(VISTA-MPX,美国Varian公司)测定.
2.5 数据分析分别用初始土壤中Hg的含量减去培养不同时间后土壤中Hg的含量,作为培养不同时间氧化物对Hg的吸附量(Xt);然后分别用零级速率方程(1)、抛物线扩散方程(2)、Elovich方程(3)、权函数方程(4)、指数方程(5)进行拟合(Zhu et al., 2000),以说明氧化物对土壤中Hg的吸附规律.
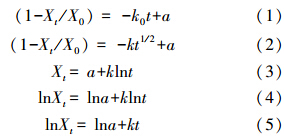
式中,Xt为在t时刻氧化物对Hg的吸附量;X0为反应达到平衡时Hg的吸附量,可通过Xt与1/t的关系外推到1/t=0求得;k0为零级方程的常数;k为其它速率方程的常数;a或lna为方程的截距.不同方程的拟合程度可以通过可决系数(R2)、标准误差(SE)及显著水平(Sig.)来比较.
3 结果与讨论(Results and Discussion) 3.1 添加铁铝氧化物对土壤Hg有效性的影响加入铁铝氧化物后土样1和土样2中有效态Hg含量随时间的变化规律如图 1所示.从图中可以看出,在最初几天氧化物的加入使土壤中有效态Hg的含量迅速下降,土样1中有效态Hg的含量从开始的3.58 mg · kg-1下降到第7 d的0.46 mg · kg-1,然后缓慢降低,到实验结束时,土壤中有效态Hg的含量降低了94.60%.土样2中Hg的含量一直下降,从最初的2.10 mg · kg-1下降到第14 d的0.14 mg · kg-1,下降率达到93.11%.
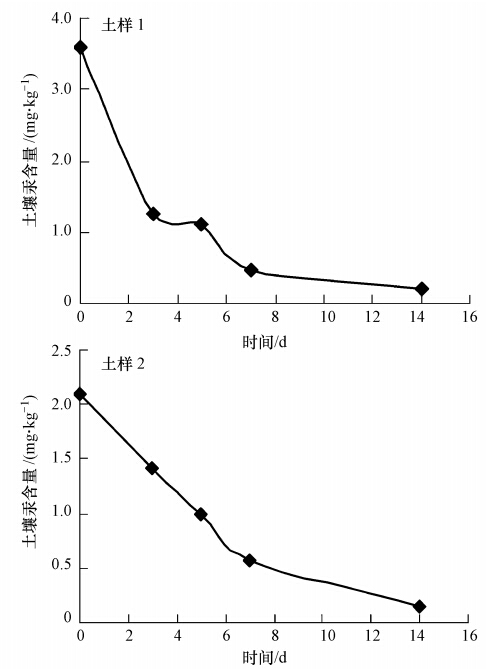 |
| 图 1 添加铁铝氧化物后土壤有效态Hg含量随时间的变化规律 Fig. 1 Changes of available Hg content after Fe-Al oxides added in soil |
添加铁锰氧化物后土壤有效态Hg含量的变化如图 2所示.氧化物加入到土壤后,由图可知,随着时间的推移土样1和土样2中有效态Hg的含量均持续降低,第5 d两种土壤中有效态Hg的含量均减少了60%以上;14 d后,两种土样中有效态Hg的含量分别降低了88.69%和87.85%.
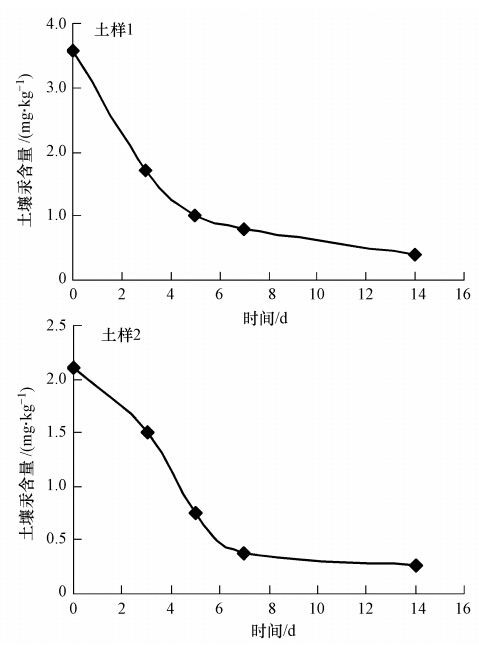 |
| 图 2 添加铁锰氧化物后土壤有效态Hg含量随时间的变化规律 Fig. 2 Changes of available Hg content after Fe-Mn oxides added in soil |
当今世界每年都向环境排放大量的重金属污染物,据不完全估计,平均每年排放的Hg约15万t(杭小帅等,2013).国家土壤环境质量标准(表 1)中三级标准的全Hg含量为1.5 mg · kg-1以上,本实验所采用的两种土壤中有效态Hg含量均远远高于三级标准.通过铁锰及铁铝复合氧化物在Hg污染土壤中的添加,可以看出两种氧化物在土样1和土样2中的添加均明显改善了土壤质量,在实验第5 d土样1中两种处理的有效态Hg含量接近1.0 mg · kg-1,土样2中两种氧化物处理的有效态Hg含量均低于1.0 mg · kg-1,与二级质量标准中全汞含量持平(根据土壤pH从表 1选择);而到实验第14 d,两种氧化物处理下,两种土壤中有效态Hg含量小于或接近0.15 mg · kg-1,基本达到一级质量标准中全汞的水平.这充分说明两种氧化物对土壤中Hg污染具有显著的修复作用,对土壤污染治理具有重要的作用.
| 表 1 土壤环境质量标准(GB 15618—1995) Table 1 Environmental quality st and ard for soils |
有关环境中重金属的去除方式有很多报道,其中包括沉淀、蒸发、膜处理、离子交换等(Chiarle et al., 2000;Tang et al., 2007;Basha et al., 2009).而在去除低浓度重金属时,吸附被认为是一种效率高、花费低的方式(Neda et al., 2013),且包括一些矿物材料在内的很多吸附剂被应用在对重金属的吸附上.环境中氧化物的形式有很多种,但在实际环境中氧化物很难以单一氧化物的形式存在,多数氧化物共存于环境中(Chang et al., 2010).因此,有关复合氧化物在重金属吸附方面的作用日益受到关注.研究表明,铁铝及铁锰复合氧化物对环境中砷(梁美娜等,2006;常方方等,2006)、镉(侯秀等,2009)等重金属有较强的去除作用.但不同的氧化物由于其结构和性质的不同,吸附能力有较大的差别.本研究表明,两种铁复合氧化物均为良好的土壤Hg吸附剂,且铁铝氧化物对两种土样中Hg的吸附作用均高于铁锰氧化物.说明铁铝氧化物对Hg表现出更强的吸附能力,两种氧化物之间的差异,还需后续通过对其结构及性质的的研究进一步阐明.而氧化物加入土壤后,土壤中汞的有效性急剧下降,这主要是由于土壤汞形态发生转变的原因,氧化物的加入致使土壤有效态汞转变为氧化物结合态汞,从而活性降低.
3.3 铁铝氧化物对土壤Hg吸附作用的曲线拟合表 2是铁铝氧化物对土样1和土样2中Hg吸附作用的曲线拟合参数.从表中可以看出,Elovich方程和权函数方程可以较好地描述氧化物对土样1中Hg的吸附规律,均达到显著水平,但相比之下权函数方程拟合的误差(0.073)较小,因此,铁铝氧化物对土样1中Hg的吸附规律可以用方程lnXt =0.542+0.265lnt来描述.铁铝氧化物对土样2 中Hg的吸附作用拟合曲线中,抛物线扩散方程、Elovich方程和权函数方程3种方程的拟合度均较高,R2分别为0.949、0.984和0.942,并且均达到显著水平.其中,Elovich方程的拟合度最高,显著系数达到0.08,且误差最小为0.084,因此,铁铝氧化物对土样2 中Hg的吸附规律可用方程Xt = 1.459+0.748lnt来描述.
| 表 2 铁铝氧化物对土壤Hg吸附作用的曲线拟合参数 Table 2 The curve fitting parameter of the adsorption effect of Fe-Al binary oxide on Hg in soil |
铁锰氧化物对土壤中Hg的吸附作用拟合参数见表 3,结果显示,铁锰氧化物对土样1中Hg的吸附规律以Elovich方程拟合效果最优,R2、Sig.和SE分别为0.935、0.033和0.170;其次是权函数方程也有较高的拟合度,且达到显著水平.土样2的结果显示,选用的几种方程中Elovich方程的可决系数最大,误差最小,但所有的方程均未达到显著水平.
| 表 3 铁锰氧化物对土壤Hg吸附作用曲线拟合参数 Table 3 The curve fitting parameter of the adsorption effect of Fe-Al binary oxide on Hg in soil |
用来描述吸附、解吸动力学过程的数学模型包括两类:一类是建立在化学动力学模型基础上的,如一级反应动力学方程;另一类是经验性方程,如Elovich方程及权函数方程等(Mehdi et al., 2011).各方程的物理意义不尽相同:抛物线方程反映了吸附-解吸过程中的扩散转运机制;Elovich表面反应动力学模型常用于土壤及矿物吸附反应的动力学研究,它表明吸附速率随着吸附量(或覆盖度)的增加呈指数减少(陈文等,2007;Ho et al., 2004).为了解复合氧化物对土壤Hg的吸附动力学机制,采用零级速率方程、抛物线扩散方程、Elovich方程、权函数方程及指数方程对试验数据进行拟合,综合以上方程的可决系数及显著水平(表 2、3),发现Elovich方程最能反映两种氧化物对土壤中Hg的吸附过程,其次是抛物线方程或权函数方程,表明氧化物对土壤中Hg的固定主要与Hg在固体表面覆盖率及扩散作用有关.
4 结论(Conclusions)1)矿物材料在环境重金属去除中的应用越来越多,本研究结果表明,两种铁氧化物对土壤中Hg的有效性有较大的影响.14 d内,添加铁铝氧化物后,两种土壤中的有效态Hg含量分别降低了94.6%和93.1%;添加铁锰氧化物后,两种土样中的有效态Hg含量分别降低了88.6%和87.9%,可见两种氧化物是土壤中Hg的有效吸附剂.
2)方程拟合结果显示,铁铝氧化物对土壤中Hg的吸附规律以Elovich方程和权函数方程拟合度较好,其次是抛物线方程.铁锰氧化对土壤中Hg的吸附规律与Elovich方程符合最好,零级速率方程及指数方程拟合效果则相对较差.
致谢: 特别感谢中国科学院生态环境研究中心的曲久辉老师和兰华春老师在文献传递方面给予的帮助.
| [1] | Basha S, Murthy Z V P, Jha B. 2009. Sorption of Hg (Ⅱ) onto carica papaya: experimental studies and design of batch sorber[J]. Chemical Engineering Journal, 147(2/3):226-234 |
| [2] | Basu T, Gupta K, Ghosh U C. 2012. Performances of As(V) adsorption of calcined synthetic iron (Ⅲ)-aluminum(Ⅲ) mixed oxide in the presence of some groundwater occurring ions[J]. Chemical Engineering Journal, 183:303-314 |
| [3] | Chang F F, Qu J H, Liu R P, et al. 2010. Practical performance and its efficiency of arsenic removal from groundwater using Fe-Mn binary oxide[J]. Journal of Environmental Sciences, 22(1):1-6 |
| [4] | 常方方, 曲久辉, 刘锐平, 等. 2006. 铁锰复合氧化物的制备及其吸附除砷性能[J].环境科学学报, 26 (11): 1769-1774 |
| [5] | 陈文, 魏群, 张伟. 2007. 涂铁砂吸附镉的动力学研究[J].环境科学与技术, 30(9):36-38 |
| [6] | Chiarle S, Ratto M, Rovatti M.2000.Mercury removal from water by ion exchange resins adsorption[J].Water Research, 34(11):2971-2978 |
| [7] | 杭小帅, 王火焰, 周健民. 2013. 长江三角洲地区土壤重金属污染的防治与调控[J].土壤通报, 44(1):245-251 |
| [8] | 杭小帅, 周健民, 王火焰, 等. 2007.粘土矿物修复重金属污染土壤[J].环境工程学报, 1(9): 113-120 |
| [9] | Ho Y S, Mckay G.2004. Sorption of copper from aqueous by peat[J]. Water, Air and Soil Pollution, 158: 77-97 |
| [10] | 侯秀, 王祖伟. 2009. 铁锰氧化矿物添加对土壤镉有效态及生物效应的影响[J].农业环境科学学报, 28(11):2313-2317 |
| [11] | 梁美娜, 刘海玲, 朱义年, 等. 2006.复合铁铝氢氧化物的制备及其对水中砷(V)的去除[J].环境科学学报, 26(3):438-446 |
| [12] | Mehdi J S, Ali M, Ataallah S.2011.Mercury(Ⅱ) removal from aqueous solutions by adsorption on multi-walled carbon nanotubes[J]. Korean Journal of Chemical Engineering, 28(4):1029-1034 |
| [13] | Miyata N Y, Tani Y, Sakata M, et al. 2007. Microbial manganese oxide formation and interaction with toxic metal ions[J]. Bioscience and Bioengineering, 104(1): 1-8 |
| [14] | Neda A, Tahereh K.2013.Acomparison on efficiency of virgin and sulfurized agro-based adsorbents for mercury removal from aqueous systems[J]. Adsorption, 19:189-200 |
| [15] | Tang X H, Zhang X M, Guo C C, et al. 2007. Adsorption of Pb2+ on chitosan cross linked with triethylene tetramine[J].Chemical Engineering and Technology, 30(7): 955-961 |
| [16] | Tessier A, Campbell P G C, Bisson M.1979.Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry, 51:844-851 |
| [17] | Thomas D B, Dennis N S, Richard A H, et al.1999. Mercury measurement and its control, what we know, have learned, and need to further investigate[J]. Air and Waste Manage Association, 6:1-9 |
| [18] | 王梅, 黄标, 孙维侠, 等. 2011.强烈人为作用下城镇周围有效态汞的空间变异及其积累迁移规律[J].土壤学报, 48(3):506-514 |
| [19] | 姚爱军, 青长乐, 牟树森. 2004.土壤矿物对有效态汞的吸持特性研究[J].中国生态农业环境, 12 (4): 129-131 |
| [20] | 张林静, 张琼, 郑袁明, 等. 2013.环境修复中锰氧化物与变价重金属交互作用的研究进展[J].环境科学学报, 33(6):1519-1526 |
| [21] | Zhu D W, Chen X H, Cheng D S, et al.2000.Electrical characteristics and desorption kinetics of soil boron[J]. Pedosphere, 10(1):61-68 |
 2014, Vol. 34
2014, Vol. 34

