2. 环境保护部南京环境科学研究所, 南京 210042;
3. 国家环境保护土壤环境管理与污染控制重点实验室, 南京 210042
2. Nanjing Institute of Environmental Science, Ministry of Environmental Protection, Nanjing 210042;
3. State Environmental Protection Key Laboratory of Soil Envionmental Mangement and Pollution Control, Nanjing 210042
随着我国工业化、城市化进程的加快,近年来在城镇周边出现了大量的废弃农药厂、化工厂,并遗留下一系列的场地土壤污染问题.重金属和有机氯农药是两种典型的土壤污染物,在土壤中经常被同时发现,并构成复合污染.这些污染物有可能通过土-气、土-水等圈层的循环对人体健康产生危害(丛鑫等,2008),对周边土壤环境的生态安全构成威胁,因而亟需对这类土壤进行治理修复.但目前适用于此类复合污染场地土壤的修复技术还相对匮乏,很多单纯针对有机物或重金属污染场地的技术,包括气提、热脱附、生物修复等都难以实现两类污染物的同时治理(庄绪亮,2007).而对于有机物和重金属复合污染场地的修复,化学淋洗被认为是很有应用前景的技术.表面活性剂是一种常用的土壤淋洗剂,主要包括化学和生物表面活性剂.但化学表面活性剂由于其对微生物的毒害性和难生物降解性,容易在环境中造成二次污染(Banat et al,2000).生物表面活性剂因其毒性小、易于生物降解及“绿色”的生产工艺等特性(Mulligan,2005;李玉双等,2011),在污染土壤的淋洗修复中越来越受到关注.
鼠李糖脂作为目前研究和应用最为广泛的生物表面活性剂,具有对有机物和重金属同时强化解吸的效果(Mulligan et al., 2001a;彭立君,2008).它可通过胶束疏水内核的分配作用,对污染土壤中的多种有机污染物包括杀虫剂(Mata-Sandoval et al., 2001)、PAHs(Lafrance et al., 1998;Bordas et al., 2005;Noordman et al., 1998)、石油烃(Urum et al., 2004)等达到增溶和淋洗效果.此外,鼠李糖脂特有的羧基、羟基结构使得它还能与重金属形成可溶性螯合物,因此,也可作为重/非金属(如Cr、Cd、As等)污染土壤的强化淋洗剂(Mulligan et al., 2001b;Asci et al., 2008;Wang et al., 2009).尽管鼠李糖脂在污染土壤修复领域具有广阔的应用前景,但目前关于鼠李糖脂对有机氯农药和重金属复合污染的同步淋洗修复还未见报道.
因此,本文选取林丹作为土壤有机氯农药代表,Pb、Cd作为重金属代表,研究鼠李糖脂对林丹的增溶效果及其影响因素,鼠李糖脂对重金属Pb、Cd的配合能力及其影响因素,鼠李糖脂在土壤上的吸附行为,鼠李糖脂对林丹及重金属复合污染土壤的同步淋洗效果.以期为有机物重金属复合污染土壤的修复提供理论基础.
2 材料与方法(Materials and methods) 2.1 供试材料模拟污染土壤的配制:于南京紫金山周边采集清洁土壤,自然风干,研磨后过10目(2 mm)筛,四分法取1.0 kg,与一定体积的Pb(NO3)2、Cd(NO3)2溶液混合(土壤Pb、Cd的目标含量为500 mg · kg-1),充分搅拌后自然风干;再研磨过10目筛,与林丹(γ六六六)正己烷溶液混合(林丹的目标含量为100 mg · kg-1),搅拌均匀,避光风干,待正己烷充分挥发后,转移至密封封口瓶中静置老化2个月,待用.使用前测定土壤中林丹、Pb、Cd的总含量分别为120.1、581.1、554.3 mg · kg-1.供试土壤pH为5.1(水土比,2.5 ∶ 1,mL · g-1),土壤有机质含量为44.3 g · kg-1,CEC为32.8 cmol · kg-1.根据国际制土壤质地分类标准,供试土样为砂质壤土,其中,粗砂含量占32.6%,细砂含量占32.4%,粉粒含量占28.7%,粘粒含量占6.3%.
2.2 试剂鼠李糖脂(纯度95%)购自湖州紫金生物有限公司,SP葡聚糖凝胶C25树脂、Pipes缓冲液购置于上海楷洋生物有限公司,林丹(纯度98.5%)购置于Dr. Ehrenstorfer GrmbH,Cd(NO3)2、Pb(NO3)2、 NaCl等均为分析纯,硝酸、高氯酸等为优级纯.
2.3 仪器加速溶剂萃取仪(Dionex ASE300,美国),气相色谱仪(GC,Agilent 6890N,美国),配备电子捕获检测器(ECD)和HP5色谱柱(30.0 m×0.32 mm×0.25 μm),火焰原子吸收分光光度计AAS(PerkinElmer AA800,美国),电感耦合等离子体质谱ICPMS(Thermal Scientific Xseries,美国),恒温振荡器(Eppendorf Innova 43,德国),高速冷冻离心机(HITACHI CR21 G Ⅲ,日本),表面张力仪(JK99B,上海中晨),DKZ系列电热恒温振荡水槽,石墨消解仪(DEENA美国),SE812J氮吹仪,pH计(Sartorius PB21,德国),Millipore系列纯化水机等.
2.4 实验方法 2.4.1 鼠李糖脂临界胶束浓度及组分的测定鼠李糖脂临界胶束浓度(Critical micelle concentration,CMC)的测定采用表面张力仪DuNouy环法(Berselli et al., 2004):配置系列浓度的鼠李糖脂溶液,分别测定其表面张力,以表面张力对表面活性剂浓度的对数作图,曲线转折点相对应的浓度即为鼠李糖脂的CMC值.鼠李糖脂组成由LCESIMS分析(李克斌等,2004).
2.4.2 鼠李糖脂对林丹的增溶实验实验采用批量平衡法,在40 mL具塞玻璃瓶(盖顶为聚四氟乙烯密封垫)中进行.向瓶中加入一定体积的林丹正己烷溶液(保证林丹过量),待正己烷挥发殆尽,加入10 mL系列浓度的鼠李糖脂溶液(pH=7.0±0.1).将样品水平置于恒温振荡器上,(25±1)℃下振荡48 h后,4000 r · min-1离心3 min,取上清液经0.45 μm醋酸纤维膜过滤.取一定体积滤液,加入适量正己烷,振荡器上振荡萃取45 min,于4000 r · min-1离心10 min,加盐破除乳化,取上层萃取液1 mL,用GCECD分析林丹含量.实验设3个平行样.选择合适的鼠李糖脂浓度,考察不同pH(5.0~10.0)及盐度条件(NaCl浓度为0~1 mol · L-1)对增溶的影响.3组平行实验结果表明,正己烷对溶液中林丹萃取的回收率为81.0%~101.1%,相对标准偏差为8.9%.
2.4.3 鼠李糖脂对Pb、Cd的配合实验实验采用批量平衡法,向200 mL HDPE瓶(提前在酸中浸泡24 h)中依次加入一定体积的鼠李糖脂溶液、0.4 mL 1000 mg · L-1的Pb(NO3)2或Cd(NO3)2溶液(重金属最终浓度40 mg · L-1)、5 mL(0.2 mol · L-1)的Pipes缓冲液及100 mg SP Sephadex C25树脂(OchoaLoza et al., 2001),溶液最终体积为10 mL.用1 mol · L-1 NaOH及HNO3调节溶液pH至7.0±0.1.将样品水平置于恒温振荡器上,(25±1)℃及200 r · min-1下振荡2 h后,4000 r · min-1离心3 min,取上清液4 mL,加入0.2 mL浓硝酸,振荡1 h,用AAS及ICPMS分别测定其中Pb、Cd的浓度.选取合适的鼠李糖脂浓度,进一步考察不同pH条件(5.0~10.0)对配合的影响.
实验采用批量平衡法,在40 mL具塞玻璃瓶中进行,每组3个平行.向瓶中依次加入20 mL鼠李糖脂溶液及2.0 g风干后的清洁土,调节体系pH至7.0±0.1.将样品水平置于恒温振荡器上,(25±1)℃下振荡48 h后,5000 r · min-1离心10 min,取上清液过0.45 μm滤膜.采用表面张力仪DuNouy环法(Berselli et al., 2004)测定水相中鼠李糖脂含量.选择合适的鼠李糖脂浓度,考察不同pH条件(5.0~10.0)对鼠李糖脂在土壤上吸附的影响.
2.4.5 鼠李糖脂对林丹及重金属污染土壤的同步淋洗实验采用批量平衡法,在玻璃瓶中加入2.0 g污染土壤及20 mL鼠李糖脂溶液.设置鼠李糖脂浓度(0~50000 mg · L-1)及pH条件(5.0~10.0),于振荡器上恒温振荡24 h后,在10000 r · min-1下离心10 min,将上清液过0.45 μm滤膜.用正己烷萃取并用GCECD分析淋洗液中的林丹含量.另取滤液4 mL,加入0.2 mL浓硝酸,振荡1 h,用AAS及ICPMS分别测定Pb、Cd的含量.
2.4.6 鼠李糖脂淋洗前后土壤中重金属形态的测定在玻璃瓶中加入2.0 g模拟污染土样,鼠李糖脂浓度为1%,体系pH 7.0,按2.4.5节的方法进行土壤淋洗实验.将淋洗后的土壤自然风干,用Tessier连续提取法(Fernandez-Perez et al., 2000)将土壤中重金属按照可交换态、碳酸盐结合态、铁锰氧化物结合态和有机结合态进行逐级分离后测定,提取后的土样进一步经王水高氯酸消解后,分析其中残渣态重金属含量.以上重金属含量测定采用原子吸收分光光度法.
2.4.7 林丹的测定GCECD分析条件:进样量为 1.0 μL(不分流进样),载气流量1.0 mL · min-1(99.999%高纯氮),进样口温度 225 ℃,检测器温度300 ℃;程序升温:100 ℃保持 2 min,以20 ℃ · min-1升温到195 ℃,再以 3 ℃ · min-1升温到 270 ℃,保持5 min.
3 结果(Results) 3.1 鼠李糖脂组成及基本性质表 1结果显示,鼠李糖脂由5种单体组成,其主要成分为单鼠李糖脂(Rha),约占83.6%.各单体中,RhaC10C10所占比例最高,约为67.2%,其次为RhaRhaC10C10,占到16.4%.由各单体相对分子质量及相对丰度信息经加权推算得出,该鼠李糖脂混合物的平均相对分子质量为523.7.同时,由表面张力仪测得鼠李糖脂的CMC值约为50 mg · L-1.
| 表1 鼠李糖脂样品中各单体组分的含量情况 Table.1 Monomer compositions and relative abundances of rhamnolipids |
由图 1可知,当鼠李糖脂浓度低于CMC时,其对林丹的溶解没有明显的促进作用;而随鼠李糖脂浓度的提高,林丹的溶解度显著增大,总体上呈正线性关系.当鼠李糖脂浓度为1000 mg · L-1时,林丹的表观溶解度达到30.6 mg · L-1.表面活性剂对难溶有机物溶解的促进主要是通过其胶束增溶作用.当鼠李糖脂溶液浓度大于CMC时,溶液内形成大量胶束缔合体,林丹溶解于胶束提供的疏水微环境,从而显著提高其在水相中的表观溶解度(陈静等,2006).
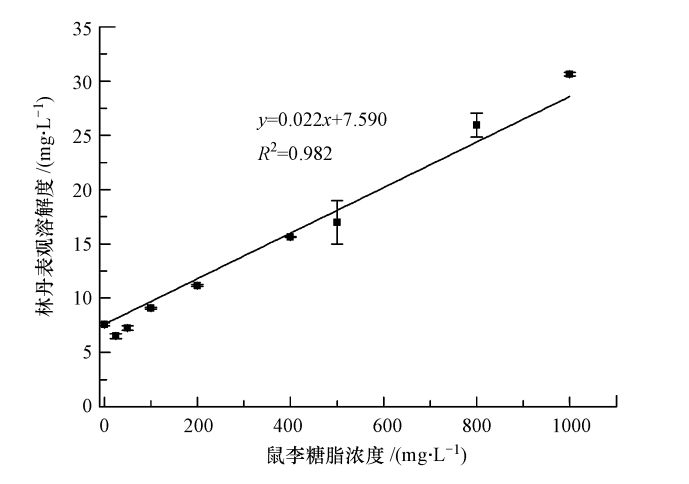 |
| 图 1 鼠李糖脂对林丹的增溶曲线 Fig. 1 Solubilization of lindane by rhamnolipids |
摩尔增溶比(MSR)通常用来定量描述表面活性剂对溶质的增溶能力,MSR可通过下式计算:
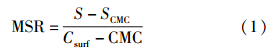
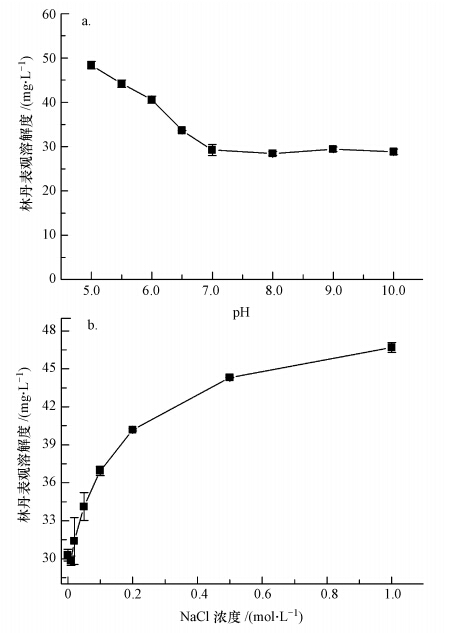 |
| 图 2 pH(a)及离子强度(b)对鼠李糖脂增溶林丹的影响(鼠李糖脂加入浓度为1000 mg · L-1) Fig. 2 Effect of pH(a) and NaCl(b)on solubilization of lindane by rhamnolipids(initial rhamnolipids concentration was1000 mg · L-1) |
由图 2a可知,pH对鼠李糖脂的增溶作用有较大影响.pH为5.0时增溶效果最好,对应林丹的表观溶解度为48.3 mg · L-1;随着pH的提高,林丹的表观溶解度直线降低;pH为7.0时,林丹的表观溶解度降低至29.3 mg · L-1;而pH从7.0提高到10.0时,鼠李糖脂的增溶效果基本保持稳定.这种变化主要与不同pH条件下鼠李糖脂胶束结构的变化有关.Champion等(1995)利用电子显微镜观察了 pH在5.5~8.0范围内鼠李糖脂的不同形态及转化情况,研究发现,pH为5.5~6.0时,鼠李糖脂在溶液中主要以菌褶形式存在,pH=6.0~6.8时囊泡为主要形态,pH=6.8~8.0时囊泡逐渐消失,胶束结构占绝对比例.结合本实验可知,鼠李糖脂的菌褶结构对林丹的增溶更为有效;另一方面,由于鼠李糖脂的酸碱平衡常数pKa约为6.8,当pH 由中性到碱性时,更多的鼠李糖脂分子带有负电荷,向外的亲水基团之间的静电排斥力增大使得胶束压缩变小,因而增溶能力变小(万金忠,2011).故实验当中随pH增大,鼠李糖脂对林丹的增溶能力下降,当pH大于7.0之后,鼠李糖脂对林丹的增溶能力降到最低.
如图 2b所示,林丹溶解度随盐度的增加而增加.Paria等(2008)的研究表明,增大溶液离子强度可明显降低离子型表面活性剂的CMC值,形成更多胶束,从而促进对有机物的增溶作用.另外,离子强度的提高可增强鼠李糖脂胶束内部的极性,使胶团的双电层压缩增强,减少了表面活性剂离子头之间的相互排斥作用,增大有机物在胶束内部的分配,从而增强鼠李糖脂对林丹的增溶(郭利果等,2009).
3.3 鼠李糖脂对重金属Pb、Cd的配合作用 3.3.1 鼠李糖脂对Pb、Cd的配合曲线鼠李糖脂对Pb、Cd的配合作用如图 3所示.由图可知,当鼠李糖脂浓度为0 mg · L-1时,溶液中Pb和Cd的浓度分别为3.43和0.981 mg · L-1,即91.4%和97.5%的Pb、Cd被SP葡聚糖凝胶C25树脂吸附.随着鼠李糖脂浓度的提高,由于鼠李糖脂的配合作用,溶解态(水相)Pb和Cd含量不断增加,总体上溶液中Pb的含量远高于Cd,表明鼠李糖脂对Pb的配合能力强于Cd.当鼠李糖脂浓度为10000 mg · L-1时,高达81.1%的Pb被鼠李糖脂结合,而鼠李糖脂的浓度为40000 mg · L-1时,其对Cd的配合量为76.8%.对于Pb,鼠李糖脂浓度在100~250 mg · L-1范围内时,两者配合大体成线性关系,配合摩尔比(Pb/RL)约为0.2.而对于Cd,鼠李糖脂浓度在100~2000 mg · L-1范围内时,两者配合摩尔比成线性关系,配合摩尔比(Cd/RL)约为0.05.OchoaLoza等(2001)研究了鼠李糖脂对Al3+、Pb2+、Cd2+等13种重金属离子的配合,发现配合常数存在Al3+>Cu2+>Pb2+>Cd2+>Zn2+>Fe3+>Hg2+>Ca2+、Co2+>Ni2+>Mn2+>Mg2+>K+的趋势,与本研究中两种重金属的配合趋势相同.
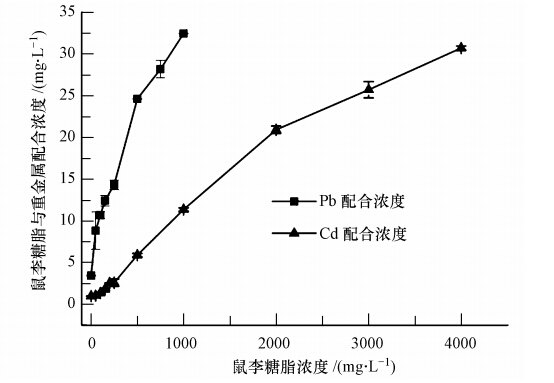 |
| 图 3 不同浓度鼠李糖脂对Pb、Cd的配合 Fig. 3 The complexation of Pb and Cd with rhamnolipids |
如图 4a所示,当pH在5.5~7.0范围内时,鼠李糖脂(200 mg · L-1)对Pb的配合效率变化不大,随pH继续上升,配合效率有所下降.而对于Cd,随pH值的升高,鼠李糖脂(4000 mg · L-1)对其配合效率却显著增加,尤其是pH在5.5~7.0范围内时,配合效率呈线性增加.
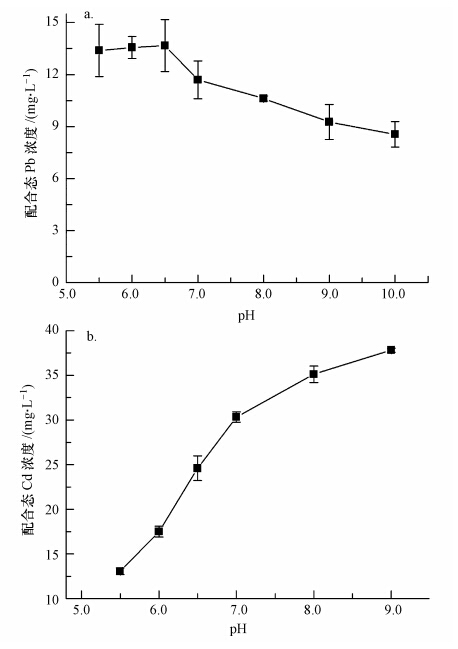 |
| 图 4 pH对鼠李糖脂配合Pb(a)和Cd(b)的影响 Fig. 4 Effect of pH on the complexation of Pb(a) and Cd(b)with rhamnolipids |
pH对鼠李糖脂配合重金属的影响包括两个方面的作用:一方面,随着pH的升高,鼠李糖脂分子的形态结构有较大变化,由片状变为囊泡状,最后变为胶束,结构趋于开放,亲水基团更容易与重金属结合;同时,pH升高,鼠李糖脂中羧基氢原子解离,羧基能与更多重金属离子形成配合体;另一方面,pH的变化会影响重金属在溶液中的形态,OH-过高时,容易形成重金属氢氧化物沉淀,会掩蔽有机金属络合物的形成(Spark et al., 1997).而Pb对OH-的溶度积为1.2×10-15,比Cd的溶度积2.2×10-14小,故随着pH的上升,Pb更易形成沉淀.
3.4 鼠李糖脂在土壤上的吸附行为 3.4.1 鼠李糖脂在土壤上的吸附等温曲线鼠李糖脂在供试土壤上的吸附等温曲线见图 5.由图可知,鼠李糖脂在土壤上的吸附量随平衡浓度的增加而持续增大,总体上吸附等温线可以用线性Temkin方程较好地拟合(林玉锁,1994).曲线的斜率即为Kd,不难得出鼠李糖脂吸附的Kd值为22.2 L · kg-1,与Holt等(1989)报道的阴离子表面活性剂C12LABS 在土壤上的 Kd值(20 L · kg-1)相当,但远高于戴树桂等(1999)报道的阴离子表面活性剂十二烷基硫酸钠的 Kd值(8.47)及十二烷基苯磺酸钠的 Kd值(13.6).鼠李糖脂在土壤上的吸附主要涉及3方面的作用:①鼠李糖脂结构中的疏水基使其具有疏水的性质,从而吸附在土壤矿物表面;②土壤有机质与疏水碳链的相互作用,对鼠李糖脂产生了分配吸附;③亲水基团跟土壤表面的氢键作用和静电吸引.本实验供试土壤有机质含量为44.29 g · kg-1,并且土壤粘粉粒含量占到35%,土壤有机质及粘粉粒含量均较高,因此,该土壤对鼠李糖脂吸附能力较强.
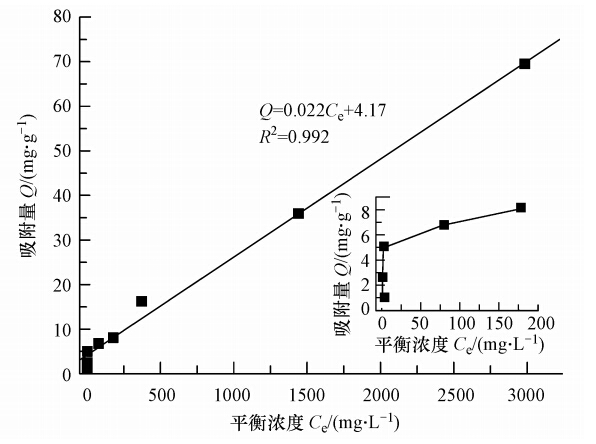 |
| 图 5 鼠李糖脂在土壤上的吸附等温线 Fig. 5 Sorption isothems of rhamnolipids on soil |
由图 6可知,当pH从5.5上升至9.0时,鼠李糖脂在土壤上的吸附量略有增加,而pH在7.0~9.0范围内鼠李糖脂在土壤上的吸附量增加趋势放缓.当pH为9.0时,土壤吸附的鼠李糖脂占41.1%,达到最大,而当pH达到10.0后,吸附量有所下降,鼠李糖脂吸附损失为29.4%.
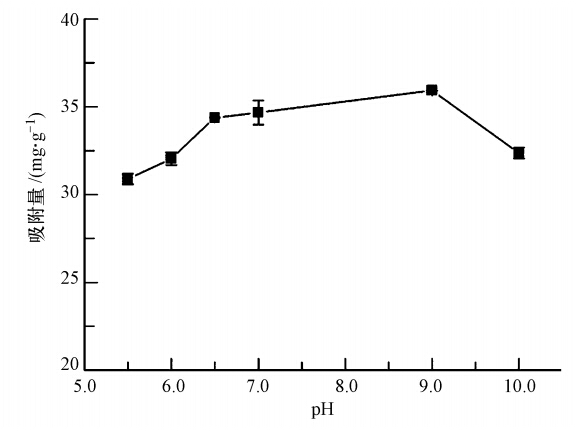 |
| 图 6 pH对鼠李糖脂在土壤上吸附的影响(鼠李糖脂初始浓度为5000 mg · L-1) Fig. 6 Effect of pH on the adsorption of rhamnolipids on soil(initial rhamnolipids concentration was 5000 mg · L-1) |
鼠李糖脂对林丹及重金属复合污染土壤的淋洗效果如图 7所示.由图可知,鼠李糖脂对土壤中林丹解吸的促进效果较为明显.由于鼠李糖脂对林丹有较好的增溶效果,故当鼠李糖脂浓度从0 g · L-1增加到10 g · L-1时,林丹的去除率从17.1%提高到73.8%;继续增加鼠李糖脂浓度,林丹的去除率无明显提高.对于重金属Pb和Cd,当鼠李糖脂浓度低于1000 mg · L-1时,重金属的去除效果不明显,均低于5%,与去离子水淋洗效果相差无几.随鼠李糖脂浓度增加,Cd的去除率迅速增加,当表面活性剂浓度达到30000 mg · L-1时,Cd的解吸率接近100%.而鼠李糖脂对Pb去除效果较差,当鼠李糖脂浓度为40000 mg · L-1时,其去除率仅为18.0%.总体来说,当鼠李糖脂浓度较低时,由于土壤的吸附作用,溶液中鼠李糖脂有效浓度较低,故当鼠李糖脂浓度高于5000 mg · L-1时,对3种污染物的解吸才开始有显著的促进效果,且Cd的解吸效果明显高于Pb.研究表明,Cd与土壤有机质的作用明显弱于Pb,移动性也远高于Pb(彭立君,2008).因此,尽管鼠李糖脂在水相中对Pb的配合能力强于Cd,其对Cd的淋洗效果仍然明显高于Pb.朱清清等(2010)研究发现,皂角苷对土壤中Cd和Pb的去除率分别为45.6%和17.6%,与本研究中的趋势一致.
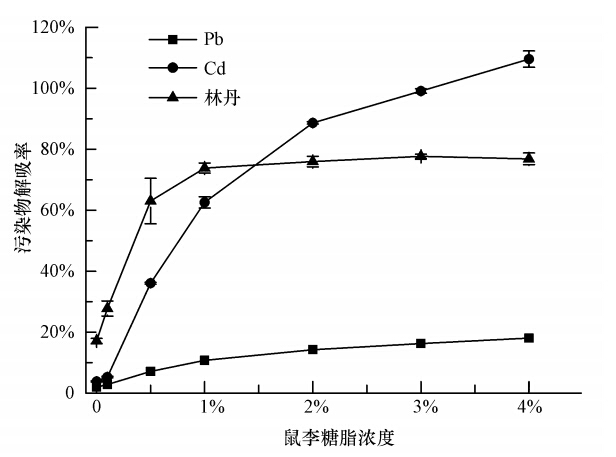 |
| 图 7 不同浓度鼠李糖脂对林丹及重金属复合污染土壤的解吸效果 Fig. 7 Washing effect of lindane and heavy metals from contaminated soil with different concentrations of rhamnolipids |
如图 8所示,pH对3种污染物去除率的影响趋势大体相同,当体系pH从5.0上升到7.0时,污染物去除率增加,而随pH继续升高,污染物的去除率下降,其中,Cd的下降速度最快.pH为7.0时,鼠李糖脂对污染物的去除达到了最佳效果.pH主要通过改变鼠李糖脂及污染物在土壤上的吸附行为,改变水相中鼠李糖脂形态结构及其与污染物的相互作用等方面来影响李糖脂解吸复合污染物的效果.其一,随着pH的增加,土壤有机质的溶解性显著提高,污染物分子在土壤上的吸附减弱,因此,有利于污染物的解吸(罗玲等,2004);而pH超过7.0时,重金属容易形成沉淀,溶解性显著降低,又会抑制污染物释放.其二,pH升高后鼠李糖脂的吸附呈现出先增加后降低的趋势,相应地,对污染物解吸表现为先降低后升高.其三,pH升高,鼠李糖脂对林丹的增溶能力下降,对Pb的配合能力下降,而对Cd的配合能力持续上升.通过以上3方面因素的综合分析,不难得出,pH对鼠李糖脂淋洗复合污染土壤的影响结果与第一个因素(即pH对土壤中污染物吸附行为的影响)有一定的一致性.当pH值超过7.0之后,鼠李糖脂在土壤上的吸附量继续增加,有效浓度降低,而重金属移动性变差,故污染物解吸率降低.总体而言,pH对鼠李糖脂淋洗复合污染土壤的影响较为复杂,实验得到的最优淋洗pH为7.0左右.
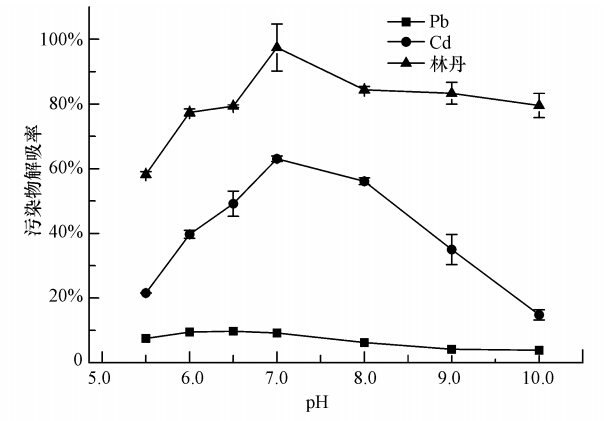 |
| 图 8 pH对鼠李糖脂同步解吸土壤中林丹及重金属复合污染土壤的影响(鼠李糖脂加入浓度为10000 mg · L-1) Fig. 8 Effect of pH on the washing of lindane and heavy metals combined contaminated soil with rhamnolipids(rhamnolipids concentration was 10000 mg · L-1) |
10000 mg · L-1鼠李糖脂淋洗前后土壤中各重金属形态分级结果如图 9所示.由图可知,重金属Pb在土壤中主要以碳酸盐结合态、铁锰氧化物结合态及弱有机态的形式存在,且3种形态分布相当.鼠李糖脂解吸后可交换态Pb的含量降低最为明显,去除率达到59.6%,而碳酸盐结合态、铁锰氧化物结合态及有机结合态的去除率仅分别为16.1%、15.1%和4.55%,残渣态反而有所升高.重金属Cd在土壤中主要以可交换态存在,淋洗后其去除率达到了50.19%,而其余几种形态的含量经淋洗后均有不同程度的增加.鼠李糖脂对于各形态重金属的解吸效果差异较大.结合3.5.1节结果可知,鼠李糖脂对土壤中可交换态重金属解吸效果较好,而供试土中Cd主要以该形态存在,故淋洗效率较高,而可交换态Pb只占到Pb总量的11.7%,故淋洗效率较低.
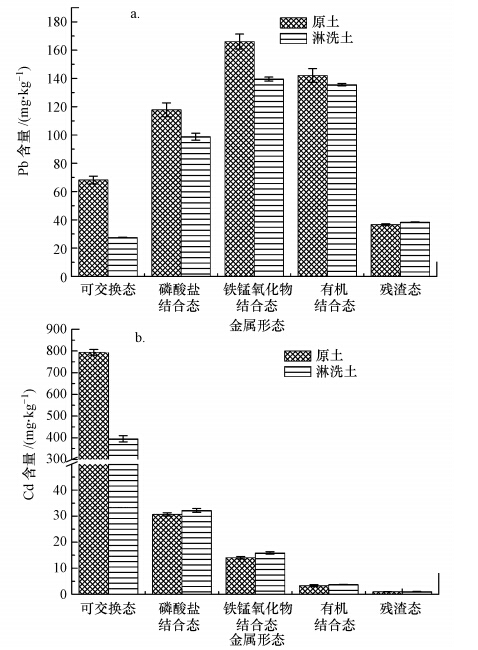 |
| 图 9 淋洗前后土壤中Pb(a)和Cd(b)各形态含量变化(鼠李糖脂加入浓度为10000 mg · L-1) Fig. 9 Speciation of Pb(a) and Cd(b)in the soils before and after washing treatment(rhamnolipids concentration was10000 mg · L-1) |
1)鼠李糖脂对林丹有很好的增溶作用,pH的提高对增溶有抑制作用,而盐度的增加促进了林丹的溶解.鼠李糖脂与Pb的配合强于Cd,pH由5.5提高到7.0,鼠李糖脂与Pb的配合变化不大,而pH继续提高,配合强度随之下降;而鼠李糖脂与Cd的配合随pH的增加而逐渐增加.
2)鼠李糖脂在土壤上的吸附等温曲线符合线性方程.pH对鼠李糖脂在土壤上的吸附影响不太明显,在pH为9.0时吸附达到最大,随后吸附量明显下降.
3)鼠李糖脂对林丹及Pb、Cd复合污染土壤的淋洗效果较好.总体来说,当鼠李糖脂浓度大于0.5%时,对3种污染物的去除开始有显著的效果,去除效力Cd>Pb,并且在pH为7.0时淋洗效果最好.同时,鼠李糖脂对不同形态的重金属去除能力有所差异,其中,对可交换态重金属的去除最为有效.
| [1] | Asci Y, Nurbas M, Acikel Y S.2008.A comparative study for the sorption of Cd(Ⅱ) by soils with different clay contents and mineralogy and the recovery of Cd(Ⅱ) using rhamnolipid biosurfactant[J].Journal of Hazardous Materials, 154(1/3):663-673 |
| [2] | Banat I M, Makkar R S, Cameotra S S.2000.Potential commercial applications of microbial surfactants[J].Applied Microbiology and Biotechnology, 53(5): 495-508 |
| [3] | Berselli S G, Milone P, Canepa D, et al.2004.Effects of cyclodextrins, humic substances, and rhamnolipids on the washing of a historically contaminated soil and on the aerobic bioremediation of the resulting effluents[J].Biotechnology and Bioengineering, 88(1):111-120 |
| [4] | Bordas F, Lafrance P, Villemur R.2005.Conditions for effective removal of pyrene from an artificially contaminated soil using Pseudomonas aeruginosa 57SJ rhamnolipids[J].Environmental Pollution, 138: 69-76 |
| [5] | 陈静, 胡俊栋, 王学军, 等.2006.表面活性剂对土壤中多环芳烃解吸行为的影响[J].环境科学, 25(2): 361-365 |
| [6] | 丛鑫, 薛南冬, 梁刚, 等.2008.某有机氯农药企业搬迁遗留场地表层土壤中污染物残留特征研究[J].农业环境科学学报, 27(3): 850-854 |
| [7] | Champion J T, Gilkey J C, Lamparski H, et al.1995.Electron-microscopy of rhamnolipid (biosurfactant) morphology-effects of pH, cadmium, and octadecane[J].Journal of Colloid and Interface Science, 170(2):569-574 |
| [8] | 戴树桂, 董亮, 王臻.1999.表面活性剂在土壤颗粒物上的吸附行为[J].中国环境科学, 19(5): 392-396 |
| [9] | Fernandez-Perez V, L de Castro M D.2000.Micelle formation for improvement of continuous subcritical water extraction of polycyclic aromatic hydrocarbons in soil prior to high-performance liquid chromatography-fluorescence detection[J].Journal of Chromatography, A 902(2):357-367 |
| [10] | 郭利果, 苏荣国, 梁生康, 等.2009.鼠李糖脂生物表面活性剂对多环芳烃的增溶作用[J].环境化学, 28(4): 510-514 |
| [11] | Holt M S, Mathus E, Waters J.1989.The concentrations and fate of linear alkylbenzene sulphonate in sludge amended soils[J].Water Reserch, 23(6): 749-759 |
| [12] | 李克斌, 刘惠君, 马云, 等.2004.不同类型表面活性剂在土壤上的吸附特征比较研究[J].应用生态学报, 15(11):2067-2071 |
| [13] | 李玉双, 胡晓钧, 孙铁珩, 等.2011.污染土壤淋洗修复技术研究进展[J].生态学杂志, 30(3): 596-602 |
| [14] | 林玉锁.1994.Langmuir, Temkin和Freundlich方程应用于土壤吸附锌的比较[J].土壤, (5): 269-272 |
| [15] | 罗玲, 欧晓明, 廖晓兰.2004.农药在土壤中的吸附机理及其影响因子研究概况[J].化工技术与开发, 33 (1): 12-16 |
| [16] | Lafrance P, Lapointe M.1998.Mobilization and co-transport of pyrene in the presence of Pseudomonas aeruginosa UG2 bio-surfactants in sandy soil columns[J].Ground Water Monit Remediat, 18:139-147 |
| [17] | Mata-Sandoval J C, Karns J, Torrents A.2001.Influence of rhamnolipids and Triton X-100 on the biodegradation of three pesticides in aqueous phase and soil slurries[J].Journal of Agricultural and Food Chemistry, 49(7):3296-3303 |
| [18] | Mulligan C N.2005.Environmental applications for biosurfactants[J].Environmental Pollution, 33(2): 183-198 |
| [19] | Mulligan C N, Yong R N, Gibbs B F.2001a.Heavy metal removal from sediments by biosurfactants[J].Journal of Hazardous Materials, 85(1/2):111-125 |
| [20] | Mulligan C N, Yong R N, Gibbs B F.2001b.Surfactant-enhanced remediation of contaminated soil: a review[J].Engineering Geology, 60(1/4):371-380 |
| [21] | Noordman W H, Ji W, Brusseau M L, et al.1998.Effects of rhamnolipid biosurfactants on removal of phenanthrene from soil[J].Environ Sci Technol, 32:1806-1812 |
| [22] | Ochoa-Loza F J, Artiola J F, Maier R M.2001.Stability constants for the complexation of various metals with a rhamnolipid biosurfactant[J].Journal of Environmental Quality, 30(2):479-485 |
| [23] | 彭立君.2008.鼠李糖脂修复重金属和多环芳烃(PAHs)复合污染土壤研究[D].长沙:湖南大学.28-47 |
| [24] | Paria S.2008.Surfactant-enhanced remediation of organic contaminated soil and water[J].Advances in Colloid and Interface Science, 138(1): 24-58 |
| [25] | Spark K M, WellsJ D, Johnson B B.1997.The interaction of a humic acid with heavy metals[J].Australian Journal of Soil Research, 35(1):89-101 |
| [26] | Urum K, Pekdemir T.2004.Evaluation of biosurfactants for crude oil contaminated soil washing[J].Chemosphere, 57(9):1139-1150 |
| [27] | 万金忠.2011.有机氯杀虫剂污染土壤的化学淋洗修复研究.武汉:华中科技大学.17-23 |
| [28] | Wang S L, Mulligan C N.2009.Arsenic mobilization from mine tailings in the presence of a biosurfactant[J].Applied Geochemistry, 24(5):928-935 |
| [29] | 朱清清, 邵超英, 张琢, 等.2010.生物表面活性剂皂角苷增效去除土壤中重金属的研究[J].环境科学学报, 30(12): 2491-2498 |
| [30] | 庄绪亮.2007.土壤复合污染的联合修复技术研究进展[J].生态学报, 27(11):4871-4876 |
 2014, Vol. 34
2014, Vol. 34


