2. 中国科学院上海应用物理研究所 嘉定园区 上海 201800
2. Shanghai Institute of Applied Physics, Chinese Academy of Sciences, Jiading Campus, Shanghai 201800, China
熔盐堆是一种具有安全、核燃料可循环、经济性好等特点的先进高温堆。熔盐由于其在高温下化学性质稳定、传热性能优异,常被选作熔盐堆冷却剂的候选熔盐[1]。同时熔盐堆的稳定性也决定于熔盐的高温热稳定性。熔盐除了在熔盐堆中发挥着重要作用,熔盐自身又可以作为传蓄热介质应用于在聚光太阳能发电(Concentrating Solar Power, CSP)系统[2]中。本文主要以NaNO3-KNO3 (60%(wt)~ 40%(wt))为基盐,Na2CO3作为添加剂,研究了Na2CO3对NaNO3-KNO3 (60%(wt)~40%(wt))熔盐高温热稳定性的影响,该研究可以为添加剂对熔盐的改性在核能领域中的应用提供一定的参考。
太阳盐(Solar salt) (NaNO3-KNO3, 60%(wt)~ 40%(wt))熔盐由于其使用温度范围广、工作压力低、经济性好、热物性优异,目前常作为高温传热蓄热介质被广泛应用于太阳能发电等新能源领域[3-8]。但Solar salt熔盐在高温下不稳定,易分解导致熔盐劣化,进而引发一系列问题[9]。因此对其高温热稳定性的研究至关重要[10]。杜宝强等[11]研究了氯离子对Solar salt熔盐热物性的影响,结果表明:Cl-的加入会使Solar salt熔盐的热稳定性变差,NO2-含量升高;Zhang等[12]研究了纯度对Solar salt熔盐的热物性的影响,结果表明:纯化过的熔盐与未纯化的相比具有更高的热稳定性;倪海鸥等[13]研究了SO42-对质量比为1:1的NaNO3-KNO3熔盐结构的影响,结果表明:在熔盐冷凝结晶时SO42-会优先与Na+结合,并且在常温下以固溶体的形式存在,在200 ℃时混合盐的结构会发生显著改变;Bonk等[14]研究了不同条件下Solar salt熔盐的热稳定性,结果表明:在空气气氛下560 ℃的Solar salt中硝酸盐含量相对稳定,而在氮气气氛下亚硝酸盐含量明显增加。
本文制备了Solar salt及含Na2CO3的Solar salt熔盐,并在600 ℃下热处理240 h。利用热分析、成分分析等方法研究了添加Na2CO3对Solar salt熔盐热稳定性的影响。
1 实验部分 1.1 主要原料及试剂本实验中采用的原料为NaNO3、KNO3和Na2CO3,均从国药集团化学试剂有限公司采购,纯度为AR级。
1.2 实验方法先将NaNO3、KNO3放入干燥箱中150 ℃下干燥24 h除水,然后将NaNO3、KNO3分别按质量配比6:4称量后共混,将共混后放入石墨坩埚中搅拌均匀,迅速将样品置于井式高温炉中,在空气气氛,300 ℃下恒温10 h,使样品熔化、充分混匀,形成NaNO3-KNO3 (Solar salt)熔盐。
在Solar salt熔盐添加1%(wt)的Na2CO3 (Solar salt+Na2CO3),充分混合后放入石墨坩埚中搅拌,再将混合熔盐转移至红外加热炉中,300 ℃下恒温2 h,常压下加热、结晶,冷却至室温。
1.3 测试与表征 1.3.1 稳定温度范围热稳定性的测量采用法国塞塔拉姆仪器公司的同步热分析仪。选用经过高温恒重处理过的石墨坩埚。本次实验采用10 ℃·min-1的升温速率,测试过程中采用气流量为20 mL·min-1的Ar气。
1.3.2 阴离子浓度利用美国戴安离子色谱仪ICS-2100检测了阴离子浓度。采用1.0 mL·min-1的KOH溶液为固定相。
1.3.3 pH测试采用梅特勒SevenEasy pH计测量了熔盐的pH值。该pH计测量范围是0~14,相对精度为±0.01。
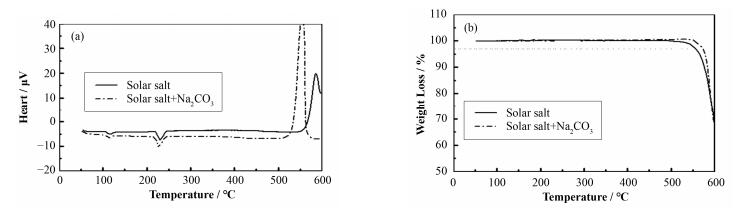
2 结果与讨论 2.1 对熔盐熔点、分解温度的影响熔盐的稳定温度范围(ΔT)直接关系着熔盐的使用温度范围,也直接与热转换效率相关,因而,稳定温度范围对于熔盐作为传蓄热介质至关重要。本文利用同步热分析仪分别考察了熔盐的熔点和分解温度。未处理的Solar salt熔盐和Solar salt+Na2CO3熔盐的差示扫描量热分析(Differential Scanning Calorimetry, DSC)与热重分析(Thermogravimetric Analysis, TG)曲线如图 1(a)、(b)所示。从图 1(a)可以看出,Solar salt熔盐和Solar salt+Na2CO3分别在105 ℃和107 ℃出现一个小峰,这是由于NaNO3- KNO3的固态相变引起的。随着温度的升高,熔盐开始熔化,其熔点分别是224 ℃和222 ℃,表明添加了Na2CO3使Solar salt熔盐的熔点降低了2 ℃。随着温度的升高过于500 ℃,DSC曲线上出现了明显的吸热峰,这是由于熔盐分解吸热而导致的。图 1(b)是Solar salt和Solar salt+Na2CO3熔盐的TG曲线。采用TG测试热分解温度与升温速率有关,当升温速率为10 ℃∙min-1时,质量损失达到3%时的温度定义为分解温度[15],本文选用此标准来衡量熔盐的分解温度。从图 1(b)中可以看出,Solar salt熔盐的分解温度为555 ℃,Solar salt+Na2CO3熔盐的分解温度为573 ℃。两种熔盐的熔点与分解温度及稳定温度范围见表 1。从表 1可以看出,Solar salt熔盐的稳定温度范围是224~555 ℃,Solar salt+Na2CO3熔盐的稳定温度范围是222~573 ℃,添加Na2CO3使Solar salt熔盐的热稳定性提升了18 ℃,使稳定温度范围扩大了20 ℃,说明添加Na2CO3可提高Solar salt熔盐的分解温度,扩大稳定温度范围。
|
图 1 Solar salt和Solar salt+Na2CO3熔盐的DSC (a)和TG (b)曲线 Figure 1 DSC (a) and TG (b) curves of Solar salt and Solar salt+Na2CO3 |
| 表 1 未处理与处理后熔盐的熔点、分解温度以及热稳定温度区间 Table 1 Melting point, decomposition temperature and thermal stability temperature range of untreated and treated molten salt |
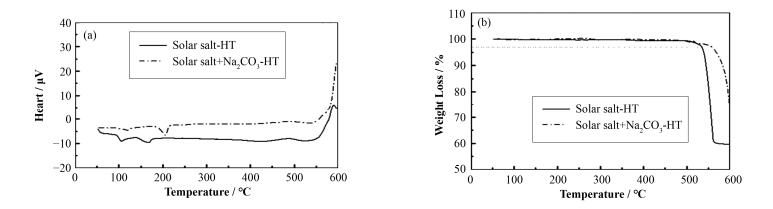
图 2(a)和(b)是在600 ℃保温240 h后的Solar salt(标记为Solar salt-HT)和Solar salt+Na2CO3(标记为Solar salt+Na2CO3-HT)熔盐的DSC和TG曲线。从图 2(a)中可以看出,两种盐在81 ℃均出现一个小峰,这是由于NaNO3-KNO3的固态相变引起的。Solar salt-HT熔盐和Solar salt+Na2CO3-HT分别在96 ℃和108 ℃出现一个小的放热峰,同理,这是由于NaNO3-KNO3的固态相变引起的。随着温度的升高,Solar salt-HT熔盐和Solar salt+Na2CO3-HT熔盐的熔点分别为148 ℃和190 ℃,说明在600 ℃保温240 h后,Solar salt熔盐的熔点降低了81 ℃;Solar salt+Na2CO3熔盐的熔点降低了37 ℃。Solar salt和Solar salt+Na2CO3熔盐在600 ℃下分解,而使熔盐的组成发生变化,在600 ℃保温240 h后,NO3-会分解生成NO2-,熔盐由原来的硝酸盐变为硝酸盐-亚硝酸盐的混合物,进而使得熔盐的熔点降低。同样,DSC曲线在高温端的吸热峰是由于熔盐分解而引起的。图 2(b)是在600 ℃下保温240 h后的Solar salt熔盐和Solar salt+Na2CO3熔盐的TG曲线,从图 2(b)中可以看出,两种熔盐的分解温度分别为534 ℃和558 ℃。在600 ℃保温后,两种的分解温度分别下降了21 ℃和15 ℃,Solar salt-HT的稳定温度范围是148~534 ℃,添加Na2CO3的稳定温度范围为190~558 ℃,见表 1。虽然在600 ℃保温24 h后,添加Solar salt+Na2CO3的稳定温度范围小于Solar salt熔盐,但添加Na2CO3更有助力于稳定熔点。
|
图 2 Solar salt-HT和Solar salt+Na2CO3-HT熔盐的DSC (a)和TG (b)曲线 Figure 2 DSC (a) and TG (b) curves of Solar salt-HT and Solar salt+Na2CO3-HT molten salts after heat treatment at 600 ℃ |
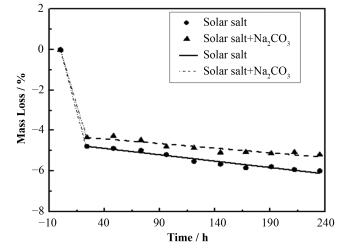
分别将Solar salt熔盐和Solar salt+Na2CO3熔盐在600 ℃保温中,每隔一定时间取出称量,记录质量随时间的变化曲线,见图 3。可以看出在600 ℃下保温240 h后,Solar salt和Solar salt+Na2CO3熔盐的质量损失率分别为6%和5.21%,说明添加Na2CO3使Solar salt熔盐的质量损失率减小了0.79%。在前24 h内,质量急剧下降,这可能是由于熔盐本身存在一定的自由水,加热后自由水挥发导致的。随后,质量变化随着时间的延长而趋缓,基本与实践成线性关系,表现出稳定的质量损失速率。将两种盐的质量损失(w)随时间(t)的变化关系进行线性拟合,见式(1)和(2),拟合得到的斜率分别为-0.00625和-0.00453,说明Solar salt+Na2CO3熔盐的质量损失速率小于Solar salt熔盐。从长期来看,Na2CO3的加入能够抑制Solar salt熔盐的高温分解。图 1(b)、图 2(b)和图 3都说明,无论从短期还是长期来看,添加Na2CO3都会有效地抑制熔盐的质量损失,提高Solar salt熔盐的热稳定性。
|
图 3 Solar salt和Solar salt+Na2CO3熔盐在600 ℃保温过程中质量损失率随时间变化曲线 Figure 3 Mass loss rate curve of Solar salt with Na2CO3 and pure Solar salt after heat treatment at 600 ℃ |
| $ {w_{{\rm{Solar}}\;{\rm{salt}}}} =-4.65-0.006\;25t $ | (1) |
| $ {w_{{\rm{Solar}}\;\;{\rm{salt}} + {\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}}} =-4.25-0.004\;53t $ | (2) |
Solar salt熔盐高温分解反应主要有两种:硝酸盐分解为亚硝酸根与氧气;硝酸根分解为氧化物与氮氧化合物[16-17]。基于这一分解机理,对Solar salt熔盐中的亚硝酸根含量与比例、pH进行了分析。
表 2给出了Solar salt和Solar salt+Na2CO3熔盐以及Solar salt-HT和Solar salt+Na2CO3-HT熔盐的阴离子浓度分析结果。从表 2中看出,Solar salt和Solar salt+Na2CO3熔盐中的阴离子主要是NO3-,NO2-的浓度占比很小,主要来源于原料中的NO2-。Solar salt-HT和Solar salt+Na2CO3-HT熔盐中的主要阴离子有NO3-和NO2-,说明熔盐的主要分解产物包括亚硝酸盐,即经过热处理的熔盐是硝酸盐-亚硝酸的混合物,这也是导致热处理后熔盐熔点降低的主要原因。Solar salt-HT熔盐中的NO2-为26.95%,而Solar salt+Na2CO3-HT盐中NO2-为15.08%,进一步说明添加Na2CO3有利于提升Solar salt熔盐的高温热稳定性,这与TG和质量随时间变化的试验结果是一致的。
| 表 2 4组样品的阴离子浓度检测结果 Table 2 The results of the determination of the concentration of anions in four groups of samples (%) |
Solar salt和Solar salt+Na2CO3熔盐以及Solar salt-HT和Solar salt+Na2CO3-HT熔盐的pH检测结果见表 3。Solar salt水溶液在室温下呈近似中性,而添加了1%的Na2CO3的Solar salt水溶液呈碱性,这是由于Na2CO3本身是强碱弱酸盐,溶于水后呈弱碱性。相较于未600 ℃高温处理的Solar salt和Solar salt+Na2CO3熔盐,在600 ℃下保温240 h后,Solar salt熔盐的pH值升高,而Solar salt+Na2CO3熔盐的pH降低,但两者均略显弱碱性,这是由于硝酸盐分解后产生了部分氧化物,水解后略呈碱性。
| 表 3 4组样品的pH测试结果 Table 3 pH test results of four groups of samples |
上述实验结果表明:添加了Na2CO3之后,二元硝酸盐变成了三元硝酸盐,熔点相对于纯Solar salt熔点变低,同时混合盐的分解温度也提高了,这主要是因为碳酸根离子的加入,削弱了金属阳离子对硝酸根离子中大Π键的极化作用。金属离子对碳酸根中氧离子也有反极化作用,但是加热时硝酸盐更容易分解,碳酸根离子的加入弱化了阳离子对硝酸根离子的极化作用,使混合熔盐整体上更趋于稳定。
3 结语本文研究了Na2CO3对Solar salt熔盐的高温热稳定性影响。结果表明:添加1%的Na2CO3可使Solar salt熔盐的稳定温度范围扩大20 ℃,在600 ℃下保温240 h后,使Solar salt熔盐的质量损失率减小了0.79%,热稳定性提高3.2%。Solar salt和Solar salt+Na2CO3熔盐在600 ℃下保温240 h后,其主要产物包括硝酸盐、亚硝酸盐和少量氧化物,进一步证明了Na2CO3的加入有助于抑制Solar salt熔盐的分解,提高其热稳定性。实际上随着Na2CO3含量的提高,Na2CO3在Solar salt熔盐中的比重变大,对Solar salt熔盐的热稳定性的提升效率也会增大。当Na2CO3的含量增大到某一特定值时,对Solar salt熔盐的热稳定性的提升效果达到最优,至于最优配比以及影响机制我们会在后续实验中进行讨论。该研究也为添加剂在熔盐堆中对部分熔盐的改性提供了一定的参考。
| [1] |
江绵恒, 徐洪杰, 戴志敏. 未来先进核裂变能——TMSR核能系统[J]. 中国科学院院刊, 2012, 7(3): 366-374. JIANG Mianheng, XU Hongjie, DAI Zhimin. Advanced fission energy program-TMSR nuclear energy system[J]. Bullet in Chinese Academy of Sciences, 2012, 7(3): 366-374. DOI:10.3969/j.issn.1000-3045.2012.03.016 |
| [2] |
袁炜东. 国内外太阳能光热发电发展现状及前景[J]. 电力与能源, 2015, 36(4): 487-490. YUAN Weidong. Development status and prospect of solar thermal power generation at home and abroad[J]. Power and Energy, 2015, 36(4): 487-490. DOI:10.11973/dlyny201504006 |
| [3] |
Mills D. Advances in solar thermal electricity technology[J]. Solar Energy, 2004, 76(1): 19-31. DOI:10.1016/S0038-092X(03)00102-6 |
| [4] |
Kearney D, Kelly B, Herrmann U, et al. Engineering aspects of a molten salt heat transfer fluid in a trough solar field[J]. Energy, 2004, 29(5): 861-870. DOI:10.1016/S0360-5442(03)00191-9 |
| [5] |
Ignatiev V V, Feynberg O S. Molten-salt reactors:new possibilities, problems, and solutions[J]. Atomic Energy, 2012, 112(3): 157-165. DOI:10.1007/s10512-012-9537-2 |
| [6] |
Wilkinson W L. Environmental impact of electricity generation[J]. Transactions of the Royal Society of South Africa, 2001, 56(2): 131-133. DOI:10.1080/00359190109520511 |
| [7] |
Liu M, Bell S. Review on concentrating solar power plants and new developments in high temperature thermal energy storage technologies[J]. Renewable & Sustainable Energy Reviews, 2016, 53(09): 1411-1432. DOI:10.1016/j.rser.2015.09.026 |
| [8] |
金愿, 张鹏. 几种典型熔盐冷却剂的热物性研究[J]. 核技术, 2016, 39(5): 050604. JIN Yuan, ZHANG Peng. Research on thermo-physical properties of several typical molten salt coolants[J]. Nuclear Techniques, 2016, 39(5): 050604. DOI:10.11889/j.0253-3219.2016.hjs.39.050604 |
| [9] |
Bradshaw R W, Meeker D E. High-temperature stability of ternary nitrate molten salts for solar thermal energy systems[J]. Solar Energy Materials, 1990(21): 51-60. DOI:10.1016/0165-1633(90)90042-Y |
| [10] |
程进辉. 传蓄热熔盐的热物性研究[D]. 上海: 中国科学院上海应用物理研究所, 2014. CHENG Jinhui. Study on molten salt thermos-physical properties for heat transfer and storage[D]. Shanghai: Shanghai Institute of Applied Physics, Chinese Academy of Sciences, 2014. http://cdmd.cnki.com.cn/Article/CDMD-80014-1014042720.htm |
| [11] |
杜宝强, 王怀有, 李锦丽, 等. 氯离子对Solar salt熔盐热物性的影响及结构分析[J]. 应用化工, 2017, 46(6): 1086-1088. DU Baoqiang, WANG Huaiyou, LI Jinli, et al. Effect of chloride ion on the thermal properties of Solar salt molten salt and its structure analysis[J]. Applied Chemical Industry, 2017, 46(6): 1086-1088. DOI:10.16581/j.cnki.issn1671-3206.20170505.036.issn1671-3206.20170505.036 |
| [12] |
Zhang H, Zhao Y, Li J, et al. Preparation and thermal properties of high-purified molten nitrate salt materials with heat transfer and storage[J]. High Temperature Materials & Processes, 2015, 34(8): 1-8. DOI:10.1515/htmp-2014-0147 |
| [13] |
倪海鸥, 孙泽, 黄龙, 等. 杂质SO42-对混合硝酸盐结构的影响分析[J]. 储能科学与技术, 2016, 5(2): 210-214. NI Haiou, SUN Ze, HUANG Long, et al. Analysis of the influence of impurity SO42- on the structure of mixed nitrate[J]. Energy Storage Science and Technology, 2016, 5(2): 210-214. DOI:10.3969/j.issn.2095-4239.2016.02.013 |
| [14] |
Bonk A, Martin C, Braun M, et al. Material investigations on the thermal stability of solar salt and potential filler materials for molten salt storage[C]. AIP Conference Proceedings, 2017, 1850: 080008. DOI: 10.1063/1.4984429.
|
| [15] |
Gimenez P, Fereres S. Effect of heating rates and composition on the thermal decomposition of nitrate based molten salts[J]. Energy Procedia, 2015, 69: 654-662. DOI:10.1016/j.egypro.2015.03.075 |
| [16] |
Yuvaraj S, Lin F Y, Chang T H, et al. Thermal decomposition of metal nitrates in air and hydrogen environments[J]. Journal of Physical Chemistry B, 2003, 107(4): 1044-1047. DOI:10.1021/jp026961c |
| [17] |
Nissen D A, Meeker D E. Nitrate/nitrite chemistry in sodium nitrate-potassium nitrate melts[J]. Inorganic Chemistry, 1983, 22(5): 716-721. DOI:10.1021/ic00147a004 |


