2. 中国核动力研究设计院 成都 610005
2. Nuclear Power Institute of China, Chengdu 610005, China
151Sm是一种长寿命(半衰期为90 a)裂变产物,对151Sm含量的精确测量可以为环境科学、生命科学、核数据等领域提供非常重要的信息。Sm属于稀土元素,近年来随着稀土资源的开发和在工农业、畜牧业及医药学等领域的应用,稀土元素不断地进入环境和生物体内,因此精确测定样品中151Sm的含量对于环境、生态和人体健康的研究都有重要意义[1]。
目前稀土能否通过血-脑屏障进入脑组织一直是存在争议的问题[2-7],采用151Sm作为示踪核素对大鼠进行示踪试验,可以为解决稀土能否进脑提供帮助。采用151Sm作为示踪核进行动物试验具有以下几点优势:1) 151Sm的半衰期较长,可以进行长期的动物示踪试验;2) 151Sm的衰变方式为β-衰变,伴随γ射线(γ射线能量为21keV,分支比为0.031%),不用担心生物辐射损伤和安全问题;3) 150Sm(n,γ)151Sm的生成截面达104靶,使得151Sm的制备较容易。
但是,环境样品或生物示踪样品中的151Sm的含量极低(生物样品中稀土元素的固有含量一般在10-6-10-9量级[8]),放射性弱,这就使得用衰变计数法和普通质谱法等常规方法难以对其进行测量。加速器质谱[9-10]是20世纪70年代末国际上发展起来的一门超高灵敏核分析技术,是实现151Sm高灵敏测量的有效方法。151Sm 的加速器质谱(Accelerator Mass Spectra,AMS)测量在国际上尚属首次,具有一定的创新性。但是AMS是相对测量,需要标准样品。本文介绍了中国原子能科学研究院用于AMS测量的151Sm实验室参考标准的研制。
1 放射性核素151Sm的合成及样品的溶解由于自然界不存在放射性核素151Sm,需要通过人工方法来生产。151Sm是将富集Sm2O3(150Sm的丰度为87.34%)在中国原子能科学研究院(China Institute of Atomic Energy,CIAE)的重水反应堆 中辐照产生的,主要反应为150Sm(n,γ)151Sm,反应 截面约为104靶,平均热中子注量率为 5.11×1013个·s-1·cm-2,照射时间约432h。
以热的优级纯浓硝酸溶解辐照后的Sm2O3样品,溶解后才能用于热电离同位素质谱仪(Thermal Ionization Mass Spectrometry,TIMS)测量和系列参考标准样品的配制。
2 同位素比值的精确测定为了满足AMS测量不同含量样品的需要,我们取适量辐照后的151Sm样品,然后加入稳定同位素(154Sm)稀释,得到不同同位素比151Sm/154Sm的系列参考标准。因此,必须准确测量稀释前样品中的同位素比值(151Sm/150Sm)。
采用中国核动力研究设计院(Nuclear Power Institute of China,NPIC)的Finnigan MAT 262 TIMS,对辐照后样品的同位素比(151Sm/150Sm)进行了精确测定。首先对天然的氧化钐的同位素丰度和富集氧化钐样品(富集150Sm)的同位素比进行了TIMS测量,测量结果见表 1、2。由表 1、2可以看出,TIMS测量值在误差范围内与给定值符合得很好。由于Sm的电离电位为5.6 eV,涂样时不用添加发射剂,高压为10 kV,接收器为法拉第杯。辐照后样品中同位素比的测量结果为:151Sm/150Sm=(3.750±0.002)×10-3(见表 3)。
| 表 1 天然Sm2O3同位素丰度的测定值 Table 1 Measured results of isotope abundance for natural abundance Sm2O3. |
| 表 2 未辐照的富集Sm2O3同位素比的测定值 Table 2 Measured results of isotope ratios for unirradiated enriched Sm2O3. |
| 表 3 辐照后样品中151Sm/150Sm、152Sm/150Sm 与151Sm/152Sm同位素比的测量结果 Table 3 Measured results of isotope ratios of 151Sm/150Sm,152Sm/150Sm and 151Sm/152Sm for irradiated samples. |
经反应堆辐照生产得到的151Sm样品其151Sm/150Sm比值为(3.750±0.002)×10-3。由于Sm的稳定同位素较多,为降低AMS测量时151Sm附近同位素的干扰,选用154Sm丰度为98.61%的富集稳定同位素样品Sm2O3作为稀释剂。用稀释剂(富集同位素154Sm的Sm2O3)进行逐级稀释,制得三种低同位素比(151Sm/154Sm)的参考标准。最终得到同位素比分别为(9.25±0.08)×10-7、(8.87±0.08)×10-8、(8.08±0.08)×10-9系列参考标准,以满足151Sm/154Sm比值在10-7-10-9范围内样品的AMS测量。
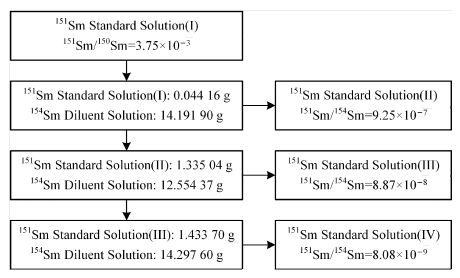
如图 1所示,具体稀释流程:
|
图 1 151Sm系列标准样品稀释流程图 Figure 1 Flow chart for preparing 151Sm standards by multistage dilution. |
1) 称取辐照后Sm2O3的硝酸溶液0.93378 g(标样I,其中151Sm/150Sm=3.750×10-3),并用高纯水稀释10倍(溶液1)。
2) 称取0.172 96 g 154Sm2O3粉末,加5 mL 1:1硝酸溶解后,转移至塑料瓶中,并用高纯水稀释至60 mL(溶液2),称重60.446 6 g。
3) 称取溶液1重0.04416 g,溶液2重14.19190g,混匀,即得151Sm/154Sm约10-7的标准(标样Ⅱ)。
4) 称取标样Ⅱ溶液1.33504 g,溶液2重12.55437g,混匀,即得151Sm/154Sm约10-8的标样(标样Ⅲ)。
5) 称取标样Ⅲ溶液重1.433 70 g,溶液2重14.29760 g,混匀,即得151Sm/154Sm约10-9(标样Ⅳ)。
4 溶液浓度的测定和参考标准比值计算为了计算稀释后的参考标准的同位素比值151Sm/154Sm,必须准确测定溶液1和溶液2中Sm的浓度,采用了同位素稀释质谱法得到两种溶液Sm的浓度。下面以溶液1中Sm浓度的测定为例。
称取适量天然丰度Sm2O3配成溶液,然后分别取溶液1和天然丰度Sm2O3溶液适量混合,测量混合后样品中的150Sm/152Sm。根据同位素稀释法原理,由式(1)可以计算出溶液1中Sm的浓度。
| ${{C}_{\operatorname{X}}}=\frac{{{B}_{0/2}}-{{C}_{0/2}}}{{{C}_{0/2}}-{{A}_{0/2}}}\cdot \frac{{{b}_{2}}}{{{a}_{2}}}\cdot \frac{{{C}_{\operatorname{Y}}}{{G}_{\operatorname{Y}}}}{{{G}_{\operatorname{X}}}}$ | (1) |
式中:CX为溶液1中Sm的浓度,mol·g-1;A0/2为溶液1中150Sm/152Sm;B0/2为天然钐中150Sm/152Sm;
C0/2为混合液中150Sm/152Sm;a2为溶液1中152Sm的丰度;b2为天然钐中152Sm的丰度;CY为天然钐溶液浓度,mol·g-1;GX为溶液1的重量,g;GY为天然钐溶液的重量,g。
以上相关参数可以由表 1、4-6得到,根据式(1)可以计算得到溶液1中Sm的浓度(表 7)。
| 表 4 天然Sm2O3同位素丰度比的测定值 Table 4 Measured values of isotope ratios for natural abundance Sm2O3. |
| 表 5 溶液1中Sm同位素丰度的测定结果 Table 5 Measured results of isotope abundance in solution 1. |
| 表 6 溶液1中Sm同位素丰度比的测定结果 Table 6 Measured results of isotope ratios in solution 1. |
| 表 7 溶液1中Sm浓度的测定结果 Table 7 Measured valves of Sm concentration in solution 1. |
由同位素稀释质谱法可以得到溶液1中Sm的浓度平均值为1.228×10-6 mol·g-1。同理可以通过测量溶液2中同位素的丰度及同位素丰度比,得到溶液2中Sm的浓度为1.424×10-5 mol·g-1。
根据以上两种溶液的质量、浓度及151Sm和154Sm的丰度可以计算得到稀释后参考标准的同位素比值151Sm/154Sm。
5 AMS测量样品Sm2O3的研制CIAE的AMS测量样品为固体,为满足AMS测量需将上述参考标准制备成固体形式。同时样品化学形式直接决定着负离子的引出形式和引出效率,关系到对其同量异位素等干扰的抑制程度。采用富集的154Sm2O3和天然丰度的Eu2O3在离子源引出不同形式的负离子,引出束流情况为:SmO- > SmO2- > SmO3- > SmO4-,EuO- < EuO2- < EuO3- < EuO4-(见表 8、9)。实验结果表明,在151Sm的AMS测量中,样品采用Sm2O3,引出SmO-负离子,可以对其同量异位素151Eu起到一定的抑制作用,可将151Eu的干扰压低约7倍。所以样品最终要制备成Sm2O3形式。
| 表 8 富集154Sm2O3引出的束流强度 Table 8 Beam current from the enriched 154Sm2O3. |
| 表 9 天然Eu2O3引出的束流强度 Table 9 Beam current from the nature abundance Eu2O3. |
将钐的标准溶液在烧杯中缓慢蒸至近干,用10mL 0.03mol·L-1盐酸溶解。加入饱和草酸溶液得到草酸钐沉淀,用5mL 0.2%草酸重复洗涤3次,然后将沉淀转移至铂坩埚中,放于马弗炉内升温至900°C煅烧2h,制备成Sm2O3,冷却后称重保存。
6 结语研制了151Sm/154Sm的比值分别为(9.25±0.08)×10-7、(8.87±0.08)×10-8、(8.08±0.08)×10-9 151Sm的AMS实验室参考标准。同时对同位素比的TIMS测定方法进行了研究,成功建立了151Sm同位素比的TIMS测定方法,并且应用同位素稀释质谱法测量了标准溶液(I)和稀释剂溶液中Sm的浓度。
| [1] |
倪嘉缵.
稀土生物无机化学[M]. 北京: 科学出版社, 1994 : 162 .
NI Jiazan. Bioinorganic chemistry of rare earth elements[M]. Beijing: Science Press, 1994 : 162 . (  0) 0)
|
| [2] |
Xiao H Q, Li F L, Zhang Z Y, et al. Accumulation and distribution of samarium-153 in rat brain after intraperitoneal injection[J].
Biological Trace Element Research, 2005, 104 (1) : 33 –40.
DOI: 10.1385/BTER:104:1:033 ( 0) 0)
|
| [3] |
Xiao H Q, Li F L, Zhang Z Y, et al. Distribution of ytterbium-169 in rat brain after intravenous injection[J].
Toxicology Letter, 2005, 155 : 247 –252.
DOI: 10.1016/j.toxlet.2004.09.021 ( 0) 0)
|
| [4] |
Evans C H.
Biochemistry of the lanthanides[M]. New York: Plenum Press, 1990 .
( 0) 0)
|
| [5] |
Pennick M, Demmos K, Damment S J P. Absolute bioavailability and disposition of lanthanum in healthy human subjects administered lanthanum carbonate[J].
The Journal of Clinical Pharmacology, 2006, 46 : 738 –746.
DOI: 10.1177/0091270006289846 ( 0) 0)
|
| [6] |
Kato M, Sugihara J, Nakamura T, et al. Electron microscopic study of the blood-brain barrier in rats with brain edema and encephalopthy due to acute hepatic failure[J].
Gastroenterologia Japonica, 1989, 24 (2) : 135 –142.
( 0) 0)
|
| [7] |
Xu J, Ling E A. Studies of the ultrastructure and permeability of the blood-brain barrier in the developing corpus callosum in postnatal rat brain using electron dense tracers[J].
Journal of Anatomy, 1994, 184 (2) : 227 –237.
( 0) 0)
|
| [8] |
易健民, 阎建辉, 周宁波. 生物样品中微量稀土元素的测定[J].
精细化工中间体, 2003, 33 (3) : 61 –62.
YI Jianmin, YAN Jianhui, ZHOU Ningbo. Determination of trace rare earth elements in biological samples[J]. Fine Chemical Intermediates, 2003, 33 (3) : 61 –62. (  0) 0)
|
| [9] |
Muller R A. Radioisotope dating with a cyclotron[J].
Science, 1977, 196 : 489 –494.
DOI: 10.1126/science.196.4289.489 ( 0) 0)
|
| [10] |
Elmore D, Phillips F M. Accelerator mass spectrometry for measurement of long-lived radioisotopes[J].
Science, 1987, 236 : 543 –550.
DOI: 10.1126/science.236.4801.543 ( 0) 0)
|


