2. 上海科技大学 上海 201210;
3. 中国科学院大学 北京 100049
2. ShanghaiTech University, Shanghai 201210, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China
多相催化在能源与环境研究中地位显著。该过程贡献了全球国民生产总值的20%左右。多维度的表征分析手段是我们从事多相催化研究的利器。理想的催化表面分析工作应当能建立表界面结构影响活性和选择性的内在关系,进而设计实际催化剂[1]。由于温度与压力等真实反应条件对表征的制约,存在“材料鸿沟、压力鸿沟”[2],是多相催化的基础研究与产业应用直接相关的主要问题。近年来多相催化领域[1, 3-4]针对在工业条件下进行实验室方法表征,提出了相对“In situ”(原位)的“Operando”(服役状态)概念。In situ强调表征环境具有严格的反应环境参数控制;Operando在此基础上更强调表征的过程中存在可观测的反应实际转化率[5]。Operando技术的发展使得表面催化研究更接近工业反应条件。近些年,同步辐射原位表征手段层出不穷,在推动理解催化机理、提高反应效率等方面取得了许多重要成果[6]。然而在如何把同步辐射相关的原位表征手段和其他辅助表征手段相结合方面还有很大的发展空间。针对这一需求,我们开发了以热化学催化过程为目的的Operando表征原型装置。对装置的温控、压控、采样速度和反应器操作进行了优化设计。该装置可以为同步辐射原位表征完成预评价和筛选工作,也可以平行完成部分反应动力学表征,并有可能通过进一步改装增加光学窗口界面,直接作为原位表征池应用在线站上[7]。
设计灵活模拟真实反应条件的表征平台,科学地设计实验过程,可将暂态过程和非同位素稳态实验的结果结合起来,在较大温度和压力范围快速完成催化剂的在线评价和基本动力学测试。根据我们近年的经验积累[5, 8],结合暂态[9]和稳态[4, 10]两类实验优势,可以缩小复杂表面-产物同步检测反应(包括稳态同位素反应)实验的范围,为从原子和分子层面上理解催化反应动力学寻找适合的切入点。
本文将介绍一种符合以上理念的模拟反应条件在线表征催化的新型质谱反应装置。该装置可以在液氮温区至500 ℃的温度范围、0.1-2 MPa或更高的压力范围内模拟反应,并通过质谱在上述压力温度区间以秒级时间分辨率和千万分之一灵敏度对反应物和产物连续实时采样监控。特别是这一在线质谱微反应装置可以与现有的同步辐射线站相连接而形成一个原位多维度、多方法原位表征平台。本文将对此装置的设计、性能及其对纳米Au/TiO2、铜粉催化剂的表征进行说明和讨论。
1 催化在线表征装置技术指标 1.1 -160 -500 ℃的实验温区催化反应的研究涉及广泛的工作温区:动力学基元步骤研究(如CO在Au/TiO2催化剂表面氧化滴定[11-12])要求低温范围接近液氮温区;而模拟工业条件下稳态反应(如费托合成[13])则要求350-500 ℃甚至更高的温度范围。因此,对实验装置的设计要求为灵活控制从-160-500 ℃的温度区域,并达到程控升温的精度要求。
1.2 工业条件压力下反应催化有关的工业反应,均有一定压力要求,如工业合成氨反应[14]、甲醇合成反应[15-17]。甲醇合成反应通常在4-6 MPa下进行,该反应对气压指数依赖系数约为1.4[17]。即若在常压下开展甲醇合成研究,产物转化率将低于十万分之一。模拟工业条件,在反应进行中的温度和压力下从事催化剂在线表征,有助于更真实地表征催化反应与探索反应机理。
1.3 装置模块化、小型化与操作简便依前所述,结合不同催化体系,装置需要灵活迅速的完成暂态和稳态定制反应,因此应突出模块化、小型化的要求。装载界面模块化:适合多种样品体系切换,可根据反应条件环境(如氧化、还原、腐蚀)轻松调整反应器材料。反应器尺寸小型化:首先可以不改变装置材质保障高压装置可靠性;其次,减少了死体积内气体吹扫,为动力学瞬态过程研究提高时间分辨率;再次是有效控温。如前述反应器在低温区需使用液氮降温,使用量与反应器总质量成正比。而液氮无论在比热和气化热上都远小于水。如使用市售最小型管式炉,加热及反应部分一般在10 kg左右,即使热交换充分,至少需要15-20 L液氮才能完成一次从室温开始的降温。考虑通常液氮在制冷传输热交换不充分,往往一增压罐约50 L液氮消耗完才能基本冷却10 kg的管式炉,这对实验室操作来说是不现实的。
2 反应装置结构与技术要领 2.1 反应装置结构 2.1.1 反应系统本文所描述的新型反应装置是与课题组开发的在线红外质谱(Infrared spectra-Mass Spectra, IR-MS)表征平台兼容的反应系统中的一种,与平台的质谱探测装置对接,由课题组最近设计成功,并申请专利。装置核心部分包括:管式微反应器和加热模块。附属部件包括防氧化金属外壳、绝热非金属外壳、制冷及保护气体回路等。
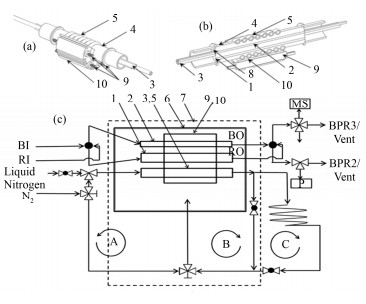
管式微反应器:结构示意图见图 1(a)、(b),图 1中1、2、3、8依次代表反应管活动插口、对照空管活动插口、制冷管出入固定接口、热电偶活动插口;4、5分别代表管式炉结构体及缠绕在管式炉结构体外的制冷盘管;6、7代表防氧化金属外壳,绝热非金属外壳;9、10代表加热部件。管式微反应器直径为29 mm,总长12 cm,突出反应器尺寸小型化特点。结构体使用圆柱形金属块加工。由于不锈钢耐高温,纯铜导热好,500 ℃以上使用不锈钢,频繁用于低温实验使用纯铜。微反应器中间部分提供多个轴向直管插口。活动插口的设计突出装载界面模块化特点,便于反应区材料和样品自由切换。更换实验催化体系可通过在几分钟内切换反应炉管实现。同时炉管材质能自由选用多种金属(铜、钛、不锈钢)或玻璃(石英、硼化玻璃),腐蚀性反应环境选用耐腐蚀金属如哈氏合金(HASTELLOY C-276)。反应炉管外径6 mm。对照空管活动插口中接入3 mm同材质对照炉管,其与反应炉管平行,并在同一个加热控温区内。对照空管试验中一般不填装催化剂,通过四通阀切换到质谱检测,即可方便的扣除无催化剂时的反应本底背景,提高质谱评价的精度和可靠性。主要针对极少量催化剂的评价或产物中有质谱碎片重叠的情况。
|
图 1 管式微反应器结构(a、b)和装置冷却气路(c) Figure 1 Scheme of tube microreactor (a, b) and illustration of cooling circuit (c). |
加热部件模块:内径与微反应器外径相同,通过接触式传热。根据使用时需要的加热功率、预热时间长短等具体要求可采用电热丝、加热棒(图 1(a)中9)或热流道弹簧加热圈等加热。加热采用比例积分微分(Proportion Integration Differentiation, PID)程控方式,热电偶安装在前述管式炉结构微反应器活动插口中,距离反应炉管和对照空管中央位置小于3 mm,共两支:一支为温控反馈热电偶;另一支验证温度,也可提供过热保护开关的参考温度。目前使用K型铠装热电偶和铂铠装热电阻,程控温度范围从液氮温区到1100 ℃,覆盖催化动力学研究的全部温域。
制冷回路:依据需求切换使用液氮或制冷气体(压缩空气/增压氮气),通过双球阀配合三通经由前述盘管实现降温。直接制冷结束后排出的气体,视使用温区具体情况通过循环回路引回金属外壳内作为保护气体。制冷盘管简化为直管。
可开合的金属外壳和非金属材质透明外壳:用于容纳和保护管式微反应器及加热部件,并减少空气对流降低环境对反应的影响。
2.1.2 气路系统与采样系统气路系统:气体成分与压力控制单元。上游气体通过多个质量流量计(Mass Flow Controller, MFC)精确配比定压的在线混气,背压阀调节压力,经图 1(c)左侧四通阀切换进入微反应器,实现反应表征所需的暂态与稳态输入。由于气路以及微反应器采用小截面管道,理论上无死体积,仅由于气体在管道输运中的扩散会造成切换界面的有限混合。切换时间最快小于1 s。
高压反应质谱在线采样系统:通过放置在质谱前的分子泵预抽毛细管,将反应气体引入质谱进行分析,实现高压反应下的质谱采样,模拟工业条件。依照炉管采用连接体系,气压范围即可以达到相应材料体系要求。使用金属材质炉管时,依使用卡套设计标准,反应器内部配合相应的背压阀最高则可达10 MPa以上。
2.2 反应装置技术要领高效制冷的实现:微反应器结构体圆柱面做螺旋凹槽处理,钎焊6 mm紫铜制冷盘管,可保证液氮或制冷气体与装置核心部分充分的热交换,同时紫铜盘管也可以将外部加热模块的热量均匀传递到内部。经过测试,采用这种制冷结构,冷却总重约1 kg的装置核心部分从室温到邻近液氮温度(-196 ℃),仅需1 L液氮,时间约20 min,与超高真空下的样品台制冷速度相当。整个制冷过程,制冷管出口温度与反应区中心温度相差保持在10 ℃以内,热交换效率达80%。一般的小型液氮增压罐即可保证多次实验升降温过程的需求。
制冷尾气作为保护气体的利用:微反应器工作温区大,裸露工作会造成装置在低温形成冷凝水,高温表面被过度氧化。因此设计保护气体回路和外壳结构,利用液氮或增压氮气制冷后的尾气作为反应部的保护气体,如图 1(c)所示。制冷尾气回吹入金属外壳内,保护其内部为无氧环境。加热模块、微反应器连同金属外壳放置在有机玻璃罩内,阻止吹扫后的氮气扩散,消除装置带电部分在低温时形成流动冷凝水可能。
制冷回路制冷物质对金属外壳内吹扫可选择如图 1(c)中所示的A、B、C路径。路径A直接吹扫:制冷气体直接进入金属外壳,不对反应装置核心部分降温,适用大于250 ℃高温控制状态。路径B尾气通过散热器回收吹扫:制冷气体对反应装置核心部分降温后,经装置非金属外壳外的散热片达到室温后再引入金属外壳内,适用-100-300 ℃的温度区间。路径C尾气直接回收吹扫:制冷气体/液氮经过反应装置核心部分后直接通过有机玻璃罩内部管路引入金属外壳内,适用于-196-50 ℃的温度区间。跨以上温区控温需要适时切换制冷线路,也可以通过安装气动阀门及温控开关自行设计自动制冷切换互锁。
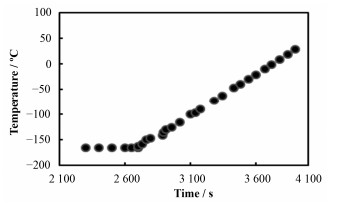
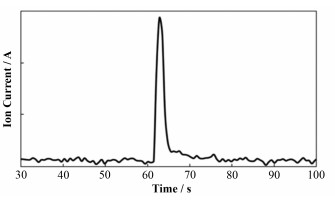
3 CO预吸附低温TPD实验反应装置在-165-45 ℃下程序升温控温效果如图 2所示。最初20℃由于热传递效果不明显,控温略有抖动。在-130 ℃以上温度-时间为良好线性关系。质谱对监测区气流突变的信号响应见图 3。实验中用氦气测漏吹枪改变毛细管附近的氦气成分。吹枪流速经调节钢瓶减压阀降至最低,开启吹枪后瞬间关闭。从图 3中可见,质谱气体信号响应曲线基本无时间间隔,上升沿的时间常数已在质谱采样时间分辨率以内。因此反应装置在低温下升温控制可靠,而且质谱仪对反应仪器核心部分的常压高压区可以完成实在线采样。
|
图 2 -165 ℃程序升温时质谱时间-温度关系 Figure 2 Temperature control vs. time during heating process from -165 ℃. |
|
图 3 质谱对常压下氦气吹扫脉冲的响应 Figure 3 The response of the mass spectrometry to the helium gas pulse at ambient pressure. |
课题组选择低温下Au/TiO2催化剂对CO的脱附过程测试作为开展针对性研究的对象。
Green等[11-12]通过-153 ℃低温环境红外准原位表征CO氧化过程-153 ℃下,对已经CO吸附饱和的Au/TiO2催化剂红外观察发现,CO在Au与TiO2上都有吸附。保持-153 ℃条件,用分压为133 Pa O2吹扫预吸附CO饱和的Au/TiO2催化剂,红外显示CO/TiO2吸收峰逐渐消失,CO2/TiO2吸收峰逐渐增强(2341 cm−1),显示TiO2位点上预吸附的CO被氧化。此过程中CO/Au的吸收峰强度基本不变。以上结果结合密度泛函理论(Density Functional Theory, DFT)计算,提出CO在金钛体系双位点反应机理。但受实验条件的限制,该课题组并未能实现气体产物的质谱采集,反应压力也非在常压下,因此未提供表面CO2/TiO2为反应中间体的直接证据。
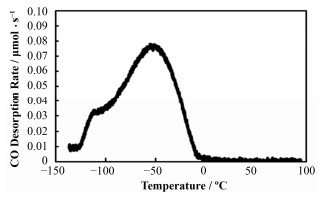
课题组利用新型装置开展了相同体系的在线动力学测试,以上述研究为基础对低温下CO与金钛体系相互作用作进一步的认识。实验中Au/TiO2催化剂按照文献[10, 18]方式合成,Au 8.0wt%,透射电子显微镜(Transmission Electron Microscope, TEM)及X射线衍射(X-Ray Diffraction, XRD)峰宽拟和均显示平均粒径为3.0 nm。仅以预先吸附CO的Au/TiO2催化剂的程序升温脱附(Temperature Programmed Desorption, TPD)实验为例:将100 mg Au/TiO2催化剂装入石英样品管,0.1 MPa气压、200 ℃预还原处理后,在常压氦气吹扫保护下,降温至-150 ℃。从0 ℃至-150 ℃冷却时间为15 min(前级冷却管道充分预冷条件下)。-150 ℃下,催化剂在3% CO气氛还原,载气为氦气。氦气充分吹扫管道与反应装置内多余的CO后,继续在氦气保护下程序升温,升温速率为10 ℃·min-1。通过质谱采集气体产物信号,可得低温下CO程序升温脱附的信号(图 4)。
|
图 4 CO预吸附的Au/TiO2催化剂TPD曲线 Figure 4 TPD signal of reduced Au/TiO2 catalyst. |
与以上实验相似,在稳定控制温度气压的基础上,结合高时间分辨的质谱采样,通过改变以上实验过程的气流组分、温度变化等在线控制参数,该装置可以完成对催化剂的化学比表面积、转化率、反转频率等反应参数的在线评价,也可以完成TPD、程序升温还原(Temperature Programmed Reduction, TPR)、程序升温氧化(Temperature Programmed Oxidation, TPO)以及反应对温度依赖的Arrhenius图等反应动力学的测试分析。因此可以通过本装置,对类似上述Au/TiO2催化剂的实验条件[13-14]进行模拟重复,并将研究范围扩展到更大的动态温度范围。
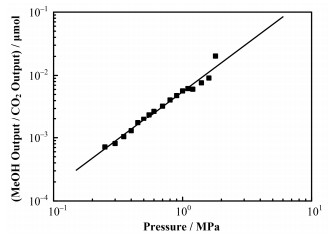
以甲醇合成反应作为研究对象,280 ℃下,反应装置装载3.0 g金属铜(Alfa aesar,编号42689)作为对照催化剂,粒径为10 μm。经过N2O滴定实验测定金属活性位点[19-20]可以确认,催化剂金属表面积在反应前后一致,没有烧结。甲醇合成实验中,样品首先在280 ℃下在氢气中充分还原,再通入1:5:14的Ar/CO2/H2混合气体(Ar为载气,作为质谱信号标定),总流量为20 mL·min-1。实验中反应气压从0.25 MPa起步,达到平衡后通过标定质谱信号得到相应转化率。重复以上步骤,逐步将气压增加到1.8 MPa。得到CO2转化率与气压的响应,如图 5所示。数据拟合结果表明,金属铜在低转化率下反应速率的气压指数为1.5,与之前在氧化物载体上的结果[15, 17]比较基本一致。这个实验证明装置在高压下可以保持灵活的工作状态。
|
图 5 甲醇合成反应CO2转化率与压力的关系 Figure 5 CO2 conversion rate vs. pressure in methanol synthesis. |
本文描述了一台新型催化研究在线表征反应装置的研制和特点。该装置是课题组Operando催化研究平台核心反应装置之一,直接为质谱提供采样,特别为催化剂的在线表征设计。可在-150-500 ℃的温度控温,并适应0.1-2 MPa下的实验环境质谱在线采样,结合气流控制,可完成多种催化剂在线评价和动力学性能测试。装置通过模块化与小型化设计,可轻松切换气路,改变探针分子,在几分钟的时间内更换反应管与对照样品管,快速地执行不同催化剂与不同探针反应的测试。通过装置在CO在Au/TiO2催化剂上的低温脱附等测试,体现了装置在常压时-150 ℃的低温区热力学表征性能。此装置既适合迅速完成催化剂的筛选优化,也随时可以对特征样品完成进一步的动力学表征,为同平台上的红外质谱反应器测试提供准备和补充,是通过在线表面方法表征了解催化剂反应性能的有力工具。
| [1] |
Yates J T, Campbell C T. Surface chemistry:key to control and advance myriad technologies[J].
Proceedings of the National Academy of Sciences, 2011, 108 (3) : 911 –916.
DOI: 10.1021/cen-v070n013.p022 ( 0) 0)
|
| [2] |
路军岭, 高鸿钧, 时东霞. 原子尺度上的异质催化[J].
物理, 2007, 36 (05) : 370 –376.
DOI: 10.3321/j.issn:0379-4148.2007.05.009 LU Junling, GAO Hongjun, SHI Dongxia. Heterogeneous catalysis on an atomic scale[J]. Physics, 2007, 36 (05) : 370 –376. DOI: 10.3321/j.issn:0379-4148.2007.05.009 (  0) 0)
|
| [3] |
Lerou J J, Ng K M. Chemical reaction engineering:a multiscale approach to a multiobjective task[J].
Chemical Engineering Science, 1996, 51 (10) : 1595 –1614.
DOI: 10.1016/0009-2509(96)00022-X ( 0) 0)
|
| [4] |
Meunier F C. The design and testing of kinetically-appropriate operando spectroscopic cells for investigating heterogeneous catalytic reactions[J].
Chemical Society Reviews, 2010, 39 (12) : 4602 –4614.
DOI: 10.1039/B919705M ( 0) 0)
|
| [5] |
Yang Y, Mei D, Peden C H F, et al. Surface-bound intermediates in low-temperature methanol synthesis on copper:participantsDO and spectators[J].
ACS Catalysis, 2015, 5 (12) : 7328 –7337.
DOI: 10.1021/acscatal.5b02060 ( 0) 0)
|
| [6] |
常睿, 邰仁忠, 刘志, 等. 同步辐射近常压光电子能谱及其应用[J].
核技术, 2012, 35 (7) : 481 –485.
CHANG Rui, TAI Renzhong, LIU Zhi, et al. Synchrotron radiation-based ambient pressure photoelectron spectroscopy and its applications[J]. Nuclear Techniques, 2012, 35 (7) : 481 –485. (  0) 0)
|
| [7] |
Yang T Y, Wen W, Yin G Z, et al. Introduction of the X-ray diffraction beamline of SSRF[J].
Nuclear Science and Techniques, 2015, 26 (2) : 020101 .
DOI: 10.13538/j.1001-8042/nst.26.020101 ( 0) 0)
|
| [8] |
Yoon K, Yang Y, Lu P, et al. A highly reactive and inter-resistant catalytic system based on platinum nanoparticles embedded in the nner surfaces of CeO2 hollow fibers[J].
Angewandte Chemie International Edition, 2012, 51 (38) : 9543 –9546.
DOI: 10.1002/anie.201203755 ( 0) 0)
|
| [9] |
Widmann D, Behm R J. Active oxygen on a Au/TiO2 catalyst:formation, stability, and CO oxidation activity[J].
Angewandte Chemie International Edition, 2011, 50 (43) : 10241 –10245.
DOI: 10.1002/anie.201102062 ( 0) 0)
|
| [10] |
Enger B C, Frøseth V, Yang J, et al. SSITKA analysis of CO hydrogenation on Zn modified cobalt catalysts[J].
Journal of Catalysis, 2013, 297 : 187 –192.
DOI: 10.1016/j.jcat.2012.10.013 ( 0) 0)
|
| [11] |
Green I X, Tang W, Neurock M, et al. Spectroscopic observation of dual catalytic sites during oxidation of CO on a Au/TiO2 catalyst[J].
Science, 2011, 333 (6043) : 736 –739.
DOI: 10.1126/science.1207272 ( 0) 0)
|
| [12] |
Green I X, Tang W, McEntee M, et al. Inhibition at perimeter sites of Au/TiO2 oxidation catalyst by reactant oxygen[J].
Journal of the American Chemical Society, 2012, 134 (30) : 12717 –12723.
DOI: 10.1021/ja304426b ( 0) 0)
|
| [13] |
Schulte H J, Graf B, Xia W, et al. Nitrogen-and oxygen-functionalized multiwalled carbon nanotubes used as support in iron-catalyzed, high-temperature fischer-tropsch synthesis[J].
ChemCatChem, 2012, 4 (3) : 350 –355.
DOI: 10.1002/cctc.201100275 ( 0) 0)
|
| [14] |
Vasileiou E, Kyriakou V, Garagounis I, et al. Ammonia synthesis at atmospheric pressure in a BaCe0.2Zr0.7Y0.1O2.9 solid electrolyte cell[J].
Solid State Ionics, 2015, 275 : 110 –116.
DOI: 10.1016/j.ssi.2015.01.002 ( 0) 0)
|
| [15] |
Robbins J L, Iglesia E, Kelkar C P, et al. Methanol synthesis over Cu/SiO2 catalysts[J].
Catalysis Letters, 1991, 10 (1-2) : 1 –10.
DOI: 10.1007/BF00764730 ( 0) 0)
|
| [16] |
Yang Y, Mims C A, Mei D H, et al. Mechanistic studies of methanol synthesis over Cu from CO/CO2/H2/H2O mixtures:the source of C in methanol and the role of water[J].
Journal of Catalysis, 2013, 298 : 10 –17.
DOI: 10.1016/j.jcat.2012.10.028 ( 0) 0)
|
| [17] |
Yang Y, Mims C A, Disselkamp R S, et al. Isotope effects in methanol synthesis and the reactivity of copper formates on a Cu/SiO2 catalyst[J].
Catalysis Letters, 2008, 125 (3-4) : 201 –208.
DOI: 10.1007/s10562-008-9592-4 ( 0) 0)
|
| [18] |
Zanella R, Giorgio S, Henry C R, et al. Alternative methods for the preparation of gold nanoparticles supported on TiO2[J].
The Journal of Physical Chemistry B, 2002, 106 (31) : 7634 –7642.
DOI: 10.1021/jp0144810 ( 0) 0)
|
| [19] |
Luys M J, van Oeffelt P H, Pieters P, et al. The adsorptive decomposition of nitrous oxide on supported copper catalysts:the influence of the metallic dispersion and type of support on the subsurface oxidation[J].
Catalysis Today, 1991, 10 (3) : 283 –292.
DOI: 10.1016/0920-5861(91)80008-W ( 0) 0)
|
| [20] |
Luys M J, Van Oeffelt P H, Brouwer W G J, et al. Surface and sub-surface oxidation of copper and supported copper catalysts by nitrous oxide[J].
Applied Catalysis, 1989, 46 (1) : 161 –173.
DOI: 10.1016/S0166-9834(00)81401-3 ( 0) 0)
|


