2. 广西大学轻工与食品工程学院, 南宁, 530004
2. Light Industry and Food Engineering College, Guangxi University, Nanning 530004
二氧化硫含量是白砂糖的一项重要质量指 标。最新的白砂糖国家标准 GB317—2006 对二氧 化硫指标[1]进行更为严格的修订:一级、二级白 砂糖≤30 mg/kg,优级白砂糖≤15 mg/kg,精制白 砂糖≤6 mg/kg。
国标 GB317—2006 中规定,白砂糖中二氧化 硫的测定方法参照 GB/T5009.34—2003《食品中 亚硫酸盐的测定》 , 即四氯汞钠-盐酸副玫瑰苯胺 比色法[2]。该方法使用了有毒试剂四氯汞钠,且 用量较大,对环境造成汞污染,同时也危害到有 关化验人员的身体健康。本文采用三乙醇胺吸收 —盐酸副玫瑰苯胺分光光度法测定白砂糖中的二 氧化硫,并与国标方法进行比较,结果令人满意。
UV2501PC 紫外/可见分光光度计;25 mL 带塞 比色管;恒温水浴槽
三乙醇胺吸收液[3]:将 0.5 g 三乙醇胺(含量 75%~85%),1 gEDTA,0.8 g 氨基磺酸铵稀释 至 1 L,配制为 0.05%的三乙醇胺吸收液。
盐酸副玫瑰苯胺溶液[4]:25 mL 0.2%盐酸副 玫瑰苯胺溶液+30 mL 磷酸(85%)+ 12 mL 浓盐 酸,摇匀,避光贮存。
二氧化硫标准溶液:称取 0.5 g 亚硫酸氢钠, 溶于 200 mL 三乙醇胺吸收液中,马上进行标定。 按标定计算的结果,立即用三乙醇胺吸收稀释成 每毫升含 3μg 二氧化硫的标准溶液置于冰箱中 贮存备用,可稳定 1 个月。
2 mol/L 氢氧化钠溶液;0.5 mol/L 氢氧化钠 溶液;0.25 mol/L 硫酸溶液。
以上所用试剂均为分析纯,水为去离子水。
吸取 0.0、1.0、2.0、3.0、5.0、10.0 mL二氧化硫标准溶液,分别置于比色管中,用三乙 醇胺吸收液定容至 10 mL。各管中分别加入 2 mL 甲醛、1 mL 盐酸副玫瑰苯胺溶液,充分混匀后, 室温下静置 20 min。用 1 cm 比色皿,用零管调 节零点,于波长 579 nm 处测定吸光度,绘制标准 曲线。
称取 10.00 g 白砂糖,用少量水溶解,置于 100 mL 容量瓶中,加入 4 mL 氢氧化钠溶液(0.5 mol/L) ,混匀,5 min 后加入 4 mL 硫酸(0.25 mol/L) ,然后加入 20 mL 三乙醇胺吸收工作液, 用水稀释至刻度,混匀。
吸取 5 mL 白砂糖样液,用三乙醇胺吸收液定 容至 10 mL,再加入 2 mL 甲醛、1 mL 盐酸副玫瑰 苯胺溶液,充分混匀后,室温下静置 20 min。用 1 cm 比色皿,于波长 579 nm 处测定吸光度,按 标准曲线和国标方法计算公式计算结果。
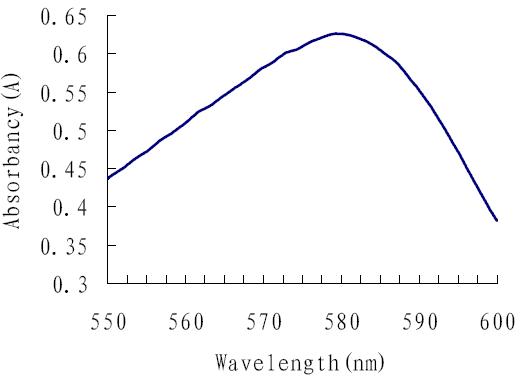
吸取 5.0 mL 二氧化硫标准溶液于比色管中, 用三乙醇胺吸收液定容至 10 mL,再加入 2 mL 甲 醛、1 mL 盐酸副玫瑰苯胺溶液,充分混匀后,室 温下静置 20 min,在 500~600 nm 波长范围内测 定吸光度 A,绘制吸收光谱图,结果见图 1。图 1 可见,该紫红色物质在波长 579 nm 处有最大吸收 峰。因此,本次实验以 579 nm 作为测定波长。
|
图 1 吸收光谱图 |
二氧化硫、甲醛、盐酸副玫瑰苯胺溶液三者 发生显色反应。因此,甲醛的用量会影响到整个 实验测定的最终结果。
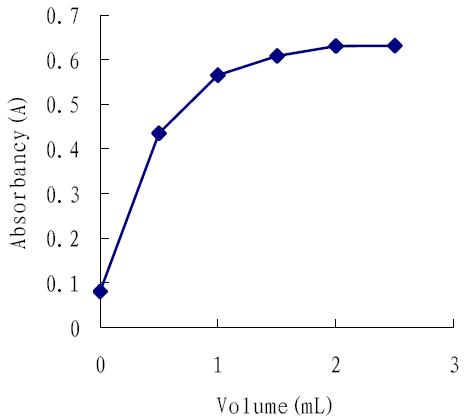
吸取 5.0 mL 二氧化硫标准溶液于比色管中, 改变甲醛用量 (0.0、 0.5、 1.0、 1.5、 2.0、 2.5 mL) , 分别测定不同体积的甲醛对吸光度的影响。从图 2 可以看出,甲醛用量为 2.0 mL 时,吸光度值出 现最大,同时,再增加甲醛的用量,吸光度变化 不明显。因此,本次实验选择甲醛的用量为 2.0 mL。
|
图 2 甲醛用量对反应体系的影响 |
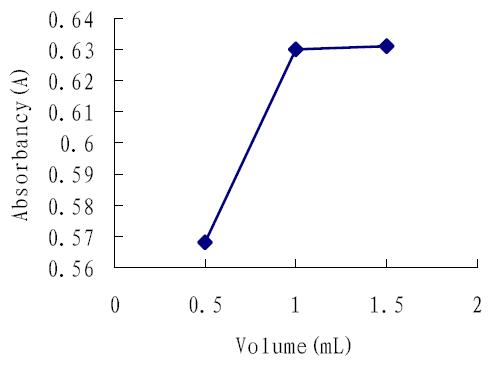
盐酸副玫瑰苯胺的用量也会影响到整个实验 测定的最终结果。吸取 5.0 mL 二氧化硫标准溶液 于比色管中,改变盐酸副玫瑰苯胺的用量(0.5、 1.0、1.5 mL) ,分别测定不同体积的甲醛对吸光 度的影响。如图 3 所示,盐酸副玫瑰苯胺用量为 0.5 mL 时,吸光度值明显偏低,即显色反应不完 全;盐酸副玫瑰苯胺用量为 1.0 mL 和 1.5 mL 时, 吸光度值无明显变化。因此,考虑显色反应完全 和节约实验成本两个因素,本次实验选择盐酸副玫瑰苯胺的用量为 1.0 mL。
|
图 3 盐酸副玫瑰苯胺用量对反应体系的影响 |
二氧化硫与三乙醇胺生成稳定的阴离子复合 物。因此,三乙醇胺的用量极大地影响到整个测 定过程。资料表明,三乙醇胺浓度太低,阴离子 复合物不够稳定;三乙醇胺浓度太高,显色颜色 浅,灵敏度低,检出限不能满足要求。
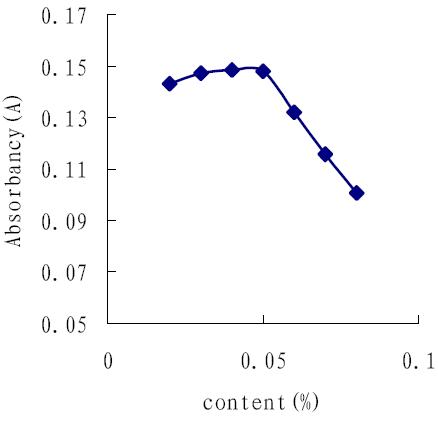
吸取 1.0 mL 二氧化硫标准溶液,用不同浓度 的三乙醇胺吸收液定容至 10 mL,再加入 2.0 mL 甲醛、1.0 mL 盐酸副玫瑰苯胺溶液,充分混匀后, 室温下静置 20 min, 在 579 nm 波长测定吸光度 A, 绘制曲线。图 4 可以看出,三乙醇胺的浓度大于 0.08%灵敏度较低。综合考虑灵敏度和稳定性两 个因素,采用 0.05%三乙醇胺比较合理。
|
图 4 三乙醇胺含量对吸光度的影响 |
吸取 5.0 mL二氧化硫标准工作溶液于比色管 中,根据糖厂所在区域的特殊性,选择 15~30℃ 为测定范围,在不同温度下测定其稳定时间(即 吸光度最大值出现时间,表示显色完全并稳定) , 见表 1。
| 表 1 稳定时间与温度的关系 |
在实际测定中,可以不用水浴控制温度,以 减少操作的繁琐性。我们可以根据表 1,选择与 室温最为接近的显色温度以确定稳定时间。如本 次实验测定时室温为 24℃,可选择 20 min 为稳 定时间。
测定不同含量的二氧化硫标准溶液吸光度, 测定数据见表 2。
| 表 2 二氧化硫含量及其吸光度 |
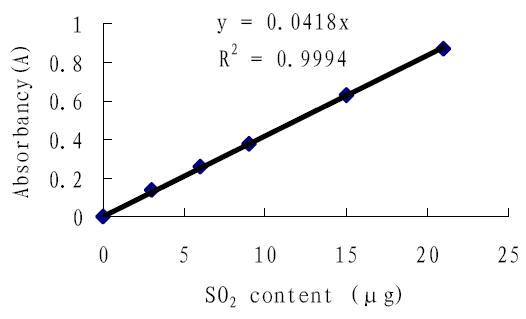
以二氧化硫含量 A 为 X 轴,吸光度 Abs 为 Y 轴,绘制标准曲线,如图 5 所示。
|
图 5 二氧化硫标准曲线图 |
结合标准曲线方程 Abs = 0.0418A 和国标方
法计算公式,得出最终计算公式为: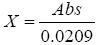
计算出白砂糖中二氧化硫浓度在 0~60 mg/kg 范围内与吸光度 Abs 呈良好的线性关系, 相关系数 R2= 0.9994。按吸光度 Abs = 0.01 时所 对应得二氧化硫浓度计算检出限,白砂糖样品中 的二氧化硫的检出限为 0.50 mg/kg。
取 4 个不同糖厂生产的白砂糖样品,重复测 定 6 次,计算出相对标准偏差为 4.0%。
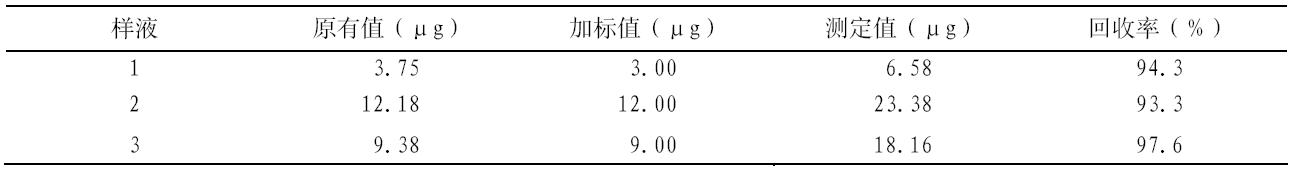
取 3 个不同糖厂生产的白砂糖样品,配制好 样液后,加入一定量的二氧化硫标准溶液,测定 其含量并计算回收率,回收率在 93.3%~97.6% 之间,结果见表 3。
| 表 3 样液的加标回收率 |
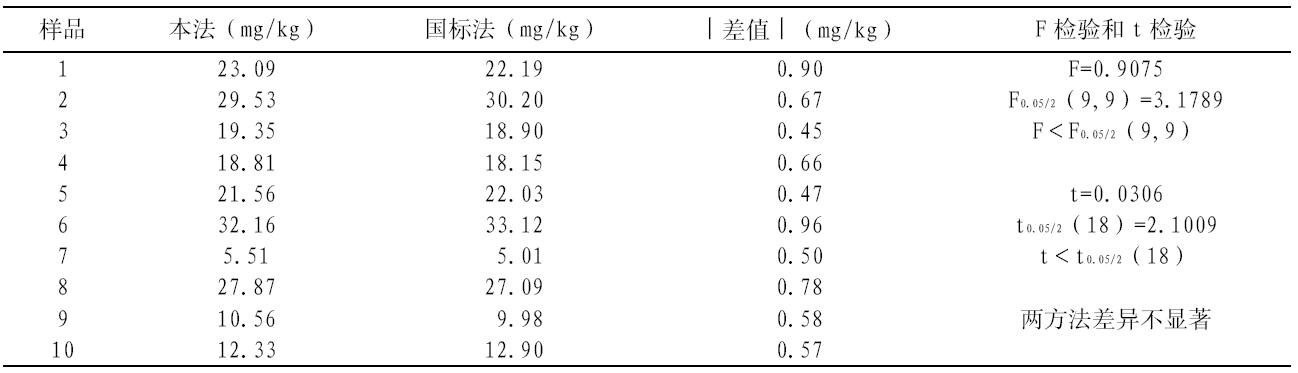
取 10 个不同糖厂生产的白砂糖样品, 分别用 本法和国标法对其二氧化硫含量进行测定, 同时, 对两组数据进行 F 检验和 t 检验[5],测定和检验 结果见表 4。 F 检验和 t 检验通过说明了两种方法 测定结果差异不显著。
| 表 4 本法与国标法的测定结果比较 |
本文研究了三乙醇胺溶液吸收—盐酸副玫瑰 苯胺分光光度法在测定白砂糖中二氧化硫的应 用。结果表明,该方法操作简便快速,重现性较 好,测定结果与国标法无显著差异,由于检出限 相对较低, 更适合于二氧化硫含量小于 1mg/kg 的精糖中二氧化硫的测定。并且该方法操作过程中 采用无汞试剂,对环境污染小,初步确定应可用 于白砂糖中二氧化硫的测定。
| [1] | 中国国家标准化管理委员会,GB317-2006白砂糖[S]. 北京:中国标准出版社,2006. ( 1) 1)
|
| [2] | 中国国家标准化管理委员会,GB/T5009.34-2003食品中亚硫酸盐的测定[S]. 北京:中国标准出版社,2003. ( 1) 1)
|
| [3] | 倪燕,欧红,三乙醇胺吸收光度法测定笋干和白糖中的二氧化硫[J]. 四川省卫生管理干部学院学报,2000(4):251-252. ( 1) 1)
|
| [4] | 中国国家标准化管理委员会,GB/T15262-1994环境空气·二氧化硫的测定·甲醛吸收-副玫瑰苯胺分光光度法[S]. 北京:中国标准出版社,1994. ( 1) 1)
|
| [5] | 汪荣鑫,数理统计[M]. 西安:西安交通大学出版社,1986:259. ( 1) 1)
|
 2009
2009