2. 中国科学院研究生院, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
地幔矿物的理想化学式中不含H, 但实际的矿物晶体中通常都有以点缺陷形式存在的OH.这些微量的结构水对地幔岩石矿物的电导率、弹性波速、离子扩散机制、流变特征和部分熔融条件有着重要的影响,对于流体交代、拆离、拆沉、底侵等地质作用也有很大的作用(Kushiro et al.,1968; Karato et al.,1986; Wood, 1995; Mei et al.,2002; Dixon et al.,2004; Wang et al.,2004; 黄晓葛等,2005; Mao et al.,2008; 黄小刚等,2012; Dai and Karato, 2009,2014a).因此,研究地幔矿物中水的溶解度具有显著的地质意义,这也是近几十年来人们对此项工作很有兴趣的原因.
上地幔(莫霍面-410 km)的主要造岩矿物是橄榄石、辉石和石榴石,其中,橄榄石含量最大.上地幔和下地幔的过渡带(410~660 km)主要由瓦兹利石(Wadsleyite)和林伍德石(Ringwoodite)组成,它们是橄榄石的高压相.地幔矿物中OH的溶解度是指一定的实验条件下OH达到饱和状态时与地幔矿物的质量比,通常表示为H2O在矿物中的质量分数(单位为ppm wt H2O),也有学者表示为矿物中H和Si的数量比(单位为H/106Si).直接测量矿物中水含量的方法主要是傅里叶转换红外光谱(FTIR)和二次离子探针(SIMS),相比之下,二次离子探针只能用来标定水含量,而傅里叶转换红外光谱还可用来研究矿物中水的结合机制.同一种矿物中OH通常具有多种结合机制,不同的矿物中OH的结合机制也有差别,这些结合机制在矿物的红外光谱中对应着不同的吸收波段.地幔矿物的水溶解度受化学成分和物理化学条件的影响,各因素对不同矿物的影响程度或效果是不同的.在高温高压实验条件下各种矿物均具有一定的结合水的能力,其中,上地幔矿物中水的溶解度变化很大(通常为102~104 ppm wt),过渡带矿物中水的溶解度通常为104-3×104 ppm wt(Rauch and Keppler, 2002; Demouchy et al.,2005; Mosenfelder et al.,2006; Mookherjee and Karato, 2010; Zhang et al.,2013; Yang et al.,2014).天然的上地幔矿物中通常也含有微量的水,出露地表的林伍德石(Ringwoodite)中更是检测出了质量分数为1.5%的水,这说明地幔转换带很可能是一个巨大的“水库”(Pearson et al.,2014).
1 研究方法及过程目前,获得地幔矿物中水溶解度的方法主要有两种,一种是通过测量矿物的电导率反推出水的溶解度(Huang et al.,2005; Dai and Karato, 2014b),另一种则是直接测量(白武明等,1993; Keppler and Rauch, 2000; Hauri et al.,2002).用电导率间接推导是一种反演的方法,对于宏观的地质探测工作具有实际意义,直接测量的方法则更适于微观物质中水溶解度的精确研究.直接测量地幔矿物水溶解度的方法也主要有两种:傅里叶转换红外光谱和二次离子探针.相比之下,二次离子探针只能用来标定水含量,而傅里叶转换红外光谱还可以通过吸收波段的变化特征研究OH的各种结合机制.两种研究方法通常配合使用,以验证最终的实验结果.
具体的实验过程可以简述为:(1)检测成分.通过电子探针(EPMA)检测合成样品或天然样品的化学组成.(2)组装样品.样品的尺寸通常较小,单晶样品沿着平行于晶轴的方向切割并将某一晶面打磨光滑,多晶样品则不必考虑晶轴的问题.在组装的过程中需要考虑含水矿物、固体氧缓冲剂及硅缓冲矿物的组合,确保样品囊处于封闭状态.(3)持续热压.在一定的高温高压条件下,维持足够的时间(必须使样品达到水饱和状态).(4)红外波谱分析及二次离子探针分析.在利用红外波谱测量时,如果矿物样品是单晶,通常需要测量各轴向的极化波谱;如果矿物样品是多晶,通常只测量其非极化波谱.实验结束后,利用相应的计算模型和参数计算样品的水溶解度,并对最终的结果进行分析和解释.
利用傅里叶转换红外光谱计算水溶解度的常用公式主要有Bell等(2003)、Paterson(1982)和Beer-Lambert公式(Paterson, 1982; Bell et al.,2003; Bolfan-Casanova et al.,2014).Bell等(2003)计算公式为



地幔矿物中水溶解度的影响因素可分为内部因素和外部因素.其中,内部因素包括矿物的晶体结构和化学组成,外部因素包括水逸度、温度、压力、氧逸度及硅活度等.
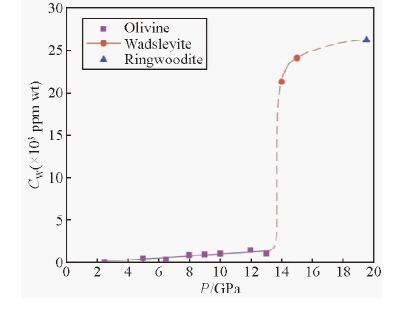
2.1 晶体结构不同矿物的水含量分配实验结果显示,各矿物结合OH的能力是不同的(Grant et al.,2007b,2007c),这可能主要是因为各类矿物具有自己独特的晶体结构.Kohlstedt等.(1996)研究了橄榄石的α、β和γ相矿物中水的溶解度(表 1),取相同压力条件下的最大水含量数据绘制图 1,由图 1可知α相的矿物在压力升高的过程中水含量是缓慢增加的,但从α相向β相转变的过程中矿物的水含量发生了突变(图 1).橄榄石不同高压相矿物的化学组成几乎不变,但是晶体结构却发生了显著变化,这说明矿物中水溶解度的变化与晶体结构的差异具有明显的关系.
|
|
表 1 水在橄榄石不同高压相中的溶解度 (引自Kohlstedt et al.,1996) Table 1 Water solubility of different high pressure phases of olivine(refer from Kohlstedt et al.,1996) |
矿物的晶体结构是影响OH的结合机制及其数量的重要因素,这是导致各种共生矿物中水的溶解度在相同实验条件下存在差异的主要原因.虽然,前人利用密度泛函理论和量子力学嵌入式集群方法计算了橄榄石中OH缺陷可能的位置及相应的红外吸收峰,但是并没有从理论上推导出晶体结构对OH数量的影响参数(Brodholt and Refson, 2000; Braithwaite et al.,2003).关于晶体结构影响矿物中水溶解度的微观原理需要进一步利用量子力学和物理化学的方法去研究.
2.2 化学组成一些金属离子对矿物中水溶解度具有显著的影响,甚至可以使部分实验条件与水溶解度的关系发生明显的转变.同一种地幔矿物中水溶解度可能受多种金属离子的影响,同一种金属离子也可能对不同的地幔矿物产生完全相反的作用.
水在橄榄石中的溶解度随着Fe2+含量的增加而系统性的增大(赵永红等,2004).在其他实验条件不变的情况下,随着三价离子(Al3+、Fe3+、Cr3+等)含量的增加,水在斜方辉石的溶解度显著增加(Rauch and Keppler, 2002; Mierdel et al.,2007; Zhang et al.,2013).斜方辉石中Al3+的存在使温度对水溶解度的影响也产生了相反的变化,含铝斜方辉石的水溶解度与温度呈负相关关系,而无铝斜方辉石的水溶解度与温度是正相关的(Zhang et al.,2013).水在顽辉石中的溶解度随着Na+的增加而变小(Stalder et al.,2008).Mg2+含量是影响石榴石中水溶解度的变量,它们之间呈正相关关系(表 2)(Mookherjee and Karato, 2010).
|
|
表 2 地幔矿物中水溶解度与化学成分的关系(据Rauch and Keppler, 2002; 赵永红等,2004; Mierdel et al.,2007; Stalder et al.,2008; Mookherjee and Karato, 2010; Zhang et al.,2013) Table 2 Chemical compositions dependence of water solubility in mantle minerals(refer from Rauch and Keppler, 2002; 赵永红等,2004; Mierdel et al.,2007; Stalder et al.,2008; Mookherjee and karato, 2010; Zhang et al.,2013) |
水逸度(fH2O)是控制地幔物质化学及物理性质的关键因素(Otsuka and Karato, 2011),它与具体的物质体系及温度、压力相关.地幔矿物中水的溶解度与水逸度具有直接的相关性,在所有相关研究中水逸度都是重要的控制因素.
在前人建立的地幔矿物水溶解度计算公式中,水逸度的指数通常随着研究对象的不同而发生变化(Kohlstedt et al.,1996; Otsuka and Karato, 2011).Kohlstedt等(1996)拟合了α相橄榄石中水溶解度的公式为
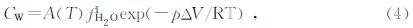
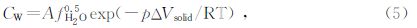
上地幔的横向温度梯度能够造成同一深度中水含量的巨大变化,热的地幔柱有可能从周围浅的上地幔吸收水(Mierdel and Keppler, 2004).研究温度与地幔矿物中水溶解度的关系可以进一步验证类似的地质问题.
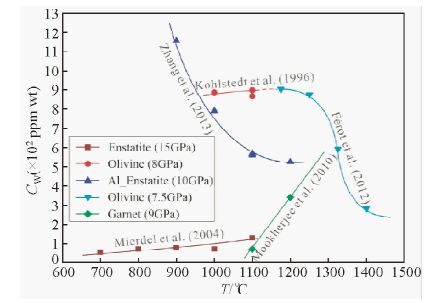
橄榄石的水溶解度与温度的关系可以概括为:水溶解度随着温度的升高而系统性地增加,但是当温度升高到一定程度使得矿物发生部分熔融后,水的溶解度开始下降(Kohlstedt et al.,1996; Smyth et al.,2006; Férot and Bolfan-Casanova, 2012).斜方辉石中水的溶解度与温度的关系受Al含量的影响,含铝的斜方辉石中水溶解度随温度的升高而降低,不含铝的斜方辉石则正好相反(Demouchy et al.,2005; Zhang et al.,2013).镁铝榴石中水的溶解度在温度较低时比较小,但是随着温度的升高而使石榴石发生部分熔融后,其水溶解度会大幅度的增加(图 2)(Mookherjee and Karato, 2010).
由式(4)和(5)可知,在水逸度和压力均保持不变且A也为常数时,温度和ΔV同时会造成矿物中水的溶解度的变化,所以在分析温度对水溶解度的影响前,首先应该探讨不同温度下体积的变化情况.
2.5 压 力上地幔矿物处在逐渐过渡的压力环境,随着深度的增加压力会不断变大,同种矿物在不同的深度可能因此具有不同的水含量.地球内部存在压力异常区域,熔融的岩浆向上的侵入的过程就是一个降压过程,地幔捕掳矿物中的水含量在压力降低的过程中也可能发生一定的变化.研究压力与地幔矿物中水溶解度的关系是解决此类问题的关键.
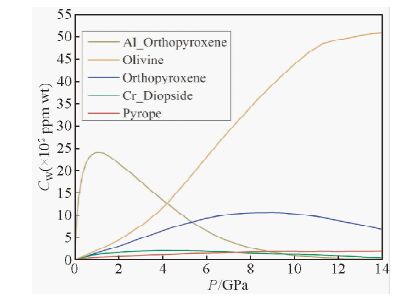
部分学者认为,橄榄石、斜顽辉石中水溶解度随着压力的升高而增加(Withers and Hirschmann, 2007; Ardia et al.,2012),硬玉中水溶解度却随着压力的升高而减小(Bromiley and Keppler, 2004).然而,根据Mookherjee和Karato(2010)地幔矿物中水溶解度与压力的关系图,可以大致地得出结论:大多数上地幔矿物中水的溶解度随着压力的增加而变大,当达到一定的压力后,水的溶解度趋于稳定或开始下降(图 3).可见,不同学者的认识还存在一定的差别,压力与地幔矿物中水溶解度的关系还需要更加深入的研究.
2.6 氧逸度氧逸度是地球内部地球化学过程中的一个重要参数.幔源的样品指示岩石圈的氧逸度是不均匀的,上地幔石榴石橄榄岩区域自上向下的氧逸度(fO2)是不断减小的(Grant et al.,2007a).实验证明,氧逸度对橄榄石中羟基的类型及水溶解度均具有一定的影响(Bell et al.,2004; Grant et al.,2007a).在2.0 GPa和1100~1300 ℃下,橄榄石的水溶解度随着氧逸度的增加而增大,低氧逸度(Fe-FeO)下退火的橄榄石中水的溶解度是较高氧逸度(Ni-NiO)下退火的橄榄石中水溶解度的一半.3355和3325 cm-1波段的吸收强度随着氧逸度的增加而增强,这被认为与Fe2+氧化为Fe3+的过程及相应的结合机制有关(Grant et al.,2007a).
橄榄石与氧气反应的过程中产生了点缺陷:Fe·Me和(或)Fe′ Si(Nakamura and Schmalzried, 1983; Tsai and Dieckmann, 2002).这个过程可以用Kröger-Vink符号描述为
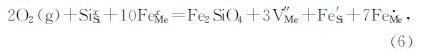
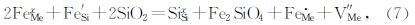
橄榄石在压力较大(>2.5 GPa)并且氧逸度较高(Ni-NiO)的实验中没有发现3355和3325 cm-1的吸收波段(Kohlstedt et al.,1996),这说明氧逸度对橄榄石中水溶解度及OH类型的作用还可能受到压力的影响,这需要进一步的研究.
2.7 硅活度Si4+是构成硅酸盐骨架的重要组成部分,位于硅氧四面体中心.当温度、压力达到一定程度时,Si4+可以被其他金属离子(Fe3+ 、Ti4+、Al3+等)及H+替代,高的aSiO2在一定程度上抑制了四面体位置被H+或它金属离子所占据,从而影响矿物中羟基缺陷的类型及水的溶解度.研究发现,低的aSiO2下合成的橄榄石样品的红外波谱中仅存在3620~3450 cm-1主要波段,而高的aSiO2下合成的橄榄石样品却在3160、3220和3660 cm-1处出现额外的波段.这种变化被解释为:在aSiO2较低时,样品中主要是质子化的硅空位;在aSiO2较高时,样品中主要是以Mg2+空位为主(Lemaire et al.,2004).
Smyth等(2006)研究了与斜硅镁石(低硅)共生的橄榄石及与斜顽辉石(高硅)共生的橄榄石中水的溶解度,发现结果近似,说明aSiO2在一定的温度压力条件下对橄榄石中水溶解度的影响比较小.天然地幔橄榄石的红外光谱通常与由斜方辉石缓冲条件下合成的橄榄石的红外光谱不一致,这可能由于橄榄石在上升的过程中与母岩浆发生了硅的再平衡(Otsuka and Karato, 2011).
3 不同矿物中水的溶解度地幔矿物结合水的能力不同,OH的结合机制也存在一定的差异.随着实验条件的变化,水溶解度也会呈现一定规律的变化.高温高压条件下水合样品的水溶解度通常比天然样品中水含量大,这可能有三种原因:(1)地幔矿物中的水达到了饱和状态,但是在上升的过程中向外发生了扩散;(2)地幔矿物中的水未达到饱和状态,而且在上升的过程中向外发生了扩散;(3)地幔矿物中的水未达到饱和状态,在上升的过程中没有向外扩散.
3.1 橄榄石天然橄榄石样品中水的溶解度通常在100 ppm wt 以下,最大可达400 ppm wt(Miller et al.,1987; Bell and Rossman, 1992; Bell et al.,2004; Peslier and Luhr, 2006; Ragozin et al.,2014).高温高压下水合橄榄石中的水溶解度通常在103 ppm wt左右,最大可达8×103 ppm wt以上(Kohlstedt et al.,1996; Mosenfelder et al.,2006; Bolfan-Casanova et al.,2014).
橄榄石中水的溶解度受化学组成、温度、压力、水逸度、氧逸度及硅活度的综合影响(Zhao et al.,2001; Smyth et al.,2006; Walker et al.,2007; Gaetani et al.,2014).据不同的实验条件,前人获得了橄榄石水溶解度随影响因素变化的函数关系.赵永红等(2004)在1000-1300 ℃和300 MPa下研究了温度和铁含量对橄榄石水溶解度的影响,其中,氧逸度是由Ni-NiO固相缓冲对来控制,硅活度由顽辉石来控制,最终拟合了水溶解度对有限变量的函数:
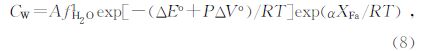
Ardia等(2012)结合Tenner等(2011)的实验数据,得到了水合橄榄岩中的橄榄石在5~13 GPa和1450 ℃下的水溶解度公式为
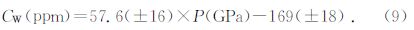
Gaetani et al.(2014)在1~2 GPa和1200 ℃下,研究了水逸度和氧逸度对橄榄石中水溶解度并建立了公式为
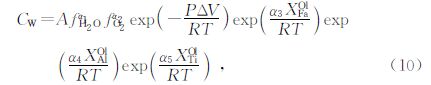
橄榄石中OH的吸收峰被分为两组:GroupⅠ(3650~3450 cm-1)和GroupⅡ(3450~3200 cm-1),其中,GroupⅠ对应的结合机制包括了Si空位和Ti4+相关机制,GroupⅡ对应的结合机制包括了M空位和Me3+(Fe3+、Al3+等)相关机制(Kohlstedt et al.,1996; Berry et al.,2005; Walker et al.,2007).
3.2 辉 石辉石的体积总量在上地幔中仅次于橄榄石.大量的研究结果显示,单斜辉石和斜方辉石是水在上地幔中的重要宿主矿物(Bell and Rossman, 1992; Bolfan-Casanova, 2005; Skogby, 2006).在对自然样品的研究中发现辉石中水含量比伴生的橄榄石中水含量更多,这与辉石和橄榄石水含量分配实验数据在一定程度上是不符合的,这说明在降温降压的过程中辉石比橄榄石更容易保存内部的结构水(Berry et al.,2005).
3.2.1 单斜辉石单斜辉石是上地幔的重要组成矿物,它在出露的榴辉岩中体积约为一半左右.来自橄榄岩捕掳体中的单斜辉石水浓度通常在400 ppm wt以下;来自榴辉岩捕掳体中的单斜辉石水浓度变化很大,最大可达3020 ppm wt(Koch-Müller and Matsyuk, 2004; Katayama and Nakashima, 2003).合成的样品中水的溶解度通常是102~103 ppm wt, 最大为2200 ppm wt(Skogby, 1994; Mosenfelder and Rossman, 2013).由公式(5)可知,单斜辉石中水的溶解度受温度、压力、水逸度等因素影响.
透辉石-钙铁辉石和普通辉石的红外光谱中具有四个吸收波段:3650~3620、3550~3520、3470~3450和3360~3350 cm-1 .其中,透辉石的红外波谱中吸收最强烈的位置是3640和3460 cm-1,普通辉石则位于3635 cm-1.绿辉石的波谱与成分有着显著的关系,富含硬玉成分时具有平行于nγ的3470~3460 cm-1极化波段,富含透辉石成分时具有平行于nα的3620 cm-1处的极化波峰.在10 GPa下合成的水饱和硬玉的红外光谱在3613和3373 cm-1是显著的尖锐波段(Bromiley and Keppler, 2004).
OH在单斜辉石中的结合机制被认为有以下几种:(1)OH占据O2的位置并指向邻近硅酸盐链的O3,对应于透辉石在3650~3620 cm-1的吸收波段;(2)OH占据O2的位置并指向邻近的M2空位,对应于绿辉石在3540~3500 cm-1及3465~3445 cm-1的nγ极化波段;(3)Si空位周围形成水榴石缺陷[VSi(OH)4]X,这是通过原子计算机模拟方法获得的透辉石和硬玉中OH最有利的结合方式,[AlSi(OH)4]X缺陷在两种矿物相中都可能存在(Bromiley and Keppler, 2004; Gatzemeier and Wright, 2006).
3.2.2 斜方辉石斜方辉石是组成上地幔的重要矿物之一,体积含量大约为20~40%(Ringwood, 1975).天然斜方辉石的水浓度通常在40~400 ppm wt之间(Mosenfelder and Rossman, 2013).水合样品中水溶解度变化很大(Rauch and Keppler, 2002; Mierdel and Keppler, 2004),富铝顽辉石中水的溶解度最大可达104 ppm wt(Zhang et al.,2013).
Zhang等(2013)拟合了斜方辉石中水溶解度计算公式,其表达式为

天然斜方辉石的红外波谱中,吸收波段主要包括低波数段(2600~3350 cm-1)和高波数段(3350~3700 cm-1)(Mosenfelder and Rossman, 2013).水合顽辉石的红外光谱通常在3070和3360 cm-1附近形成两个主要的吸收波段,分别称为A4和A3波段.A4波段比A3波段更宽.这两个波段在平行于nγ(//c)的极化波谱中吸收强度最大,而在平行于nβ(//a)的极化波谱中几乎不具有吸收强度.在较低的硅活度和更高的压力下合成的顽辉石,除了3070和3360 cm-1外,在3590和3690 cm-1附近也观察到了吸收波段,它们在平行于nβ的极化波谱中具有最大的吸收强度.这两个吸收波段分别被称为A2和A1波段.据推测,A1和A2波段与质子补偿Si4+空位有关,A3和A4波段与质子补偿Mg2+ 空位有关(Stalder et al.,2008; Mierdel and Keppler, 2004; Grant et al.,2006; Stalder and Skogby, 2002; Stalder et al.,2012).
3.3 石榴子石石榴子石在上地幔浅部的体积分数约为20%,在出露的榴辉岩中甚至达到了80%(Mookherjee and Karato, 2010).钙铝榴石和钙铁榴石中水的含量很高,分别可达1 wt%和6 wt%,来自上地幔天然样品中的水含量通常在5~10 ppm wt之间,有时可以达到50~100 ppm wt(Peslier and Luhr, 2006).Mookherjee和Karato(2010)在5~9 GPa和1373~1473 K的实验结果显示:镁铝榴石的水溶解度最小约为100 ppm wt, 最大可达1000 ppm wt.在一定的温度压力范围内,石榴子石中水溶解度差别较大,这可能和样品中化学成分的细微差异有关(Lu and Keppler, 1997; Withers et al.,1998; Mookherjee and Karato, 2010).
Mookherjee和Karato(2010)的研究显示:(1)镁铝榴石的水溶解度随着镁含量的增加而变大,且镁含量与压力是正相关关系.(2)在7 GPa和1373 ℃时,出现熔融相的矿物中水的溶解度几乎是未出现熔融相矿物的10倍,说明水在镁铝榴石发生部分熔融的过程中更倾向进入矿物中.(3)水逸度对镁铝榴石的水溶解度影响巨大,水逸度指数r约为0.4.
镁铝榴石的红外波谱在3630 cm-1周围具有宽的不对称吸收波段,低压时在3615、3566和3496 cm-1出现多个次级的吸收峰.石榴石中水的结合机制有可能是H+与Al3+耦合替代Si4+(Mookherjee and Karato, 2010).化学反应可表示为
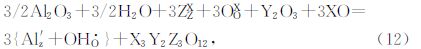
|
图 1 橄榄石不同高压相矿物中水溶解度与压力的关系(据 Kohlstedt et al.,1996) Fig. 1 Pressure dependence of water solubility in different high pressure phases of olivine (refer from Kohlstedt et al.,1996) |
|
图 2 上地幔矿物中水溶解度与温度的关系(据Kohlstedt et al.,1996; Mierdel and Keppler, 2004; Mookherjee and Karato, 2010; Férot and Bolfan-Casanova, 2012; Zhang et al.,2013) Fig. 2 Temperature dependence of water solubility in mantle minerals(refer from Kohlstedt et al., 1996; Mierdel and Keppler, 2004; Mookherjee and Karato, 2010; Férot and Bolfan-Casanova, 2012; Zhang et al.,2013) |
|
图 3 上地幔矿物中水的溶解度与压力的关系 (据Mookherjee and Karato, 2010) Fig. 3 Pressure dependence of water solubility in mantle minerals(refer from Mookherjee and Karato, 2010) |
|
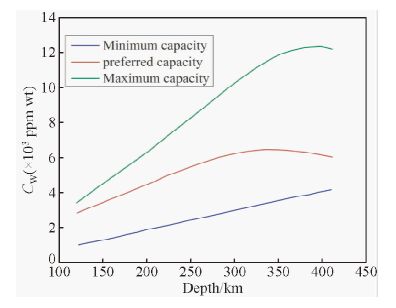
图 4 不同假设条件下(文中已讨论)上地幔的储水能力模型(据Hirschmann et al.,2005) Fig. 4 Model storage capacity of theupper mantlefor different assumptions discussed in the text(refer from Hirschmann et al.,2005) |
|
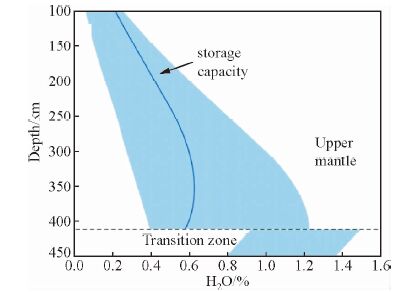
图 5 上地幔及地幔转换带的储水能力模型 (据Hirschmann et al.,2005) Fig. 5 Model storage capacity of the upper mantle and the transition zone (refer from Hirschmann et al.,2005) |
瓦兹利石和林伍德石是橄榄石的高压相,是地幔过渡带(410~660 km)的主要矿物.大量实验表明,瓦兹利石和林伍德石的水溶解度较高,通常为1~3 wt%(Kohlstedt et al.,1996; Demouchy et al.,2005; Panero et al.,2013).Deon等(2011)发现在12.2 GPa和1200 ℃时,水在共生的橄榄石、瓦兹利石和林伍德石中的质量分配系数为:Dwad/olwater=3.7、Dring/olwater=1.5和Dwad/ringwater=2.5.
目前,尚未发现天然的瓦兹利石,合成样品的水溶解度最大可达3 wt%(Inoue et al.,1995).Demouchy等(2005)研究发现,压力为15 GPa, 温度从900 ℃升高到1400 ℃时,瓦兹利石中水的溶解度由2.2 wt%降至0.9 wt%.说明在一定的压力下,瓦兹利石中水溶解度随着温度的升高而减小.在温度为1200 ℃时,压力从14 GPa升高到18 Gpa的过程中溶解度也系统性地减小(Demouchy et al.,2005).Blanchard等(2013)认为瓦兹利石中OH的结合机制包含了以下四种类型:完全质子化的镁离子空位,完全质子化的硅离子空位,一个镁离子和两个氢离子占据硅离子空位,与硅离子向正常空位的迁移相关的OH缺陷(Blanchard et al.,2013).Yang等(2014)在650~900 ℃和14.2~18.4 GPa下通过原位测量,发现瓦兹利石的红外吸收波段主要包括了3200~3400和3600 cm-1,它们可能分别与O1的质子化(电荷由Mg2+空位补偿)及M3边缘弯曲的氢键有关.
出露于地表的天然林伍德石中水溶解度达到了1.5 wt%,而合成样品最大可达2.6 wt%以上(Kohlstedt et al.,1996; Pearson et al.,2014).Ohtani et al.(2000)发现随着温度的升高,与含水流体共生的林伍德石中水溶解度逐渐变小.Panero et al.(2013)通过在低温、高压下以同步加速为基础的傅里叶转换红外光谱分析,得到样品中OH的结合机制包含了三种:[]″Mg+2(H)·、[]'''Si+4(H)·、Mg″Si+2(H)·,其中,[]″Mg+2(H)·对应的吸收波段为3100 cm-1和3270 cm-1(也有可能包括2654 cm-1),[]'''Si+4(H)·对应的波段为3640 cm-1,Mg″Si+2(H)·对应的波段为2800 cm-1.
4 地幔不同深度的储水能力Hirschmann等(2005)根据Kohlstedt等(1996)的数据拟合橄榄石中水的溶解度与深度的对应关系为

根据上式可以获得不同深度橄榄石中水的溶解度,结合其他共生矿物中水的溶解度与橄榄石中水溶解度的假设关系及Irifune和Issiki(1998)中上地幔不同深度的矿物组成,便可知上地幔不同深度的储水能力.当辉石与橄榄石中水的溶解度相同时,石榴石中水的溶解度与橄榄石中水的溶解度在2000 ppm wt之前也相同(之后保持定值),得到上地幔不同深度的最低储水能力曲线.当辉石和石榴石中水溶解度与橄榄石中水溶解度的比值分别为10和2.5时,得到上地幔不同深度的最大储水能力曲线.然而,实验结果显示最大的储水能力位于350 km处(0.65 wt%),在410 km处逐渐减小为0.55 wt%,据此得到与实验结果更加符合的变化曲线(图 4)(Hirschmann et al.,2005).
在图 4的基础上,Hirschmann等(2005)根据前人对瓦兹利石的研究成果,得到了地幔转换带及上地幔的储水能力(图 5),并认为地幔物质对流过程中橄榄岩不断发生部分熔融的原因是内部水含量超过了可被允许的最大储存能力.
Ohtani等(2004)认为地幔深处具有四个潜在的脱水位置:俯冲带的地幔楔、地幔转换带、上地幔顶部含水林伍德石和超级含水相B分解的位置、下地幔深处含水相D(G)分解的位置.可见水在整个地幔的分布是非常复杂的,需要我们综合多种方法和途径去认识,而水的溶解度是认识整个地球内部水分布的重要参考因素.实验结果与天然样品的分析相结合是探索地质问题的有效途径,伴随着科学技术的发展,实际探测的技术和实验模拟的方法越来越成熟,这为深入认识包括地球内部水的分布等问题打好了基础(金振民,1997;董树文等,2012;周春银和金振民,2014).
5 存在的问题及今后的研究方向目前,对地幔矿物中水溶解度的研究已较为成熟,高温高压实验条件已经可以模拟大部分地幔环境,矿物中的水含量及OH的结合机制也可以通过SIMS及FTIR等方法较为准确的获得,橄榄石、辉石、石榴石、瓦兹利石、林伍德石等主要的名义上无水矿物的水溶解度都已被研究.然而,依然存在以下问题:
1 )无法准确得到地幔的物理条件和化学组成,导致实验结果可能与实际情况存在一定的差异,所以要准确研究地幔中水的实际含量,需要对地幔的物理化学状况进行更加深入的探究.
2)一些类型的辉石和石榴石尚未被研究,已研究的矿物数据也比较有限,要准确得到整个地幔的储水能力及分布状况,需要对各圈层主要的造岩矿物进行系统研究.
3 )氧逸度对矿物中水溶解度的影响程度还不够清楚,目前只对橄榄石进行过相应研究,有必要在不同的氧逸度条件下对主要的地幔矿物进行研究.
4)对天然样品的研究较少,天然样品中原始的水含量目前尚不可知.如果能够利用出露于地表的地幔矿物中的水含量及其向外的扩散速率,则有可能解决这个问题.
5 )没有解决地幔矿物是否处于水饱和状态的问题,这使得实验结果无法直接应用于地质问题的分析.要解决这个问题,还需要更进一步的实验创新和理论探索.
6)对水进入矿物的微观机理研究不够,尽管已提出多种结合机制,然而对水进入矿物的过程并没有详细的解释.
7 )上地幔矿物中水溶解度的拟合公式还不够完善,需要进一步将矿物的水溶解度与晶体结构、成分和物理化学条件等有机结合,建立完善的理论体系.
8)地球内部的水对板块运动、岩浆活动、地震等地质作用的影响还没有深入探索,这是未来需要重点研究的方向.
致 谢 对本课题组老师及师兄师姐的指导和关怀深表谢意.
| [1] | Ardia P, Hirschmann M M, Withers A C, et al. 2012. H2O storage capacity of olivine at 5-8 GPa and consequences for dehydration partial melting of the upper mantle[J]. Earth and Planetary Science Letters, 345-348: 104-116. |
| [2] | Bai W M, Sun Z T, Bai Q, et al. 1993. Solubility of hydrogen in olivine[J]. Progress in Geophysics (in Chinese), 8(4): 257. |
| [3] | Bell D R, Rossman G R. 1992. Water in the Earth’s mantle: the role of nominally anhydrous minerals[J]. Science, 25(5050): 1391-1397. |
| [4] | Bell D R, Rossman G R, Maldener J, et al. 2003. Hydroxide in olivine: a quantitative determination of the absolute amount and calibration of the IR spectrum[J]. Journal of Geophysical Research, 108(B2): 2015. |
| [5] | Bell D R, Rossman G R, Moore R O. 2004. Abundance and partitioning of OH in a high pressure magmatic system: megacrysts from the Monastery Kimberlite, South Africa[J]. Journal of Petrology, 45(8): 1539-1564. |
| [6] | Berry A J, Hermann J, O'Neill H S C, et al. 2005. Fingerprinting the water site in mantle olivine[J]. Geology, 33(11): 869-872. |
| [7] | Blanchard M, Roberge M, Balan E, et al. 2013. Infrared signatures of OH-defects in wadsleyite: A first-principles study[J]. American Mineralogist, 98(11-12): 2132-2143. |
| [8] | Bolfan-Casanova N. 2005. Water in the Earth’s mantle[J]. Mineralogical Magazine, 69(3): 229-258. |
| [9] | Bolfan-Casanova N, Montagnac G, Reynard B. 2014. Measurement of water contents in olivine using Raman spectroscopy[J]. American Mineralogist, 99(1): 149-156. |
| [10] | Braithwaite J S, Wright K, Catlow C R A. 2003. A theoretical study of the energetics and IR frequencies of hydroxyl defects in forsterite[J]. Journal of Geophysical Research, 108(B6): 2284. |
| [11] | Brodholt J P, Refson K. 2000. An ab initio study of hydrogen in forsterite and a possible mechanism for hydrolytic weakening[J]. Journal of Geophysical Research, 105(B8): 18977-18982. |
| [12] | Bromiley D B, Keppler H. 2004. An experimental investigation of hydroxyl solubility in jadeite and Na-rich clinopyroxenes[J]. Contributions to Mineralogy and Petrology, 147(2): 189-200. |
| [13] | Dai L D, Karato S. 2009. Electrical conductivity of wadsleyite at high temperatures and high pressures[J]. Earth and Planetary Science Letters, 287(1-2): 277-283. |
| [14] | Dai L D, Karato S. 2014a. High and highly anisotropic electrical conductivity of the asthenosphere due to hydrogen diffusion in olivine[J]. Earth and Planetary Science Letters, 408: 79-86. |
| [15] | Dai L D, Karato S. 2014b. The effect of pressure on the electrical conductivity of olivine under the hydrogen-rich conditions[J]. Physics of the earth and Planetary Interiors, 232: 51-56. |
| [16] | Demouchy S, Deloule E, Frost D J, et al. 2005. Pressure and temperature-dependence of water solubility in Fe-free wadsleyite[J]. American Mineralogist, 90(7): 1084-1091. |
| [17] | Deon F, Koch-Müller M, Rhede D, et al. 2011. Water and Iron effect on the P-T-x coordinates of the 410-km discontinuity in the Earth upper mantle[J]. Contributions to Mineralogy and Petrology, 161(4): 653-666. |
| [18] | Dixon J E, Dixon T H, Bell D R, et al. 2004. Lateral variation in upper mantle viscosity: Role of water[J]. Earth and Planetary Science Letters, 222 (2): 451-467. |
| [19] | Férot A, Bolfan-Casanova N. 2012. Water storage capacity in olivine and pyroxene to 14 GPa: Implications for the water content of the Earth’s upper mantle and nature of seismic discontinuities[J]. Earth and Planetary Science Letters, 349-350: 218-230. |
| [20] | Gaetani G A, O’Leary J A, Koga K T, et al. 2014. Hydration of mantle olivine under variable water and oxygen fugacity conditions[J]. Contributions to Mineralogy and Petrology, 167(2): 965. |
| [21] | Gatzemeier A, Wright K. 2006. Computer modelling of hydrogen defects in the clinopyroxenes diopside and jadeite [J]. Physics and Chemistry of Minerals, 33(2): 115-125. |
| [22] | Grant K J, Kohn S C, Brooker R A. 2006. Solubility and partitioning of water in synthetic forsterite and enstatite in the system MgO-SiO2-H2O±Al2O3[J]. Contributions to Mineralogy and Petrology, 151(6): 651-664. |
| [23] | Grant K J, Brooker R A, Kohn S C, et al. 2007a. The effect of oxygen fugacity on hydroxyl concentrations and speciation in olivine: Implications for water solubility in the upper mantle[J]. Earth and Planetary Science Letters, 261(1-2): 217-229. |
| [24] | Grant K J, Ingrin J, Lorand J P, et al. 2007b. Water partitioning between mantle minerals from peridotite xenoliths[J]. Contributions to Mineralogy and Petrology, 154(1): 15-34. |
| [25] | Grant K J, Kohn S C, Brooker R A. 2007c. The partitioning of water between olivine, orthopyroxene and melt in the system albite-Forsterite-H2O[J]. Earth and Planetary Science Letters, 260(1-2): 227-241. |
| [26] | Hauri E, Wang J H, Dixon J E, et al. 2002. SIMS analysis of volatiles in silicate glasses 1. Calibration, matrix effects and comparisons with FTIR[J]. Chemical Geology, 183(1-4): 99-114. |
| [27] | Hirschmann M M, Aubaud C, Withers A C. 2005. Storage capacity of H2O in nominally anhydrous minerals in the upper mantle[J]. Earth and Planetary Science Letters, 236(1-2): 167-181. |
| [28] | Huang X G, Bai W M, Xu Y S, et al. 2005. Influence of hydrogen on electrical conductivity of wadsleyite and ringwoodite with its geodynamics implications[J]. Acta Petrologica Sinica (in Chinese), 21(6): 1743-1748. |
| [29] | Huang X G, Huang X G, Bai W M. 2012. Study on the electrical conductivity of carbonated peridotite[J]. Chinese Journal of Geophysics (in Chinese), 55(9): 3144-3151, doi: 10.6038/j.issn.0001-5733.2012.09.032. |
| [30] | Huang X G, Xu Y H, Karato S. 2005. Water content in the mantle transition zone from the electrical conductivity of wadsleyite and ringwoodite[J]. Nature, 434(7034): 746-749. |
| [31] | Inoue T, Yurimoto H, Kudoh Y. 1995. Hydrous modified spinel, Mg1.75SiH0.5O4: a new water reservoir in the mantle transition region[J]. Geophysical Research Letters, 22(2): 117-120. |
| [32] | Jin Z M. 1997. The progresses and perspectives of high-T and high-P experimental study in China[J]. Chinese Journal of Geophysics (in Chinese), 40(S): 70-81. |
| [33] | Karato S, Paterson M S, Fitzgerald J D. 1986. Rheology of synthetic olivine aggregates: Influence of grain size and water[J]. Journal of Geophysical Research, 91(B8): 8151-8176. |
| [34] | Katayama I, Nakashima S. 2003. Hydroxyl in clinopyroxene from the deep subducted crust: evidence for H2O transport into the mantle[J]. American Mineralogist, 88(1): 229-234. |
| [35] | Keppler H, Bolfan-Casanova N. 2006. Thermodynamics of water solubility and partitioning[J]. Review in Mineralogy and Geochemistry, 62(1): 193-230. |
| [36] | Keppler H, Rauch M. 2000. Water solubility in nominally anhydrous Minerals measured by FTIR and 1H MAS NMR: the effect of sample preparation[J]. Physics and Chemistry of Minerals, 27(6): 371-376. |
| [37] | Koch-Müller M, Matsyuk S S, Wirth R. 2004. Hydroxyl in omphacites and omphacitic clinopyroxenes of upper mantle to lower crustal origin beneath the Siberian platform[J]. American Mineralogist, 89(7): 921-931. |
| [38] | Kohlstedt D L, Keppler H, Rubie D C. 1996. Solubility of water in the α, β and γ phases of (Mg, Fe)2SiO4[J]. Contributions to Mineralogy and Petrology, 123(4): 345-357. |
| [39] | Kushiro I, Syono Y, Akimoto S-I. 1968. Melting of a peridotite nodule at high pressures and high water pressures[J]. Journal of Geophysical Research, 73(18): 6023-6029. |
| [40] | Lemaire C, Kohn S C, Brooker R A. 2004. The effect of silica activity on the incorporation mechanisms of water in synthetic forsterite: a polarised infrared spectroscopic study[J]. Contributions to Mineralogy and Petrology, 147(1): 48-57. |
| [41] | Lu R, Keppler H. 1997. Water solubility in pyrope to 100 kbar[J]. Contributions to Mineralogy and Petrology, 129(1): 35-42. |
| [42] | Mao Z, Jacobsen S D, Jiang F, et al. 2008. Single-crystal elasticity of wadsleyites, β-Mg2SiO4, containing 0.37-1.66 wt.% H2O[J]. Earth and Planetary Science Letters, 266(1-2): 78-89. |
| [43] | Matveev S, O'Neill H S C, Ballhaus C, et al. 2001. Effect of silica activity on OH- IR spectra of olivine: implications for low-aSiO2 mantle metasomatism[J]. Journal of Petrology, 42(2): 721-729. |
| [44] | Mei S, Bai W, Hiraga T, et al. 2002. Influence of melt on the creep behavior of olivine-basalt aggregates under hydrous conditions[J]. Earth and Planetary Science Letters, 201(3-4): 491-507. |
| [45] | Mierdel K, Keppler H. 2004. The temperature dependence of water solubility in enstatite[J]. Contributions to Mineralogy and Petrology, 148(3): 305-311. |
| [46] | Mierdel K, Keppler H, Smyth J R, et al. 2007. Water solubility in aluminous orthopyroxene and the origin of Earth’s asthenosphere[J].. Science, 315(5810): 364-368. |
| [47] | Miller G H, Rossman G R, Harlow G E. 1987. The natural occurrence of hydroxide in olivine[J]. Physics and Chemistry of Minerals, 14(5): 461-472. |
| [48] | Mookherjee M, Karato S. 2010. Solubility of water in pyrope-rich garnet at high pressures and temperature[J]. Geophysical Research Letters, 37(3): L03310. |
| [49] | Mosenfelder J L, Deligne N I, Asimow P D, et al. 2006. Hydrogen incorporation in olivine from 2-12 GPa[J]. American Mineralogist, 91(2-3): 285-294. |
| [50] | Mosenfelder J L, Rossman G R. 2013a. Analysis of hydrogen and fluorine in pyroxenes: II. Clinopyroxene[J]. American Mineralogist, 98(5-6): 1042-1054. |
| [51] | Mosenfelder J L, Rossman G R. 2013b. Analysis of hydrogen and fluorine in pyroxenes: I. Orthopyroxene[J]. American Mineralogist, 98(5-6): 1026-1041. |
| [52] | Nakamura A, Schmalzried H. 1983. On the nonstoichiometry and Point defects of olivine[J]. Physics and Chemistry of Minerals, 10(1): 27-37. |
| [53] | Ohtani E, Mizobata H, Yurimoto H. 2000. Stability of dense hydrous magnesium silicate phases in the systems Mg2SiO4-H2O and MgSiO3-H2O at pressures up to 27 GPa[J]. Physics and Chemistry of Minerals, 27(8): 533-544. |
| [54] | Ohtani E, Litasov K, Hosoya T, et al. 2004. Water transport into the deep mantle and formation of a hydrous transition zone[J]. Physics of the Earth and Planetary Interiors, 143-144: 255-269. |
| [55] | Otsuka K, Karato S. 2011. Control of the water fugacity at high pressures and temperatures: Applications to the incorporation mechanisms of water in olivine[J]. Physics of the Earth and Planetary Interiors, 189(1-2): 27-33. |
| [56] | Panero W R, Smyth J R, Pigott J S, et al. 2013. Hydrous ringwoodite to 5 K and 35 GPa: Multiple hydrogen bonding sites resolved with FTIR spectroscopy[J]. American Mineralogist, 98(4): 637-642. |
| [57] | Paterson M S. 1982. The determination of hydroxyl by infrared absorption in quartz, silicate glasses, and similar materials[J]. Bulletin de Mineralogy, 105: 20-29. |
| [58] | Pearson D G, Brenker F E, Nestola F, et al. 2014. Hydrous mantle transition zone indicated by ringwoodite included within diamond[J]. Nature, 507(7491): 221-224. |
| [59] | Peslier A H, Luhr J F. 2006. Hydrogen loss from olivines in mantle xenoliths from Simcoe (USA) and Mexico: mafic alkalic magma ascent rates and water budget of the sub-continental lithosphere[J]. Earth and Planetary Science Letters, 242(3-4): 302-319. |
| [60] | Ragozin A L, Karimova A A, Litasov K D, et al. 2014. Water content in minerals of mantle xenoliths from the Udachnaya pipe kimberlites (Yakutia)[J]. Russian Geology and Geophysics, 55(4): 428-442. |
| [61] | Rauch M, Keppler H. 2002. Water solubility in orthopyroxene[J]. Contributions to Mineralogy and Petrology, 143(5): 525-536. |
| [62] | Ringwood A E. 1975. Composition and Petrology of the Earth’s Mantle[M]. New York: McGraw-Hill, 1-618. |
| [63] | Skogby H. 1994. OH incorporation in synthetic clinopyroxene[J]. American Mineralogist, 79(3-4): 240-249. |
| [64] | Skogby H. 2006. Water in natural mantle minerals I: Pyroxenes[J]. Reviews in Mineralogy and Geochemistry, 62(1): 155-167. |
| [65] | Smyth J R, Frost D J, Nestola F, et al. 2006. Olivine hydration in the deep upper mantle: Effects of temperature and silica activity[J]. Geophysical Research Letters, 33(15): L15301. |
| [66] | Stalder R, Skogby H. 2002. Hydrogen incorporation in enstatite[J]. European Journal of Mineralogy, 14(6): 1139-1144. |
| [67] | Stalder R, Kronz A, Simon K. 2008. Hydrogen in corporation in enstatite in the system MgO-SiO2-H2O-NaCl[J]. Contributions to Mineralogy and Petrology, 156(5): 653-659. |
| [68] | Stalder R, Prechtel F, Ludwig T. 2012. No site-specific infrared absorption coefficient for OH-defects in pure enstatite[J]. European Journal of Mineralogy, 24(3): 465-470. |
| [69] | Tsai T L, Dieckmann R. 2002. Variation of the oxygen content and point defects in olivines, (FexMg1-x)2SiO4, 0.2≤x≤1.0[J]. Physics and Chemistry of Minerals, 29(10): 680-694. |
| [70] | Walker A M, Hermann J, Berry A J, et al. 2007. Three water sites in upper mantle olivine and the role of titanium in the water weakening mechanism[J]. Journal of Geophysical Research, 112(B5): B05211. |
| [71] | Wang Z Y, Hiraga T, Kohlstedt D L. 2004. Effect of H+ on Fe-Mg interdiffusion in olivine, (Fe, Mg)2SiO4[J]. Applied Physics Letters, 85(2): 209-211. |
| [72] | Withers A C, Hirschmann M M. 2007. H2O storage capacity of MgSiO3 clinoenstatite at 8-13 GPa, 1100-1400 ℃[J]. Contributions to Mineralogy and Petrology, 154(6): 663-674. |
| [73] | Withers A C, Wood B J, Carroll M R. 1998. The OH content of pyrope at high pressure[J]. Chemical Geology, 147(1-2): 161-171. |
| [74] | Wood B J. 1995. The effect of H2O on the 410-Kilometer seismic discontinuity[J]. Science, 268(5207): 74-76. |
| [75] | Yang X Z, Keppler H, Dubrovinsky L, et al. 2014. In-situ infrared spectra of hydroxyl in wadsleyite and ringwoodite at high pressure and high temperature[J]. American Mineralogist, 99(4): 724-729. |
| [76] | Zhang B H, Matsuzaki T, Wu X P. 2013. Water solubility in orthopyroxene: Dependence on temperature and Al content[J]. Chinese Science Bulletin, 58(32): 3895-3902. |
| [77] | Zhao Y H, Ginsberg S, Kohlstedt D L. 2001. Experimental investigation on water solubility in olivine single crystals with different Fe content[J]. Acta Petrologica Sinica (in Chinese), 17(1): 123-128. |
| [78] | Zhao Y H, Ginsberg S B, Kohlstedt D L. 2004. Solubility of hydrogen in olivine: dependence on temperature and iron content[J]. Contributions to Mineralogy and Petrology, 147(2): 155-161. Dong S W, Li T D, Chen X H, et al. 2012. Progress of deep exploration in mainland China: A review[J]. Chinese Journal of Geophysics (in Chinese), 55(12): 3884-3901, doi: 10.6038/j.issn.0001-5733.2012.12.002. |
| [79] | Zhou C Y, Jin Z M. 2014. The “bright lamp” into the deep Earth:experiments at high pressure and high temperature[J]. Chinese Journal of Nature (in Chinese), 36(2): 79-88. |
| [80] | 白武明, 孙泽天, 白泉,等. 1993. 氢在橄榄石中的溶解度[J]. 地球物理学进展, 8(4): 257. |
| [81] | 董树文, 李廷栋, 陈宣华,等. 2012. 我国深部探测技术与实验研究进展综述[J]. 地球物理学报, 55(12): 3884-3901, doi: 10.6038/j.issn.0001-5733.2012.12.002. |
| [82] | 黄晓葛, 白武明, Xu YouSheng, 等. 2005. 水对Wadsleyite和Ringwoodite电导率的影响及地球动力学意义[J]. 岩石学报, 21(6): 1743-1748. |
| [83] | 黄小刚, 黄晓葛, 白武明. 2012. 碳酸盐化橄榄岩的电性研究[J]. 地球物理学报, 55(9): 3144-3151, doi: 10.6038/j.issn.0001-5733.2012.09.032. |
| [84] | 金振民. 1997. 我国高温高压实验研究进展和展望[J]. 地球物理学报, 40(S): 70-81. |
| [85] | 赵永红, Ginsberg S, Kohlstedt D L. 2004. 橄榄石水溶性与含铁量相关性的实验研究[J]. 岩石学报, 17(1): 123-128. |
| [86] | 周春银, 金振民. 2014. 照亮地球深部的“明灯”——高温高压实验[J]. 自然杂志, 36(2): 79-88. |
 2015, Vol. 30
2015, Vol. 30


